Ces dernières années, le pronostic du cancer du sein métastatique HER2-positif a été considérablement amélioré grâce au développement de nouvelles molécules telles que le conjugué anti-body-drug (ADC) trastuzumab-deruxtecan et l’inhibiteur de tyrosine kinase ciblant HER2, le tucatinib. A tel point qu’une approche thérapeutique curative a même été présentée au San Antonio Breast Cancer Symposium 2020. Néanmoins, les mécanismes de résistance inexpliqués, les métastases du SNC et le choix de la bonne séquence thérapeutique dans les stades avancés, en particulier, constituent encore aujourd’hui des défis majeurs dans la pratique clinique quotidienne.
Un coup d’œil sur la survie globale des patientes atteintes d’un cancer du sein métastatique HER2-positif le prouve : beaucoup de choses ont changé au cours des 20 dernières années. Alors que la médiane de survie globale (OS) dépassait à peine 20 mois en 2001, elle était de plus de 40 mois en 2019, avec une survie à 8 ans de 37% [1]. L’introduction du traitement ciblé sur HER2 avec le trastuzumab, le pertuzumab et le trastuzumab emtansine (T-DM1) a certainement joué un rôle déterminant dans cette évolution. Mais selon Nancy Lin, une meilleure sélection des patients et une détection plus précoce sont également des facteurs importants qui ont contribué à l’amélioration du pronostic.
Développement actuel : révolution dans la troisième et la quatrième ligne
Outre le trastuzumab, le pertuzumab et le T-DM1, d’autres agents innovants ciblant HER2 ont été introduits récemment et sont actuellement utilisés principalement dans les traitements de troisième et quatrième ligne. Ainsi, au cours des deux dernières années, un standard thérapeutique a également pu être établi pour les patientes dont la maladie a progressé (aperçu 1).

Là où en 2018, après l’échec du traitement T-DM1, différentes combinaisons de trastuzumab ou de chimiothérapie au lapatinib étaient encore utilisées – souvent au petit bonheur la chance -, il existe aujourd’hui des options plus prometteuses. En fonction de l’atteinte intracrânienne, des comorbidités et des préférences, on applique d’abord soit le trastuzumab-deruxtecan, soit le tucatinib. Après le traitement de première ligne par trastuzumab/pertuzumab combiné à une chimiothérapie par taxane, le traitement de deuxième ligne par T-DM1 est donc poursuivi comme jusqu’à présent. Si celle-ci échoue, les nouvelles substances actives interviennent en alternance. Au final, le standard thérapeutique a pu être étendu de deux à quatre lignes au cours des deux dernières années – avec des effets durables sur le résultat clinique.
Au cœur de cette évolution positive se trouve la recherche sur le trastuzumab-deruxtecan et le tucatinib. Le trastuzumab-deruxtecan est un conjugué anti-body-drug (ADC) à trois composants. Un inhibiteur de la topoisomérase I extrêmement puissant, qui traverse la membrane, est couplé à un anticorps monoclonal ayant la même séquence d’acides aminés que le trastuzumab par l’intermédiaire d’une liaison clivable. La demi-vie du conjugué intact est de six jours. Les études cliniques ont montré jusqu’à présent un taux de réponse objective d’environ 60% chez les patientes prétraitées par le T-DM1, mais aucune étude randomisée n’a été réalisée à ce jour [2].
D’autre part, l’utilisation du tucatinib est examinée de près dans l’étude randomisée et contrôlée HER2CLIMB [3]. L’ajout de l’inhibiteur de tyrosine kinase HER2-sélectif au traitement par trastuzumab et capécitabine a permis d’augmenter la survie médiane sans progression de 5,6 à 7,8 mois et la survie globale médiane de 17,4 à 21,9 mois. Bien qu’il n’existe pas de données à long terme, ces premiers résultats sont prometteurs compte tenu du très mauvais pronostic après progression sous T-DM1.
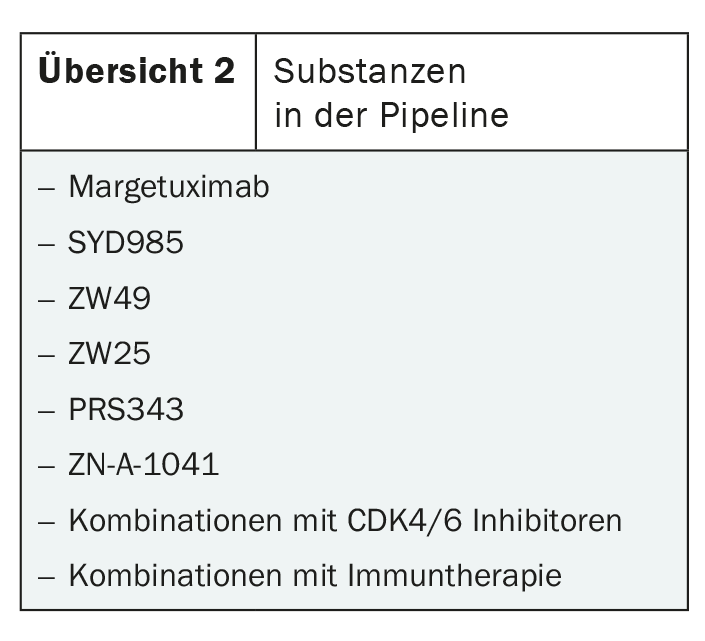
Outre le trastuzumab-deruxtecan et le tucatinib, de nombreuses autres substances sont dans le pipeline. Elles vont de la margetuximab, un anticorps monoclonal dirigé contre HER2, aux conjugués anticorps-toxine comme SYD985, en passant par des combinaisons avec l’immunothérapie ou des inhibiteurs de CDK4/6 (aperçu 2). Reste à savoir si ces approches façonneront à l’avenir le traitement du carcinome mammaire HER2-positif métastatique. En tout cas, ce n’est pas l’innovation qui manque.
Focus sur les métastases du SNC
Dans sa présentation, Nancy Lin a souligné à plusieurs reprises l’importance des métastases du SNC. En effet, même si le pronostic du cancer du sein métastatique HER2-positif s’est nettement amélioré, le nombre de métastases cérébrales ne diminue pas et n’a pas encore été réduit par les thérapies adjuvantes ciblées sur HER2. L’introduction du T-DM1 a certes permis de réduire le taux global de récidive, mais sans effet sur les récidives du SNC, qui représentent toujours une part importante des premières récidives [4]. Il est impressionnant de constater que le risque de métastases cérébrales augmente continuellement avec la durée de la maladie, apparemment sans atteindre un plateau. Ce fait souligne l’importance du développement d’options thérapeutiques et de mesures préventives.
Actuellement, le rôle des inhibiteurs de tyrosine kinase ciblant HER2, tels que le lapatinib et le neratinib, est particulièrement étudié dans le traitement des personnes atteintes de métastases du SNC. En combinaison avec la capécitabine, les taux de réponse du SNC varient entre 18 et 66%, selon le traitement antérieur, avec une prolongation de la survie sans progression (PFS) d’environ deux mois [5]. Le tucatinib semble apporter des avantages plus importants en termes de survie globale et de taux de récidive du SNC par rapport au lapatinib et au neratinib.
Ainsi, dans l’étude randomisée et contrôlée HER2CLIMB, la SSP du SNC des patientes présentant des métastases cérébrales actives était de 9,5 mois sous traitement par tucatinib, contre 4,1 mois dans le bras contrôle [6]. Selon Nancy Lin, les conjugués anti-body-drug, combinés de manière appropriée, pourraient également jouer un rôle à l’avenir dans le traitement du carcinome mammaire HER2-positif avec métastases du SNC, malgré leur taille. Ainsi, en 2020, des résultats correspondants à l’utilisation de l’ADC T-DM1 ont été publiés [7]. Le trastuzumab-deruxtecan pourrait également être utilisé dans ce cas, une approche actuellement à l’étude.
L’association de conjugués anti-body-drug et d’inhibiteurs de tyrosine kinase ciblant HER2 est potentiellement prometteuse. Jusqu’à présent, il s’agissait de musique d’avenir, mais deux études sont en cours pour tester cette idée de base. Alors que l’étude HER2CLIMB examine la combinaison de T-DM1 et de tucatinib, l’étude TBCRC 022 s’intéresse à la combinaison de T-DM1 et de nératinib.
Double blocage de HER2 ?
Outre les métastases du SNC, le choix de la séquence thérapeutique optimale représente également un défi majeur, notamment avec le développement continu de nouvelles molécules et donc d’un plus grand choix de substances. Lors du San Antonio Breast Cancer Symposium , Nancy Lin a surtout évoqué la pertinence d’un double blocage de HER2 après la progression de la maladie. Elle a souligné que, par exemple, l’association du trastuzumab et de l’ITK lapatinib pouvait apporter des avantages cliniques. La poursuite du traitement par trastuzumab/pertuzumab parallèlement au traitement par ITK serait supérieure au traitement par ITK seul.
Même si les choses sont de plus en plus claires sur ce point, de nombreuses autres questions restent en suspens. Ainsi, on manque de données claires sur l’utilisation séquentielle de différents inhibiteurs de tyrosine kinase, y compris en ce qui concerne les résistances croisées potentielles.
Musique d’avenir : arrêt des thérapies et approches curatives
Avec l’augmentation du nombre de survivants à long terme, la question se pose de savoir si et quand le traitement oncologique peut être arrêté en cours de route. Ou de manière plus provocante : Une partie des patientes est-elle guérie ? Dans l’analyse à long terme de l’étude CLEOPATRA, un quart des participantes n’avaient toujours pas rechuté après huit ans de traitement de première ligne [1]. Afin de réduire au maximum les risques liés à l’arrêt du traitement, il n’existe pas encore de marqueurs appropriés de la réapparition de l’activité de la maladie dans le cas du cancer du sein HER2+, à l’instar de la maladie résiduelle minimale dans le cas de la leucémie. Un tel paramètre est actuellement recherché et pourrait, selon Lin, ouvrir la voie à une vie sans traitement pour les personnes concernées dans un avenir proche [8].
Une approche curative primaire est également possible en raison des progrès actuels, a déclaré l’experte. Une guérison serait particulièrement réaliste dans les cas de carcinomes mammaires HER2-positifs métastasés non traités, appelés cas de novo. Celle-ci serait donc envisageable pour 40% des patientes atteintes d’un cancer du sein métastatique HER2-positif. Par exemple, le traitement séquentiel par THP (docétaxel, trastuzumab et pertuzumab) suivi de TDM-1/Tucatinib, trastuzumab-Deruxtecan, méthodes locales et traitement d’entretien par HP (trastuzumab et pertuzumab) et tucatinib pendant un an représente une possibilité.
Même s’il reste encore un long chemin à parcourir avant d’arriver à la cure et à l’arrêt des traitements, les développements rapides de ces dernières années les ont mis à portée de main. Lin a même prédit des changements fondamentaux dans le traitement du cancer du sein métastatique HER2-positif au cours de la prochaine décennie et a qualifié les recherches actuelles de pionnières en conclusion de son exposé. Nous restons à l’écoute.
Source : San Antonio Breast Cancer Symposium 8-11.12.2020, ES7 Educational Session “Treatment of HER2-positive metastatic breast cancer – advances and challenges”, Nancy Lin (Dana-Faber Cancer Institute Harvard Medical School)
Littérature :
- Swain SM, et al : Pertuzumab, trastuzumab, et docetaxel pour le cancer du sein métastatique HER2-positif (CLEOPATRA) : résultats de fin d’étude d’une étude de phase 3, randomisée, en double aveugle et contrôlée par placebo. Lancet Oncol 2020 ; 21(4) : 519-530.
- Modi S, et al : Trastuzumab Deruxtecan in Previously Treated HER2-Positive Breast Cancer. N Engl J Med 2020 ; 382(7) : 610-621.
- Murthy RK, et al : Tucatinib, Trastuzumab, et Capecitabine pour le cancer du sein métastatique HER2-Positive. N Engl J Med 2020 ; 382(7) : 597-609.
- von Minckwitz G, et al : Trastuzumab Emtansine for Residual Invasive HER2-Positive Breast Cancer. N Engl J Med 2019 ; 380(7) : 617-628.
- Freedman RA, et al : TBCRC 022 : Un essai de phase II de nératinib et de capécitabine pour les patients atteints de cancer du sein positif au récepteur du facteur de croissance épidermique humain 2 et de métastases cérébrales. J Clin Oncol 2019 ; 37(13) : 1081-1089.
- Lin NU, et al : Efficacité intracrânienne et survie avec le tucatinib plus le trastuzumab et la capécitabine pour les cancers du sein HER2-positifs précédemment traités avec des métastases cérébrales dans l’essai HER2CLIMB. J Clin Oncol 2020 ; 38(23) : 2610-2619.
- Montemurro F, et al : Trastuzumab emtansine (T-DM1) chez les patients atteints de cancer du sein métastatique HER2-positif et de métastases cérébrales : analyse finale exploratoire de la cohorte 1 de KAMILLA, un essai clinique de phase IIIb à un seul bras. Ann Oncol 2020 ; 31(10) : 1350-1358.
- Parsons HA, et al : Détection sensible de la maladie résiduelle minimale chez les patients traités pour un cancer du sein de stade précoce. Clin Cancer Res 2020 ; 26(11) : 2556-2564.
InFo ONKOLOGIE & HÄMATOLOGIE 2021 ; 9(1) : 26-27 (publié le 21.2.21, ahead of print)