L’obiettivo dell’intervento chirurgico per il tumore al pancreas è quello di rimuovere il tumore nel tessuto sano, con la migliore distanza di sicurezza possibile tra il margine del tumore e le superfici di resezione. I tumori resecabili hanno un’aspettativa di vita più lunga. I carcinomi pancreatici borderline resecabili sono definiti in base al grado di infiltrazione degli organi vicini. Nella nuova linea guida S3, il margine di incisione nella valutazione istopatologica è descritto in modo più dettagliato rispetto al passato. Si deve dedurre una prognosi sfavorevole se il rapporto tra i linfonodi colpiti e quelli liberi da tumore (rapporto linfonodale) è ≥0,2. Le terapie neoadiuvanti sembrano essere un’opzione molto promettente.
Con l’8%, il tasso di sopravvivenza a 5 anni del cancro al pancreas è ancora il più basso di tutti i tumori maligni a livello mondiale. Tuttavia, il trattamento chirurgico è ancora di importanza centrale, in quanto è l’unica procedura potenzialmente curativa [1]. La diagnostica pre-campo è completa e comprende i seguenti esami, oltre alle indagini di base:
- Laboratorio di routine
- Marcatori tumorali CA 19-9 e CEA
- HbA1c
- Diagnostica funzionale con elastasi fecale e test tensore del glucosio orale
- Radiografia del torace
- Sonografia
- Strato sottile rinforzato con mezzo di contrasto
- TAC addome
- Colangiopancreaticografia a risonanza magnetica (MRCP)
- Esofago-gastro-duodenoscopia
- Endosonografia
- Colangiopancreaticografia retrograda endoscopica (ERCP) con tentativo di prelievo di campioni o posizionamento di stent nell’ittero grave.
In casi selezionati, dovrebbe essere discussa la laparoscopia di stadiazione: Se la diagnostica per immagini non mostra risultati chiari riguardo alle metastasi nel peritoneo e/o nel fegato, ma la metastasi è probabile a causa di un valore elevato di CA 19-9 >1000 U/ml, o se il precedente tentativo endosonografico di conferma bioptica della malignità non ha avuto successo [2].
La terapia neoadiuvante può consentire la probabilità di resezione a seconda del grado di risposta e rendere possibile una successiva resezione del tumore. I tumori che non sono ragionevolmente resecabili devono essere trattati con la chemioterapia attraverso una porta i.v. precedentemente impiantata, con intento palliativo, secondo l’attuale linea guida S3.
Principi dell’operazione
L’obiettivo dell’intervento è rimuovere il tumore nel tessuto sano con la migliore distanza di sicurezza possibile tra il margine del tumore e le superfici di resezione (situazione R0) [3,4]. La procedura standard per un tumore resecabile della testa del pancreas (incluso il processus uncinatus) è la pancreaticoduodenectomia parziale, come una cosiddetta operazione di Whipple classica o che preserva il piloro, con la corrispondente dissezione linfonodale (Fig. 1) [5].
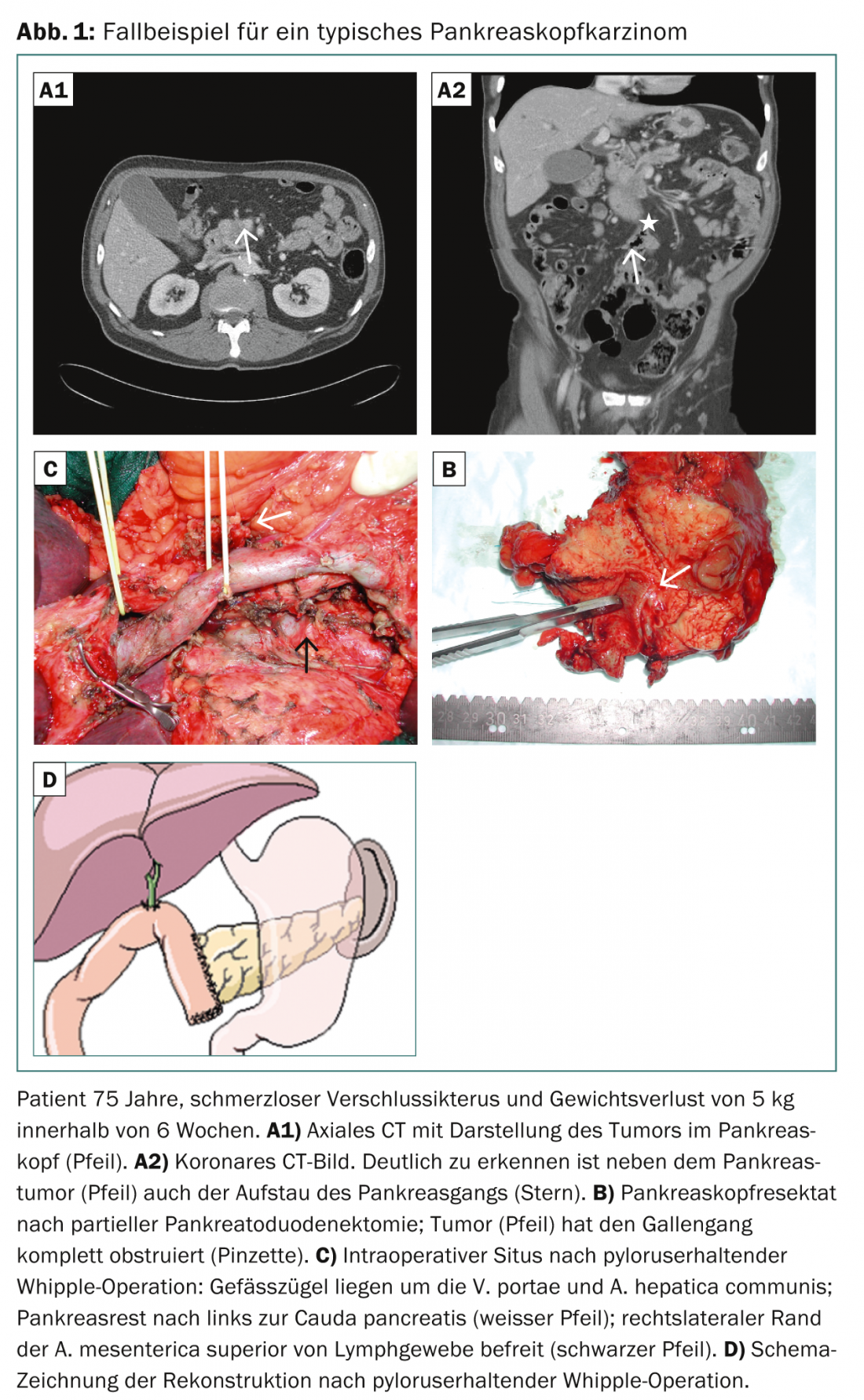
Il livello di dissezione dei linfonodi comprende i linfonodi peripancreatici e periduodenali, i linfonodi situati sul lato destro dell’arteria mesenterica inferiore e i linfonodi nel legamento epatoduodenale. La linfoadenectomia radicale estesa (interaortocavale, arteria mesenterica superiore sinistra) non migliora la prognosi ed è piuttosto controindicata a causa dell’elevata morbilità postoperatoria aggiuntiva con fistola del colon e diarrea massiva [6]. Se il tumore si trova sul lato sinistro della vena mesenterica superiore (corpo o coda pancreatica), si esegue la resezione sinistra con splenectomia e la corrispondente dissezione linfonodale locale.
Se solo intraoperatoriamente risulta evidente l’esistenza di metastasi a distanza (peritoneo/fegato) o che il tumore non può essere resecato localmente in modo significativo, si deve procedere con la chirurgia palliativa. Se la conferma istologica non è ancora possibile, il tumore viene sottoposto a biopsia per confermare la diagnosi in modo tale che vi sia solo una bassa probabilità di morbilità per quanto riguarda una fistola pancreatica (ad esempio, transduodenale o attraverso il dotto biliare). La protezione del carcinoma chiaro è una conditio sine qua non per la successiva chemioterapia palliativa o neoadiuvante. Le resezioni delle metastasi epatiche di solito non sono utili.
In caso di colestasi, viene creata un’anastomosi biliodigestiva e lo stent del dotto biliare viene rimosso intraoperatoriamente. In questa situazione, di solito è consigliabile creare una gastroenterostomia transmesocolica aggiuntiva anche in assenza di stenosi duodenale esistente. La combinazione di entrambe le procedure è la ricostruzione a doppio bypass.
La resecabilità chirurgica determina la prognosi
Nonostante l’alta qualità delle moderne tecniche di imaging, la resecabilità di un tumore pancreatico può essere valutata solo dal chirurgo viscerale. L’esperienza del chirurgo e del centro giocano un ruolo centrale in questo caso. I pazienti dovrebbero quindi essere presentati in centri con un numero elevato di casi, in modo da poter valutare la resecabilità locoregionale. I tumori resecabili hanno un’aspettativa di vita più lunga. Oggi si possono raggiungere tassi di sopravvivenza a 5 anni del 24-36% dopo la resezione oncologica con chemioterapia adiuvante. L’infiltrazione degli organi vicini non esclude necessariamente la resezione R0. La resezione estesa (en bloc) necessaria per questo promette una prognosi paragonabile a quella della chirurgia standard e dovrebbe essere eseguita nei centri pancreatici [7].
L’NCCN (National Comprehensive Cancer Network) definisce i carcinomi pancreatici borderline resecabili in base all’estensione dell’infiltrazione degli organi vicini (Tab. 1) . Una “muratura” dell’arteria mesenterica superiore o del tronco celiaco superiore a 180° non è considerata ragionevolmente resecabile, ma ad oggi, secondo il consenso degli esperti, non è una controindicazione assoluta alla resezione. Tuttavia, bisogna essere consapevoli che i tassi di morbilità e letalità perioperatoria aumentano [8]. Al contrario, l’infiltrazione della vena porta, della vena mesenterica superiore e della vena lienale non sono controindicazioni assolute. Le resezioni in blocco del pancreas e dei segmenti venosi portali hanno un tasso di complicanze paragonabile alle operazioni senza infiltrazioni dei vasi venosi portali [3,9]. I dati a lungo termine di alcuni studi mostrano prognosi paragonabili agli interventi senza resezioni venose parziali. L’infiltrazione della vena porta superiore a 2 cm, invece, è considerata critica ed è un fattore prognostico negativo [10].

Indicazioni per l’inserimento di uno stent del dotto biliare
I tumori dell’area della testa del pancreas sono solitamente caratterizzati da un ittero indolore e richiedono un ERCP. Tuttavia, l’inserimento di uno stent del dotto biliare porta molto spesso alla colonizzazione batterica della bile (circa il 73%) e alla colangite consecutiva, che aumenta ulteriormente la morbilità nelle resezioni pancreatiche [11]. L’indicazione per il posizionamento dello stent deve quindi essere fatta in consultazione con i chirurghi viscerali e deve essere rigorosa. Tuttavia, se l’intervento chirurgico non può essere eseguito tempestivamente in caso di rapido aumento dell’ittero (oltre dieci volte la norma), l’indicazione allo stenting è indispensabile (criteri di “buona pratica clinica”, GCP).
Ritrattamento istopatologico standardizzato
La distanza minima dai confini della sezione è stata oggetto di molte controversie nel recente passato, dopo la ridefinizione ‘arbitraria’ della classificazione R da parte del ‘Royal College of Pathologists’ (RCP). L’RCP postula già una situazione R1 se sono presenti cellule tumorali <1 mm al margine di resezione, ma non sono rilevabili cellule tumorali nel sito di incisione. Nella nuova linea guida S3, si è quindi deciso di descrivere più dettagliatamente il margine di incisione circonferenziale (ventrale, mediale e posteriore) nella valutazione istopatologica (concetto di CRM basato sulla valutazione istologica dei carcinomi colorettali):
- Le resezioni R0 sono descritte come CRM-negative (R0-wide) se le cellule tumorali sono >1 mm dal margine di resezione.
- Le resezioni R0 sono descritte come CRM-positive (R0-stretto) se la distanza delle cellule maligne dalla superficie di taglio è <1 mm (Fig. 2).
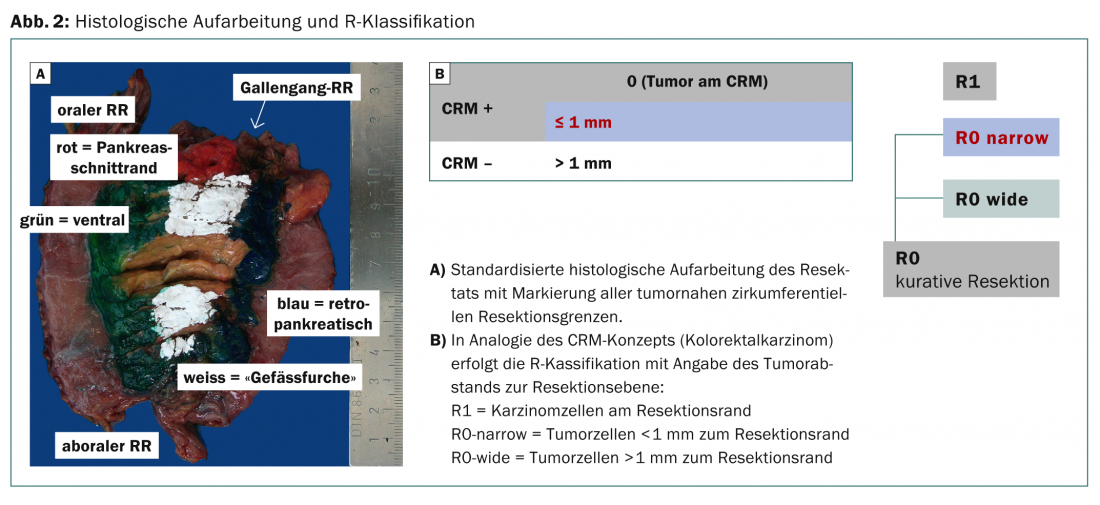
Studi recenti dimostrano che l’assenza di cellule tumorali sul bordo dell’incisione è il criterio decisivo (corrisponde alla precedente definizione R secondo l’UICC) [12]. L’obiettivo del nuovo work-up istologico standardizzato è quello di ottenere dati migliori per stimare la prognosi e la probabilità di recidiva in futuro.
Il rapporto linfonodale è un fattore prognostico
Nella nuova linea guida S3 sul cancro al pancreas, oltre al work-up istologico standardizzato, è richiesta una linfoadenectomia di almeno dieci linfonodi locoregionali. Questi vengono elaborati in modo da poter indicare il rapporto linfonodale, cioè il rapporto tra linfonodi colpiti e non colpiti (raccomandazione GCP). Si deve dedurre una prognosi sfavorevole se il rapporto tra linfonodi colpiti e linfonodi liberi da tumore è ≥ 0,2 [13].
Nessuna resezione per metastasi a distanza
Se le metastasi a distanza sono già state rilevate prima dell’intervento, di solito il trattamento chirurgico non è consigliabile. Queste includono metastasi d’organo, ad esempio nel fegato e nei polmoni, carcinomatosi peritoneale con ascite o metastasi linfonodali al di fuori delle aree locoregionali (considerate metastasi a distanza). Se le metastasi a distanza precedentemente sconosciute vengono scoperte intraoperatoriamente, la resezione comporta un aumento della morbilità perioperatoria e non comporta alcun beneficio in termini di sopravvivenza. Tuttavia, sono disponibili solo pochi dati in letteratura su questo sito [14].
Terapia neoadiuvante per il cancro al pancreas
I dati degli studi sui concetti di terapia neoadiuvante nei pazienti con tumori resecabili o borderline resecabili (chemioradioterapia o chemioterapia seguita da radioterapia) sono finora insufficienti, ma le terapie neoadiuvanti sembrano essere un’opzione molto promettente [15,16]. In singoli studi unicentrici, è stato possibile ottenere la resecabilità secondaria e migliorare la prognosi dei pazienti affetti. In particolare, sono ora disponibili regimi di chemioterapia intensificata più performanti (FOLFIRINOX e gemcitabina/abraxane), che per la prima volta consentono una regressione tumorale significativa.
Anche se finora non sono stati pubblicati studi controllati e randomizzati, i concetti di terapia neoadiuvante potrebbero diventare consolidati [17]. Ad esempio, i pazienti sono attualmente reclutati in cinque diversi studi che stanno valutando il valore del trattamento neoadiuvante anche nei pazienti classificati come resecabili e borderline resecabili o borderline resecabili. studiare i tumori pancreatici localmente avanzati. L’obiettivo è quello di ottenere un maggior numero di resezioni tumorali R0 con intento curativo, per migliorare la sopravvivenza a lungo termine dei pazienti con tumore al pancreas.
Letteratura:
- Seufferlein T, et al.: Dtsch Arztebl Int 2014; 111: 396-402.
- Doi R, et al: Surg Today 2008; 38: 1021-1028.
- Wagner M, et al: Br J Surg 2004; 91: 586-594.
- Hartwig W, et al: Ann Surg 2011; 254: 311-319.
- Chromik AM, et al: Oncologist 2012; 18: 269-282.
- Kahlert C, et al: Chirurg 2008; 79: 1115-1122.
- Nikfarjam M, et al: J Gastrointest Surg 2009; 13: 915-921.
- Yamada S, et al: Pancreas 2009; 38: e13-17.
- Bachellier P, et al: Am J Surg 2001; 182: 120-129.
- Ouaissi M, et al: World J Surg 2010; 34: 2648-2661.
- van der Gaag NA, et al: N Engl J Med 2010; 362: 129-137.
- Janot MS, et al: Arch Surg 2012 di Langenbeck; 397: 917-925.
- Michalski CW, et al: Br J Surg 2007; 94: 265-273.
- Gleisner AL, et al: Cancer 2007; 110: 2484-2492.
- Chen KT, et al: Ann Surg Oncol 2014; 21: 662-669.
- Rose JB, et al: Ann Surg Oncol 2014; 21: 1530-1537.
- Hammel P, et al: Risultati finali dello studio internazionale LAP 07 di fase III. Abstracts delle riunioni ASCT 2013; 31: LBA4003.
InFo ONCOLOGIA & EMATOLOGIA 2014; 2(7): 10-13