In ottobre, si è svolto a Basilea il congresso annuale delle Società tedesca, austriaca e svizzera di ematologia e oncologia medica. Un simposio scientifico incentrato sulla gestione del rischio e dell’età nel mieloma multiplo. I pazienti affetti da mieloma di età superiore ai 75 anni possono beneficiare di un trattamento adattato e meno tossico, in quanto si verificano meno effetti collaterali e la terapia deve essere interrotta meno spesso a causa degli effetti avversi.
La diagnosi e il trattamento del mieloma multiplo (MM) sono cambiati molto negli ultimi anni. La valutazione del rischio individuale del paziente sta diventando sempre più importante. Pertanto, il Dr. med. Marc Raab, Ospedale Universitario di Heidelberg (D), ha posto la domanda nella sua conferenza: Quale terapia è giusta: adattata al rischio, orientata alla MRD o “taglia unica”?
Le comorbidità influenzano la scelta degli agenti terapeutici
Il trattamento sempre più personalizzato del MM si basa sulla comprensione di come i fattori specifici del paziente, della malattia e del trattamento influenzino i tassi di sopravvivenza e la qualità della vita. L’età è stata a lungo considerata il parametro più importante e unico per valutare la trapiantabilità. Oggi, tuttavia, sappiamo che la sola età (fino a circa 75 anni) non è un motivo per non sottoporsi a un trapianto di cellule staminali. Importanti per valutare la capacità del paziente di seguire la terapia sono anche le comorbidità, la citogenetica e la conoscenza delle tossicità specifiche dei farmaci.
L’insufficienza renale è una comorbidità significativa e associata negativamente alla prognosi. Il 30% di tutti i pazienti con MM sono colpiti nel corso della malattia, e il 10% richiede addirittura l’emodialisi. Il farmaco di scelta per questi pazienti è il bortezomib.
Anche le tossicità influiscono sulla scelta dell’agente; per esempio, si consiglia cautela nell’uso di antracicline o carfilzomib in pazienti con malattie cardiache, o di agenti che causano neuropatia in pazienti con diabete mellito.
Negli ultimi anni, si è appreso di più sull’eterogeneità genetica e clinica della malattia di MM. Le attuali linee guida riconoscono il valore di un approccio adattato al rischio, basato, tra l’altro, sulle analisi FISH. I diversi sottotipi di MM rispondono in modo diverso alle diverse classi di farmaci. I pazienti con del(17p) e/o t(4;14) e/o +1q21 hanno una prognosi piuttosto sfavorevole. I pazienti con un t(4;14)-MM rispondono bene al bortezomib e nei pazienti con una delezione 17p, la chemioterapia convenzionale ha un effetto limitato.
Che ruolo ha la “malattia minima residua” (MRD)?
Con la terapia di prima linea, la remissione può essere raggiunta in quasi tutti i pazienti. Tuttavia, la “malattia minima residua” (MRD) rimane un problema. Per la loro diagnosi sono disponibili diversi metodi, tutti con vantaggi e svantaggi. Il metodo meglio documentato e più rapido (risultato disponibile il giorno successivo) è la citometria a flusso, mentre la diagnostica genetica richiede più tempo. La MRD ha un alto significato prognostico, quindi un obiettivo terapeutico importante è quello di rendere il maggior numero possibile di pazienti privi di MRD. Tuttavia, ci sono molte domande senza risposta riguardo alla MRD:
- Quale tecnica deve essere utilizzata per diagnosticarla (affidabilità, disponibilità)?
- Quando deve essere fatta la diagnosi?
- Quali sono le conseguenze di quale stato MRD?
Il relatore era dell’opinione che la valutazione della MRD non è ancora adatta all’uso clinico quotidiano, ma che dovrebbe essere effettuata negli studi clinici. Questi potrebbero rispondere a una serie di domande, ad esempio se la terapia di mantenimento debba essere modificata a causa della MRD o se la MRD possa svolgere un ruolo nell’approvazione di nuovi farmaci.
Trapianto di cellule staminali per la recidiva di MM
All’inizio della sua conferenza, il Prof. Dr. med. Nicolaus Kröger, Ospedale Universitario di Amburgo-Eppendorf (D), ha definito il trapianto di cellule staminali di salvataggio (STX): un STX autologo o allogenico in pazienti in cui la terapia precedente ha fallito. Questo include i pazienti che si sono già sottoposti a STX, ma anche i pazienti senza STX precedente. L’STX di recupero è diventato sempre più comune in Europa dal 2006. Il condizionamento viene quasi sempre effettuato con il melfalan.
Studi retrospettivi mostrano che i seguenti fattori hanno un’influenza favorevole sull’esito della STX di salvataggio autologa: remissione più lunga dopo la prima STX, età più giovane del paziente, bassi livelli di beta2-microglobulina e un minor numero di terapie di salvataggio prima della STX di salvataggio.
In uno studio prospettico di Cook et al. I pazienti con recidiva di MM sono stati trattati con STX di salvataggio autologo o convenzionalmente con ciclofosfamide [1]. La sopravvivenza complessiva è stata la stessa in entrambi i gruppi, ma il tempo alla progressione (PFS) è stato significativamente più lungo nel gruppo di pazienti con STX (19 contro 11 mesi).
Le linee guida attuali (2015) per la STX di salvataggio includono i seguenti principi [2]:
- Nei pazienti eleggibili al trapianto con una recidiva dopo una terapia primaria che non consisteva nella STX autologa, la STX autologa come parte della terapia di salvataggio deve essere considerata standard.
- La STX autologa di salvataggio è una terapia appropriata per i pazienti con recidiva in cui la remissione è durata più di 18 mesi dopo la prima STX autologa.
- La STX autologa di salvataggio può essere utilizzata come terapia ponte fino alla STX allogenica.
Attualmente, la STX di salvataggio autologa precoce per la recidiva è in fase di studio nello studio prospettico GMMG. Un’altra area di ricerca riguarda le strategie per affrontare la MRD dopo il trapianto. Esistono diverse strategie per questo, ad esempio l’immunoterapia o la vaccinazione. Ci sono ancora pochi dati che confrontano la STX di salvataggio autologa e allogenica. Questi dati sono più a favore della STX autologa, ma si tratta di dati retrospettivi di pazienti selezionati. La conclusione del relatore:
- Sia la STX autologa che quella allogenica come terapia di salvataggio nei pazienti con recidiva di MM sono opzioni di trattamento efficaci e sempre più utilizzate.
- Una remissione più lunga dopo la prima STX è un fattore prognostico positivo per la seconda STX.
- La terapia di mantenimento dopo la STX deve essere ulteriormente studiata.
- Con la STX allogenica, il rischio di recidiva di MM è più basso, ma la mortalità indipendente dalla recidiva è più alta rispetto alla STX autologa.
- Attualmente si stanno studiando nuovi regimi di trattamento con tossicità attenuata.
Pazienti anziani con MM: determinare la fragilità
Il MM è prevalentemente una malattia delle persone anziane: Oltre il 60% delle diagnosi e circa il 75% dei decessi a causa del MM colpiscono persone di età superiore ai 65 anni, come ha spiegato la PD Dr. med. Katja Christina Weisel, Ospedale Universitario di Tubinga (D), nella sua conferenza. Negli ultimi anni, la prognosi del MM è migliorata in modo significativo grazie alle nuove opzioni terapeutiche. In una coorte di pazienti diagnosticati nel 2001-2005, la sopravvivenza mediana è stata di 4,6 anni, e nella coorte diagnosticata dal 2006 al 2010, era già di 6,1 anni. I pazienti di età superiore ai 70 anni beneficiano meno di questi progressi rispetto a quelli più giovani, ma diversi studi hanno dimostrato che le nuove sostanze migliorano significativamente la sopravvivenza anche nei pazienti con MM di età superiore ai 75 anni. Le tossicità sono particolarmente importanti in questo gruppo di pazienti, perché le tossicità ematologiche di grado 3-4 e le interruzioni della terapia a causa degli effetti collaterali riducono il tasso di sopravvivenza. Nei pazienti anziani, le terapie dovrebbero quindi essere ben tollerate.
Tuttavia, i pazienti anziani costituiscono un gruppo molto eterogeneo: alcuni sono ancora molto in forma, altri fragili. Nelle persone fragili, la resistenza ai fattori di stress – come il cancro e la sua terapia – è ridotta. Ma come valutare la fragilità di un paziente? In uno studio pubblicato di recente, Palumbo et al. uno strumento di valutazione in grado di calcolare la probabilità di tossicità e di sopravvivenza nei pazienti anziani con MM di nuova diagnosi, in base a fattori come l’età, lo stato funzionale e le comorbilità [3]. Dal 1° ottobre 2015, questo strumento di calcolo è disponibile online all’indirizzo www.myelomafrailtyscorecalcu lator.net.
Regimi doppi nei pazienti di età superiore a 75 anni
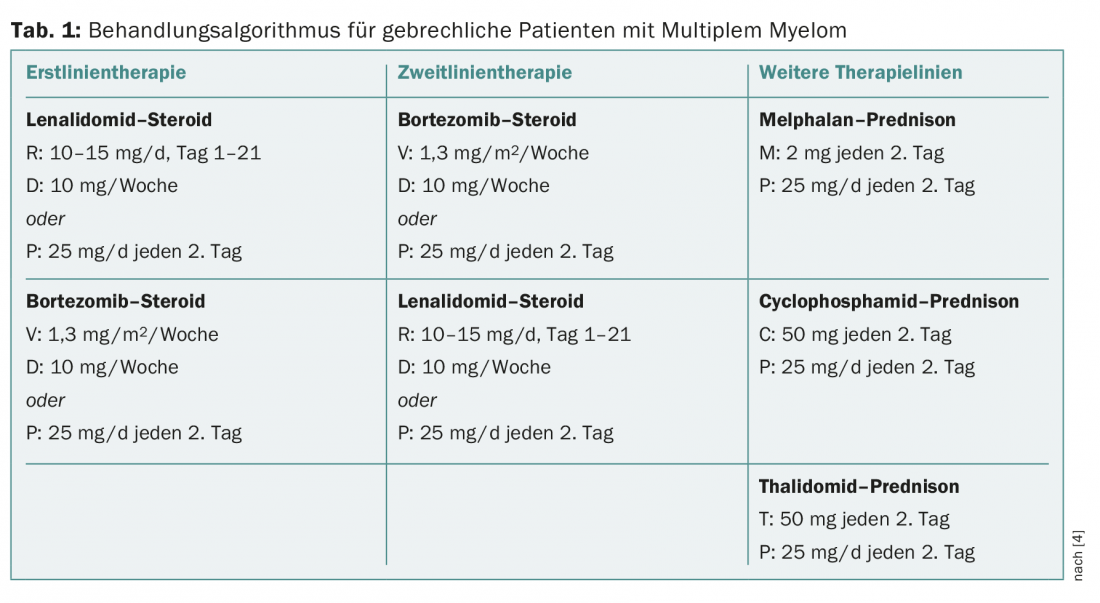
La terapia standard per il MM di nuova diagnosi è solitamente una tripla combinazione. Tuttavia, nei pazienti di età superiore ai 75 anni, questi regimi causano un alto tasso di effetti collaterali. Studi recenti dimostrano che un regime a due farmaci nei pazienti di età superiore ai 75 anni riduce il tasso di effetti collaterali e migliora la sopravvivenza. Nei pazienti fragili, si raccomanda di somministrare il bortezomib solo una volta alla settimana: Il tasso di sopravvivenza non diminuisce, le polineuropatie sono significativamente meno numerose e le interruzioni della terapia sono meno frequenti. Lo studio FIRST ha dimostrato che è anche possibile dimezzare la dose di desametasone nei pazienti di età superiore ai 75 anni, senza ridurre le possibilità di sopravvivenza. Il relatore ha formulato le seguenti raccomandazioni per la terapia dei pazienti con MM di età superiore ai 75 anni (Tab. 1):
- Dosare lenalidomide con maggiore attenzione;
- Dosare completamente il bortezomib, ma somministrarlo solo una volta alla settimana;
- Dimezzi la dose di desametasone.
Fonte: Riunione annuale delle Società tedesca, austriaca e svizzera di ematologia e oncologia medica, 9-13 ottobre 2015, Basilea.
Letteratura:
- Cook G, et al.: Chemioterapia ad alto dosaggio più trapianto di cellule staminali autologhe come terapia di consolidamento nei pazienti con mieloma multiplo recidivato dopo un precedente trapianto di cellule staminali autologhe (NCRI Myeloma X Relapse [Intensive trial]): studio randomizzato, in aperto, di fase 3. Lancet Oncol 2014 Jul; 15(8): 874-885.
- Giralt S, et al: Società Americana di Trapianto di Sangue e Midollo, Società Europea di Trapianto di Sangue e Midollo, Rete di Studi Clinici sul Trapianto di Sangue e Midollo e Gruppo di Lavoro Internazionale sul Mieloma Conferenza di Consenso sul Trapianto di Cellule Ematopoietiche di Salvataggio in Pazienti con Mieloma Multiplo Recidivato. Biol Blood Marrow Transplant 2015 Sep 30. pii: S1083-8791(15)00641-2. doi: 10.1016/j.bbmt.2015.09.016.
- Palumbo A, et al: La valutazione geriatrica predice la sopravvivenza e le tossicità nei pazienti anziani con mieloma: un rapporto dell’International Myeloma Working Group. Sangue 2015; 125(13): 2068-2074.
- Larocca A, Palumbo A: Come tratto i pazienti con mieloma fragile. Blood 2015 Aug 31. pii: blood-2015-05-612960.
InFo ONCOLOGIA & EMATOLOGIA 2015; 3(11-12): 28-31