L’insufficienza cardiaca è il motivo più comune di ricovero in ospedale nelle persone di età superiore ai 65 anni. Chiarire la causa della malattia è essenziale per fornire ai pazienti una terapia mirata. I pazienti con amiloidosi ATTR cardiaca sono un importante sottogruppo HFpEF per il quale esiste un’opzione terapeutica specifica che ha dimostrato di migliorare la prognosi.
Se si sospetta un’insufficienza cardiaca (HF), è necessario ottenere il parametro NT-proBNP e/o eseguire un’ecocardiografia transtoracica. Quest’ultima è la procedura di imaging centrale nella diagnosi di HF. Nei pazienti con sintomi tipici e livelli elevati di NTproBNP (≥125 pg/ml), è probabile la presenza di insufficienza cardiaca [1]. L’ecocardiografia può già fornire indicazioni iniziali sulle possibili cause di insufficienza cardiaca (ad esempio, disturbi del movimento della parete, viziatura delle valvole, processi infiltrativi, cardiomiopatie, disfunzione diastolica) [1]. Metodi più avanzati per determinare la causa dell’HF includono la risonanza magnetica cardiaca (cardiomiopatia ischemica, amiloidosi, miocardite) o la scintigrafia (malattia coronarica, amiloidosi ATTRwt) [2].
La classificazione classica dell’insufficienza cardiaca si basa sui risultati della frazione di eiezione ventricolare sinistra in HFrEF (HF con frazione di eiezione ridotta, <40%); HFmrEF (HF con frazione di eiezione moderatamente ridotta, 40-49%) e HFpEF (HF con frazione di eiezione conservata, ≥50%).
Criteri diagnostici di HFpEF secondo la linea guida ESC attuale
Secondo la linea guida ESC sulla gestione dell’insufficienza cardiaca, aggiornata nel 2021, i tre criteri essenziali per l’HFpEF sono [3]:
- Sintomi e segni di insufficienza cardiaca
- LVEF ≥50%
- Evidenza oggettiva di anomalie cardiache strutturali e/o funzionali coerenti con la disfunzione diastolica del ventricolo sinistro e pressioni di riempimento LV elevate, compresi i peptidi natriuretici elevati.
I pazienti con HFpEF sono in media più anziani e più spesso di sesso femminile rispetto a chi soffre di HFrEF e HFmrEF. L’HFpEF è anche associata alla fibrillazione atriale, alla malattia renale cronica (CKD) e ad altre comorbidità non cardiovascolari [4]. Chiarire l’eziologia sottostante è molto importante nell’HFpEF per iniziare un trattamento farmacologico mirato (Fig. 1) .
Identificare e trattare i pazienti con ATTR-CM
Uno studio prospettico su 120 soggetti ha mostrato che il 13% dei pazienti di età superiore ai 60 anni ricoverati per insufficienza cardiaca con frazione di eiezione preservata (HFpEF) aveva l’amiloidosi ATTR (wtATTR-KM) come malattia di base [5]. L’amiloidosi cardiaca da transtiretina (ATTR-CM) comporta il deposito di transtiretina mal ripiegata. Si distingue tra la variante sporadica di tipo selvatico (wtATTR) e la forma mutata ereditaria (mATTR). L’ATTR-CM può essere controllata attraverso la diagnostica per immagini (risonanza magnetica cardiaca o scintigrafia) e l’immunofissazione con determinazione delle catene leggere libere; per la diagnosi definitiva, è necessario eseguire una biopsia e/o un test genetico [6]. Mentre la somministrazione di terapie farmacologiche classiche per l’insufficienza cardiaca, come gli ACE-inibitori, gli antagonisti del recettore dell’angiotensina-1 e i beta-bloccanti, ha mostrato un chiaro beneficio in termini di sopravvivenza nei pazienti con HFrEF, ciò non è avvenuto nei pazienti con HFpEF [7–9]. A causa dei rischi di effetti collaterali, occorre prestare attenzione all’uso di beta-bloccanti, inibitori del sistema renina-angiotensina-aldosterone e diuretici nei pazienti con ATTR-CM [6].
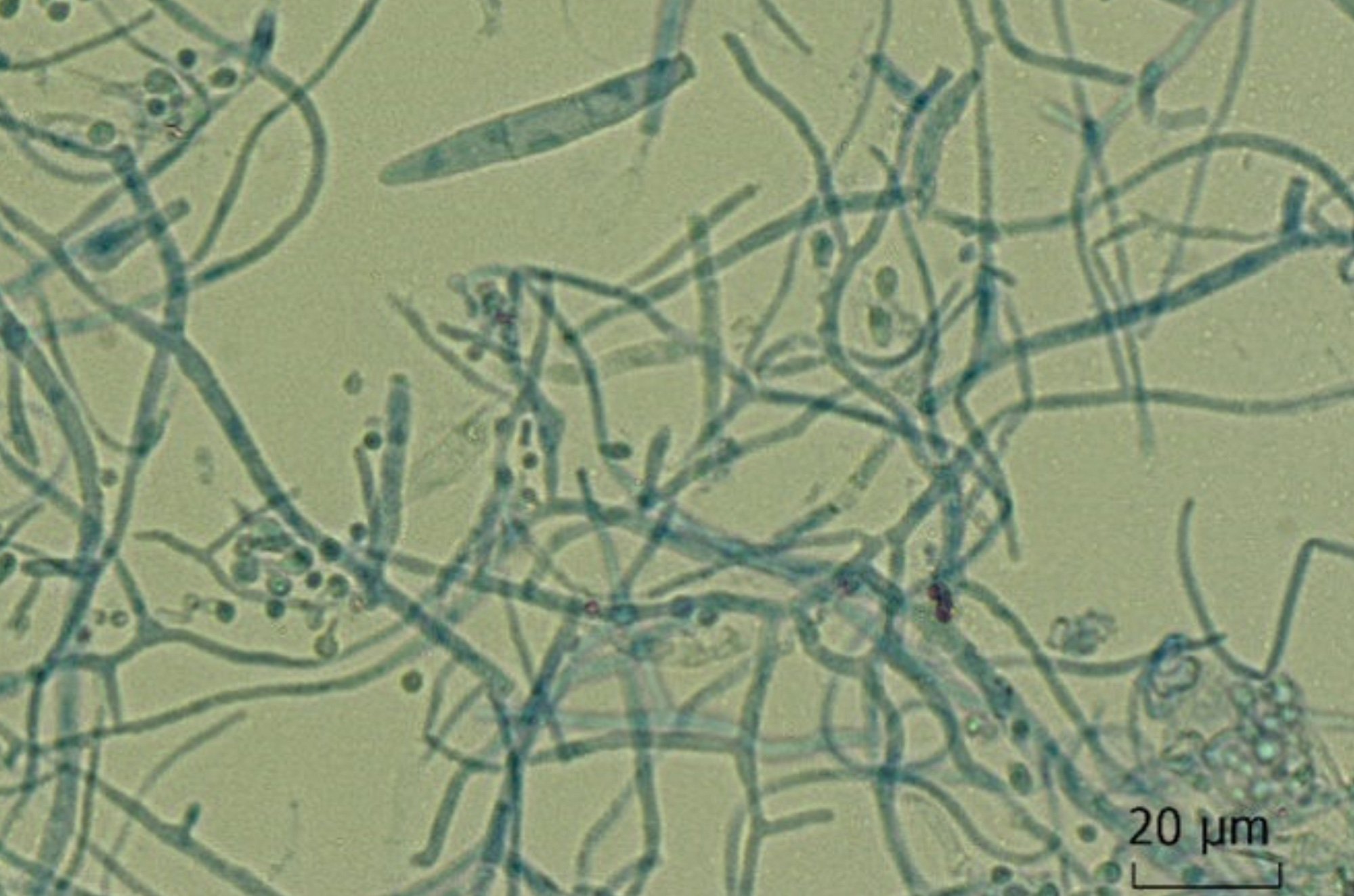
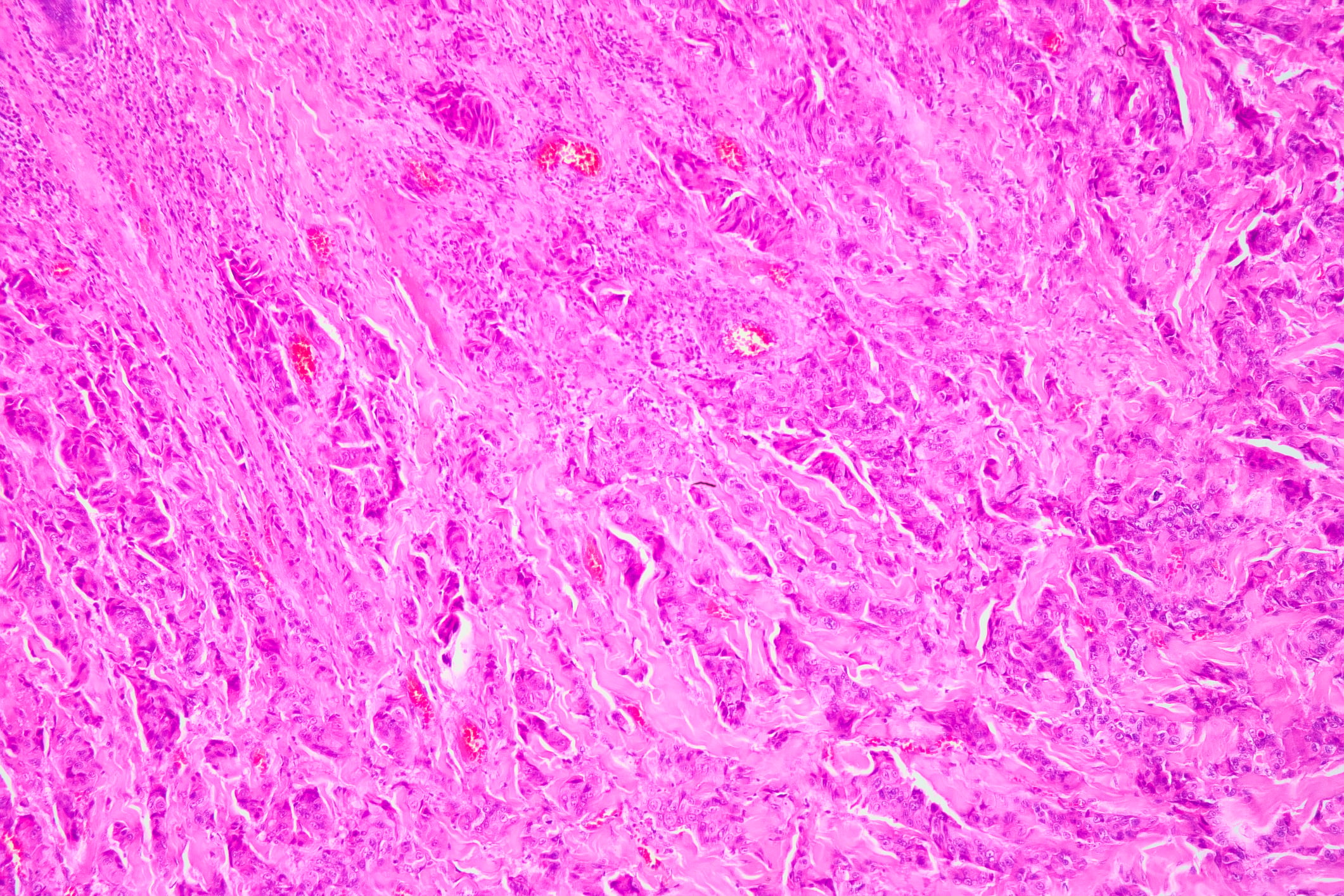
| Forme di amiloidosi con manifestazione cardiaca Nelle amiloidosi, le proteine si depositano sotto forma di aggregati fibrillari insolubili come risultato di un cambiamento conformazionale. Le forme sistemiche di amiloidosi che colpiscono il cuore sono, in particolare, le amiloidosi a catena leggera (AL) e ATTR. Quest’ultima provoca la deposizione di transtiretina mal ripiegata. Si distingue tra la forma wild-type (wtATTR) e la forma mutata (mATTR). Oltre ai biomarcatori cardiaci specifici, oggi sono disponibili moderne tecniche di imaging non invasive, come la risonanza magnetica cardiaca o le tecniche scintigrafiche, che possono essere utilizzate in aggiunta all’ecocardiografia convenzionale per diagnosticare l’amiloidosi cardiaca e valutarne la gravità. |
| a [12] |
Con Tafamidis (Vindaquel®), per i pazienti ATTR è disponibile un’opzione terapeutica specifica per il trattamento dell’insufficienza cardiaca. Gli studi hanno dimostrato che questo stabilizzatore di tetrameri può rallentare la progressione della cardiomiopatia e ridurre il rischio di ospedalizzazione [10,11]. La tafamidis si lega selettivamente con alta affinità alla transtiretina, rallentando la dissociazione dei tetrameri TTR in monomeri TTR e riducendo così l’ulteriore aggregazione delle fibrille amiloidi [10]. Nello studio ATTR-ACT, il braccio tafamidis ha ridotto la mortalità per tutte le cause e le riospedalizzazioni cardiovascolari nei pazienti con wtATTR e mATTR [10].
Letteratura:
- Wallner M, et al: Insufficienza cardiaca: raccomandazioni attuali per la pratica. Swiss Med Forum 2022; 22(46): 750-755.
- Messner M, Zaruba MM: Nuovi sviluppi nella farmacoterapia dell’insufficienza cardiaca. Austrian Journal of Cardiology 2021; 28 (3-4): 104-110.
- McDonagh TA, et al: Linee guida ESC 2021 per la diagnosi e il trattamento dell’insufficienza cardiaca acuta e cronica: sviluppate dalla Task Force per la diagnosi e il trattamento dell’insufficienza cardiaca acuta e cronica della Società Europea di Cardiologia (ESC) con il contributo speciale della Heart Failure Association (HFA) dell’ESC. European Heart Journal 2021; 42: 3599-3726.
- Linea guida tascabile ESC: Insufficienza cardiaca acuta e cronica, Società tedesca di cardiologia (DGK) 2021, https://leitlinien.dgk.org, (ultimo accesso 27.06.2023)
- Gonzalez-Lopez E, et al: L’amiloidosi transtiretina di tipo selvaggio come causa di insufficienza cardiaca con frazione di eiezione preservata. Eur Heart J 2015; 36(38): 2585-2594.
- Feldmann K, Hamm CW, Assmus B: Diagnostica nel sospetto di amiloidosi cardiaca. Dtsch Med Wochenschr 2020; 145(16): 1162-1168.
- Ponikowski P, et al.: Linee guida ESC 2016 per la diagnosi e il trattamento dell’insufficienza cardiaca acuta e cronica: la Task Force per la diagnosi e il trattamento dell’insufficienza cardiaca acuta e cronica della Società Europea di Cardiologia (ESC)Sviluppate con il contributo speciale della Heart Failure Association (HFA) dell’ESC. Eur Heart J 2016; 37(27): 2129-2200.
- Iwano H, Little WC. Insufficienza cardiaca: cosa c’entra la frazione di eiezione? J Cardiol 2013; 62(1): 1-3.
- Schwartzenberg S, et al: Effetti della vasodilatazione nell’insufficienza cardiaca con frazione di eiezione conservata o ridotta implicazioni delle diverse fisiopatologie sulla risposta alla terapia. J Am Coll Cardiol 2012; 59(5): 442-451.
- Maurer MS, et al: Trattamento con tafamidis per i pazienti con cardiomiopatia amiloide transtiretina. N Engl JMed 2018; 379(11): 1007-1016.
- Barroso FA, et al: Sicurezza ed efficacia a lungo termine di tafamidis per il trattamento della polineuropatia amiloide ereditaria da transtiretina: risultati fino a 6 anni. Amiloide 2017; 24(3): 194-204.
- Yilmaz A, et al: Diagnosi e terapia dell’amiloidosi cardiaca. Cardiologia 2019; 13: 264-291.
PRATICA GP 2023; 18(7): 24-25