Riunendo campi di ricerca che in precedenza venivano perseguiti indipendentemente l’uno dall’altro, come le neuroscienze, il metabolismo e la diabetologia, nonché la psicologia, la conoscenza cresce anche per malattie complesse come l’obesità umana. La Dott.ssa Olivia M Farr e il Prof. Christos S Mantzoros della Harvard Medical School stanno lavorando duramente per chiarire i percorsi di comunicazione tra il cervello e il tessuto adiposo. A Monaco di Baviera, in occasione del 52° Congresso Europeo di Diabetologia EASD, hanno mostrato ciò che è già noto.
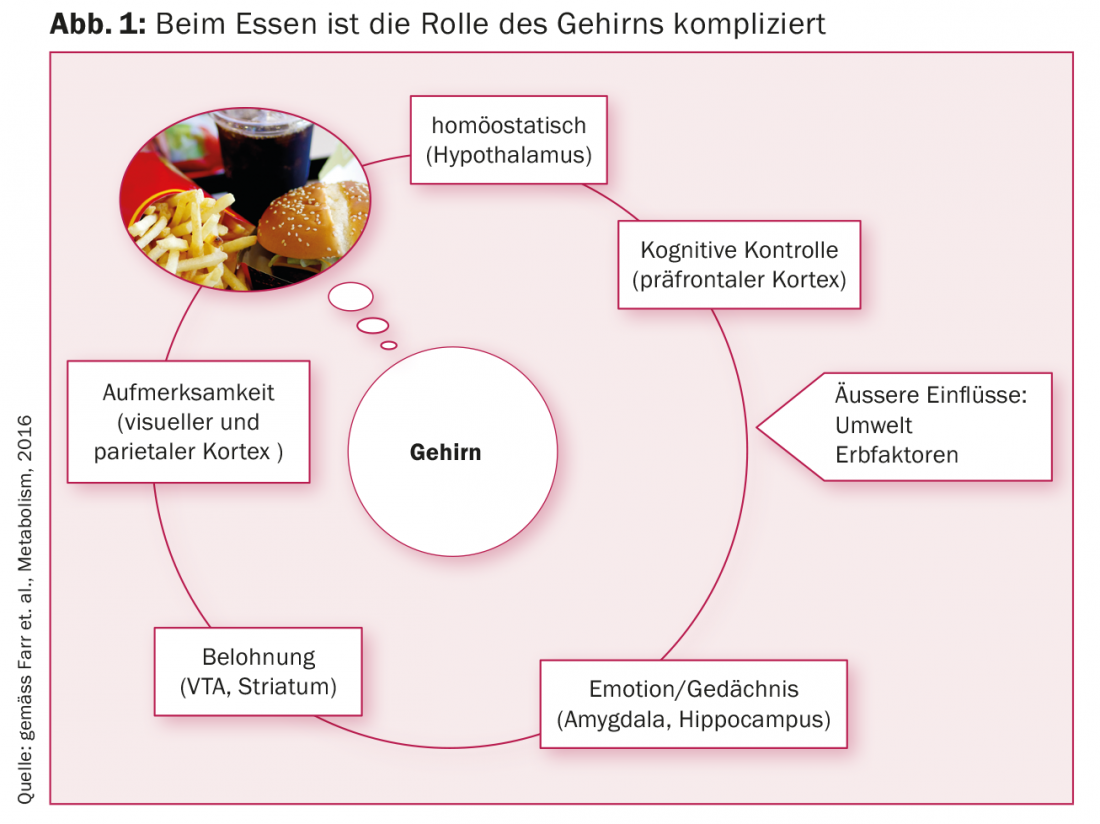
Il cervello riceve costantemente segnali da tutti gli organi coinvolti nel metabolismo. Elabora le informazioni e a sua volta dà comandi a tutte le cellule metabolicamente attive, con l’obiettivo di stabilire e mantenere l’omeostasi. Quali siano i centri di commutazione del cervello che controllano il nostro metabolismo per adattarlo in modo ottimale all’ambiente circostante, è noto finora solo in modo criptico. “Il cervello integra le informazioni dall’interno e dall’esterno, vogliamo sapere dove sono esattamente i punti di commutazione”, ha spiegato il Prof. Christos S Mantzoros della Harvard Medical School al Congresso Europeo sul Diabete a Monaco (Fig. 1).
Mangiamo perché c’è del cibo
Una spiegazione dell’attuale epidemia di obesità è molto semplice: raramente mangiamo quando abbiamo fame, ma perché semplicemente ci fa sentire bene, ha un buon sapore e c’è tanta offerta. Il motivo per cui alcune persone rimangono magre mentre altre diventano obese è la grande scatola nera. Secondo il dottor Farr e il professor Mantzoros, i protagonisti sono gli adipociti e alcuni centri cerebrali. “L’effetto di ricompensa dei buoni filler è paragonabile alla cocaina”, ha sottolineato il dottor Farr (Fig. 2).

Il tessuto adiposo addominale non è solo responsabile dell’immagazzinamento dei trigliceridi. Inoltre, regola i processi metabolici e infiammatori in molteplici modi che vanno ben oltre l’immagazzinamento di energia sotto forma di grasso. Gli effetti noti sono sul sistema cardiovascolare, sulla sensibilità all’insulina e sulla secrezione di insulina. Se lo scambio di segnali tra il sistema nervoso centrale e il tessuto adiposo va fuori controllo a causa di influenze interne e/o esterne, si va verso il malfunzionamento e inizia un circolo vizioso [1].
Leptina e cervello
Il Prof. Mantzoros e il suo gruppo di ricerca sono particolarmente interessati alle sostanze messaggere leptina, irisina e adiponectina dagli adipociti, ma si concentrano anche su grelina, insulina e PYY. Utilizzando la risonanza magnetica funzionale (fMRI), ad Harvard stanno studiando negli animali e negli esseri umani quali regioni del cervello si “accendono” quando viene mostrato un cibo appetitoso, ad esempio. La dottoressa Olivia M Farr ha sottolineato che il cervello complesso degli esseri umani è difficile da confrontare con quello di altri mammiferi. Un problema fondamentale dell’attuale epidemia di obesità, dal punto di vista neuropsicologico, è che i cibi grassi e ipercalorici sono percepiti come molto desiderabili e sono disponibili quasi ovunque, ha spiegato il dottor Farr.
“Dove nasce il desiderio, come sono distribuiti i recettori della leptina, cosa succede quando somministriamo la leptina ricombinante?” sono le domande attuali sulla leptina. La funzione di base di questo proormone è quella di segnalare al cervello quando le riserve di energia sono sufficientemente piene. Se l’ormone non può essere prodotto a causa di un cambiamento nel materiale genetico, il cervello non riceve il segnale di sazietà. Di conseguenza, il cibo viene ingerito senza ritegno e si sviluppa un sovrappeso estremo. La leptina ricombinante non può essere utilizzata per trattare l’obesità, ma è un’opzione per la lipodistrofia legata all’HIV. Questo è il primo risultato clinicamente rilevante di Harvard [2].
Mangiatori emotivi
Nella loro ricerca dei recettori della leptina e del modo in cui potrebbero essere influenzati, i ricercatori di Harvard hanno studiato, tra l’altro, la lorcaserina. Questo agonista del recettore 2c della serotonina-5-idrossitriptamina potrebbe trattare efficacemente i pazienti obesi che mangiano principalmente per motivi emotivi e/o come ricompensa, ha spiegato il Prof. Mantzoros. Si crea una sensazione di sazietà e l’assunzione di calorie viene rallentata. La fMRI ha mostrato un’attività ridotta nella corteccia parietale e visiva e nell’insula e nell’amigdala. Quelle aree che rispondono fortemente alle offerte di cibo nei mangiatori emotivi [3].

Anche le regioni cerebrali responsabili della ricompensa e coinvolte nel comportamento alimentare mostrano una struttura divergente rispetto alle persone normopeso. Il sovrappeso e l’obesità sono associati anche a cambiamenti nei neurotrasmettitori del cervello. In particolare, il sistema degli oppioidi è diverso da quello delle persone di peso normale. A questo proposito, si ipotizza che il sovrappeso e l’obesità siano paragonabili alle dipendenze, alle voglie eccessive e alla mancanza di autocontrollo e al bisogno di quantità sempre maggiori di cibo. Questo è stato dimostrato da scienziati finlandesi e pubblicato nel “Journal of Neuroscience” [4]. L’obiettivo della ricerca sarà ora quello di scoprire se questi cambiamenti derivano dall’assunzione incontrollata di cibo o se sono dovuti a una predisposizione genetica.
Glucagone e cervello
Perché i pazienti diabetici che assumono l’analogo del peptide glucagone-simile liraglutide perdono peso? Questa domanda è stata studiata anche ad Harvard. La liraglutide attiva il recettore GLP-1, che è coinvolto nella regolazione dell’appetito e attiva i centri cerebrali che portano alla sensazione di sazietà. Di conseguenza, le persone trattate mangiano meno e perdono peso. Inoltre, la liraglutide stimola la secrezione di insulina e diminuisce la secrezione di glucagone, portando a una riduzione della glicemia postprandiale e a digiuno [5].
Il Prof. Matthias H. Tschöp e il suo gruppo di ricerca presso l’Istituto Helmholtz per il Diabete e l’Obesità di Monaco di Baviera hanno anche deciso di analizzare in modo più dettagliato il ruolo del cervello nell’equilibrio degli zuccheri nel sangue. La loro conclusione, pubblicata sulla rivista scientifica Nature, è che la normale regolazione del glucosio nel sangue dipende da una partnership tra le cellule produttrici di insulina del pancreas, da un lato, e i circuiti neuronali nell’ipotalamo e in altre regioni del cervello, dall’altro [6]. Secondo il nuovo modello, la leptina attiva il sistema di regolazione nel cervello, che poi aumenta l’utilizzo del glucosio – anche attraverso altri ormoni indipendenti dall’insulina. Questi contribuiscono al metabolismo degli zuccheri in modo simile all’insulina. Affinché il diabete di tipo 2 si manifesti, entrambi i sistemi devono essere disturbati allo stesso tempo.
Gli scienziati hanno anche dimostrato che gli astrociti rispondono alla leptina. Questo è un fattore importante per la sensazione di sazietà. Poiché è stato dimostrato che sia la leptina che l’insulina hanno un’influenza sugli astrociti, i ricercatori propongono di sviluppare un nuovo modello che, oltre alle cellule nervose, tenga conto anche degli astrociti come regolatori del metabolismo e della sensazione di fame. Sperano che il quadro più dettagliato apra nuove prospettive per lo sviluppo di farmaci.
Fonte: 52a Riunione annuale dell’EASD, 12-16 settembre 2016, Monaco di Baviera, Germania.
Letteratura:
- Farr OM, et al.: Regolazione del sistema nervoso centrale dell’alimentazione: intuizioni dall’imaging cerebrale umano. Metabolismo. 2016 Maggio; 65(5): 699-713.
- Farr OM, et al.: Applicazioni della leptina nel 2015: cosa abbiamo imparato sulla leptina e l’obesità? Curr Opin Endocrinol Diabetes Obes. 2015 Oct; 22(5): 353-9.
- Farr OM, et al: la somministrazione di lorcaserina diminuisce l’attivazione dei centri cerebrali in risposta agli indizi alimentari e questi cambiamenti correlati all’emozione e alla salienza sono correlati agli effetti di perdita di peso: uno studio clinico randomizzato, controllato con placebo, in doppio cieco, della durata di 4 settimane. Diabete. 2016 Oct; 65(10): 2943-53.
- Karlsson H K, et al: L’obesità è associata a una diminuzione della disponibilità di recettori μ-oppioidi, ma non di Dopamina D2 nel cervello. Il Journal of Neuroscience, 4 marzo 2015, 35(9): 3959-3965.
- Farr OM, et al: i recettori GLP-1 sono presenti nella corteccia parietale, nell’ipotalamo e nel midollo del cervello umano e l’analogo GLP-1 liraglutide altera l’attività cerebrale legata a spunti alimentari altamente desiderabili in persone con diabete: uno studio crossover, randomizzato, controllato con placebo. Diabetologia. 2016 Maggio; 59(5): 954-65.
- Caceres, C. et al: (2016): La segnalazione insulinica astrocitaria accoppia l’assorbimento del glucosio cerebrale con la disponibilità di nutrienti, Cell, DOI: 10.1016/j.cell.2016.07.028 www.cell.com/cell/fulltext/S0092-8674(16)30974-6.
CARDIOVASC 2016; 15(6): 33-36