Per la prima volta dall’apprezzatissimo studio FOURIER, un inibitore di PCSK9 mostra ora anche un beneficio in termini di mortalità nella prevenzione secondaria. Si tratta di alirocumab. Gli esperti stanno reagendo positivamente e stanno già discutendo di abbassare i valori target.
Breve recensione: Il Congresso ACC 2017 è stato dominato dallo studio FOURIER, che per la prima volta ha fornito dati sui tanto attesi (e fortemente richiesti) endpoint “hard” nell’inibizione di PCSK9. L’aggiunta di evolocumab ha ridotto significativamente il rischio di morte cardiovascolare, infarto miocardico, ictus, ricovero in ospedale per angina instabile o rivascolarizzazione coronarica. Evolocumab è stato superiore al placebo anche nell’endpoint secondario, che comprendeva solo la morte cardiovascolare, l’infarto miocardico o l’ictus (in aggiunta alla terapia statinica esistente con/senza ezetimibe) – in particolare, il rischio è stato ridotto di un significativo 20%. Questo con un buon profilo di sicurezza. L’ipotesi “più basso è, meglio è” sembra essere confermata, ma la grande domanda è: i risultati sono sufficienti per giustificare i prezzi non trascurabili dei farmaci della classe dei principi attivi e per utilizzare i farmaci su un fronte più ampio?
Infine – e questo è un ma cruciale – il beneficio in termini di morbilità non si è tradotto in un beneficio significativo in termini di sopravvivenza. Sebbene sia noto da altri studi che confrontano una terapia più intensiva con una moderata, la riduzione supplementare del colesterolo LDL non sempre esercita un effetto significativo sulla mortalità cardiovascolare. In alternativa, il beneficio clinico completo diventa evidente solo dopo un certo ritardo (FOURIER è stato relativamente breve, con una durata di circa due anni).
Nella pratica clinica quotidiana, tuttavia, rimanevano alcuni punti interrogativi e limitazioni nella gestione della nuova e costosa classe di principi attivi e si attendevano con ansia i primi risultati del concorrente alirocumab.
RISULTATI DELL’ODISSEA
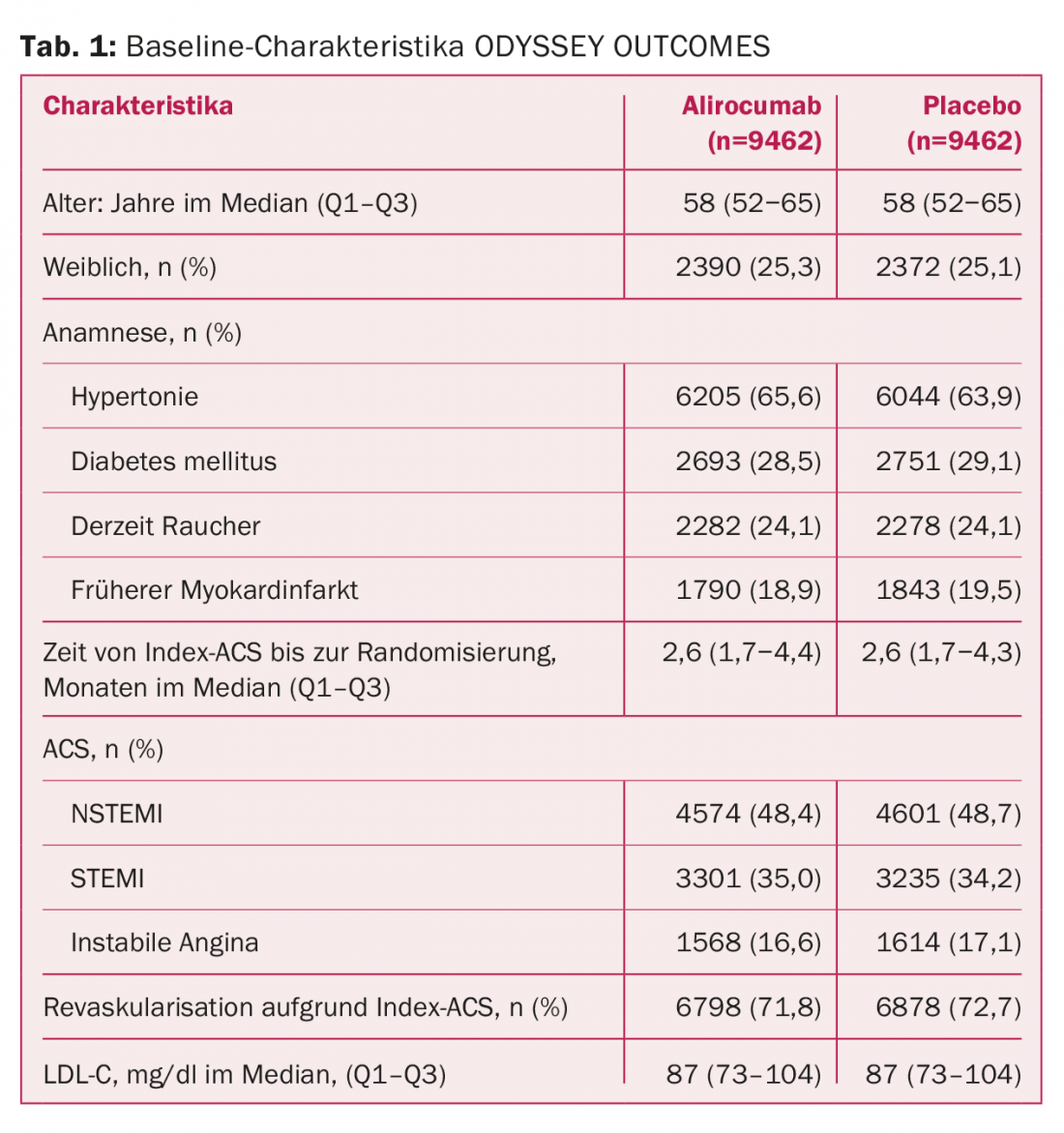
Ora sono arrivati, sotto forma dello studio ODYSSEY OUTCOMES. E nemmeno loro chiariscono con assoluta certezza tutti i punti aperti sulla terapia con PCSK9. Ciò è dovuto, da un lato, alla popolazione di studio selezionata, che è stata diversa. Invece di ben 27.000 pazienti con malattia aterosclerotica stabile e consolidata come in FOURIER, qui c’erano quasi 19.000 pazienti con sindrome coronarica acuta (SCA) negli ultimi 1-12 mesi e controllo lipidico inadeguato, cioè valori di LDL-C ≥1,8 mmol/l nonostante una terapia statinica ad alta intensità o massimamente tollerata. L’89% era in trattamento con atorvastatina/rosuvastatina ad alto dosaggio al basale, il 3% era in trattamento con ezetimibe. Un campione con un rischio chiaramente aumentato di ulteriori eventi (Tab. 1). In FOURIER, una minoranza di pazienti ha avuto un’ACS nell’anno precedente.
Il farmaco, assunto ogni due settimane, ha ridotto il rischio di eventi cardiaci avversi maggiori (MACE) di un significativo 15% rispetto al placebo. Questi includevano la morte per CHD, l’infarto miocardico non fatale, l’ictus ischemico o l’angina instabile con ricovero in ospedale. Questa è la differenza successiva a FOURIER, in cui anche la componente più “soft” della rivascolarizzazione coronarica era inclusa nell’endpoint primario. È quindi probabile che questa volta l’ostacolo per generare un vantaggio significativo sia stato un po’ più alto. Il tempo di follow-up mediano è stato di 2,8 anni.
Il tasso di infarto miocardico considerato separatamente e (questa volta anche) la mortalità per tutte le cause sono stati ugualmente migliorati, il primo dal 7,6% al 6,6% (p=0,006) e il secondo dal 4,1% al 3,5% (p=0,026, riduzione del 15%). Quando la morte per CHD e la morte cardiovascolare sono state considerate separatamente – anch’esse endpoint secondari – non sono state riscontrate differenze significative. Va detto che in uno studio globale su 1315 centri e 57 Paesi, non si può necessariamente garantire che le cause di morte siano sempre documentate correttamente se i pazienti muoiono a casa. La morte stessa, invece, può essere determinata con certezza ovunque. Il valore p di 0,026 nella mortalità per tutte le cause è considerato “nominale”, poiché questo endpoint è stato valutato statisticamente a valle (valutazione gerarchica dell’endpoint).
I pazienti hanno tollerato bene il trattamento con tassi comparabili di effetti collaterali (inclusi quelli gravi). Inoltre, non ci sono state differenze rilevanti in termini di diabete di nuova insorgenza, reazioni allergiche o eventi neurocognitivi (semmai, il farmaco tendeva ad essere superiore al placebo). Dopo oltre tre anni di trattamento in questo ampio collettivo, non è stato riscontrato alcun segnale di sicurezza con alirocumab, a parte le reazioni nel sito di iniezione.
Più è profondo, meglio è
Come FOURIER, ODYSSEY OUTCOMES sostiene l’ipotesi “più basso è meglio” e quindi un adeguamento della terapia ai livelli lipidici (invece di un orientamento esclusivo verso l’intensità delle statine, vedi la controversia sulle linee guida degli ultimi anni tra Stati Uniti ed Europa). Tuttavia, suggerisce anche che nella CHD i precedenti valori target di colesterolo LDL inferiori a 70 mg/dl non sono ancora ottimali.
All’inizio dello studio, l’LDL-C era di 87 mg/dl. Le riduzioni di LDL-C di oltre il 50% sono state osservate rapidamente e sono state per lo più sostenute durante il follow-up. Le riduzioni sono state qualitativamente paragonabili a quelle di FOURIER: dopo quattro mesi con alirocumab, l’LDL-C era di 37,6 mg/dl, rispetto a 93,3 mg/dl con placebo, una riduzione di oltre il 60%. Si tratta di valori molto chiari, a cui si è ormai abituati con l’inibizione di PCSK9.
C’è da chiedersi: il crescente successo dell’inibizione della PCSK9 creerà presto un nuovo standard, ovvero l’abbassamento dell’LDL sotto i 50 mg/dl? Infine, la dimensione del miglioramento clinico nell’endpoint primario (soprattutto in presenza di elevati livelli basali di LDL) è notevole. E dopo FOURIER, ODYSSEY OUTCOMES è il secondo studio di grandi dimensioni a dimostrare che l’abbassamento del colesterolo LDL a un intervallo di 25-50 mg/dl migliora la prognosi dei pazienti con CHD.
Al termine del follow-up dopo 48 mesi, i livelli erano ancora 53,3 vs. 101,4 mg/dl (riduzione del 54,7%). L’obiettivo dello studio era un LDL-C di 25-50 mg/dl; hanno cercato attivamente (e con una titolazione in cieco) di mantenere il maggior numero possibile di pazienti in questo intervallo target. Non è chiaro, quindi, se la riduzione a lungo termine dell’abbassamento dell’LDL-C sia legata al disegno dello studio (la dose veniva aggiustata o commutata in placebo a livelli inferiori al range target) o allo sviluppo di anticorpi neutralizzanti contro il farmaco, che sembravano verificarsi più frequentemente nel gruppo di trattamento (42 vs. 6 casi). Gli studi di un altro programma di sperimentazione chiamato SPIRE [1,2] con l’anticorpo PCSK9 bococizumab sono stati interrotti precocemente, tra le altre ragioni, proprio a causa di questo problema: a quanto pare, l’effetto di riduzione delle LDL è diminuito in modo significativo a causa della formazione dell’anticorpo. Solo i pazienti con LDL-C al basale superiore a 2,6 mmol/l hanno tratto beneficio in SPIRE 1 e 2. in FOURIER il problema non si è presentato. Secondo gli autori di ODYSSEY OUTCOMES, non c’è nemmeno motivo di ritenere che alirocumab abbia un effetto avverso dovuto agli anticorpi.
Chi ne beneficia di più?
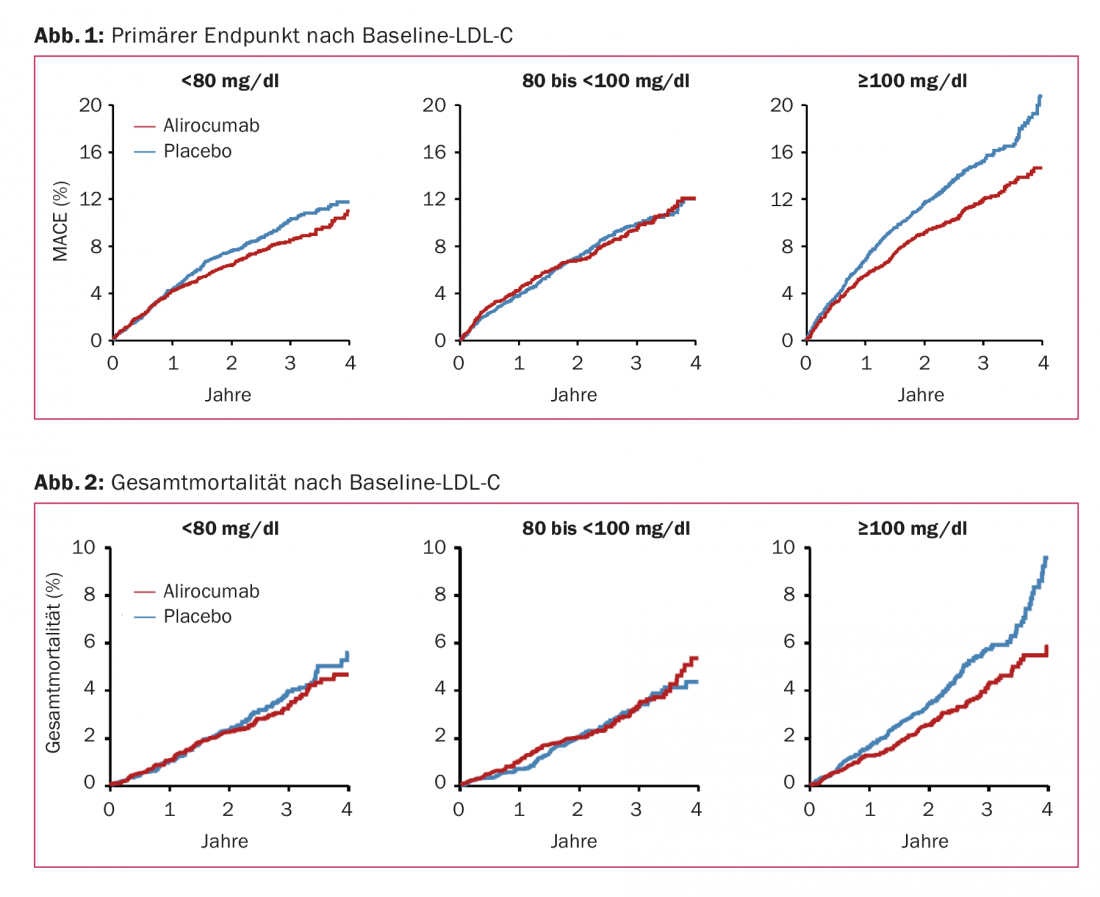
Di conseguenza, le richieste di analisi costi-benefici degli inibitori della PCSK9 non si placano nemmeno dopo l’ODYSSEY OUTCOMES, che è stato accolto complessivamente in modo positivo. Le valutazioni precedenti hanno tratto una conclusione negativa [3,4]. O si deve cambiare il prezzo o si devono definire con maggiore precisione i pazienti per i quali i benefici sono chiaramente superiori ai costi, come è stato detto più volte al congresso. È stata anche richiesta una maggiore pressione sugli assicuratori affinché rimborsino la classe di principi attivi in modo più ampio. Le analisi di sottogruppo di ODYSSEY OUTCOMES suggeriscono che i pazienti con LDL-C ≥100 mg/dl al basale (mediana 118 mg/dl) traggono particolare beneficio. Tra questi, il MACE si riduce dal 14,9% all’11,5% (HR 0,76) e la mortalità per tutte le cause dal 5,7% al 4,1% (HR 0,71). Riduzioni del rischio simili sono state riscontrate anche in questo sottogruppo per i decessi dovuti a CHD e morte cardiovascolare. Tuttavia, non vi era alcuna interazione significativa tra gli esiti primari o la mortalità per tutte le cause e i livelli basali di LDL-C (p=0,09 e p=0,12). Anche il gruppo con LDL-C basale <80 mg/dl ha sperimentato una riduzione del rischio del 14% nell’endpoint primario e dell’11% nella mortalità per tutte le cause con il farmaco (Fig. 1 e 2).
In generale, la popolazione post-ACS in ODYSSEY OUTCOMES era a rischio più elevato rispetto al campione FOURIER. Infatti, nonostante le strategie preventive basate sull’evidenza, il rischio residuo rimane alto poco dopo l’ACS ed è legato, almeno in parte, ai livelli di LDL-C. Se questi vengono ridotti precocemente dopo l’evento, ad esempio con una terapia a base di statine [5] – soprattutto ad alta intensità [6] o in combinazione con l’ezetimibe [7] – si riduce anche il rischio di ulteriori eventi (nota a margine: se il principio “prima le statine nell’ACS, meglio è” si applica in questo caso, è stato messo in discussione anche dallo studio SECURE-PCI all’ACC 18). A quanto pare, l’effetto protettivo può essere ulteriormente potenziato con una potente inibizione di PCSK9. Quindi, forse è proprio questo gruppo ad alto rischio che beneficia dell’inibizione della PCSK9 non solo in termini di morbilità, ma anche di mortalità, il che sosterrebbe meglio i prezzi elevati dei farmaci. Oltre alla diversa popolazione dello studio, anche il tempo di follow-up più lungo potrebbe aver giocato un ruolo nel miglioramento della sopravvivenza.
In ogni caso, dopo i due studi positivi FOURIER e ODYSSEY OUTCOMES, occorre ora trovare una soluzione anche in termini di costi, per poter finalmente somministrare il principio attivo a tutti i pazienti che ne trarrebbero beneficio (che, secondo le attuali evidenze, sono molti). Infine, la sicurezza, che in genere si trova anche sul lato “costo” del profilo costo-beneficio, è così buona nel caso dell’inibizione della PCSK9 che il pendolo oscillerebbe chiaramente verso il lato “beneficio” – se non si tiene conto dei prezzi dei farmaci.
Ciò che è chiaro è che ODYSSEY OUTCOMES fornisce il prossimo pezzo del puzzle in un quadro generale che sta diventando sempre più chiaro per questa classe di agenti relativamente nuova. In base alla situazione attuale degli studi, evolocumab viene preso in considerazione per i pazienti con malattia cardiovascolare aterosclerotica stabile e alirocumab per i pazienti con ACS – questo fino a nuovo avviso, purché non sia stato confermato un effetto di classe.
Alirocumab è attualmente approvato per l’uso con la dieta e in aggiunta alla dose massima tollerata di statine, con o senza altre terapie che modificano i lipidi, per il trattamento di adulti con ipercolesterolemia familiare eterozigote grave o con malattia cardiovascolare aterosclerotica clinicamente manifesta, che necessitano di un ulteriore abbassamento delle LDL-C. Secondo Limitatio, l’uso nella prevenzione secondaria è attualmente limitato ai pazienti con LDL-C >3,5 mmol/l e/o malattia cardiovascolare aterosclerotica clinica progressiva con un LDL-C >2,6 mmol/l.
Fonte: Sessione scientifica annuale dell’American College of Cardiology (ACC) 2018, 10-12 marzo 2018, Orlando
Letteratura:
- Ridker PM, et al: Efficacia e sicurezza cardiovascolare di Bococizumab nei pazienti ad alto rischio. N Engl J Med 2017; 376: 1527-1539.
- Ridker PM, et al: Variabilità della riduzione dei lipidi e formazione di anticorpi con Bococizumab. N Engl J Med 2017; 376: 1517-1526.
- Kazi DS, et al: Analisi aggiornata del rapporto costo-efficacia degli inibitori della PCSK9 in base ai risultati dello studio FOURIER. JAMA 2017; 318(8): 748-750.
- Fonarow GC, et al: Costo-efficacia della terapia con Evolocumab per ridurre gli eventi cardiovascolari nei pazienti con malattia cardiovascolare aterosclerotica. JAMA Cardiol 2017; 2(10): 1069-1078.
- Schwartz GG, et al: Effetti dell’atorvastatina sugli eventi ischemici ricorrenti precoci nelle sindromi coronariche acute: lo studio MIRACL: uno studio controllato randomizzato. JAMA 2001 Apr 4; 285(13): 1711-1718.
- Cannon CP, et al: Riduzione intensiva dei lipidi rispetto a quella moderata con le statine dopo le sindromi coronariche acute. N Engl J Med 2004 Apr 8; 350(15): 1495-1504.
- Cannon CP, et al: Ezetimibe aggiunto alla terapia con statine dopo le sindromi coronariche acute. N Engl J Med 2015 Jun 18; 372(25): 2387-2397.
CARDIOVASC 2018; 17(2): 35-38