Il numero di persone che soffrono di diabete continua ad aumentare. Secondo una stima della Federazione Internazionale del Diabete, circa 592 milioni di persone saranno colpite nel 2035. Questa malattia è associata a un aumento del rischio di mortalità, soprattutto se trattata in modo inadeguato. Una panoramica pratica della migliore strategia terapeutica individuale possibile.
Il numero di pazienti affetti da diabete continua ad aumentare. Secondo una stima della Federazione Internazionale del Diabete, il numero di persone colpite aumenterà da 382 milioni nel 2013 a 592 milioni nel 2035 in tutto il mondo [1]. La malattia è associata a un aumento del rischio di mortalità. Per esempio, una persona di 50 anni con diabete perde in media sei anni di vita rispetto a una persona sana, molti dei quali a causa di malattie cardiovascolari [2]. Con terapie sempre più efficaci e adattate individualmente, si sta cercando di contrastare questo rischio. Nel 2008, è stato dimostrato che i pazienti di 55 anni con diabete di tipo 2 e microalbuminuria possono trarre beneficio da una terapia diabetica intensificata con combinazioni multiple di farmaci e aggiustamenti dello stile di vita. L’incidenza di mortalità è diminuita del 46% (p=0,02) nel gruppo di intervento [3]. Da questi dati, è chiaro che un approccio terapeutico di successo è quello multimodale. A seconda della costellazione di risultati, il concetto generale include la cessazione del fumo, la riduzione dei lipidi con le statine, il controllo della pressione sanguigna con gli ACE-inibitori/sartani, la prevenzione secondaria con l’aspirina in presenza di malattie cardiovascolari e, naturalmente, la terapia del diabete.
Passo dopo passo
Molti medici sono ancora restii a intensificare la terapia del diabete, ma un concetto terapeutico di successo può essere sviluppato sulla base di tre fasi, secondo il Prof. Dr. Roger Lehmann, Responsabile di Diabetologia, Clinica di Endocrinologia, Diabetologia e Nutrizione Clinica, Ospedale Universitario di Zurigo.
Passo 1: Impostazione dell’obiettivo individuale HA1c
Passo 2: Determinare la migliore terapia individuale: preferenze personali e priorità mediche
Fase 3: pensi in termini di classi di sostanze – utilizzi il farmaco con le prove migliori.
Oltre ai risultati clinici, anche i desideri del paziente sono decisivi per il successo della pianificazione e dell’attuazione della terapia. Le seguenti affermazioni sono spesso fatte dal punto di vista del paziente:
- assenza di ipoglicemia
- Evitare l’aumento di peso
- una preferenza per la somministrazione orale piuttosto che per l’iniezione
- una somministrazione preferibile una volta alla settimana rispetto a quella giornaliera.
- Il numero più basso possibile di compresse richieste in totale (preferibile la terapia combinata)
Tenere conto di queste preferenze personali è fondamentale per mantenere la motivazione del paziente e quindi per il successo della terapia mirata.
Quattro domande importanti
Oltre alle preferenze personali, le circostanze cliniche sono un fattore altrettanto importante da considerare quando si determina la terapia farmacologica per il diabete. Per determinare la migliore terapia individuale, il Prof. Lehmann ha dato ai medici un catalogo composto da quattro domande.
Prima di tutto, bisogna chiarire se c’è una carenza di insulina . Questo si manifesta con un’iperglicemia sintomatica, che si manifesta clinicamente come poliuria, polidipsia, perdita di peso e carenza di volume; nel peggiore dei casi, c’è il rischio di uno scompenso metabolico. In questo caso, il paziente ha bisogno di insulina. Fondamentalmente, ci sono diversi regimi tra cui scegliere, dal principio del bolo di base, all’insulina mista con componenti a lunga e breve durata d’azione, fino alla combinazione di insulina mista e GLP-1 RA. Secondo il relatore, l’insulina mista e in particolare Tresiba dovrebbe essere favorita nel senso della fase 3, in quanto è superiore alla precedente insulina standard Lantus in termini di prevenzione dell’ipoglicemia grave e notturna e di riduzione dei 3 punti MACE (eventi cardiovascolari avversi maggiori). Se necessario, l’insulina può anche essere somministrata solo temporaneamente ed eventualmente interrotta nel corso della terapia individuale del diabete mellito di tipo 2.
La seconda domanda clinica riguarda la velocità di filtrazione glomerulare (GFR). Con un GFR <30 ml/min, si devono somministrare inibitori della DPP-4 e, se necessario, insulina basale aggiuntiva. Tuttavia, questa combinazione è un compromesso, in quanto può provocare ipoglicemia e aumento di peso. Tra gli inibitori della DPP-4, il linagliptin è da preferire, in quanto non richiede l’aggiustamento della dose al suddetto GFR.
Con un GFR compreso tra >45-60 ml/min, si raccomanda innanzitutto la metformina, con la combinazione precoce con gli inibitori SGLT2, oppure con un BMI >28 kg/m², la combinazione con GLP-1 RA. Il Prof. Lehmann ha sottolineato che una combinazione precoce con un dosaggio inferiore ha più senso e spesso ha meno effetti collaterali rispetto alla monoterapia con un aumento costante della dose. Se questa combinazione non è sufficiente per raggiungere l’obiettivo definito congiuntamente, si può aggiungere anche un inibitore della DPP-4 o l’insulina basale o la gliclazide come rappresentante delle sulfoniluree. Bisogna tenere presente che la combinazione di più farmaci con lo stesso meccanismo d’azione non porta alcun vantaggio. Una combinazione di GLP-1 RA e inibitori della DPP-4 deve quindi essere evitata. Gli inibitori del GLP-1 RA e del SGLT2 sono particolarmente indicati per i pazienti con funzione renale compromessa, in quanto diversi studi hanno dimostrato che i farmaci hanno un effetto nefroprotettivo oltre a ridurre la mortalità [4–6]. Gli inibitori SGLT2 hanno il vantaggio di poter essere assunti per via orale e il costo del trattamento è inferiore rispetto agli agonisti del recettore GLP-1, che devono essere iniettati. Il relatore ha nominato empagliflozin tra gli inibitori SGLT2 e liraglutide e semaglutide nel gruppo GLP-1RA come farmaci con le migliori evidenze.
Se il GFR scende a >30 – <45 ml/min, deve essere somministrata solo metà della dose di metformina.
Oltre alla questione della funzionalità renale, anche la presenza di malattie cardiovascolari è decisiva per la scelta del farmaco. Se questo può essere dimostrato, si può seguire la raccomandazione terapeutica per un GFR >45-60 ml/min. Anche nei pazienti asintomatici, cioè per lo più non diagnosticati, questa procedura non cambia quasi mai. Solo la terapia di prima linea riceve un’opzione aggiuntiva con la combinazione diretta di metformina e inibitori della DPP-4, oltre alle opzioni di combinazione già menzionate in precedenza. L’escalation avviene con gliclazide (sulfonilurea) o insulina basale.
La quarta domanda clinica è se il paziente diabetico ha un’insufficienza cardiaca . Se questo si afferma , la metformina in combinazione con gli inibitori SGLT2 è la prima scelta.
Nel corso, si possono aggiungere gli inibitori della DPP-4 o, successivamente, l’insulina basale.
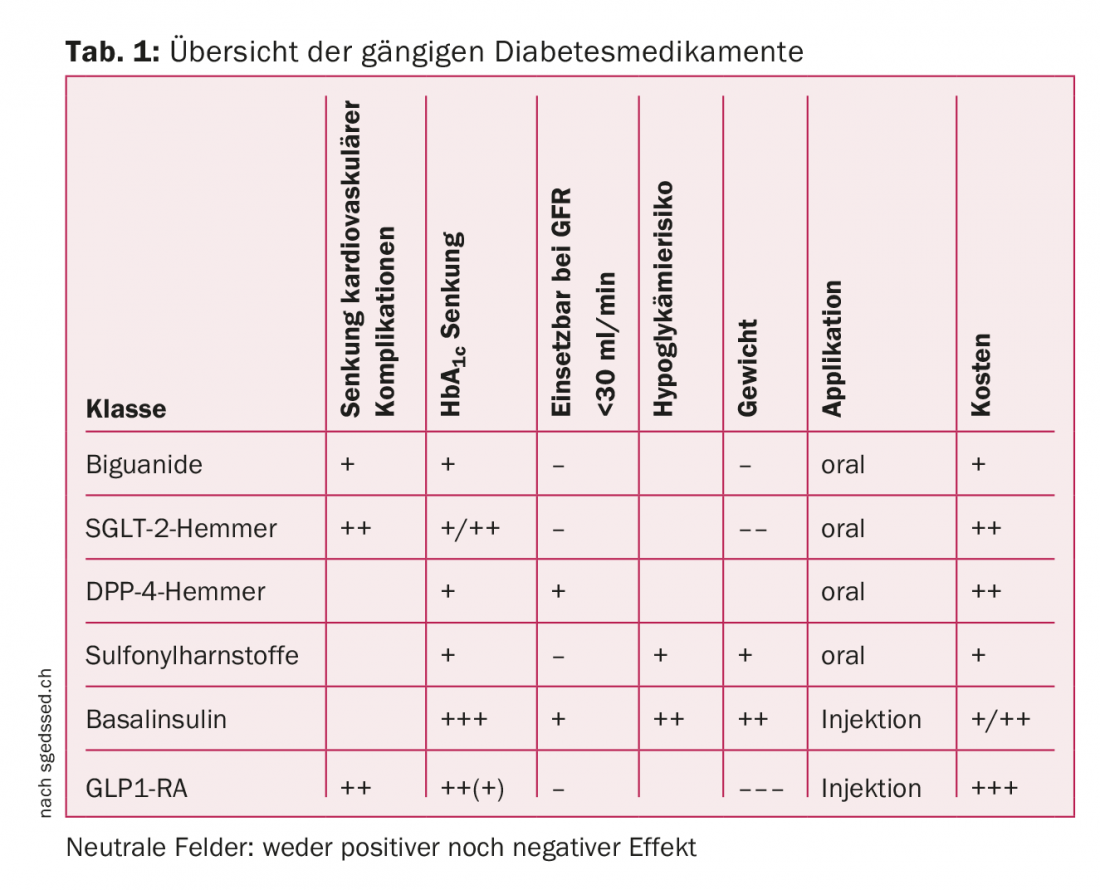
La tabella 1 fornisce una panoramica dei diversi farmaci menzionati.
Da portare a casa
Sulla base dei dati disponibili, il Prof. Lehmann ha sottolineato l’importanza degli inibitori SGLT2 e del GLP 1 RA nel regime di trattamento del diabete di tipo 2. In studi endpoint di grandi dimensioni, empagliflozin (GLP-1 RA) e liraglutide (inibitore SGLT-2) hanno dimostrato di ridurre la mortalità complessiva e cardiovascolare, di fornire una nefroprotezione e, con l’effetto favorevole sullo sviluppo del peso e sul rischio di ipoglicemia, di avere un beneficio aggiuntivo nel contesto della terapia multifattoriale del diabete. [4–6]. Prima di iniziare la terapia, è necessario discutere esplicitamente del fatto che esiste un rischio maggiore di sviluppare infezioni urogenitali con gli inibitori SGLT-2, a causa della glucosuria.
Se i risultati clinici o i desideri del paziente cambiano nel corso della terapia, il regime terapeutico stabilito deve essere riconsiderato. Secondo il relatore, un’intensificazione tempestiva della terapia è fondamentale per una terapia adeguata. Se questo viene ritardato di un anno e allo stesso tempo la glicemia è scarsamente controllata, si verifica un aumento significativo degli eventi cardiovascolari [7].
Fonte: Medidays Zurigo, 4-8 settembre 2017
Letteratura
- www.idf.org/diabetesatlas, 6a edizione, 2013
- Rao Kondapally Seshasai S, et al: Diabete mellito, glucosio a digiuno e rischio di morte per cause specifiche. N Engl J Med 2011; 364(9): 829-841.
- Gaede P, et al.: Effetto di un intervento multifattoriale sulla mortalità nel diabete di tipo 2. N Engl J Med 2008; 358(6): 580-591.
- Marso SP, et al: Liraglutide ed esiti cardiovascolari nel diabete di tipo 2. N Engl J Med 2016; 375(4): 311-322.
- Zinman B, et al: Empagliflozin, esiti cardiovascolari e mortalità nel diabete di tipo 2. N Engl J Med 2015; 373(22): 2117-2128.
- Wanner C, et al: Empagliflozin e la progressione della malattia renale nel diabete di tipo 2. N Engl J Med 2016; 375(4): 323-334.
- Paul SK, et al: Il ritardo nell’intensificazione del trattamento aumenta i rischi di eventi cardiovascolari nei pazienti con diabete di tipo 2. Cardiovasc Diabetol 2015; 14: 100.
CARDIOVASC 2017; 16(5): 36-38
PRATICA GP 2017; 12(10): 36-38











