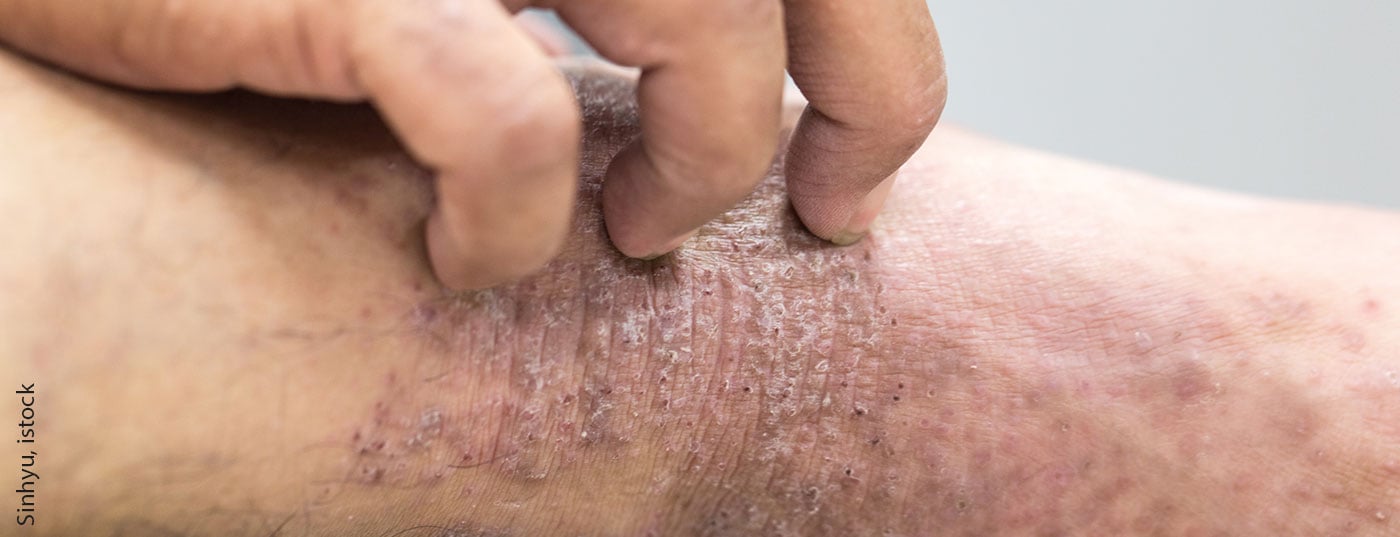
Soprattutto negli adolescenti, la dermatite atopica da moderata a grave è associata a un alto livello di sofferenza. Nello studio pivotal, dupilumab ha fornito un sollievo rapido e duraturo delle lesioni cutanee e del prurito. Anche la qualità di vita legata alla salute è migliorata in modo significativo. Dupilumab è attualmente l’unico biologico approvato in Svizzera per questo gruppo di pazienti.
Swissmedic ha esteso l’autorizzazione all’immissione in commercio di Dupixent® (dupilumab) per il trattamento della dermatite atopica da moderata a grave nel novembre 2020 agli adolescenti di età compresa tra i 12 e i 17 anni con dermatite atopica da moderata a grave, quando la terapia con farmaci topici da prescrizione non fornisce un controllo adeguato della malattia o non è raccomandata. [1]. Soprattutto per i pazienti adolescenti con dermatite atopica moderata o grave, c’è bisogno di opzioni di trattamento efficaci con pochi effetti collaterali. La terapia a lungo termine con glucocorticoidi è efficace solo in misura limitata ed è associata a effetti collaterali come l’atrofia cutanea. Una dermatite atopica trattata in modo inadeguato può avere effetti negativi a livello fisico, psicologico e psicosociale. I disturbi dell’ansia e del sonno, così come la depressione e l’esclusione sociale sono comuni tra le persone colpite [2]. “La dermatite atopica da moderata a grave può influenzare la vita di un adolescente in molti modi, incidendo sia sul suo benessere fisico che psicologico”, afferma la PD Lisa Weibel, MD, Capo del Dipartimento di Dermatologia Pediatrica dell’Ospedale Pediatrico Universitario di Zurigo [3].
Miglioramento rapido e duraturo del prurito e delle lesioni cutanee
L’approvazione di dupilumab per gli adolescenti da parte di Swissmedic si basa sui dati clinici del programma LIBERTY AD. L’efficacia e la sicurezza della monoterapia con l’inibitore di IL4/IL13 alla dose di 200 mg o 300 mg ogni due settimane è stato valutato in uno studio multicentrico, randomizzato, in doppio cieco, controllato con placebo, su 251 pazienti di età compresa tra 12 e 17 anni con dermatite atopica da moderata a grave che avevano avuto una risposta inadeguata alla terapia topica [4]. Panoramica dei risultati importanti dopo il periodo di trattamento di 16 settimane:
- EASI-75: il 42% dei pazienti trattati con dupilumab rispetto all’8% dei pazienti trattati con placebo ha ottenuto un miglioramento di almeno il 75% delle lesioni cutanee (EASI-75)* [4].
- IGA 0/1: il 24% dei pazienti ha ottenuto IGA** 0 o 1 con dupilumab rispetto al 2% con placebo [4].
- Miglioramento dell’EASI: i pazienti trattati con dupilumab hanno mostrato un miglioramento medio dell’EASI del 66% rispetto al basale, rispetto al 24% dei pazienti trattati con placebo [4].
- Riduzione del prurito: con dupilumab, il 37% dei pazienti ha ottenuto un miglioramento clinicamente rilevante del prurito di almeno quattro punti sulla scala di valutazione numerica del prurito di picco (NRS); con il placebo, questa percentuale era del 5% [5].
- Miglioramento della qualità di vita: il 61% dei pazienti trattati con dupilumab rispetto al 20% dei pazienti trattati con placebo ha ottenuto un miglioramento clinicamente significativo della qualità di vita di almeno 6 punti nel Children’s Dermatology Life Quality Index (CDLQI) [5].
- Misura dell’eczema orientata al paziente (POEM): con dupilumab, il 63% dei pazienti ha avuto un miglioramento di almeno 6 punti nella gravità della malattia, misurata dalla misura dell’eczema orientata al paziente (POEM). Questo valuta vari aspetti, tra cui il sonno. Con il placebo, questa percentuale era del 10% [5].
* EASI = Indice di area e gravità dell’eczema
** IGA = Valutazione Globale dello Sperimentatore
|
Alto carico di malattia negli adolescenti con dermatite atopica “Gli adolescenti con dermatite atopica moderata o grave non adeguatamente controllata devono affrontare diversi problemi che possono avere effetti duraturi sulla loro vita. I sintomi fisici e gli effetti psicologici della dermatite atopica da moderata a grave possono impedire agli adolescenti di partecipare pienamente alla vita di tutti i giorni, come la scuola, lo sport e altre attività del tempo libero”, afferma la PD Lisa Weibel, MD, Capo del Dipartimento di Dermatologia Pediatrica dell’Ospedale Pediatrico Universitario di Zurigo [3]. “Dallo studio di fase III sappiamo che dupilumab riduce significativamente il prurito e le lesioni cutanee. Inoltre, migliora la qualità della vita legata alla salute negli adolescenti in questa fase importante della loro vita”. |
Non è richiesta la determinazione dei valori di laboratorio
In termini di tollerabilità, non c’è stata alcuna differenza rispetto all’esperienza precedente negli adulti: Le reazioni più comuni durante il trattamento con dupilumab sono state reazioni al sito di iniezione e congiuntivite [1,4]. Il trattamento con dupilumab non richiede la determinazione dei valori di laboratorio all’inizio o durante il trattamento [1]. Dupixent® (dupilumab) è disponibile come siringa preriempita in due dosi (200 mg e 300 mg). Negli adolescenti con dermatite atopica da moderata a grave, il dosaggio dipende dal peso corporeo. Dupilumab viene iniettato per via sottocutanea, in una dose iniziale di 400 mg (<60 kg) o 600 mg (≥60 kg), seguita da 200 mg o 300 mg ogni due settimane. L’iniezione può essere effettuata in una clinica/studio o può essere praticata a casa dal paziente, dopo le opportune istruzioni da parte del personale sanitario. Negli adolescenti, si raccomanda di somministrare dupilumab sotto la supervisione di un adulto [1].
Fonte: Sanofi-Aventis
Letteratura:
- DUPIXENT®: Informazioni per gli esperti, www.swissmedicinfo.ch, (ultimo accesso 19.03.2021)
- Langan SM, et al: Dermatite atopica. Lancet 2020; 396(10247): 345-360.
- “Swissmedic approva l’uso di DUPIXENT® (dupilumab) per il trattamento della dermatite atopica da moderata a grave, ora anche per gli adolescenti a partire dai 12 anni”, Sanofi-Aventis (Svizzera) SA, 24.02.2021.
- Simpson EL: JAMA Dermatol 2020; 156; 44-56.
- Paller AS, et al: Am J Clin Dermatol. 2020; 21(1): 119-131.
- Gandhi NA, et al: Nat Rev Drug Discov 2016; 15: 35-50.
PRATICA GP 2021; 16(5): 28