I cambiamenti nella dieta e l’esercizio fisico si rivelano spesso insufficienti come misure contro l’obesità patologica. Finora, la chirurgia bariatrica è stata l’unica misura mirata per molti pazienti obesi. Nel frattempo la situazione è cambiata. Con i mimetici dell’incretina, si può ottenere una sostanziale riduzione del peso con un parallelo miglioramento della qualità di vita. Mentre i GLP-1-RA imitano l’ormone incretino glucagone-like peptide(GLP)-1, i doppi agonisti GIP/GLP-1 attivano anche i recettori del peptide insulinotropico glucosio-dipendente (GIP).
L’obesità è una malattia complessa e multifattoriale che aumenta il rischio di malattie secondarie come il diabete di tipo 2, le malattie cardiovascolari, i danni renali e il cancro [1–3]. Sia l’obesità che il diabete sono causati e influenzati da una serie di determinanti genetici e fattori ambientali [4]. L’obesità nasce come risultato di un bilancio energetico positivo – tuttavia, le cause dello squilibrio tra energia fornita e consumata sono eterogenee e complesse.
Gli analoghi dell’incretina come “game changer” – perdere peso senza morire di fame
Il peptide simile al glucagone-1 (GLP-1) e il peptide insulinotropico dipendente dal glucosio (GIP ) sono incretine. Queste sostanze imitano gli ormoni del corpo del tratto gastrointestinale, che fanno sentire sazi, aumentano la combustione dei grassi e stimolano la secrezione di insulina [5,6]. “I farmaci per l’obesità possono replicare una, due o tre incretine in una molecola e sono quindi efficaci in misura diversa”, ha spiegato la Prof.ssa Susanne Reger-Tan, MD, Responsabile del Centro di Eccellenza per il Diabete presso la Clinica di Endocrinologia, Diabetologia e Metabolismo dell’Ospedale Universitario di Essen (D) [1]. Il trattamento con gli analoghi dell’incretina, spesso indicati dai media come “iniezioni per la perdita di peso”, porta a una sostanziale perdita di peso nelle persone affette da obesità e senza la fastidiosa sensazione di fame. “In base allo stato attuale delle conoscenze, questo nuovo approccio farmacologico è davvero una svolta nel trattamento dell’obesità”, afferma il Prof. Reger-Tan. Tuttavia, si tratta di un intervento nell’organismo. “L’uso deve avvenire dopo un’attenta analisi dei rischi e dei benefici nel contesto delle indicazioni per cui queste sostanze sono approvate, e deve essere accompagnato da una terapia di base multimodale per ottenere risultati sostenibili”.
In questo Paese sono stati approvati due GLP-1 RA e un agonista doppio GIP/GLP-1.
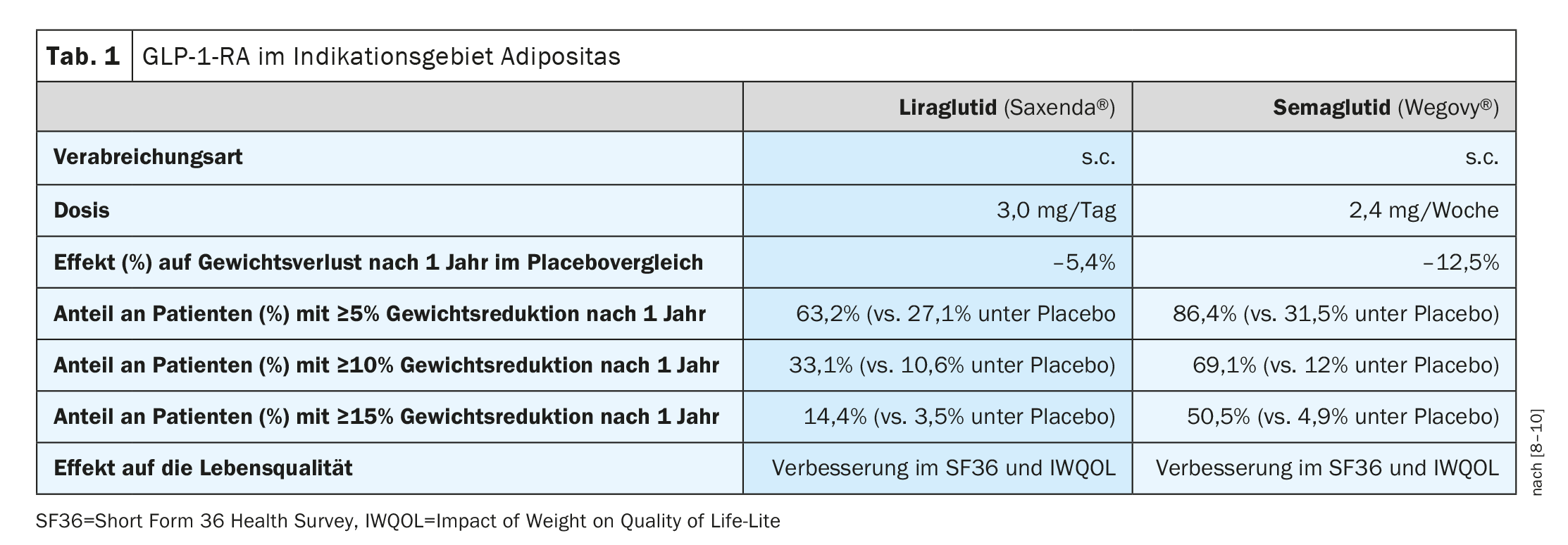
Oltre a Saxenda® (liraglutide 3 mg), disponibile da tempo in Svizzera per la terapia dell’obesità in pazienti obesi a partire dai 12 anni, anche Wegovy® (semaglutide 2,4 mg) ha ricevuto l’approvazione di Swissmedic per questa indicazione nel 2022 (Tab. 1) [7]. Entrambi i principi attivi appartengono al gruppo degli agonisti del recettore GLP-1 (GLP-1-RA) – noti anche come “incretinimici/analoghi dell’incretina”. Sia Saxenda® che Wegovy® sono analoghi a lunga durata d’azione dell’incretina GLP-1. Gli effetti di queste sostanze si basano, tra l’altro, sulla promozione della sintesi e del rilascio di insulina e sull’inibizione del rilascio di glucagone. Lo svuotamento dello stomaco viene ritardato, il che aumenta la sensazione di sazietà. Mentre Saxenda® è un farmaco approvato per gli adulti affetti da obesità, Wegovy® non è coperto dall’assicurazione sanitaria in Svizzera. Una limitazione temporanea per Saxenda® [13] si applica fino al 30.06.2026. Oltre a un IMC ≥35 kg/m2 o ≥28 kg/m2 **, è necessario mangiare almeno 500 kcal in meno al giorno rispetto a quanto il corpo brucia energia (“dieta con deficit di 500 kcal al giorno”). Inoltre, i pazienti devono dimostrare un aumento dell’attività fisica (ad esempio, con un pedometro). Il pre-trattamento con GLP-1-RA e la chirurgia bariatrica precedente o programmata sono tra i criteri di esclusione. La prescrizione può essere effettuata solo da specialisti in endocrinologia/diabetologia e presso i centri per l’obesità. Secondo l’attuale limitazione [13] Saxenda® non deve essere combinato con altri GLP-1-RA, gliptine, inibitori SGLT-2 o insulina. Quando Saxenda® viene utilizzato per la prima volta, si dovrebbe ottenere una riduzione del peso di almeno il 5% o il 7% del peso corporeo iniziale dopo 16 settimane di trattamento.
** o BMI ≥28 kg/m2 se sono presenti altre patologie concomitanti legate al peso, come il prediabete o il diabete mellito di tipo 2, l’ipertensione arteriosa o la dislipidemia.
| Agonista doppio GIP/GLP-1 La tirzepatide (Mounjaro®) è un agonista dei recettori GIP e GLP-1 da assumere una volta alla settimana. Si tratta di una singola molecola che attiva i recettori per il peptide simile al glucagone-1 (GLP-1) e il polipeptide insulinotropico dipendente dal glucosio (GIP), entrambi ormoni incretinici naturali. Entrambi i recettori GIP e GLP-1 si trovano in aree del cervello umano rilevanti per la regolazione dell’appetito. È stato dimostrato che la tirzepatide riduce l’assunzione di cibo e modula il metabolismo dei grassi. Questo ha portato a una significativa perdita di peso negli studi su pazienti obesi. Attualmente è in corso una ricerca sui triagonisti che si rivolgono al recettore del glucagone, oltre che ai recettori GIP e GLP-1. |
| a [12,13] |
Con tirzepatide (Mounjaro®) (box ), è stato approvato anche un agonista doppio GIP/GLP-1 nel 2022. La tirzepatide attiva sia il polipeptide insulinotropico dipendente dal glucosio (GIP) che i recettori del peptide 1 simile al glucagone (GLP-1). La dose iniziale di tirzepatide è di 2,5 mg una volta alla settimana. Dopo quattro settimane, la dose viene aumentata a 5 mg una volta alla settimana. Se necessario, la dose può essere aumentata a scatti di 2,5 mg, dopo almeno quattro settimane alla dose attuale. La dose massima è di 15 mg una volta alla settimana. Nel programma di sperimentazione SURPASS, a seconda della dose (5, 10 o 15 mg), è stata ottenuta una riduzione del peso corporeo del 7-14,5% con la tirzepatide entro 40-52 settimane di trattamento [11].
Letteratura:
- “Obesità: nuova era nella terapia di perdita di peso”, Società tedesca di endocrinologia (DGE), 05.09.2023.
- Collaboratori GBDO, et al: Effetti sulla salute del sovrappeso e dell’obesità in 195 Paesi per 25 anni. N Engl J Med 2017; 377: 13-27.
- Pearson-Stuttard J, et al: Onere mondiale del cancro attribuibile al diabete e all’alto indice di massa corporea: una valutazione comparativa del rischio. Lancet Diabetes Endocrinol 2018; 6:e6-e15.
- “Progetto Immunometabolismo e Microbioma intestinale ” www.udem.insel.ch/de/lehre-und-forschung/
research-focus/adipositas/immunometabolismo-e-microbioma intestinale-progetto (ultimo accesso 09.10.2023) - Nogueiras R, Nauck MA, Tschop MH: Co-agonisti degli ormoni intestinali per il trattamento dell’obesità: dal banco al letto del paziente. Nat Metab 2023; 5: 933-944.
- Ussher JR, Drucker DJ: Agonisti del recettore del peptide 1 simile al glucagone: benefici cardiovascolari e meccanismi d’azione. Nat Rev Cardiol 2023; 20: 463-474.
- Informazioni sui farmaci, www.swissmedicinfo.ch (ultimo accesso 09.10.2023)
- Wilding JPH, et al: Semaglutide una volta alla settimana negli adulti con sovrappeso o obesità. N Engl J Med 2021; 384(11): 989-1002.
- Pi-Sunyer X, et al: Uno studio randomizzato e controllato di 3,0 mg di Liraglutide nella gestione del peso. N Engl J Med 2015; 373(1): 11-22.
- Kolotkin RL, et al: Miglioramento della qualità di vita correlata alla salute in 3 anni con liraglutide 3.0 mg rispetto al placebo in partecipanti con sovrappeso o obesità. Clin 2018; 8(1): 1-10.
- Müller TD, Blüher M: Terapia dell’obesità – le farmacoterapie saranno l’alternativa alla chirurgia metabolica? [Trattamento dell’obesità: in futuro, le farmacoterapie sostituiranno la chirurgia metabolica?] Inn Med (Heidelb) 2023; 64(7): 629-635.
- “Decifrato il meccanismo d’azione della tirzepatide”, www.helmholtz-munich.de/newsroom/news/artikel/unraveling-the-mode-of-action-of-tirzepatide (ultimo accesso 10.10.2023)
PRATICA GP 2023; 18(10): 36-37