Il baricitinib, un inibitore di JAK1 e JAK2, viene spesso utilizzato per trattare l’artrite reumatoide, l’alopecia areata o una grave malattia da coronavirus. I medici australiani hanno anche studiato se il farmaco possa preservare la funzione delle cellule β e migliorare i valori metabolici nei pazienti con diabete di tipo 1 di nuova insorgenza.
La dottoressa Michaela Waibel del St Vincent’s Institute of Medical Research (SVI) di Melbourne, Australia, e i suoi colleghi hanno condotto uno studio di fase 2 in doppio cieco, randomizzato, controllato con placebo, in cui i pazienti con diabete di tipo 1 diagnosticato nei 100 giorni precedenti hanno ricevuto baricitinib (4 mg per via orale una volta al giorno) o placebo per 48 settimane [1]. L’endpoint primario era il livello medio di C-peptide, misurato dall’AUC durante un test di tolleranza con pasto misto di 2 ore. Gli endpoint secondari includevano le variazioni dei livelli di HbA1c e della dose giornaliera di insulina, nonché il controllo del glucosio mediante il monitoraggio continuo del glucosio (CGM).
Vantaggi del C-peptide
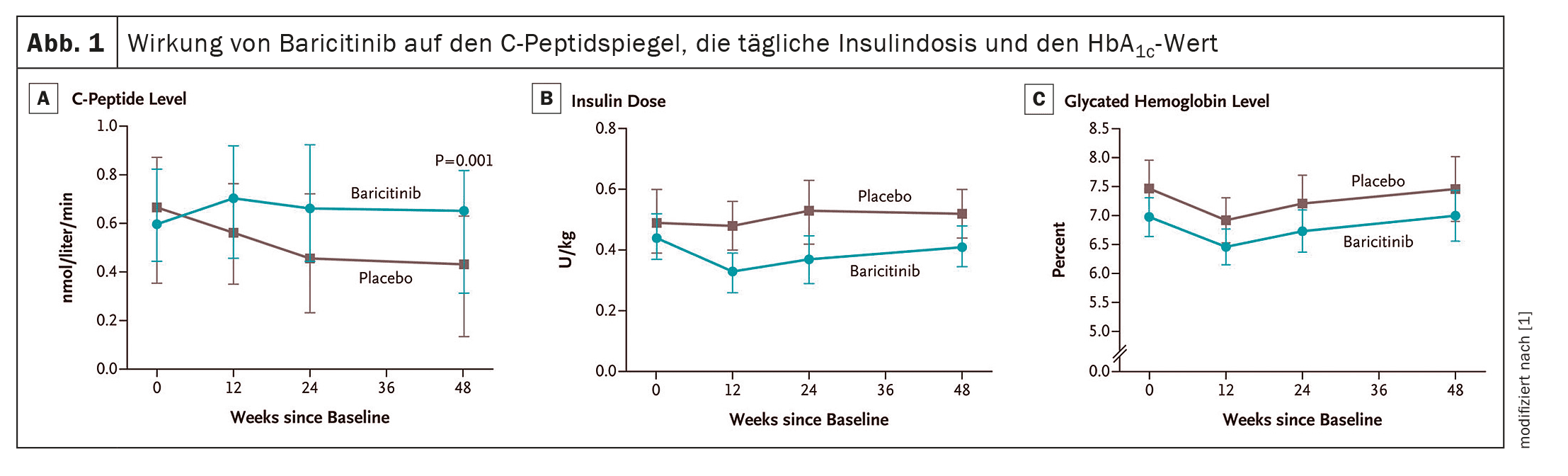
Un totale di 91 pazienti ha ricevuto baricitinib (n=60) o placebo (n=31). I risultati hanno mostrato chiari benefici in termini di endpoint primario per i pazienti che hanno ricevuto baricitinib: La mediana del livello medio di C-peptide stimolato da un pasto misto alla settimana 48 in questo gruppo era di 0,65 nmol per litro al minuto – nei controlli questo valore era solo di 0,43 nmol (p=0,001). La dose media giornaliera di insulina dopo 48 settimane era di 0,41 U per chilogrammo di peso corporeo al giorno (95% CI 0,35-0,48) nel gruppo baricitinib e 0,52 U (95% CI 0,44-0,60) nel gruppo placebo. I valori di emoglobina glicosilata erano simili nei due gruppi di studio (Fig. 1). Tuttavia, il coefficiente medio di variazione dei livelli di glucosio dopo 48 settimane, misurato mediante CGM, era del 29,6% (95% CI 27,8-31,3) nel gruppo baricitinib contro il 33,8% (95% CI 31,5-36,2) nel gruppo placebo. La frequenza e la gravità degli eventi avversi erano simili nei due gruppi di studio e nessun evento avverso grave è stato attribuito a baricitinib o al placebo.
Il dottor Waibel e i suoi colleghi hanno trovato prove che la conservazione della funzione residua delle cellule β dopo la diagnosi di diabete di tipo 1 riduce la necessità di insulina esogena ed è associata alla protezione contro le complicazioni vascolari e l’ipoglicemia grave.
Le cellule T CD8+ autoreattive nel diabete di tipo 1 si legano a un peptide autoantigene legato alle molecole HLA di classe I sulla superficie delle cellule β e vengono quindi attivate, portando al rilascio di perforina e granzimi che causano la morte delle cellule β. Gli autori hanno potuto dimostrare che l’interazione tra le cellule T CD8+ e le molecole HLA di classe I richiede molecole di segnalazione intracellulare associate alla Janus chinasi (JAK). Gli inibitori delle isoforme JAK1 e JAK2 compromettono l’espressione del complesso di istocompatibilità maggiore di classe I indotta dalle citochine nelle isole e nelle cellule dell’isolotto in coltura, compromettono l’attivazione delle cellule T CD8+ e bloccano la formazione della sinapsi immunitaria tra le cellule β e le cellule T CD8+ per prevenire la morte delle cellule β. Inoltre, le mutazioni attivanti nelle molecole di segnalazione STAT1 e STAT3, che sono a valle delle JAK, sono associate allo sviluppo del diabete autoimmune.
Il baricitinib preserva la capacità delle cellule β di secernere l’insulina
L’entità dell’effetto a 48 settimane – un aumento del 48% dei livelli mediani di C-peptide stimolato dal pasto misto nel gruppo baricitinib rispetto al placebo – era paragonabile all’entità dell’effetto di interventi come il teplizumab, la globulina antitimocita a basso dosaggio e il golimumab, che attualmente sono considerati le terapie modificanti la malattia più efficaci nei pazienti con T1D, scrivono i ricercatori. A differenza di questi agenti, che richiedono l’infusione i.v. o s.c., i pazienti non sono in grado di modificare la loro malattia. Tuttavia, a differenza di questi agenti, che richiedono l’infusione i.v. o l’iniezione s.c., l’effetto di baricitinib è stato ottenuto con l’assunzione di una singola compressa al giorno.
I risultati del loro studio indicano che il baricitinib ha migliorato le letture ottenute con il CGM. I risultati supportano l’uso del monitoraggio continuo del glucosio per valutare i risultati dell’immunoterapia nei pazienti con T1D. I pazienti del gruppo baricitinib hanno generalmente richiesto una dose giornaliera di insulina inferiore, anche se tutti i pazienti, tranne tre, hanno richiesto una terapia insulinica esogena alla fine del periodo di trattamento.
Il team del Dr. Waibel presume che in molti pazienti con diabete di tipo 1 allo stadio 3, la massa delle cellule β sia già troppo irreversibilmente danneggiata al momento della diagnosi, perché la cessazione della terapia insulinica sia un obiettivo realistico. La mediana del livello medio di C-peptide stimolato da un pasto misto al momento dello screening in questo studio era di 0,7 nmol per litro. Si può ipotizzare che iniziare il trattamento con baricitinib prima, quando i livelli di C-peptide sono più alti, possa essere più efficace nel ridurre la necessità di insulina iniettata.
I ricercatori australiani raccomandano di testare anche altri inibitori di JAK per verificarne l’effetto sul diabete di tipo 1.
Letteratura:
- Waibel M, et al.: N Engl J Med 2023; 389(23): 2140–2150; doi: 10.1056/NEJMoa2306691.
InFo DIABETOLOGIE ENDOKRINOLOGIE 2024; 1(3): 40