Nelle malattie neurodegenerative croniche come la sclerosi multipla, le cellule del sistema nervoso centrale effettuano diversi adattamenti durante la neuroinfiammazione. Le cellule più importanti coinvolte in questo processo infiammatorio sono le cellule gliali, tra cui spiccano gli astrociti. È stato riferito che gli astrociti reattivi perdono la loro funzione di supporto e assumono una funzione tossica con il progredire delle malattie.
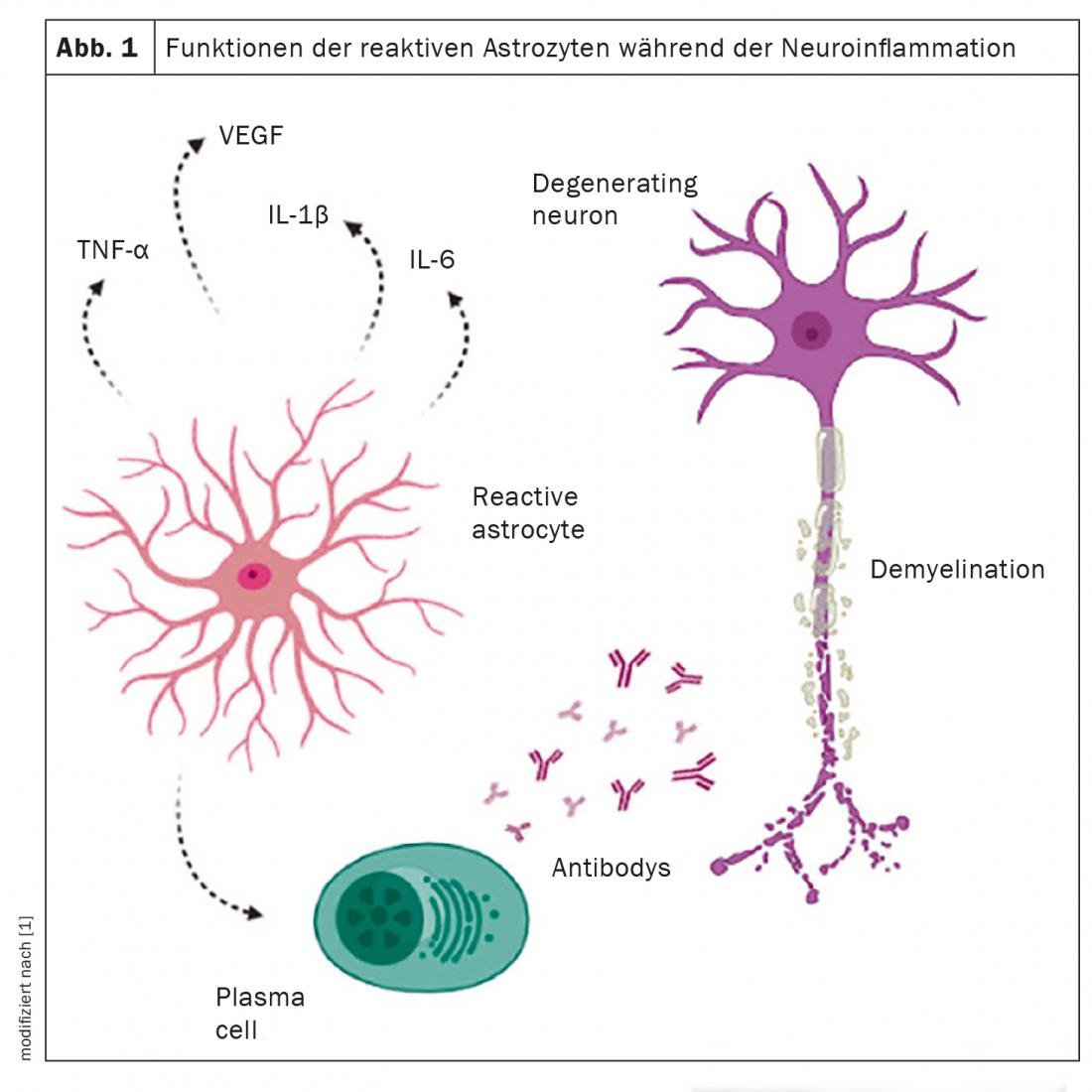
Gli astrociti sono il gruppo cellulare più abbondante in tutte le regioni del sistema nervoso centrale. A seconda del tipo di lesione, possono secernere sia citochine pro-infiammatorie (Th1, IL-1, IL-2, IL-6, IL-7 e TNF) che antinfiammatorie (Th2, IL-4, IL-10, IL-13 e TGFβ). Inoltre, sono associati a diverse funzioni fisiologiche, tra cui la secrezione di nutrienti, il mantenimento del microambiente neuronale, la permeabilità della barriera emato-encefalica e lo sviluppo di processi patologici nel cervello. Gli astrociti svolgono un ruolo complesso nella patogenesi delle malattie neurodegenerative come la sclerosi multipla (SM). Diversi studi riportano che gli astrociti reattivi perdono il loro ruolo di supporto e acquisiscono una funzione tossica con il progredire di queste malattie. Un articolo di revisione ha quindi evidenziato le caratteristiche chiave degli astrociti nello sviluppo della SM, per fornire una migliore comprensione della malattia.
Le stelle segrete del cervello
Gli astrociti appartengono alle cellule gliali, cioè alle cellule non eccitabili elettricamente del sistema nervoso. Sono costituiti da molte fibrille intrecciate, la cui struttura è chiamata filamento gliale. Possono essere suddivisi in due sottotipi principali, chiamati fibrosi o protoplasmatici, in base alle differenze nella loro morfologia cellulare e nel contenuto di filamenti gliali. Gli astrociti fibrosi si trovano principalmente nella materia bianca e hanno fibre lunghe con molti filamenti gliali nel citoplasma. Gli astrociti protoplasmatici, invece, sono diffusi nella materia grigia e hanno rami spessi. La formazione di unità neurovascolari avviene attraverso i processi astrocitari, in quanto queste cellule fungono da ponte tra i neuroni e i vasi sanguigni. Inoltre, le cellule astrocitarie possono fornire strutture e supporto metabolico ai neuroni e svolgono un ruolo importante nella regolazione della sopravvivenza neuronale, della formazione delle sinapsi e della distribuzione dei canali ionici.
I podociti astrocitici circondano strettamente le cellule endoteliali e sono fondamentali per la struttura della barriera emato-encefalica, grazie alla loro capacità di formare giunzioni strette e al loro elevato contenuto mitocondriale. Attraverso le loro interazioni con i componenti della barriera emato-encefalica (BBB), gli astrociti non solo ne regolano la funzione, ma riconoscono anche le molecole prodotte dalle cellule immunitarie periferiche, comprese le citochine. Esprimono anche numerosi recettori che permettono loro di rispondere a composti neuroattivi come neurotrasmettitori, neuropeptidi, fattori di crescita, citochine e tossine.
Il loro ruolo nel decorso della SM
La principale caratteristica patologica della SM è la presenza di lesioni infiammatorie focali e di demielinizzazione causate dalla risposta immunitaria. Il ruolo che gli astrociti svolgono nello sviluppo di queste lesioni è attivo e diverso, con diversi cambiamenti funzionali, come l’alterazione della permeabilità della barriera emato-encefalica, che promuove una risposta immunitaria deregolata al sistema nervoso centrale.
Gli astrociti rispondono alle lesioni del sistema nervoso centrale con un complesso processo di attivazione che comporta cambiamenti morfologici, trascrizionali e biochimici, nonché cambiamenti funzionali associati a una riduzione delle funzioni metaboliche omeostatiche. Questo è accompagnato da un aumento dell’espressione della proteina acida del filamento intermedio della fibrilla gliale (GFAP), che serve quindi come marcatore degli astrociti reattivi. Poiché reagiscono ai cambiamenti del loro ambiente, è difficile distinguere tra una cellula normale e un astrocita reattivo. Un astrocita reattivo è la cellula che ha reagito a una malattia o a un cambiamento del tessuto. Gli astrociti sono presenti ai margini attivi delle lesioni demielinizzanti e svolgono un ruolo chiave nella rimozione della mielina danneggiata. Queste cellule sono ipertrofiche, hanno nuclei grandi e il loro citoplasma può contenere filamenti intermedi gliali e detriti cellulari. Nelle lesioni croniche, il bordo periferico astrocitario mostra una demielinizzazione attiva e può causare ulteriori danni infiammatori che contribuiscono alla progressione della malattia.
Tuttavia, gli astrociti svolgono un doppio ruolo: non solo contribuiscono alla degenerazione assonale e alla demielinizzazione, ma creano anche un ambiente favorevole che promuove la rimielinizzazione. Tuttavia, l’influenza degli astrociti sulla patogenesi e sulla riparazione del processo infiammatorio dipende da diversi fattori, come il momento successivo alla lesione, il tipo di lesione, il microambiente circostante, l’interazione con altri tipi di cellule e i fattori che influenzano la loro attivazione. I vari fattori neurotrofici, le citochine e i fattori di crescita forniti dagli astrociti facilitano l’importante processo di riparazione nella SM. Inoltre, gli astrociti supportano ulteriormente la rimielinizzazione reclutando macrofagi/microglia, che sono responsabili della rimozione dei resti di mielina dai siti di lesione demielinizzata, consentendo così la formazione di nuova mielina.
Gli astrociti come bersaglio terapeutico
Data l’importanza degli astrociti nella patogenesi della SM, essi rappresentano un bersaglio terapeutico interessante. Nessuno dei trattamenti attualmente approvati riguarda specificamente gli astrociti. Tuttavia, diverse terapie hanno mostrato un effetto su di loro. Il dimetil fumarato (DMF) inibisce l’attivazione proinfiammatoria degli astrociti, compresa la segnalazione NF-κB, e attiva il fattore di trascrizione Nrf2, che regola la risposta antiossidante negli astrociti. Fingolimod agisce sugli astrociti inibendo la segnalazione NF-κB, riducendo l’espressione di citochine pro-infiammatorie e aumentando i fattori neurotrofici. Laquinimod riduce la segnalazione NF-κB e le risposte pro-infiammatorie degli astrociti. Il glatiramer acetato (GA) induce l’espressione di IL-10 e del fattore di crescita trasformante (TGF-β) da parte degli astrociti, ripristina le connessioni perivascolari degli astrociti con i vasi sanguigni e le sinapsi neuronali e inibisce il TNF-α.
Fonte:
- Salles D, Spindola Samartini R, de Seixas Alves MT, et al: Funzioni degli astrociti nella sclerosi multipla: una revisione. Sclerosi multipla e disturbi correlati 2022; 60: 103749.
Ulteriori letture:
- Aharoni R, Eilam R, Arnon R, et al.: Astrociti nella sclerosi multipla: componenti essenziali con diverse funzioni sfaccettate. Int J Mol Sci 2021; 22: 11.
- Ambrosini E, Remoli ME, Giacomini E, et al: Gli astrociti producono chemochine che attirano le cellule dendritiche in vitro e nelle lesioni della sclerosi multipla. J Neuropathol Exp. Neurol 2005; 64(8): 706-715.
- Batiuk MY, Martirosyan A, Wahis J, et al.: Identificazione di sottotipi di astrociti regione-specifici alla risoluzione di una singola cellula. Nat Commun 2020; 11: 1220.
InFo NEUROLOGIA & PSICHIATRIA 2022; 20(3): 35-35.