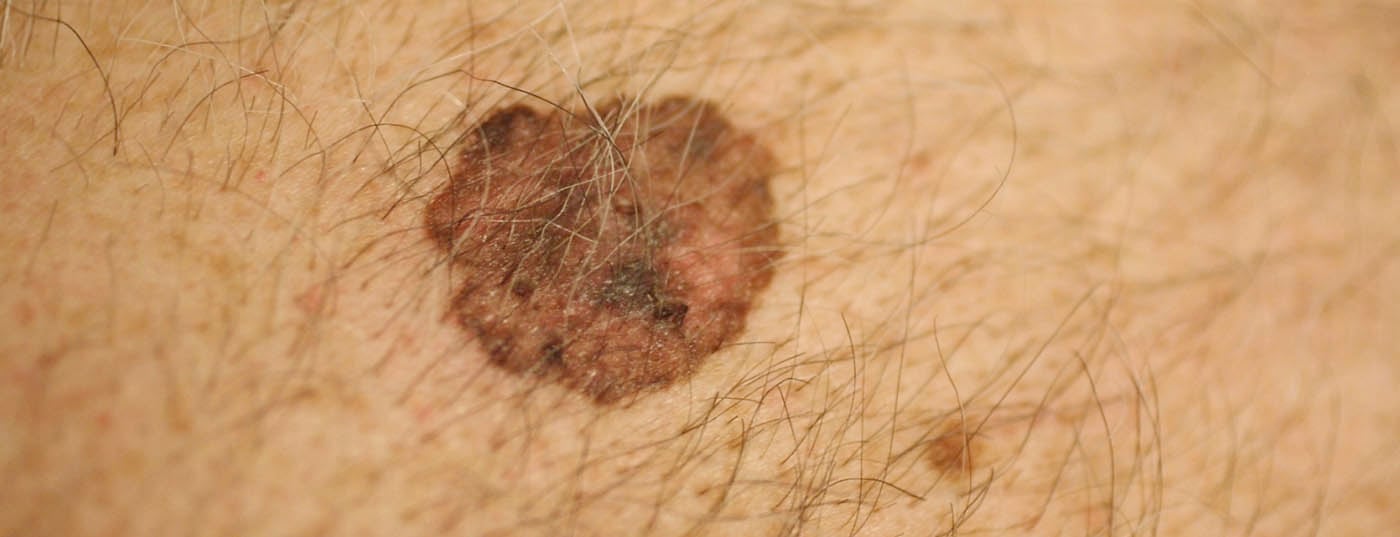
Secondo i dati dello studio attuale, più della metà dei pazienti che hanno ricevuto il trattamento adiuvante con l’anticorpo anti-PD-1 erano liberi da recidive dopo quattro anni. Si tratta di un’ulteriore conferma del track record di questa opzione terapeutica nel trattamento dei tumori melanocitici in fase avanzata con o senza mutazione BRAF.
Nel campo delle opzioni terapeutiche per i tumori melanocitici, ci sono stati molti progressi nell’ultimo decennio. In passato, per i pazienti con melanoma metastatico erano disponibili solo chemioterapie, che di solito davano solo una risposta minore e a breve termine [1]. Oggi, gli standard clinici attuali per l’immunoterapia o la terapia mirata nel melanoma metastatico non resecabile sono gli anticorpi bloccanti PD-1, la combinazione dell’inibitore PD-1 nivolumab e dell’inibitore CTLA-4 ipilimumab, nonché la combinazione di inibitori BRAF e MEK [2]. Con queste opzioni terapeutiche, si potrebbe ottenere un miglioramento significativo della sopravvivenza a lungo termine dei pazienti in stadio avanzato.
Gli inibitori del checkpoint sono efficaci indipendentemente dallo stato di mutazione BRAF
Solo il 40-50% circa di tutti i pazienti con melanoma presenta una mutazione BRAF adeguatamente bloccabile [3]. Gli inibitori del checkpoint immunitario sono disponibili come opzione di trattamento per i pazienti affetti da melanoma, indipendentemente dallo stato di mutazione. I recenti dati a lungo termine sugli inibitori del checkpoint immunitario sono promettenti. Con la combinazione di ipilimumab e nivolumab, sono stati raggiunti tassi di sopravvivenza significativamente migliori nei pazienti con metastasi a distanza non resecabili, rispetto alle opzioni terapeutiche precedenti. Sia le linee guida EADO/EORTC che le attuali linee guida ESMO raccomandano l’immunoterapia con inibitori del checkpoint come terapia di prima linea per il melanoma metastatico [4,5]. Anche nel contesto adiuvante, dopo un intervento chirurgico completo per le metastasi locoregionali, gli anticorpi PD-1 nivolumab e pembrolizumab mostrano circa un dimezzamento del tasso di recidiva, in modo che non vi sia uno stadio metastatico a distanza.
CheckMate 238 – dati impressionanti a 4 anni su nivolumab
Gli inibitori di PD-1 possono essere utilizzati come adiuvante nel melanoma maligno in stadio avanzato III o IV. Nel 2018, nivolumab è stato approvato dall’EMA come terapia adiuvante. L’obiettivo primario della terapia adiuvante è quello di prolungare la sopravvivenza globale. Tuttavia, poiché il beneficio di tale terapia può essere dimostrato solo dopo diversi anni, la sopravvivenza libera da recidiva si è affermata come un altro endpoint. Lo studio CheckMate 238 (panoramica 1) ha dimostrato la superiorità della terapia adiuvante con nivolumab rispetto a ipilimumab negli stadi IIIB/C e IV [6]. Il braccio nivolumab ha mostrato un miglioramento significativo della sopravvivenza libera da recidiva (RFS): il 70% contro il 60% era libero da recidiva a 12 mesi, il 66% contro il 53% a 18 mesi e il 63% contro il 50% a 24 mesi. La sopravvivenza libera da recidiva a 36 mesi è stata del 58% con nivolumab rispetto al 45% con ipilimumab e la tossicità è stata significativamente inferiore rispetto a ipilimumab, con un minor numero di eventi avversi di grado 3-4 (14,4% rispetto al 45,9%) [7].

Anche i dati a 4 anni dello studio CheckMate 238, pubblicato nel 2020, erano favorevoli [8]. La superiorità di nivolumab in termini di sopravvivenza libera da recidiva (RFS) rispetto a ipilumab è rimasta in questo periodo. A 4 anni, la RFS con nivolumab era del 51,7% (95% CI; 46,8-56,3) rispetto al 41,2% (36,4-45,9) con ipilimumab (hazard ratio 0,71; 95% CI; 0,60-0,86; p=0,0003). La sopravvivenza globale (OS) a 4 anni è stata del 77,9% (95% CI; 73,7-81,5) nel gruppo nivolumab e del 76,6% (72,2-80,3) nel gruppo ipilimumab (HR 0,87; 95% CI; 0,66-1,14; p=0,31).
Studio IMMUNED – risultati intermedi del trattamento combinato
In questo studio di fase II, 167 pazienti in stadio IV, dopo resezione completa e senza evidenza di metastasi recenti, hanno ricevuto nivolumab 3 mg/kg di peso corporeo o nivolumab 1 mg/kg di peso corporeo in combinazione con ipilimumab 3 mg/kg di peso corporeo per quattro somministrazioni seguite da nivolumab 3 mg/kg di peso corporeo e un terzo gruppo ha ricevuto placebo [9]. Dopo 24 mesi, la sopravvivenza libera da recidiva era del 70% nel trattamento combinato, del 42% nel gruppo nivolumab e del 14% con il placebo.
Letteratura:
- Ugurel S, et al: Sopravvivenza dei pazienti con melanoma metastatico avanzato: l’impatto delle nuove terapie – aggiornamento 2017. Eur J Cancer 2017; 83: 247-257.
- Hoeller C: Melanoma: le questioni aperte degli attuali standard terapeutici vengono affrontate successivamente. Compass Oncol 2020; 7: 117-118.
- Schadendorf D, et al: Lancet 2018; 392: 971-984.
- Garbe C, et al. Eur J Cancer 2020; 126: 159-177.
- Michielin O, et al: Melanoma cutaneo: Linee guida di pratica clinica ESMO per la diagnosi, il trattamento e il follow-up. Ann Oncol 2019; 30(12): 1884-1901.
- Jeffrey S, et al: Terapia adiuvante con nivolumab (NIVO) rispetto a ipilimumab (IPI) dopo resezione completa del melanoma in stadio III/IV: risultati aggiornati di uno studio di fase III (CheckMate 238). J Clin Oncol 2018; 36(15): 9502.
- Lamos C, Hunger RE. Inibitori del checkpoint – indicazione e uso nei pazienti con melanoma [Checkpoint inhibitors-indications and application in melanoma patients]. Z Rheumatol 2020;79(8): 818-825.
- Ascierto PA, et al: Nivolumab adiuvante rispetto a ipilimumab nel melanoma resecato in stadio IIIB-C e in stadio IV (CheckMate 238): risultati a 4 anni di uno studio multicentrico, in doppio cieco, randomizzato, controllato, di fase 3. The Lancet – Oncology 2020; 21(11): 1465-1477.
- Zaremba A, et al: Immunoterapia nel melanoma maligno. Internist 2020; 61, 669-675.
- Clinicaltrials.gov: https://clinicaltrials.gov/ct2/show/NCT02388906, (ultimo accesso 07.04.2021)
PRATICA DERMATOLOGICA 2021; 31(2): 40