Il numero di persone con SM in Svizzera è in aumento. Le indagini attuali dipingono un quadro allarmante. Ciò rende ancora più importante un trattamento efficace, adattato alla situazione di vita del paziente e al decorso della malattia. L’obiettivo dovrebbe essere quello di mantenere la partecipazione alla vita sociale il più a lungo possibile.
Fino ad oggi, si riteneva che in Svizzera vivessero circa 10.000 persone affette da sclerosi multipla (SM). Una recente indagine del Registro della SM ha dovuto rivedere questa ipotesi: almeno 15.000 persone soffrono della malattia – e la tendenza è ancora in aumento [1]. Anche il rapporto tra i sessi si sta spostando ulteriormente verso le donne. Le nuove proiezioni indicano che il 73% delle donne ne è colpito. Non è certo che questo sviluppo sia dovuto esclusivamente alla crescita della popolazione e all’aumento dell’aspettativa di vita. I meccanismi di sviluppo della malattia sono ancora in fase di decifrazione. I primi risultati indicano una disposizione genetica e una notevole influenza dei fattori ambientali. La ricerca attuale si concentra, tra l’altro, sulla neurodegenerazione [2,3]. È in gran parte responsabile dello sviluppo di disabilità dovute alla trasposizione assonale e alla perdita di neuroni. L’aumento della neurodegenerazione, che molto probabilmente inizia prima di quanto si pensasse, sembra essere una delle cause principali della progressione della malattia. La ricerca sui biomarcatori, come la proteina leggera del neurofilamento, che rileva il danno assonale o neuronale generale e può essere utilizzata per valutare meglio la prognosi del singolo paziente, sono i primi passi promettenti verso una terapia personalizzata [4].
Dal punto di vista clinico, si può distinguere il decorso recidivante-remittente da quello progressivo primario e secondario. Oltre ai sintomi neurologici, molti pazienti soffrono di deficit cognitivi, affaticamento e depressione manifesta. Poiché la SM si manifesta in forme e sfaccettature diverse, la gestione del trattamento deve essere di conseguenza completa, competente e adattata individualmente al paziente.
Il modello a pilastri come base per la terapia
Prima si può iniziare la terapia, meglio è. Oggi sono disponibili diverse opzioni terapeutiche efficaci che spesso possono rallentare notevolmente la progressione della malattia. Fondamentalmente, la terapia deve basarsi su quattro pilastri (tab. 1). L’obiettivo del trattamento è ridurre l’entità delle reazioni infiammatorie, stabilizzare le limitazioni funzionali e migliorare i sintomi che le accompagnano. L’obiettivo deve essere uno stato NEDA (No Evidence of Disease Activity)-3, cioè l’assenza di nuove lesioni alla risonanza magnetica, di ricadute della malattia e di progressione della disabilità.

Negli ultimi anni, sono stati sviluppati diversi regimi di trattamento per i diversi decorsi della malattia (tab. 2). I preparati possono essere suddivisi in quattro gruppi in base al loro meccanismo d’azione:
- Inibizione della proliferazione: azatioprina, cladribina, mitoxantrone, teriflunomide.
- Immunomodulazione: dimenthyl fumarate, glatiramer acetato, iterferone-β, iterferone-β pegilato, teriflunomide.
- Inibizione della migrazione: Fingolimod, Natalizumab
- Deplezione: Alemtuzumab, Rituximab/Ocrelizumab
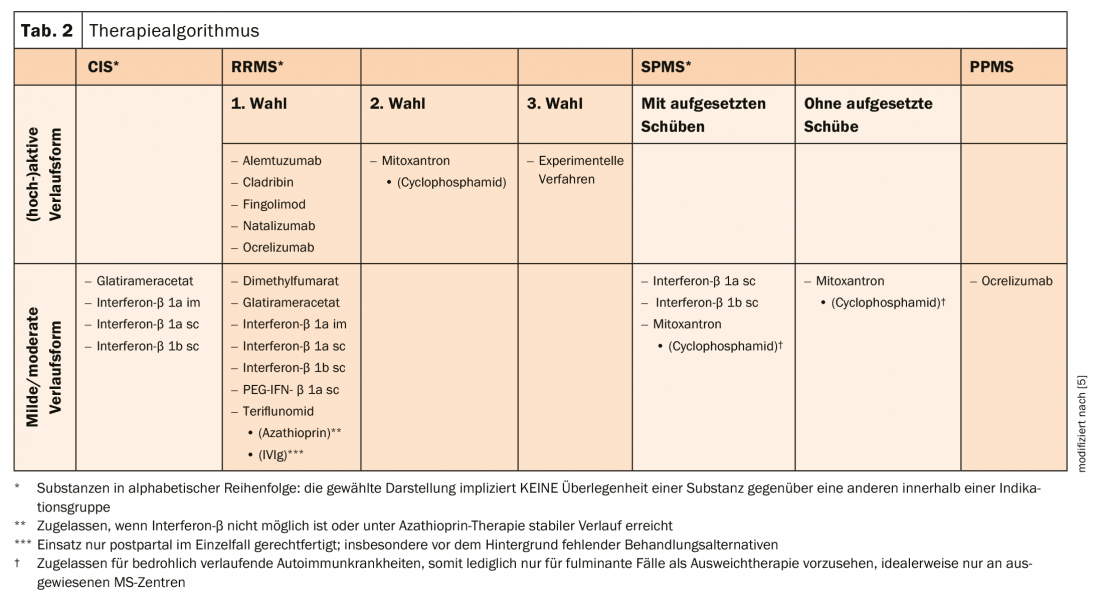
Nei decorsi moderati, l’interferone-β (IFN-β), il glatiramer acetato, le immunoglobuline e l’azatioprina sono utilizzati come terapia di base per il decorso recidivante-remittente. Questi preparati immunomodulatori inibiscono i processi dannosi e promuovono quelli protettivi del sistema immunitario. Nei pazienti con un decorso (altamente) attivo (cioè molte ricadute gravi in un breve periodo di tempo e/o una risonanza magnetica (altamente) attiva) o nei pazienti che non rispondono sufficientemente agli immunoterapici di base, vengono utilizzati i farmaci della terapia di escalation. Queste includono, ad esempio, terapie orali a breve termine come le compresse di cladribina, che colpiscono selettivamente e periodicamente i linfociti nella SM recidivante-remittente. Riducendo la conta dei linfociti, si dovrebbe ridurre la frequenza delle ricadute. Un’altra opzione è quella di bloccare il recettore della sfingosina-1-fosfato con il fingolimod, che trattiene le cellule immunitarie nei linfonodi. Le terapie infusionali mensili con l’anticorpo monoclonale natalizumab impediscono anche alle cellule immunitarie di migrare nei siti infiammatori del SNC [6–8].
Letteratura:
- www.multiplesklerose.ch/das-schweizer-ms-register/
- Ziemssen T, Derfuss T, de Stefano N, et al: Ottimizzare il successo del trattamento nella sclerosi multipla. J Neurol 2016; 263: 1053-1065
- De Stefano N, Airas L, Grigoriadis N, et al: Rilevanza clinica delle misure di volume cerebrale nella sclerosi multipla. Farmaci CNS 2014; 28: 147-156
- Barro C, Benkert P, Disanto G, et al: Il neurofilamento sierico come predittore del peggioramento della malattia e dell’atrofia del cervello e del midollo spinale nella sclerosi multipla. Cervello 2018; 141(8): 2382-2391
- www.multiple-sklerose.com/medikamente-zur-behandlung/
- www.neurologen-und-psychiater-im-netz.org/neurologie/erkrankungen/multiple-sklerose-ms/therapie
- www.mpg.de/411133/forschungsSchwerpunkt
- DGN/KKNMS: Linea guida sulla diagnosi e la terapia della sclerosi multipla
InFo NEUROLOGIA & PSICHIATRIA 2020; 18(1): 22-23