Una revisione ha riassunto i risultati di quattro studi randomizzati in doppio cieco, controllati con placebo o con riferimento, su un preparato combinato di Sabal-Urtica in uomini di età superiore ai 50 anni con LUTS associati all’IPB. Il fitopreparato si è rivelato una valida alternativa ai farmaci sintetici. Il profilo favorevole degli effetti collaterali è un punto a favore, soprattutto per la terapia a lungo termine.
In circa la metà degli uomini di età superiore ai 50 anni, si verificano cambiamenti tissutali benigni nella prostata, sotto forma di un aumento del tessuto connettivo, del muscolo e/o delle cellule epiteliali (iperplasia prostatica benigna, BPH). A causa dell’iperplasia dell’organo, la compressione dell’uretra può portare a un aumento della resistenza all’uscita della vescica – ostruzione prostatica benigna (BPO). L’IPB è la causa principale dei sintomi del tratto urinario inferiore ( LUTS), che comprendono la ritenzione vescicale, la minzione e i sintomi della minzione [1]. In particolare, gli antagonisti degli α1-adrenocettori, gli inibitori della 5α-reduttasi e i fitoterapici sono utilizzati come terapia di prima linea per i sintomi dei LUTS associati all’IPB [2].
C’è un crescente interesse per le opzioni di trattamento fitoterapico, non da ultimo perché alcuni pazienti sono insoddisfatti degli effetti avversi dei farmaci sintetici [3]. La terapia con antagonisti dell’α1-adrenoccettore e inibitori della 5α-reduttasi, ad esempio, può essere associata a effetti collaterali sessuali come disfunzione erettile e disturbi dell’eiaculazione [4]. Inoltre, per la maggior parte degli antagonisti degli α-adrenocettori viene generalmente riportato un rischio relativamente elevato di effetti collaterali legati alla vascolarizzazione [5]. Gli effetti collaterali cardiovascolari, come l’ipotensione, accompagnata da vertigini o sincope, colpiscono soprattutto gli uomini anziani – cioè il gruppo principale di pazienti con LUTS/BPH che richiedono una terapia farmacologica [6–8].
Il farmaco PRO 160/120 (Prostaplant®-F) è una promettente alternativa fitoterapica per il trattamento dei LUTS. Il preparato combinato contiene 160 mg di estratto di frutto di saw palmetto (Serenoa repens o Sabal serrulata) e 120 mg di estratto secco di radice di ortica (Urtica dioica) come principali principi attivi farmacologici (box ) [9].
| Meccanismi d’azione di PRO 160/120 La preparazione fitofarmacologica combinata di estratti di Sabal (estratto di saw palmetto) e Urtica (radice di ortica) mostra effetti sinergici. Tra l’altro, viene indotta una conversione del testosterone in diidrotestosterone e l’attività dell’aromatasi [18]. Il rilassamento del tessuto prostatico ingrossato determina una riduzione della pressione sull’uretra. Grazie al suo effetto antinfiammatorio, PRO 160/120 riduce l’irritazione della prostata [19]. È stato dimostrato che l’estratto di Saw palmetto inibisce la 5α-reduttasi senza mostrare attività di legame con gli androgeni [20,21] e provoca un’inibizione non competitiva degli α1-adrenocettori umani in vitro [22]. Inoltre, inibisce selettivamente i recettori muscarinici nel tratto urinario inferiore [23,24]. L’estratto di radice di ortica inibisce l’attività della Na+, K+-ATPasi della membrana prostatica, che può limitare il metabolismo e la crescita delle cellule prostatiche [25]. Inoltre, per entrambi gli agenti sono stati riportati effetti antiproliferativi, antiflogistici e antiedematosi [27,28]. |
Punteggio internazionale dei sintomi della prostata (I-PSS)
Negli studi inclusi nella revisione, il miglioramento dei sintomi è stato valutato utilizzando l’International Prostate Symptom Score (I-PSS) [10–13]. Si tratta di uno strumento di misurazione affidabile e valido, comunemente utilizzato per valutare i LUTS associati all’IPB, con sette domande sulla minzione, ciascuna con un punteggio da 0 a 5 [2,14]. Le domande di solito si riferiscono al mese precedente. In tutti e quattro gli studi [10–13], è stato ottenuto un miglioramento di oltre tre punti nel punteggio totale dell’I-PSS, che è classificato come un cambiamento clinicamente significativo [16]. I seguenti parametri sono stati raccolti come ulteriori endpoint: Volume del tempo di urina o volume del tempo di urina, tempo del flusso di urina, flusso medio di urina, flusso massimo di urina, volume della minzione, durata della minzione (tempo di svuotamento della vescica), volume dell’urina residua, volume della prostata, qualità della vita. Inoltre, sono stati registrati gli eventi avversi e i segnali di sicurezza diagnostica di laboratorio.
I risultati importanti dello studio in sintesi
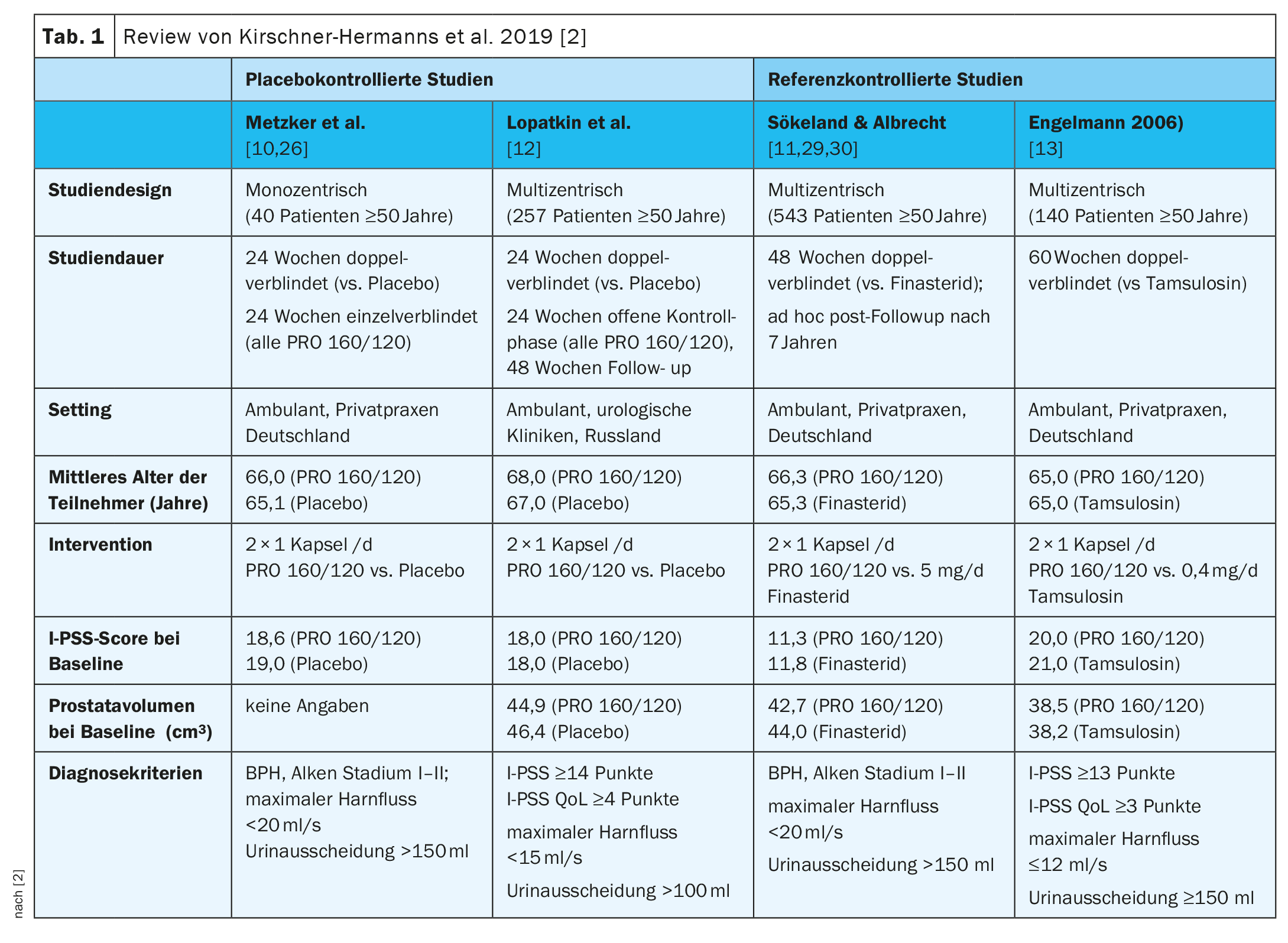
I dati principali dei quattro studi sono riportati nella Tabella 1 [2,10–13]. In Metzker et al. e Lopatkin et al. erano controllati con placebo e in Engelmann et al. e Sökeland & Albrecht per gli studi controllati di riferimento [2,10–13].
Metzker et al (n=40) [10]: Nella fase di trattamento in doppio cieco, l’I-PSS medio è diminuito dai valori basali di 18,6 punti nel gruppo PRO 160/120 e di 19,0 punti nel gruppo placebo a 11,1 e 17,6 punti alla settimana 24, rispettivamente (p=0,002; test U a due lati). In una valutazione post-hoc di questi risultati, che si è concentrata sulle voci dell’I-PSS che valutano i cosiddetti sintomi irritativi, è stato dimostrato che c’è stato un miglioramento statisticamente significativo dell’urgenza urinaria e della frequenza della minzione sotto il PRO 160/120 durante questa fase di trattamento [26]. Nella successiva fase di trattamento in singolo cieco, l’I-PSS è diminuito anche nei pazienti che sono passati dal placebo al trattamento con PRO 160/120. Tuttavia, alla settimana 48, c’è stato ancora un vantaggio a favore del gruppo che ha partecipato al braccio di trattamento attivo (PRO 160/120) in entrambe le fasi dello studio (p=0,009; test U a due lati).
Lopatkin et al. (n=257) [12]: Dopo la fase di trattamento in doppio cieco, è stata osservata una differenza di gruppo statisticamente significativa nel declino dell’I-PSS a favore del PRO 160/120; -6 punti nel braccio di trattamento e -4 punti nel braccio placebo (p<0,01, test U unilaterale stratificato). Al termine della fase di controllo, l’I-PSS si è ridotto di altri 2 punti nei pazienti ex placebo (che ora erano anche trattati con PRO 160/120) e di un altro punto nei pazienti che erano stati trattati con PRO 160/120 dall’inizio dello studio. Questa differenza tra i due gruppi di trattamento era anche statisticamente significativa (p=0,01, test U stratificato unilaterale). Al termine della fase di controllo, la riduzione dell’I-PSS medio in entrambi i gruppi di trattamento è stata di sette punti rispetto al basale, indicando che i pazienti ex placebo hanno beneficiato del trattamento con PRO 160/120 nella stessa misura dei pazienti che erano già stati trattati con PRO 160/120 dall’inizio del trattamento in doppio cieco [15]. Dopo la fase di controllo, 213 pazienti (PRO 160/120: 106; placebo: 107) hanno partecipato alla successiva estensione in aperto dello studio (settimane 49-96) [17]. Nei pazienti senza punteggi I-PSS mancanti al basale (PRO 160/120: 106; placebo: 103), è stata osservata un’ulteriore riduzione mediana del punteggio di 1 punto in ciascun gruppo, con una riduzione mediana complessiva di 9 punti in entrambi i gruppi rispetto al basale. Ciò corrisponde a una riduzione del 52,9% del punteggio totale I-PSS rispetto al basale.
Sökeland & Albrecht (n=543) [11]Al termine dello studio, i sintomi dei pazienti trattati con PRO 160/120 erano migliorati in misura simile rispetto a quelli trattati con finasteride, con l’I-PSS che aumentava da 11,3 ± 6,5 punti (PRO 160/120) e 11,8 ± 6,6 punti (finasteride) al basale a 8,2 ± 5,8 punti (PRO 160/120) e 8,0 ± 5,7 punti (finasteride) alla settimana 24. 11,8 ± 6,6 punti (finasteride) al basale a 8,2 ± 5,8 punti (PRO 160/120) e 8,0 ± 5,7 punti (finasteride) alla settimana 24 e 6,5 ± 5,8 punti (PRO 160/120) e 6,2 ± 5,2 punti (finasteride) alla settimana 48 (medie ± SD). Anche il miglioramento della qualità di vita secondo il punteggio C dell’AUA è stato simile rispetto alla finasteride. L’aumento del flusso massimo di urina con PRO 160/120 (+1,9 ml/s) e finasteride (+2,4 ml/s) si è rivelato terapeuticamente comparabile in un intervallo di equivalenza di ±1,5 ml/s (p=0,037; t-test modificato per ipotesi spostate).
Engelmann et al. (n=140) [13]: Il punteggio totale IPSS è migliorato in media di 9 punti al termine del trattamento in entrambi i gruppi, rispetto a un punteggio basale di circa 20 punti. Un totale del 32,4% dei pazienti trattati con PRO 160/120 e del 27,9% dei pazienti trattati con tamsulosina sono stati responder (cioè punteggio totale IPSS ≤7 alla fine del trattamento; p=0,034, test di non inferiorità Farrington-Manning; soglia di non inferiorità 10%). In un’analisi di sottogruppo in base al punteggio I-PSS al basale, PRO 160/120 e tamsulosina sono stati comparabilmente efficaci sia nei pazienti con sintomi moderati (I-PSS al basale ≤19 punti) che nei pazienti con sintomi gravi (I-PSS al basale ≥20 punti). La qualità di vita dei pazienti è migliorata di una mediana di 2 punti nel gruppo PRO 160/120 e di 1 punto nel gruppo tamsulosina (valori basali: 3 punti e 4 punti, rispettivamente; mediane).
Letteratura:
- S2e-Leitlinie Diagnostik und Therapie des Benignen Prostatasyndroms (BPS), Registernummer: 043-034, Langversion 5.0 – Stand Februar 2023.
- Kirschner-Hermanns R, Funk P, Leistner N: WS PRO 160 I 120 mg (una combinazione di estratto di sabal e urtica) nei pazienti con LUTS correlati all’IPB. Ther Adv Urol 2019 Oct 11;11:1756287219879533.
- Geavlete P, Multescu R, Geavlete B: L’estratto di Serenoa repens nel trattamento dell’iperplasia prostatica benigna. Ther Adv Urol 2011; 3: 193-198.
- Mirone V, et al: L’attuale trattamento dell’iperplasia prostatica benigna: impatto sulla funzione sessuale e gestione degli eventi avversi sessuali correlati. Int J Clin Pract 2011; 65: 1005-1013.
- Nickel JC, Sander S, Moon TD: Una meta-analisi del profilo di sicurezza vascolare e dell’efficacia dei bloccanti alfa-adrenergici per i sintomi correlati all’iperplasia prostatica benigna. Int J Clin Pract 2008; 62: 1547-1559.
- Logan IC, Witham MD: Efficacia dei trattamenti per l’ipotensione ortostatica: una revisione sistematica. Invecchiamento 2012; 41: 587-594.
- Man in’t Veld AJ: IPB sintomatica e ipertensione: la comorbidità influisce sulla qualità della vita? Eur Urol 1998; 34(Suppl. 2): 29-36.
- Schimke L, Schimke J: Implicazioni urologiche delle cadute negli anziani: sintomi del tratto urinario inferiore e farmaci alfa-bloccanti. Urol Nurs 2014; 34: 223-229.
- Informazioni sui farmaci, www.swissmedicinfo.ch,(ultimo accesso 15.09.2023)
- Metzker H, Kieser M, Hölscher U: Efficacia di un preparato combinato Sabal-Urtica nel trattamento dell’iperplasia prostatica benigna (BPH). Urologo B 1996; 36: 292-300.
- Sökeland J, Albrecht J: Combinazione di estratto di sabal e urtica vs. finasteride nell’IPB (stad. da I a II secondo Alken). Confronto dell’efficacia terapeutica in uno studio in doppio cieco di un anno. Urologo A 1997; 36: 327-333.
- Lopatkin N, et al: Efficacia e sicurezza a lungo termine di una combinazione di estratto di sabal e urtica per i sintomi del tratto urinario inferiore – uno studio multicentrico in doppio cieco, controllato con placebo. World J Urol 2005; 23: 139-146.
- Engelmann U, et al.: Efficacia e sicurezza di una combinazione di estratto di sabal e urtica nei sintomi del tratto urinario inferiore. Uno studio randomizzato, in doppio cieco rispetto alla tamsulosina. Arzneimittelforschung 2006; 56: 222-229.
- McConnell J, et al. (Eds): Disfunzione del tratto urinario inferiore maschile. Valutazione e gestione. In: Atti della6ª Consultazione Internazionale sui Nuovi Sviluppi nel Cancro alla Prostata e nelle Malattie della Prostata, Parigi, Francia, 24-27 giugno 2005. Pubblicazioni sulla salute, 2006.
- Sivkov A, et al: Efficacia e sicurezza a lungo termine di una combinazione di estratti di sabal e urtica nei LUTS – uno studio multicentrico in doppio cieco, controllato con placebo. Urologist A 2001; 40(Suppl. 1): S19.
- Barry MJ, et al: Misure dello stato di salute specifiche per l’iperplasia prostatica benigna nella ricerca clinica: quanto è percepibile dai pazienti il cambiamento nell’indice dei sintomi dell’American Urological Association e nell’indice di impatto dell’iperplasia prostatica benigna? J Urol 1995; 154: 1770-1774.
- Lopatkin et al: Efficacia e sicurezza di una combinazione di estratto di Sabal e Urtica nei sintomi del tratto urinario inferiore – follow-up a lungo termine di uno studio multicentrico in doppio cieco, controllato con placebo. Int Urol Nephrol 2007; 39: 1137-1146.
- Madersbacher S, et al.: Associazione tra le prescrizioni di PRO 160/120 e l’incidenza delle complicanze dell’iperplasia prostatica benigna in Germania: uno studio di coorte retrospettivo. Postgrad Med 2023; 135(2): 149-154.
- Koch E: Estratti dai frutti del saw palmetto (Sabal serrulata) e dalle radici dell’ortica (Urtica dioica): valide alternative nel trattamento medico dell’iperplasia prostatica benigna e dei sintomi associati del tratto urinario inferiore. Planta Med 2001; 67(6): 489-500.
- Casarosa C, et al.: Mancanza di effetti di un estratto liposterolico di Serenoa repens sui livelli plasmatici di testosterone, ormone follicolo-stimolante e ormone luteinizzante. Clin Ther 1988; 10: 585-588.
- Düker EM, Kopanski L, Schweikert HU: Inibizione dell’attività della 5α-reduttasi da parte degli estratti di Sabal serrulata. Planta Med 1989; 55: 587.
- Goepel M, et al.: Gli estratti di Saw palmetto inibiscono in modo potente e non competitivo gli 1-adrenocettori umani in vitro. Prostata 1999; 38: 208-215.
- 23 Abe M, et al: Caratteristiche di legame al recettore farmacologicamente rilevanti e attività inibitoria della 5α-reduttasi degli acidi grassi liberi contenuti nell’estratto di saw palmetto. Biol Pharm Bull 2009; 32: 646-650.
- Suzuki M, et al.: Caratteristiche di legame dei recettori muscarinici e alfa 1-adrenergici dell’estratto di saw palmetto nel tratto urinario inferiore del ratto. Urologia 2007; 69: 1216-1220.
- Hirano T, Homma M, Oka K: Effetti degli estratti di radice di ortica e dei loro componenti steroidei sulla Na+, K+-ATPasi dell’iperplasia prostatica benigna. Planta Med 1994; 60: 30-33.
- Popa G, Hägele-Kaddour H, Walther C: Efficacia sintomatica di un preparato combinato Sabal-Urtica nella terapia della sindrome prostatica benigna. Risultati di uno studio in doppio cieco controllato con placebo. MMW Fortschr Med 2005; 147(Originalien III): 103-108.
- Koch E, Biber A: Effetti farmacologici degli estratti di sabal e urtica come base per una terapia farmacologica razionale dell’iperplasia prostatica benigna. Urologo B 1994; 34: 90-95.
- Lichius JJ, et al.: Effetto antiproliferativo di una frazione polisaccaridica di un estratto metanolico al 20% di radici di ortica su cellule epiteliali della prostata umana (LNCaP). Farmacia 1999; 54: 768-771.
- Sökeland J: L’estratto combinato di sabal e urtica rispetto alla finasteride negli uomini con iperplasia prostatica benigna: analisi del volume della prostata e dell’esito terapeutico. BJU Int 2000; 86: 439-442.
- Sökeland J, Schläfke S: Effetti a lungo termine del PRO 160/120 nei pazienti con BPH. Uro-News Therapie Report aktuell 2007; 164: 2-3.