La modifica dello stile di vita (esercizio fisico, dieta) e la metformina rimangono i capisaldi nel trattamento del diabete mellito di tipo 2. Prima di iniziare la terapia antidiabetica, si raccomanda di fissare un obiettivo individuale di HbA1c. I vantaggi dei nuovi farmaci antidiabetici orali (OAD) sono il basso rischio di ipoglicemia, la perdita di peso o la neutralità del peso e di solito la buona tollerabilità. Gli inibitori SGLT2 inducono una perdita di glucosio a livello renale e sono efficaci solo con una funzione renale preservata. Grazie al nuovo meccanismo d’azione, possono essere combinati bene con altri OAD. In base all’efficacia e al profilo degli effetti collaterali dei nuovi farmaci antidiabetici, si dovrebbe cercare una combinazione terapeutica ottimale e individuale per ogni paziente.
Grazie alle nuove scoperte e agli sviluppi, sono stati stabiliti nuovi principi importanti nel trattamento del diabete di tipo 2 e sono stati inseriti nelle attuali linee guida: Un obiettivo individuale di HbA1c nell’intervallo 6,5-8,0% deve essere fissato per ogni paziente, tenendo conto della durata della malattia, delle malattie concomitanti, dell’aspettativa di vita, delle risorse personali e sociali. Una riduzione delle complicanze macrovascolari può essere ottenuta anche se si raggiunge un controllo ottimale sostenibile del diabete fin dall’inizio della malattia (HbA1c 6,5-7,0%). D’altra parte, una riduzione dell’HbA1c <7,0% “a qualsiasi costo” porta a frequenti ipoglicemie e a un aumento della mortalità in caso di complicanze cardiovascolari già esistenti e di lunga durata della malattia [1]. Sebbene il ruolo della metformina come terapia di prima linea insieme alla modifica dello stile di vita sia indiscusso, ci sono numerose opzioni di combinazione tra cui scegliere nella seconda fase dopo l’introduzione delle incretine e delle gliflozine, che verranno discusse in dettaglio di seguito.
Novità sui ‘vecchi’ antidiabetici orali
Metformina: Al momento o poco dopo la diagnosi di diabete di tipo 2, tutti i pazienti dovrebbero essere sottoposti a terapia con metformina, se non è possibile ottenere un controllo ottimale del diabete attraverso la modifica dello stile di vita e se il trattamento è tollerato a livello gastrointestinale. La metformina abbassa fortemente l’HbA1c, riduce le complicanze micro e macrovascolari, ritarda la progressione del diabete, non provoca ipoglicemia, favorisce la perdita di peso ed è economicamente vantaggiosa. L’insufficienza renale con un eGFR <30 ml/min è una controindicazione importante a causa del rischio di acidosi lattica pericolosa per la vita. Se l’eGFR scende a 30-45 ml/min, la terapia preesistente può essere continuata con un massimo di 1000 mg al giorno; l’inizio della terapia non è raccomandato. Il trattamento può essere ripreso a un eGFR di 45-60 ml/min, con raccomandazioni di dose massima giornaliera di 1000-2000 mg variabili [2].
È fondamentale istruire i pazienti a sospendere la terapia in caso di malattie intercorrenti (operazioni, infezioni, insufficienza cardiaca, ecc.). Se è previsto l’uso di mezzi di contrasto radiografici contenenti iodio, la metformina deve essere interrotta 48 ore prima con un eGFR <45 ml/min (somministrazione endovenosa) o <60 ml/min (somministrazione intrarteriosa). Con una funzione renale stabile documentata, il riavvio della terapia è possibile 48 ore dopo la somministrazione del contrasto [3]. A causa dell’interferenza con l’assorbimento della vitamina B12, la carenza di vitamina B12 si verifica nel 10-15% dei pazienti che assumono metformina e deve essere ricercata e sostituita se sono presenti segni, soprattutto nella polineuropatia periferica.
Gliclazide: tra le sulfoniluree disponibili, si raccomanda solo l’uso della gliclazide, in quanto le preparazioni ad azione prolungata, soprattutto la glibenclamide, presentano un rischio maggiore di ipoglicemia e il loro uso può essere associato a un aumento della mortalità [4]. Con solo un leggero aumento del rischio di ipoglicemia, la sicurezza cardiovascolare e la riduzione dell’incidenza di complicanze microvascolari sono state adeguatamente dimostrate con la gliclazide [5]. La gliclazide è un potente abbassatore di HbA1c, il cui uso è associato a un leggero aumento di peso.
Glitazoni: dei glitazoni, solo il pioglitazone è ancora disponibile, dopo che il rosiglitazone è stato ritirato dal mercato nel 2010 a causa dell’aumento degli eventi cardiovascolari osservati con la terapia. Il meccanismo d’azione si basa su un miglioramento della sensibilità all’insulina, con conseguente potente effetto di riduzione dell’HbA1c senza un aumento del rischio di ipoglicemia. I glitazoni provocano un aumento di peso a causa dell’incremento del tessuto adiposo sottocutaneo e della ritenzione di liquidi, motivo per cui non possono essere utilizzati nell’insufficienza cardiaca. Inoltre, studi recenti hanno dimostrato un’aumentata incidenza di fratture osteoporotiche nelle donne in postmenopausa [6]. L’associazione tra l’assunzione di pioglitazone e l’aumento del rischio di cancro alla vescica è stata messa in discussione o messa in prospettiva da uno studio pubblicato di recente [7]. Tuttavia, il pioglitazone è diventato meno importante con la disponibilità di nuove sostanze e ora viene utilizzato relativamente di rado, almeno in Svizzera.
Nuovi farmaci antidiabetici (orali)
Gliflozine: è noto fin dal XIX secolo che la florizina, un glicoside isolato per la prima volta dalla corteccia dei meli nel 1835, ha un effetto glucosurico. Nel 1987, la florizina è stata utilizzata per la prima volta come antidiabetico in modelli animali e poco dopo è stata riconosciuta come inibitore dei cotrasportatori di sodio e glucosio (SGLT) 1 e 2 (cotrasportatori di sodio e glucosio del rene). L’SGLT2 si trova principalmente nel tubulo prossimale dei reni, l’SGLT1 nel tubulo prossimale e nell’intestino tenue. A causa della scarsa biodisponibilità orale, la florizina non è entrata in clinica, ma ha stimolato lo sviluppo di nuovi inibitori SGLT. Finora sono disponibili tre inibitori SGLT2 relativamente selettivi, canagliflozin (Invokana®), dapagliflozin (Forxiga®) ed empagliflozin (Jardiance®), il cui uso comporta una perdita renale di glucosio di 60-90 g/d [8]. Queste sostanze abbassano l’HbA1c di circa lo 0,5-1% rispetto al placebo, indipendentemente dalla somministrazione di un inibitore SGLT2 in monoterapia o in combinazione. Si è notata una riduzione dei livelli di glucosio nel sangue sia a digiuno che postprandiale. Gli effetti collaterali benvenuti sono stati una riduzione della pressione arteriosa sistolica (2-8 mmHg in sei mesi) e una diminuzione del peso corporeo (1-3 kg in sei mesi). In caso di funzione renale compromessa (GFR <45-60 ml/min), l’effetto degli inibitori SGLT2 diminuisce rapidamente [9].
Con gli inibitori SGLT2, le micosi genitali si verificano più frequentemente (circa 10%), motivo per cui è necessario osservare una buona igiene intima. In caso di micosi, preferiamo una terapia orale singola con fluconazolo. Inoltre, anche le infezioni del tratto urinario sono un po’ più frequenti. A causa della diuresi osmotica, possono verificarsi disturbi ortostatici, per cui all’inizio della terapia si deve prendere in considerazione l’adeguamento di qualsiasi terapia diuretica esistente [8].
Non sono ancora disponibili dati a lungo termine sulla sicurezza e sulla riduzione degli endpoint micro e macrovascolari. In diversi studi è stato osservato un leggero aumento del colesterolo LDL e una diminuzione del colesterolo HDL di circa 4%. Recentemente, nei pazienti con diabete di tipo 2 è stato osservato anche un accumulo di chetoacidosi associato all’uso degli inibitori SGLT2. Nella maggior parte dei casi, è stato possibile identificare un fattore predisponente: una malattia grave, un’assunzione ridotta di cibo e liquidi o una riduzione della dose di insulina utilizzata. Vale anche la pena ricordare che le chetoacidosi si sono verificate con livelli di glucosio nel sangue solo leggermente elevati (chetoacidosi euglicemica), il che ha reso difficile la diagnosi [10]. Gli inibitori SGLT2, come la metformina, devono essere sospesi in caso di malattie intercorrenti, interventi chirurgici, ecc.
Le gliflozine possono essere combinate con metformina, gliclazide, gliptine, analoghi del GLP-1 e insulina. La combinazione con gliptina è un potente abbassamento dell’HbA1c e non provoca ipoglicemia (Fig. 1) [11]. In Svizzera, attualmente solo dapagliflozin può essere combinato con le gliptine senza approvazione preventiva. Anche la combinazione con gli analoghi del GLP-1 è potenzialmente molto efficace, ma non è ancora stata approvata in Svizzera. Gli inibitori SGLT2 possono anche essere combinati con l’insulina e spesso consentono di ridurre la dose di insulina. Sono efficaci anche nel diabete di tipo 1, ma non sono approvati per questa indicazione.
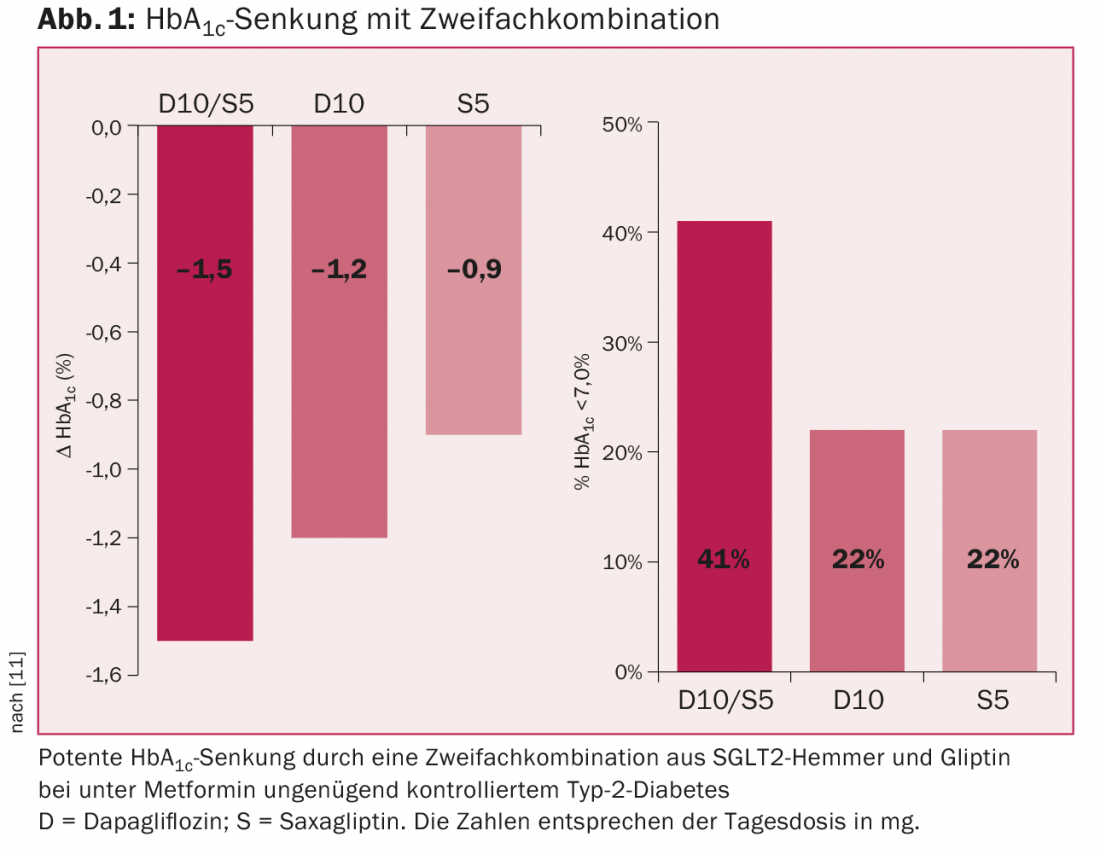
In sintesi, l’uso di un inibitore SGLT2 è particolarmente indicato per i pazienti obesi più giovani con funzione renale normale, nei quali l’ipoglicemia deve essere evitata a tutti i costi (ad esempio, gli autisti).
Incretine (gliptine e analoghi del GLP-1): Le gliptine sono inibitori della dipeptidil peptidasi 4 e quindi impediscono la rapida degradazione delle incretine, soprattutto del GLP-1 (“glucagon like peptide 1”). Il potenziamento dell’effetto delle incretine o del GLP-1 porta, tra l’altro, a un ritardo nello svuotamento gastrico, all’attivazione delle cellule β con aumento della secrezione di insulina e all’inibizione delle cellule α (secrezione di glucagone) e della gluconeogenesi nel fegato. Le gliptine migliorano quindi i livelli di glucosio nel sangue a digiuno e postprandiale. Si può prevedere una riduzione dell‘HbA1c con la monoterapia nell’intervallo 0,5-1,0% [12]. Le gliptine sono neutre dal punto di vista del peso e non causano ipoglicemia grazie al loro effetto glucosio-dipendente. In generale, le gliptine sono molto ben tollerate. Dopo che sono state sollevate preoccupazioni sulla sicurezza cardiovascolare in base ai risultati precedenti (aumento dei ricoveri per insufficienza cardiaca con saxagliptin nello studio Savor-TIMI 53), gli studi di follow-up non hanno mostrato un aumento dell’insufficienza cardiaca o del rischio cardiovascolare [13–15]. Tuttavia, non sono ancora disponibili dati a lungo termine che dimostrino una riduzione degli endpoint micro e/o macrovascolari.
Nella funzione renale moderatamente e gravemente compromessa (eGFR <30 ml/min), solo linagliptin può essere utilizzato senza aggiustare la dose. Le gliptine possono essere combinate con metformina, gliclazide, inibitori SGLT2 e insulina di base. La combinazione con la terapia insulinica intensificata non è raccomandata a causa del basso beneficio aggiuntivo.
La modifica della molecola di GLP-1 può anche impedire la sua rapida degradazione da parte della dipeptidil transferasi 4. L’applicazione sottocutanea di questi analoghi del GLP-1 raggiunge livelli di GLP-1 sovrafisiologici, per cui l’effetto degli analoghi del GLP-1 è più forte rispetto alle gliptine. La riduzione dell’HbA1c ottenuta negli studi clinici è dell’1,0-1,8%. Gli analoghi del GLP-1 attualmente disponibili si differenziano principalmente per la durata d’azione: exenatide (Byetta®) e la lixisenatide (non disponibile in Svizzera) sono ad azione breve (emivita <5 ore) e abbassano principalmente i livelli di glucosio nel sangue postprandiale, mentre i preparati a lunga durata d’azione (emivita >12 Orari: Liraglutide [Victoza®], Exenatide LAR [Bydureon®], Dulaglutide [Trulicity®] e Albiglutide [Eperzan®]) abbassano maggiormente i livelli di glucosio nel sangue a digiuno. Tutti gli analoghi del GLP-1 comportano una perdita di peso, in media di 1-4 kg, e non causano ipoglicemia. Gli effetti collaterali gastrointestinali, come nausea, gonfiore e diarrea, sono relativamente frequenti e più pronunciati con i preparati a breve durata d’azione, ma di solito si attenuano dopo qualche settimana. Se i sintomi persistono, si può tentare il trattamento con un analogo del GLP-1 alternativo a lunga durata d’azione. L’applicazione sottocutanea è quotidiana (liraglutide) o settimanale (exenatide LAR, dulaglutide, albiglutide). Gli analoghi del GLP-1 possono essere combinati con metformina, gliclazide e pioglitazone; la prescrizione contemporanea di gliptine è inutile a causa dello stesso obiettivo. Solo liraglutide può essere combinato con l’insulina di base (approvazione e rimborso) [16]. Gli analoghi del GLP-1 non sono stati studiati o approvati nella funzione renale significativamente compromessa (eGFR <30 ml/min) .
La combinazione fissa recentemente disponibile (IDegLira, Xultophy®) di un’insulina di base (Degludec, Tresiba®) con un analogo del GLP-1 (liraglutide) è un’opzione terapeutica molto potente con pochi effetti collaterali e associata a un rischio molto basso di ipoglicemia. Nei pazienti già trattati con un’insulina di base e metformina, è stata ottenuta una riduzione dell‘HbA1c dell’1,9% passando a questa terapia. La titolazione regolare della dose (una o due volte alla settimana) in base ai livelli di glucosio nel sangue al mattino è fondamentale per il successo del trattamento [17].
Conclusione
I nuovi farmaci antidiabetici aprono nuove opzioni di trattamento per i pazienti il cui diabete non è sufficientemente controllato con la metformina o con una combinazione di due farmaci. Gli inibitori SGLT2, in particolare, possono essere combinati con tutti i farmaci che abbassano la glicemia, grazie al loro speciale meccanismo d’azione. Con le terapie combinate, si può ottenere una riduzione molto potente dell‘HbA1c(>1,5%). Nessuno dei nuovi gruppi di sostanze ha ancora dimostrato di portare a una riduzione delle complicanze microvascolari e/o macrovascolari. Gli studi a lungo termine dimostrano la sicurezza cardiovascolare delle gliptine.
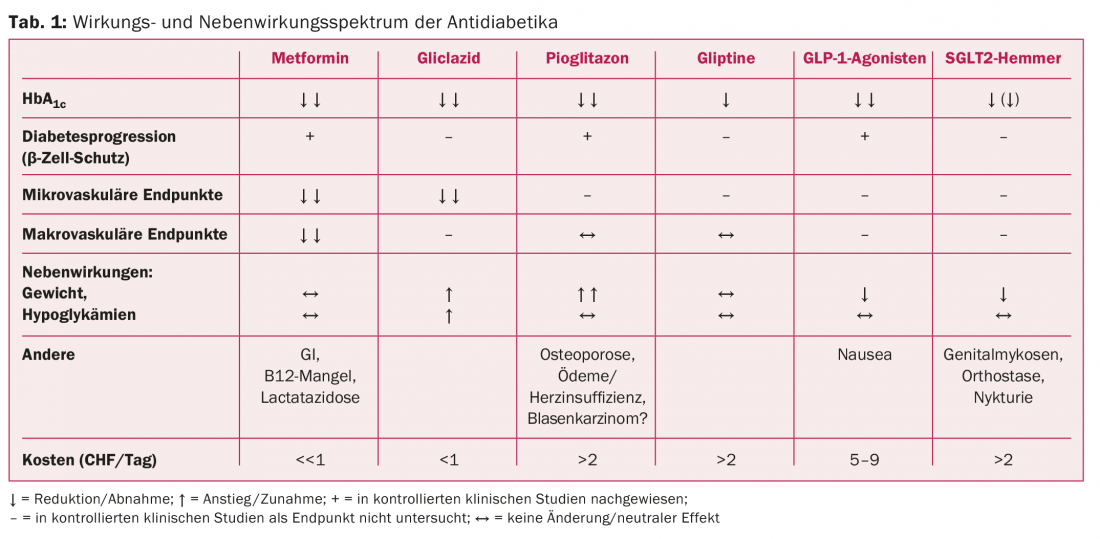
La Tabella 1 mostra lo spettro degli effetti e degli effetti collaterali dei farmaci antidiabetici.
Letteratura:
- American Diabetes Association, ADA Position Statement 2015: 7. Approcci al trattamento glicemico. Diabetes Care 2015 Jan 1; 38(Supplemento 1): S41-48.
- Inzucchi SE, et al: Metformina nei pazienti con diabete di tipo 2 e malattia renale: una revisione sistematica. JAMA 2014 Dec 24; 312(24): 2668.
- Società Svizzera di Endocrinologia e Diabetologia: Metformina e mezzi di contrasto roentgen contenenti iodio [Internet]. Linee guida. 2014 [cited 2015 Jul 29]. Disponibile su: www.sgedssed.ch/fileadmin/files/news/Metformin_und_jodhaltige_Roentgenkontrastmittel.pdf
- Simpson SH, et al: Rischio di mortalità tra le sulfoniluree: una revisione sistematica e una meta-analisi di rete. Lancet Diabetes Endocrinol 2015 Jan; 3(1): 43-51.
- Gruppo Collaborativo ADVANCE, Patel A, et al: Controllo intensivo della glicemia ed esiti vascolari nei pazienti con diabete di tipo 2. N Engl J Med 2008 Jun 12; 358(24): 2560-2572.
- Soccio RE, Chen ER, Lazar MA: I tiazolidinedioni e la promessa della sensibilizzazione all’insulina nel diabete di tipo 2. Cell Metab 2014 Oct 7; 20(4): 573-591.
- Lewis JD, et al: Uso di Pioglitazone e rischio di cancro alla vescica e altri tumori comuni nelle persone con diabete. JAMA 2015 Jul 21; 314(3): 265-277.
- Tahrani AA, Barnett AH, Bailey CJ: Gli inibitori SGLT nella gestione del diabete. Lancet Diabetes Endocrinol 2013; 1(2): 140-151.
- Vasilakou D, et al: Inibitori del cotrasportatore 2 di sodio-glucosio per il diabete di tipo 2: una revisione sistematica e una meta-analisi. Ann Intern Med 2013 Aug 20; 159(4): 262-274.
- Peters AL, et al: Chetoacidosi diabetica euglicemica: una potenziale complicazione del trattamento con l’inibizione del cotrasportatore 2 di sodio-glucosio. Diabetes Care 2015 Jun 15; dc150843 (Epub ahead of print).
- Rosenstock J, et al: Doppia terapia aggiuntiva nel diabete di tipo 2 scarsamente controllato con la monoterapia con metformina: uno studio randomizzato in doppio cieco sull’aggiunta di saxagliptin più dapagliflozin rispetto all’aggiunta singola di saxagliptin o dapagliflozin alla metformina. Diabetes Care 2015 Mar; 38(3): 376-383.
- Karagiannis T, et al: Inibitori della dipeptidil peptidasi-4 per il trattamento del diabete mellito di tipo 2 nel contesto clinico: revisione sistematica e meta-analisi. BMJ 2012; 344: e1369.
- Scirica BM, et al: Saxagliptin ed esiti cardiovascolari nei pazienti con diabete mellito di tipo 2. N Engl J Med 2013 Oct 3; 369(14): 1317-1326.
- Zannad F, et al: Esiti di insufficienza cardiaca e mortalità nei pazienti con diabete di tipo 2 che assumono alogliptin rispetto al placebo in EXAMINE: uno studio multicentrico, randomizzato, in doppio cieco. Lancet 2015 23 maggio; 385(9982): 2067-2076.
- Green JB, et al: Effetto di Sitagliptin sui risultati cardiovascolari nel diabete di tipo 2. N Engl J Med 2015 Jul 16; 373(3): 232-242.
- Meier JJ: agonisti del recettore GLP-1 per il trattamento individualizzato del diabete mellito di tipo 2. Nat Rev Endocrinol 2012 Dic; 8(12): 728-742.
- Buse JB, et al: Contributo di Liraglutide nella combinazione a rapporto fisso di Insulina Degludec e Liraglutide (IDegLira). Diabetes Care 2014 Nov; 37(11): 2926-2933.
CARDIOVASC 2015; 14(4): 4-8











