Nessun Congresso ESC senza nuovi studi sulla terapia antitrombotica dopo l’intervento coronarico percutaneo. Recentemente, la monoterapia con un bloccante P2Y12 è emersa sempre più come un’alternativa interessante alla terapia antiaggregante doppia (DAPT) con un bloccante P2Y12 più ASA, grazie al minor rischio di sanguinamento. Lo studio STOPADAPT-3 [2] affronta la questione se sia possibile fare a meno dell’ASA.
È stato riferito che i pazienti con sindrome coronarica acuta (SCA) presentano un rischio maggiore di eventi ischemici [3]. Pertanto, le attuali linee guida raccomandano gli inibitori del recettore P2Y12 più nuovi e più efficaci, come ticagrelor e prasugrel, nei pazienti con ACS, mentre il clopidogrel è ancora raccomandato nei pazienti con malattia coronarica stabile (CAD) [4,5]. Nei pazienti con ACS, le attuali linee guida raccomandano anche l’uso di anticoagulanti prima dell’intervento coronarico percutaneo (PCI), la somministrazione di agenti antiaggreganti e la terapia antiaggregante doppia prolungata (DAPT) se non c’è un rischio elevato di sanguinamento [4,5]. Inoltre, per la PCI nell’ACS viene spesso scelto l’approccio transfemorale, che è stato riportato essere associato a un rischio maggiore di sanguinamento [6]. Pertanto, i pazienti con ACS possono anche avere un rischio maggiore di sanguinamento rispetto ai pazienti con CHD stabile. Tuttavia, la presentazione clinica dell’ACS non è stata inclusa come criterio nell’Academic Research Consortium (ARC)-HBR, in parte perché non esistevano studi precedenti che confrontassero il rischio di emorragia dopo PCI tra pazienti con ACS e pazienti con CHD stabile [7].
Una meta-analisi di studi randomizzati con pazienti affetti da ACS ha riportato che la nuova generazione di stent a rilascio di farmaco (DES) riduce il rischio a lungo termine di trombosi dello stent, infarto miocardico e morte cardiaca rispetto agli stent a metallo nudo [8]. L’equilibrio tra il rischio di ischemia e di sanguinamento dopo la PCI nei pazienti con ACS potrebbe essere cambiato in modo significativo nell’era della nuova generazione di DES.
Progetto e risultati di STOPDAPT-3
Lo scopo di STOPDAPT-3 è stato quello di verificare se l’interruzione precoce della DAPT dopo l’impianto di DES nell’ACS con HBR possa ridurre il sanguinamento grave senza aumentare il rischio di complicanze cardiovascolari.
I 13.258 pazienti comprendevano 5521 pazienti (42%) con ACS (gruppo ACS) e 7737 pazienti (58%) con CHD stabile (gruppo CHD stabile). Nel gruppo ACS, c’erano 4081 pazienti (74%) con STEMI e 1440 pazienti (26%) con ACS non-ST-elevation (NSTEACS), inclusi 1235 pazienti (22%) con NSTEMI e 205 pazienti (3,7%) con UA. I pazienti sono stati suddivisi in quattro gruppi combinati in base alla presentazione clinica (ACS, CHD stabile) e alla presenza di ARC-HBR (ACS/HBR: 2502 pazienti; ACS/No-HBR: 3019 pazienti; CHD stabile/HBR: 3905 pazienti; CHD stabile/No-HBR: 3832 pazienti).
Caratteristiche di base: ACS vs. CHD stabile
Nella popolazione del presente studio, il 48% dei pazienti presentava ARC-HBR. I pazienti del gruppo ACS erano più giovani, spesso di sesso maschile e fumatori, avevano un indice di massa corporea inferiore e soffrivano più frequentemente di insufficienza cardiaca e di grave fragilità rispetto ai pazienti del gruppo CHD stabile.
In termini di caratteristiche procedurali, il numero totale di stent era maggiore, la lunghezza totale degli stent era maggiore e la dimensione minima dello stent era minore nel gruppo CHD stabile rispetto al gruppo ACS. L’accesso transfemorale è stato scelto più frequentemente nel gruppo ACS rispetto al gruppo CHD stabile. Inoltre, i pazienti del gruppo ACS hanno ricevuto statine, β-bloccanti, inibitori dell’enzima di conversione dell’angiotensina/bloccanti del recettore dell’angiotensina II, anticoagulanti orali e inibitori della pompa protonica/H2-bloccanti più frequentemente dei pazienti del gruppo CHD stabile. La prevalenza della terapia con statine ad alta intensità era molto bassa in entrambi i gruppi.
Risultati clinici a lungo termine: ACS vs. CHD stabile
Il tempo mediano di follow-up per i sopravvissuti è stato di 6,0 anni e i dati completi di follow-up clinico a 1, 3 e 5 anni sono stati ottenuti per il 96,9%, 93,4% e 78,6% dei pazienti, rispettivamente. L’incidenza cumulativa di interruzione permanente della DAPT è stata significativamente più alta nel gruppo ACS rispetto al gruppo CHD stabile, suggerendo che la durata della DAPT è stata significativamente più breve nel gruppo ACS rispetto al gruppo CHD stabile.
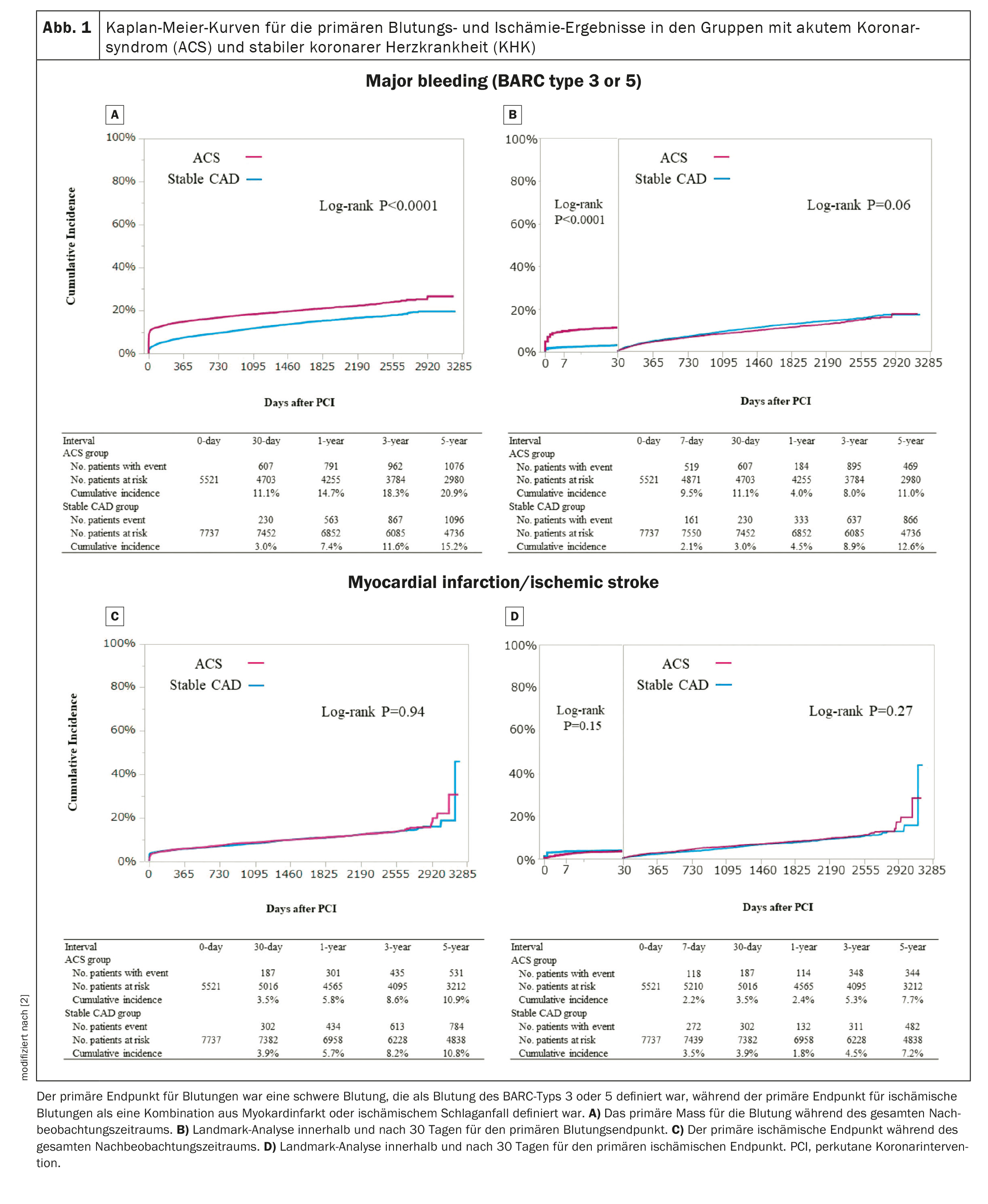
L’incidenza cumulativa a 5 anni dell’esito primario del sanguinamento (emorragie BARC di tipo 3 o 5) era significativamente più alta nel gruppo ACS rispetto al gruppo CHD stabile (Fig. 1A) [2]. Nell’analisi di riferimento a 30 giorni, l’incidenza cumulativa dell’esito primario di sanguinamento entro 30 giorni era anche significativamente più alta nel gruppo ACS rispetto al gruppo CHD stabile (Fig. 1B) [2]. Dopo l’aggiustamento per i confondenti, l’aumento del rischio di ACS rispetto alla CHD stabile per la misura primaria di sanguinamento è rimasto significativo per tutto il periodo di follow-up ed entro 30 giorni, mentre non era più significativo dopo 30 giorni. In termini di tipi di emorragia, l’incidenza cumulativa di emorragia del sito di accesso, emorragia gastrointestinale e altre emorragie era significativamente più alta nel gruppo ACS rispetto al gruppo CHD stabile, mentre l’incidenza cumulativa di emorragia intracranica non differiva tra i due gruppi. L’incidenza cumulativa dell’esito primario dell’emorragia non differiva tra STEMI e NSTEACS.
L’incidenza cumulativa a 5 anni dell’endpoint ischemico primario non differiva significativamente tra i due gruppi durante l’intero periodo di follow-up o entro 30 giorni (Fig. 1C, 1D) [2]. Dopo l’aggiustamento per il costrutto, l’aumento del rischio di ACS rispetto alla CHD stabile per la misura primaria dell’esito ischemico è rimasto non significativo. Il rischio di ACS rispetto alla CHD stabile per l’endpoint ischemico primario era significativamente più basso entro 30 giorni, ma più alto dopo 30 giorni. L’aumento del rischio di ACS rispetto alla CHD stabile è stato significativo per tutte le cause di morte, morte cardiaca, morte cardiovascolare, morte non cardiovascolare, ictus ischemico, trombosi definita dello stent e rivascolarizzazione del vaso bersaglio, ma non per l’infarto miocardico secondo la definizione ARTS. L’incidenza cumulativa dell’esito ischemico primario non differiva tra STEMI e NSTEACS.
Le caratteristiche iniziali dipendono dal quadro clinico e dalla HBR
Le caratteristiche basali e il trattamento farmacologico differivano significativamente tra le quattro categorie in base alla storia clinica (ACS e CHD stabile) e alla presenza di ARC-HBR. I pazienti del gruppo ACS/HBR erano più anziani, avevano un indice di massa corporea inferiore e soffrivano più frequentemente di insufficienza cardiaca e di grave fragilità.
I risultati clinici a lungo termine dipendono dalla presentazione clinica e dalla HBR.
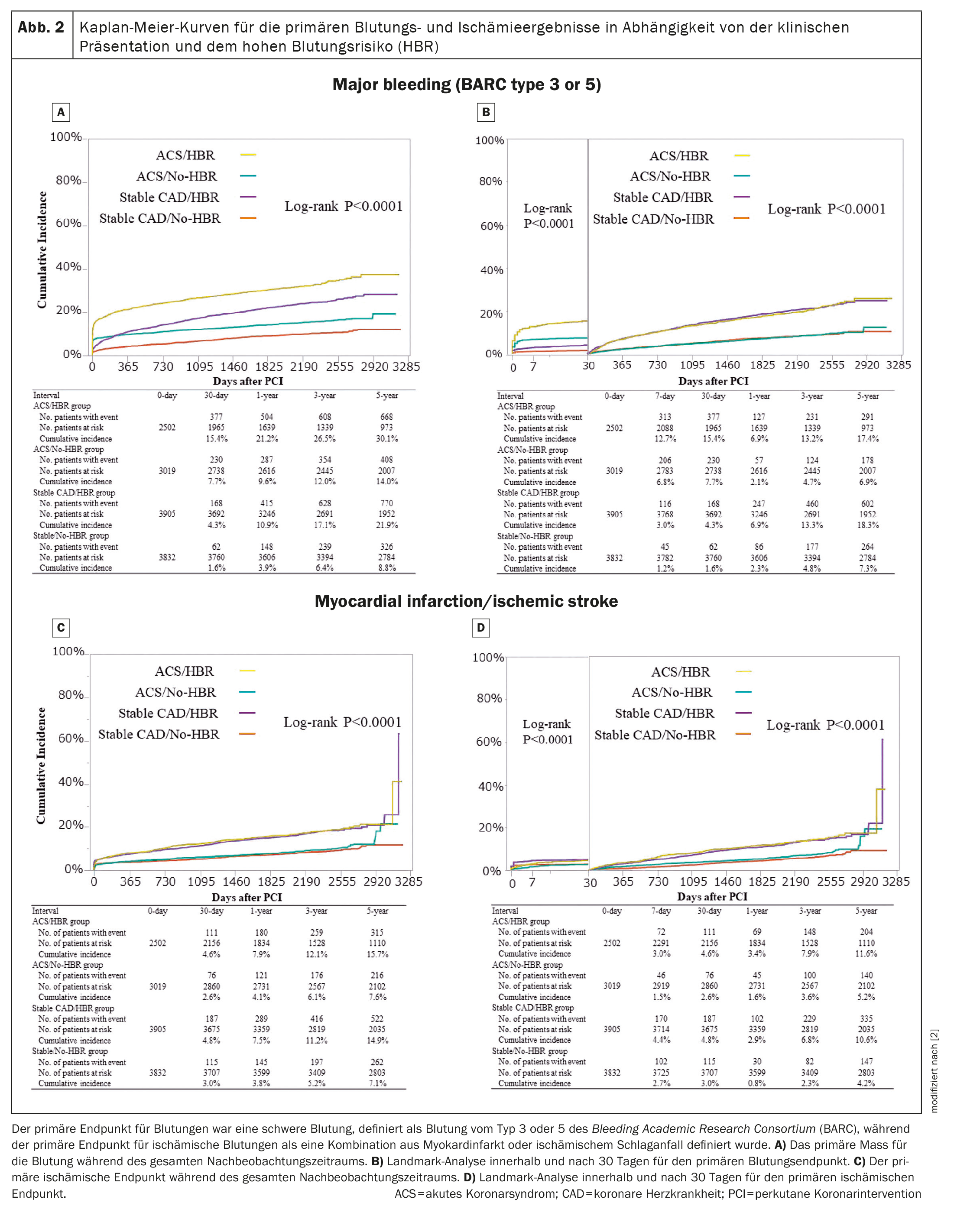
In tutti e quattro i gruppi, l’incidenza cumulativa di interruzione permanente della DAPT era più alta nel gruppo ACS/HBR. L’incidenza cumulativa a 5 anni dell’esito emorragico primario è diminuita nell’ordine di ACS/HBR, CHD/HBR stabile e ACS/no-HBR, seguito dal gruppo CHD stabile/no-HBR (Fig. 2A) [2]. Entro 30 giorni, l’incidenza cumulativa dell’esito primario di sanguinamento è stata più alta nei due gruppi ACS con e senza HBR rispetto ai due gruppi con CHD stabile con e senza HBR (Fig. 2B) [2]. Il rischio aggiustato per l’esito primario di emorragia era molto più alto nel gruppo ACS/HBR e moderatamente più alto nei gruppi ACS/no-HBR e CHD/HBR stabile rispetto al gruppo CHD/no-HBR stabile (HR 3,05 [95% CI 2,64-3,54; p<0,0001], HR 1,69 [95% CI 1,45-1,98; p<0,0001] e HR 1,89 [95% CI 1,66-2,15; p<0,0001]).
Entro 30 giorni, il rischio aggiustato per l’esito primario di sanguinamento era significativamente più alto nei due gruppi ACS con e senza HBR e moderatamente più alto nel gruppo CHD stabile/HBR rispetto al gruppo CHD stabile/no-HBR. A 30 giorni, il rischio aggiustato per l’esito primario di emorragia era significativamente più alto nei due gruppi HBR con e senza ACS rispetto al gruppo CHD stabile/non-HBR.
L’incidenza cumulativa a 5 anni dell’esito ischemico primario è stata significativamente più alta nei due gruppi HBR rispetto ai due gruppi non HBR per tutto il periodo di follow-up. L’incidenza cumulativa a 5 anni dell’esito ischemico primario era significativamente più alta nei due gruppi HBR rispetto ai due gruppi no-HBR durante l’intero periodo di follow-up (Fig. 2C) [2] ed entro e dopo 30 giorni (Fig. 2D) [2]. Il rischio aggiustato per l’esito ischemico primario era leggermente più alto nei due gruppi HBR rispetto al gruppo CHD stabile/no-HBR, mentre non differiva significativamente tra i gruppi ACS/no-HBR e CHD stabile/no-HBR.
Risultato del sanguinamento primario dopo 30 giorni a seconda del sito di accesso
L’incidenza cumulativa a 30 giorni dell’esito primario di emorragia (emorragia BARC di tipo 3 o 5) era significativamente più alta nei pazienti con accesso femorale rispetto a quelli con accesso radiale.
L’aspirina rimane la “pietra miliare” del trattamento
L’autore dello studio, il dottor Masahiro Natsuaki dell’Università di Saga in Giappone, ha riassunto i risultati dello studio STOPDAPT-3 come segue: “La strategia senza aspirina non è riuscita a ridurre l’emorragia maggiore entro un mese dopo la PCI rispetto alla strategia DAPT, ma non era inferiore in termini di endpoint cardiovascolare co-primario con un margine relativo del 50%. L’aspirina, utilizzata come componente della DAPT per un periodo limitato di un mese dopo la PCI, può aver esercitato un effetto protettivo sulle lesioni coronariche vulnerabili, in particolare nei pazienti con ACS, senza un forte aumento dei sanguinamenti maggiori. La DAPT dovrebbe rimanere la strategia standard per la PCI nell’era degli stent a rilascio di farmaco di nuova generazione”. [1]
Discutendo i risultati di STOPDAPT-3 dopo la presentazione della hot-line, Marco Valgimigli, vicedirettore di cardiologia interventistica presso l’Istituto Cardiocentro Ticino di Lugano, Svizzera, ha detto che i dati di STOPDAPT-3 non mostrano alcun beneficio per quanto riguarda i sanguinamenti maggiori e un segnale di potenziale danno in termini di trombosi subacuta dello stent se la terapia con aspirina viene omessa dopo la PCI. “I tassi assoluti di eventi sono stati estremamente bassi, pari allo 0,2% rispetto allo 0,6%, ma indubbiamente più elevati nel gruppo senza aspirina”, ha concluso Valgimigli. “Le implicazioni per la pratica clinica sono chiare. L’aspirina rimane una pietra miliare nella fase periprocedurale e acuta della PCI nei pazienti senza indicazione all’anticoagulazione orale”.
Le linee guida raccomandano una DAPT di sei mesi per i pazienti con ACS e HBR, e di 12 mesi senza HBR. Per i pazienti non affetti da ACS, la linea guida raccomanda una DAPT di 1-3 mesi.
Congresso: ESC 2023
Letteratura:
- Natsuaki M: STOPDAPT-3: una strategia antitrombotica senza aspirina per l’intervento coronarico percutaneo. Sessione Hot Line 3, Congresso ESC 2023, Amsterdam, 26 agosto 2023.
- Natsuaki M, et al: Effetti della sindrome coronarica acuta e della coronaropatia stabile sul sanguinamento e sul rischio ischemico dopo l’intervento coronarico percutaneo. Circ J. 2021; 85: 1928-1941.
- Yamaji K, et al: Esiti a lungo termine dopo l’impianto di stent coronarico nei pazienti che presentano un infarto miocardico acuto (un’osservazione del Coronary Revascularisation Demonstrating Outcome Study-Kyoto Registry Cohort-2). Am J Cardiol 2015; 116: 15-23.
- Valgimigli M, et al: 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS: The task force for dual antiplatelet therapy in coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2018; 39: 213-260.
- Nakamura M, et al: Aggiornamento mirato della linea guida JCS 2020 sulla terapia antitrombotica nei pazienti con malattia coronarica. Circ J 2020; 84: 831-865.
- Valgimigli M, et al: Accesso radiale rispetto a quello femorale nei pazienti con sindromi coronariche acute sottoposti a gestione invasiva: uno studio multicentrico randomizzato. Lancet 2015; 385: 2465-2476.
- Urban P, et al: Definire il rischio di sanguinamento elevato nei pazienti sottoposti a intervento coronarico percutaneo. Circulation 2019; 140: 240-261.
- Valgimigli M, et al: Effetti degli stent a eluizione di cobalto-cromo everolimus o degli stent di metallo nudo sugli eventi cardiovascolari fatali e non fatali: meta-analisi a livello di paziente. BMJ 2014; 349: g6427.
CARDIOVASC 2023; 22(4): 46-50 (pubblicato il 28.11.23, prima della stampa)