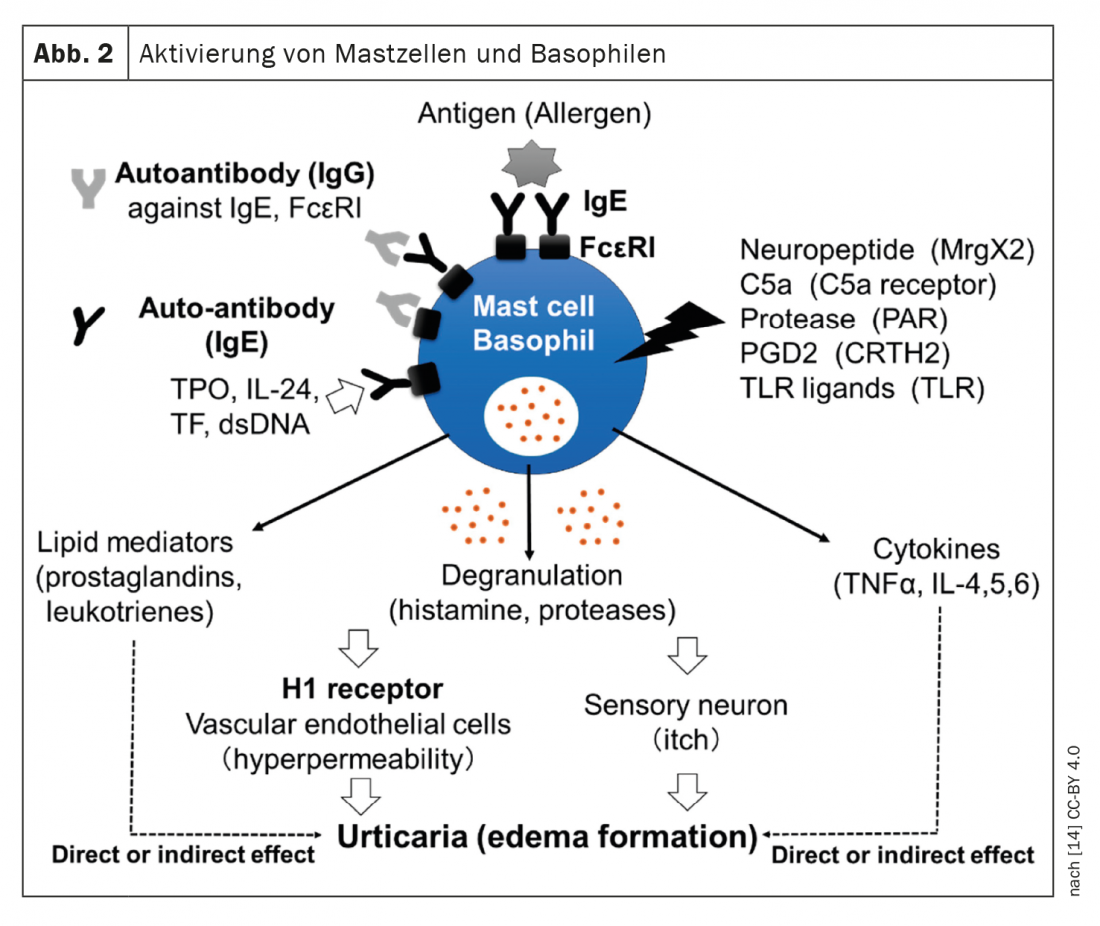
All’inizio del 2022, è stata pubblicata la nuova linea guida sull’orticaria della Società tedesca di allergologia e immunologia clinica e della Società dermatologica tedesca. Gli antistaminici di seconda generazione e l’omalizumab come add-on continuano a rappresentare il pilastro del trattamento. Ma per quanto riguarda i regimi di dosaggio, sono state incluse nuove raccomandazioni, basate sui risultati del gruppo internazionale di esperti EAACI/GA²LEN.
La linea guida S3 aggiornata è un adattamento in lingua tedesca della linea guida in lingua inglese EAACI/GA²LEN/EuroGuiDerm/APAAACI [1,2]. Il Prof. Dr. med. Torsten Zuberbier, Responsabile della Ricerca sulle Conseguenze delle Allergie presso la Clinica di Dermatologia, Venereologia e Allergologia della Charité Universitätsmedizin di Berlino, ha presentato questi dati in occasione della Riunione Annuale EEACI di quest’anno [3]. L’orticaria è una malattia comune mediata dai mastociti, caratterizzata dalla comparsa di rantoli e/o angioedema. Le opzioni di trattamento attualmente raccomandate riguardano i mediatori dei mastociti, come l’istamina, o gli attivatori, come gli autoanticorpi. (Fig.1). Mentre l’orticaria acuta è autolimitante e di solito non richiede un work-up diagnostico oltre all’anamnesi per i possibili fattori scatenanti, il work-up diagnostico nei pazienti con orticaria cronica spontanea (CSU) include un emocromo differenziale, compresa la CRP e/o la velocità di sedimentazione degli eritrociti. Nei pazienti sottoposti a cure specialistiche, devono essere raccolte anche le IgE totali e le IgG-anti-TPO. Il motivo è che i pazienti con IgE molto basse di solito non rispondono bene all’omalizumab, mentre quelli con un IgG-anti-TPO positivo di solito mostrano un’ottima risposta a questo anticorpo monoclonale, ha spiegato il Prof. Zuberbier [3]. Nei singoli pazienti, possono essere utili ulteriori test diagnostici, dice l’esperto e aggiunge: “Nel caso dell’orticaria inducibile, raccomandiamo di guardare solo le ‘soglie'”, cioè di testare gli stimoli freddi, ecc.
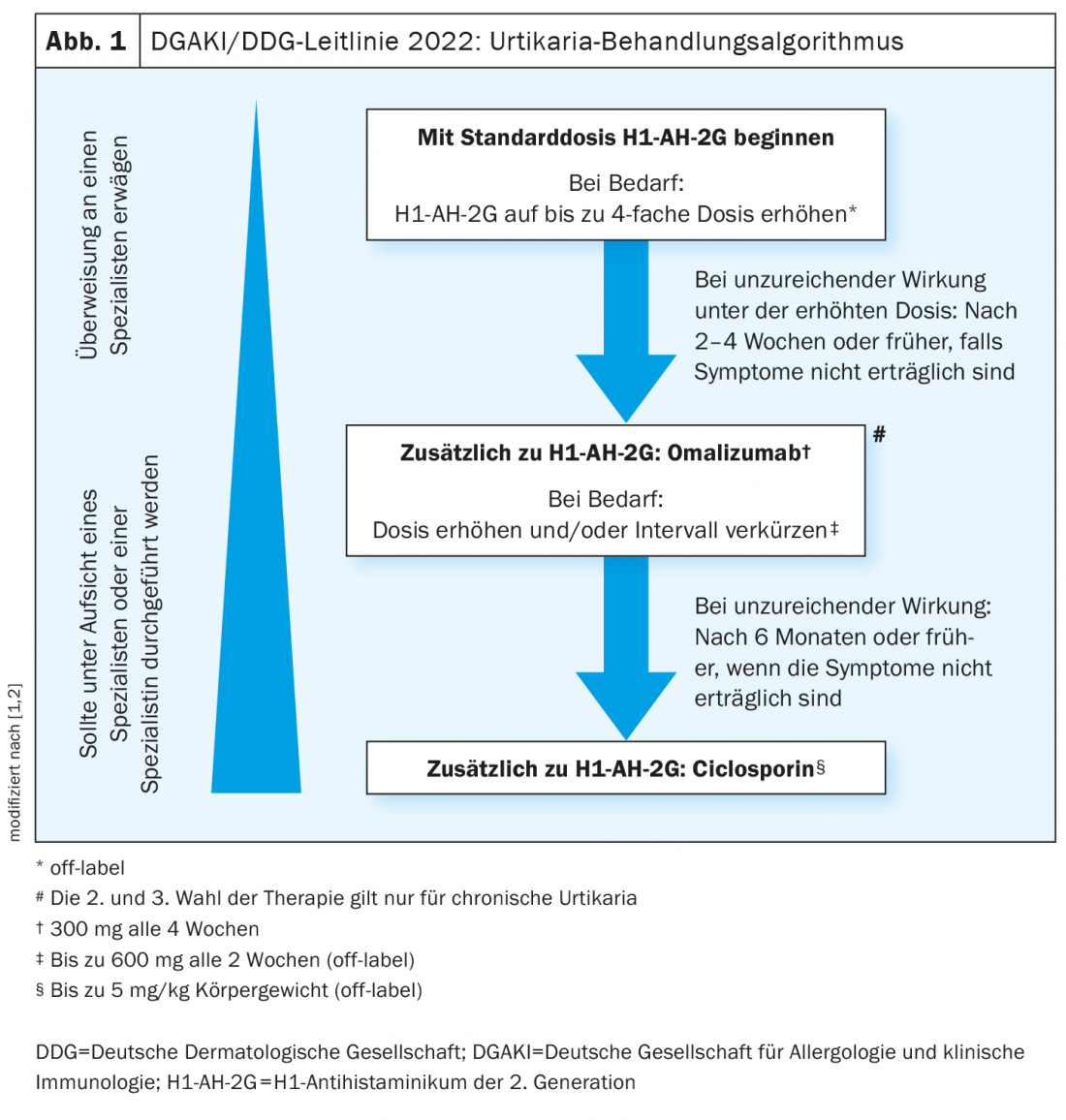
L’obiettivo terapeutico generale per tutti i pazienti affetti da orticaria è quello di ottenere un controllo completo dei sintomi.
Dosare gli antistaminici H1 di seconda generazione, ma non mescolarli.
L’attività della malattia deve essere valutata al primo esame e ad ogni esame successivo. A tale scopo si possono utilizzare questionari convalidati come l’Urticaria Activity Score (UAS) e l’Angioedema Activity Score (AAS). L’UAS7 si basa sull’UAS (box). “Per me personalmente, è lo strumento diagnostico più importante”, afferma il Prof. Zuberbier [3]. Si tratta di valori misurati molto robusti, che forniscono anche informazioni sulle fluttuazioni nel corso di una o più settimane. In questo modo, si possono rilevare le correlazioni rilevanti per la terapia.

Affinché i pazienti comprendano che è necessario un trattamento forte e costantemente efficace, è importante spiegare loro che anche quando la pelle non presenta sintomi, l’attività infiammatoria può essere presente sotto la superficie cutanea, sottolinea l’esperto. Il concetto di “infiammazione cronica minima persistente” è noto da altre malattie associate alle allergie ed è stato confermato anche nell’orticaria.
Si raccomanda di utilizzare un antistaminico H1 di seconda generazione come terapia di prima linea per tutti i tipi di orticaria [1,2] . Questi agenti annullano l’effetto dell’istamina sul recettore H1. Secondo la linea guida, le sostanze basate sull’evidenza, efficaci e approvate in Svizzera sono, ad esempio, la bilastina, la cetirizina, la desloratadina, la fexofenadina e la levocetirizina [1,2], Nei pazienti con orticaria cronica, l’aumento della dose fino a quattro volte la dose standard* è raccomandato come opzione terapeutica di seconda scelta in caso di mancata risposta. “Il dosaggio elevato aiuta a ridurre il rilascio di citochine”, spiega il Prof. Zuberbier [3]. Tuttavia, l’uso contemporaneo di diversi antistaminici H1 non è raccomandato. Uno dei motivi è che non solo le istamine, ma anche altre citochine sono coinvolte, spiega il relatore [3].
* off-label
Omalizumab come add-on: Valutare la risposta al trattamento
Nei pazienti che non mostrano una risposta sufficiente al trattamento antistaminico (dosato) dopo 2-4 settimane, si raccomanda una terapia aggiuntiva con omalizumab [1,2]. Se il dosaggio standard di 300 mg ogni 4 settimane non è efficace, recentemente è stato consigliato di prescrivere omalizumab a dosi più elevate e/o a intervalli più brevi. Gli studi supportano l’uso di omalizumab in dosi fino a 600 mg e con intervalli di 2 settimane. Esistono numerosi studi sulla previsione della risposta alla terapia. In base a ciò, i bassi valori di IgE al basale sono correlati negativamente con la risposta alla terapia con omalizumab, ma sono correlati positivamente con la risposta alla ciclosporina [3,4]. I risultati di uno studio osservazionale multicentrico [5] mostrano che un aumento della dose può essere utile in caso di mancata risposta a omalizumab. Un sottogruppo di pazienti con CSU che avevano un UAS7 >6 su omalizumab 300 mg ogni quattro settimane sono stati aumentati a 450 mg e alcuni sono stati successivamente aumentati a 600 mg, a intervalli di dose di quattro settimane ciascuno. Il 75% dei pazienti in trattamento con dose elevata ha raggiunto una UAS7 ≤6, cioè un buon controllo dei sintomi.
Come dimostra uno studio condotto durante la pandemia di Corona, i pazienti addestrati possono autosomministrarsi omalizumab a casa [6]. L’83% degli intervistati desiderava una continuazione a lungo termine della terapia nell’ambiente domestico. Le preoccupazioni relative alla somministrazione a domicilio, come gli errori di iniezione o la dimenticanza di una dose, sono state menzionate molto raramente.
Omalizumab è efficace anche dopo l’interruzione della terapia?
Il controllo completo implica una gestione flessibile dell’orticaria, afferma il Prof. Zuberbier [3]. Per esempio, a seconda dell’esito del trattamento, omalizumab può essere sospeso o può essere preso in considerazione un aumento della dose. Nello studio OPTIMA [7,8] si è potuto dimostrare che l’anticorpo anti-IgE è efficace anche dopo l’interruzione della terapia. I pazienti adulti affetti da CSU hanno ricevuto un trattamento con omalizumab 150 mg o 300 mg come add-on, in aggiunta agli antistaminici H1, a intervalli di dose di 4 settimane. 115 dei 314 pazienti CSU totali trattati in questo modo hanno raggiunto un buon controllo dei sintomi (UAS7 ≤6) alla settimana 24. Tuttavia, una media del 44,5% del gruppo da 150 mg e del 50% del gruppo da 300 mg ha avuto una ricaduta (UAS7 ≥16) 4,7 settimane dopo la sospensione di omalizumab. Dopo la ripresa della terapia con omalizumab, l’87,8% delle persone colpite ha ottenuto un nuovo controllo dei sintomi (UAS7 ≤6).
Ciclosporina A come “ultima ratio
Nei pazienti con orticaria cronica che non rispondono agli antistaminici H1 ad alto dosaggio e all’omalizumab, può essere raccomandato l’uso della ciclosporina A (CSA) in aggiunta alla terapia antistaminica. Il CSA ha un effetto immunosoppressivo e un effetto moderato e diretto sul rilascio dei mediatori dei mastociti. L’efficacia della CSA in combinazione con un antistaminico H1 modificato di seconda generazione è stata dimostrata in studi controllati con placebo [9–11] nella CSU, ma questo farmaco non può essere raccomandato come trattamento standard a causa di una maggiore incidenza di effetti avversi [10].
L’uso a lungo termine o regolare di glucocorticosteroidi sistemici non è raccomandato nella linea guida [1,2].
Congresso: Riunione annuale EEACI
Letteratura:
- Zuberbier Z, et al: Linea guida tedesca S3 sulla classificazione, diagnosi e terapia dell’orticaria, adattata dalla linea guida internazionale S3, 2022. Registro delle linee guida AWMF (013-028).
- Zuberbier T, et al: La linea guida internazionale EAACI/GA²LEN/EuroGuiDerm/APAAACI per la definizione, la classificazione, la diagnosi e la gestione dell’orticaria. Allergia 2022; 77(3): 734-766.
- “Orticaria – l’aggiornamento 2021 sulla diagnosi e la gestione”, Prof. Torsten Zuberbier, MD, Congresso ibrido EEACI, 1-3 luglio 2022.
- Ertas R, et al.: La risposta clinica all’omalizumab nei pazienti affetti da orticaria cronica spontanea è legata e prevista dai livelli di IgE e dalla loro variazione. Allergia 2018; 73(3): 705-712.
- Curto-Barredo L, et al: L’aggiornamento di Omalizumab consente il controllo dell’attività della malattia nei pazienti con orticaria cronica spontanea refrattaria. Br J Dermatol 2018; 179(1): 210-212.
- King C, et al: Rapida transizione al trattamento domiciliare con omalizumab per l’orticaria cronica spontanea durante la pandemia COVID-19: una prospettiva del paziente. World Allergy Organ J 2021; 14(10): 100587.
- Lynde C, et al: Ritiro di Omalizumab nei pazienti con Orticaria Idiopatica Cronica/Urticaria Spontanea Cronica in seguito al ritorno dei sintomi: risultati primari dello studio OPTIMA EADV. Poster presentato alla Conferenza di Dermatologia Clinica 2017.
- Sussman G, et al: Re-trattamento di Omalizumab e Step-Up nei pazienti con orticaria cronica spontanea: Studio OPTIMA. J Allergy Clin Immunol Pract 2020; 8(7): 2372-2378.e5.
- Grattan CE, et al: Studio randomizzato in doppio cieco della ciclosporina nell’orticaria cronica ‘idiopatica’. Br J Dermatol 2000; 143(2): 365-372.
- Vena GA, et al: Ciclosporina nell’orticaria cronica idiopatica: uno studio in doppio cieco, randomizzato, controllato con placebo. Giornale dell’Accademia Americana di Dermatologia. Ottobre 2006; 55(4): 705-709.
- Kulthanan K, et al: Ciclosporina per l’orticaria cronica spontanea: una meta-analisi e una revisione sistematica. J Allergy Clin Immunol Pract 2018; 6(2): 586-599.
- Mlynek A, et al.: Come valutare l’attività della malattia nei pazienti con orticaria cronica? Allergia 2008; 63(6): 777-780.
- Mathias SD, et al: Sviluppo di un diario giornaliero per i pazienti con orticaria cronica idiopatica. Ann Allergy Asthma Immunol 2010;105(2): 142-148.
- Yanase Y, et al.: Il ruolo dei fattori di coagulazione e del complemento per l’attivazione dei mastociti nella patogenesi dell’orticaria cronica spontanea. Cellule 2021; 10(7): 1759.
DERMATOLOGIE PRAXIS 2022; 32(4): 16-18 (pubblicato il 22.8.22, prima della stampa).