Nonostante il numero crescente di aneurismi cerebrali trattati per via endovascolare, molti casi richiedono una competenza chirurgica a causa della loro anatomia, forma e configurazione. Negli ultimi 20 anni, medici e ingegneri hanno lavorato instancabilmente per migliorare la terapia chirurgica ed endovascolare. Una revisione delle moderne tecniche di trattamento chirurgico ed endovascolare degli aneurismi.
Nonostante il numero crescente di aneurismi cerebrali trattati per via endovascolare, molti casi richiedono una competenza chirurgica a causa della loro anatomia, forma e configurazione. Dall’introduzione del microscopio chirurgico e delle clip fenestrate negli anni ’60 [1], sono stati compiuti grandi sforzi per migliorare l’accesso chirurgico, il design delle clip e le procedure operative, ad esempio nella chirurgia di bypass. Inoltre, le nuove tecniche di imaging intraoperatorio hanno migliorato la sicurezza delle procedure chirurgiche. Dagli anni ’90, le bobine di platino selettivamente staccabili hanno rivoluzionato il trattamento degli aneurismi cerebrali nel campo del trattamento endovascolare [2]. Poco dopo, l’introduzione di palloncini rimodellanti ha permesso di aumentare la densità di impaccamento delle bobine intra-aneuristiche e di chiudere temporaneamente un vaso rotto per via endovascolare [3]. Un decennio dopo, gli stent sono stati introdotti nella terapia endovascolare, rendendo possibile per la prima volta il trattamento degli aneurismi a base ampia [4]. In precedenza, tali aneurismi potevano essere trattati solo chirurgicamente. Negli ultimi 20 anni, medici e ingegneri hanno lavorato instancabilmente per migliorare la terapia chirurgica ed endovascolare. In questo articolo descriviamo le moderne tecniche di trattamento chirurgico ed endovascolare degli aneurismi.
Tecniche chirurgiche
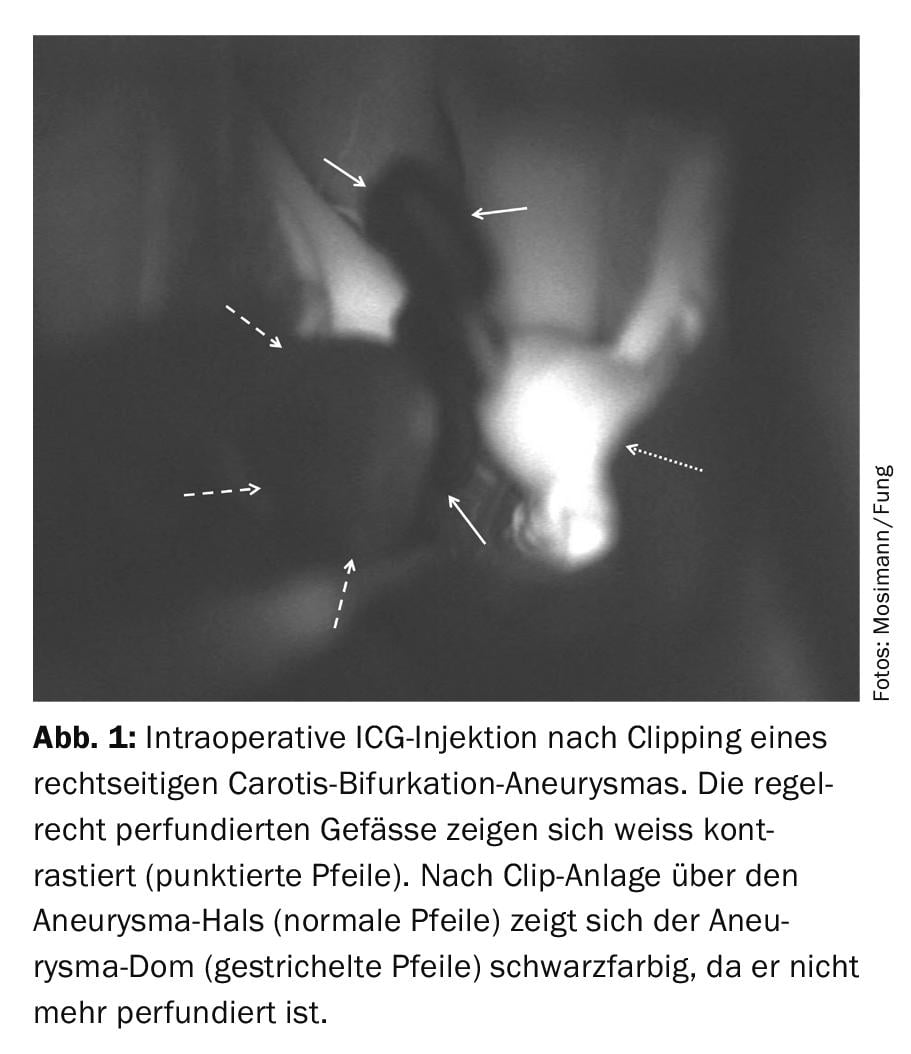
La minimizzazione dell’invasività della terapia chirurgica è il fulcro della neurochirurgia moderna. In pazienti selezionati, la chirurgia keyhole con un’apertura minima della volta cranica è possibile nonostante lo spazio chirurgico limitato e consente un recupero post-operatorio più rapido e anche risultati estetici migliori [5]. La riduzione al minimo di questi interventi è in parte resa possibile dai moderni sistemi di navigazione. Anche la tecnica di clippaggio degli aneurismi e il design delle clip stesse sono stati perfezionati. Le nuove clip per aneurisma in titanio assicurano un’elevata forza di chiusura e non causano quasi alcun artefatto da risonanza magnetica, il che migliora notevolmente le possibilità di un follow-up radiologico non invasivo [6]. Ulteriori sviluppi nel campo delle clip non ferromagnetiche e degli algoritmi di imaging potrebbero eliminare completamente il problema degli artefatti in futuro. La chirurgia ricostruttiva vascolare per gli aneurismi complessi, con l’utilizzo di più tipi di clip per aneurismi, fa parte dei moderni centri vascolari [7,8]. Inoltre, i miglioramenti nella chirurgia di bypass hanno ampliato le opzioni di trattamento chirurgico per gli aneurismi grandi e giganti (>25 mm) [9]. L’imaging intraoperatorio è un’altra area in cui sono stati fatti recenti progressi, soprattutto per valutare la pervietà dei vasi di alimentazione e drenaggio o dei perforatori durante il clipping o per valutare l’occlusione completa dell’aneurisma. Il verde di indocianina (ICG) e la fluorescina (Fl) sono traccianti endovenosi che permettono al chirurgo di visualizzare i vasi e le patologie vascolari durante l’intervento [10–12]. Dopo l’iniezione dei traccianti, i vasi vengono visualizzati a luce polarizzata con una video-angiografia integrata nel microscopio (Fig. 1). Un’altra componente dei moderni interventi neurochirurgici è il neuromonitoraggio. Qui, la funzione del cervello viene monitorata elettrofisiologicamente. L’ipoperfusione cerebrale durante la chirurgia neurovascolare può essere rilevata e corretta [13]. Tutti questi metodi e sviluppi promuovono la sicurezza del paziente e insieme contribuiscono al trattamento definitivo e a lungo termine dell’aneurisma.
Tecniche endovascolari
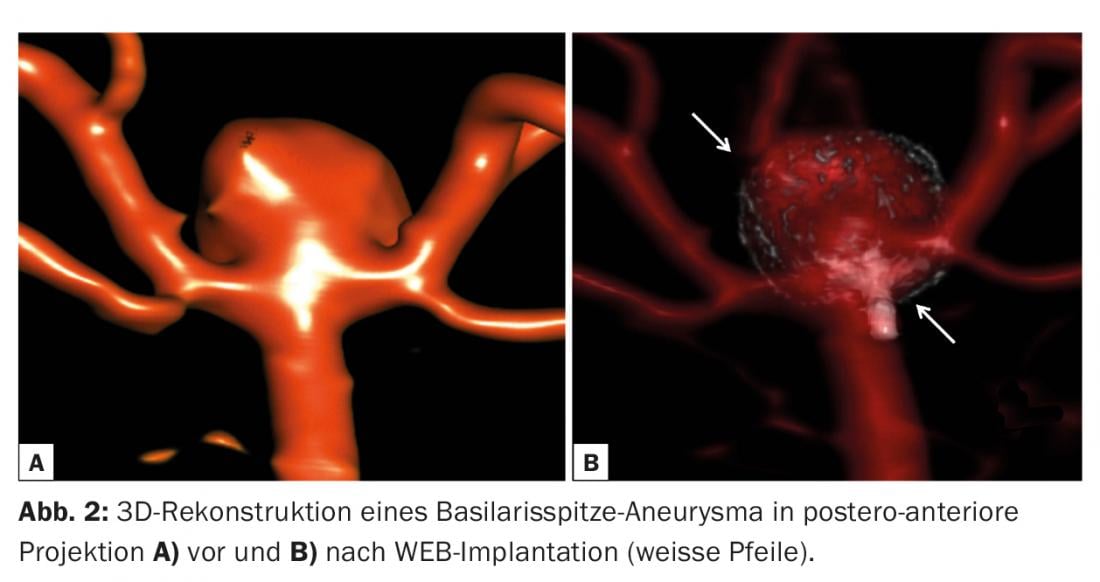
Impianti intrasacculari: Le bobine di platino standard sono disponibili in diverse forme e dimensioni e sono attualmente il gold standard per il trattamento degli aneurismi cerebrali. L’incorporazione dell’idrogel nella struttura metallica delle bobine consente una maggiore densità di impacchettamento delle bobine, creando un rigonfiamento dopo l’impianto nell’aneurisma. L’efficacia a lungo termine delle idrocoil rispetto alle coils di platino standard in termini di tassi di recidiva e di ritrattamento è controversa [14]. Recentemente sono state introdotte delle bobine simili ad ali, le bobine Medina, con l’obiettivo di prevenire la compattazione della bobina e la recidiva dell’aneurisma [15], aggiungendo del materiale supplementare al collo dell’aneurisma per fermare il flusso di sangue nell’aneurisma. Anche in questo caso, la superiorità rispetto alle bobine standard deve ancora essere dimostrata. Il dispositivo WEB è l’ultimo dispositivo intrasacculare ad essere testato in grandi registri clinici [16]. Consiste in una gabbia di nitinolo a maglie strette autoespandibili che favorisce la trombosi intrasacculare, portando all’interruzione del flusso nell’aneurisma (Fig. 2). A seconda dell’anatomia, questo dispositivo dovrebbe essere utilizzato per trattare aneurismi di grandi dimensioni e a base ampia delle biforcazioni e delle arterie terminali (biforcazione media o carotidea, aneurisma della punta basilare). La maggior parte di tutti gli aneurismi a base larga richiede uno o più stent per trattenere le bobine nel sacco aneurismatico ed evitare la ricanalizzazione. Poiché l’impianto di WEB non lascia strutture metalliche significative nel vaso portatore dell’aneurisma, non è necessaria una doppia inibizione dell’aggregazione piastrinica a lungo termine.
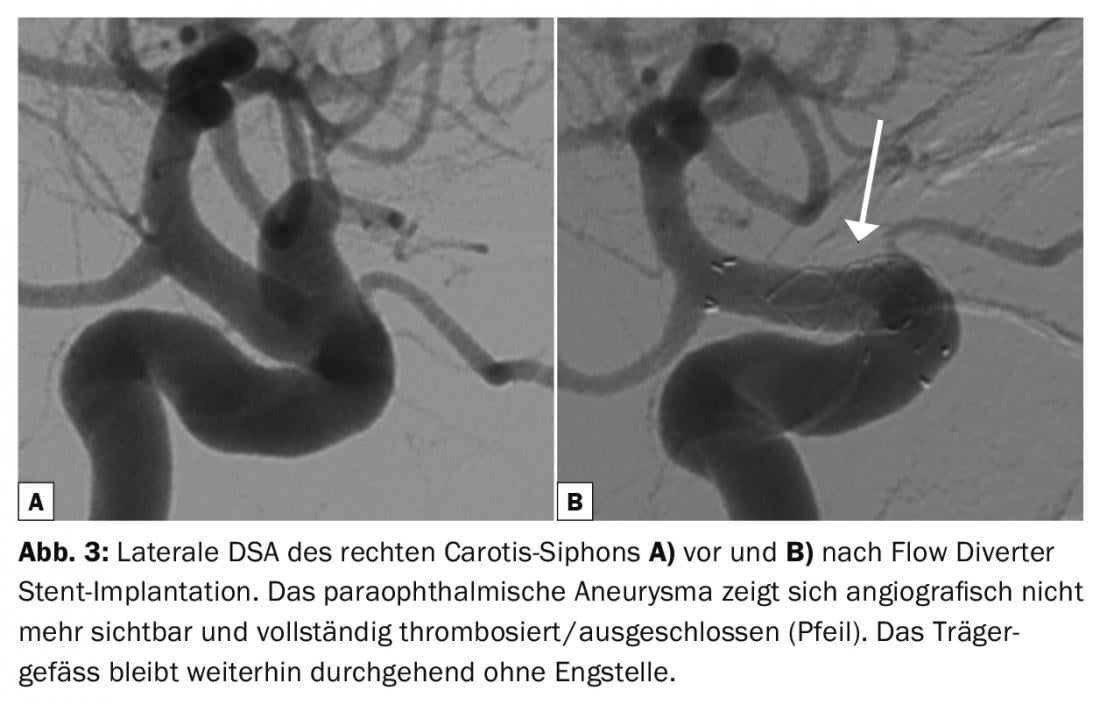
Impianti extrasacolari: L’introduzione di stent autoespandibili, flessibili e di basso profilo, che possono essere impiantati attraverso microcateteri o palloncini a doppio lume, rappresentano una svolta nel trattamento degli aneurismi distali o complessi [17]. L’ultima generazione di stent a treccia stretta, chiamati deviatori di flusso, reindirizzano il flusso sanguigno per indurre la trombosi dell’aneurisma senza riempire la sacca aneurismatica con gli impianti (Fig. 3). A volte si raccomanda un ulteriore coiling degli aneurismi giganti per escludere la rottura ritardata [18]. Attualmente si stanno valutando nuovi dispositivi di collegamento del collo che proteggono il vaso portante dell’aneurisma e il vaso efferente e preservano il flusso sanguigno durante il coiling degli aneurismi della biforcazione a base larga (Comaneci, Pulse Rider, eCLIP, pCONus) [19–22]. Il PCANvas [23] è un dispositivo sperimentale simile al pCONus che contiene una membrana aggiuntiva per aumentare l’interruzione del flusso. Gli esami clinici sono attualmente in corso.
Interventi ibridi
Alcune sale operatorie offrono strutture e materiali per interventi chirurgici ed endovascolari combinati, per consentire alle due discipline neurovascolari di collaborare direttamente.
Gli interventi ibridi non solo hanno un impatto sulla gestione chirurgica, ma possono anche contribuire ad aumentare l’efficienza dei costi.
Limitazioni
Nonostante i continui progressi della medicina, il trattamento di alcuni aneurismi rappresenta una grande sfida, a volte addirittura un’impossibilità, indipendentemente dalla tecnica scelta. In particolare, gli aneurismi fusiformi giganti dell’arteria basilare hanno un decorso spontaneo molto sfavorevole, con mortalità e morbilità elevate, a causa della loro crescita difficile da controllare. Ciò è dovuto alle emorragie, all’effetto di occupazione dello spazio e ai ripetuti colpi del tronco encefalico [24]. Sono state sperimentate molte strategie endovascolari e microchirurgiche, alcune con successo, ma tutte implicano un elevato rischio di trattamento.
Conclusione
Negli ultimi due decenni, sono state sviluppate molte tecniche chirurgiche ed endovascolari innovative. Sebbene i nuovi sviluppi endovascolari siano in primo piano, un numero rilevante di aneurismi richiede una terapia chirurgica altamente specializzata. Gli incontri interdisciplinari sono la pietra miliare di un’assistenza ottimale al paziente, indipendentemente dal metodo di trattamento preso in considerazione.
Messaggi da portare a casa
- Le nuove clip per aneurisma in titanio garantiscono un’elevata forza di chiusura e non causano quasi nessun artefatto da risonanza magnetica.
- La chirurgia ricostruttiva vascolare per gli aneurismi complessi, utilizzando più tipi di clip per aneurismi, fa parte dei moderni centri vascolari.
- Il dispositivo WEB è il più recente dispositivo intrasacculare. La sua gabbia di nitinolo a maglia stretta autoespandibile favorisce la trombosi intrasacculare.
- Gli stent flessibili e autoespandibili rappresentano una svolta nel trattamento degli aneurismi distali o complessi. I cosiddetti deviatori di flusso reindirizzano il flusso sanguigno per provocare la trombosi dell’aneurisma.
Letteratura:
- Zada G, et al: Neurosurg Focus 2009; 26: E7.
- Guglielmi G, et al: J Neurosurg 1991; 75: 8-14.
- Moret J, et al: Interv Neuroradiol 1997; 3: 21-35.
- Lanzino G, et al: J Neurosurg 1999; 91: 538-46.
- Hopf NJ, et al: Minim Invasive Neurosurg 2009; 52: 126-31.
- Horiuchi T, et al: Neurosurg Rev 2013; 36: 133-7.
- Acciarri N, et al: J Neurosurg Sci 2016; 60: 83-94.
- Yang I, et al: Neurosurgery 2008; 62: ONS371-8; discussione 8-9.
- Tayebi Meybodi A, et al: J Neurosurg 2016; 4: 1-17
- Raabe A et al: Neurosurgery 2003; 52(1): 132-9; discussione 139.
- Raabe A et al: J Neurosurg 2005; 103(6): 982-9.
- Lane B, et al: J Neurosurg 2015; 122: 618-26.
- Staarmann B, et al: World Neurosurg 2017; 100: 522-30.
- Broeders JA, et al: J Neurointerv Surg 2016; 8: 898-908.
- Sourour NA, et al: Neurosurgery 2017 (epub, ahead of print).
- Pierot L, et al: AJNR Am J Neuroradiol 2017; 38: 1151-5.
- Akmangit I, et al: AJNR Am J Neuroradiol 2015; 36: 323-9.
- Rouchaud A, et al: Neuroradiologia 2016; 58: 171-7.
- Fischer S, et al: J Neurointerv Surg 2016; 0: 1-5.
- Spiotta AM, et al: J Neurointerv Surg 2016; 8: 186-9.
- Chiu AH, et al: J NeuroSurg 2017; 17: 1-8.
- Perez MA, et al: J Neurointerv Surg 2017; 9: 39-44.
- Perez MA, et al: J Neurointerv Surg 2016; 8: 1197-201.
- Saliou G, et al: Stroke 2015; 46: 948-53.
InFo NEUROLOGIA & PSICHIATRIA 2017; 15(5): 8-10.