Con l’oligonucleotide antisenso nusinersen, nel 2017 è stato approvato il primo farmaco per il trattamento causale dei pazienti con atrofia muscolare spinale associata a 5q (5q-SMA) [1]. Il farmaco si rivolge alla causa della malattia, la mancanza della proteina SMN [1]. Studi clinici approfonditi e reali hanno dimostrato che nusinersen può portare alla stabilizzazione e persino al miglioramento della funzione motoria – in tutte le fasce di età e nei tipi di SMA I-III [2-7].
La 5q-SMA è una malattia neomuscolare progressiva autosomica recessiva [8]. Se non vengono trattati, i pazienti rischiano una degenerazione progressiva dei motoneuroni, con conseguente aumento della debolezza e dell’atrofia dei muscoli [8]. Fino all’introduzione di una terapia farmacologica efficace dal punto di vista causale, la forma infantile di 5q-SMA, in cui i sintomi sono già evidenti nei primi 6 mesi di vita, era considerata una delle cause genetiche più comuni di morte nei neonati e nei bambini piccoli [8]. Con il nusinersen (SPINRAZA®), è disponibile un’opzione terapeutica che consente di mantenere o addirittura aumentare la forza muscolare. [1-7].
Il nusinersen porta alla formazione di quantità maggiori di proteina SMN [9].
La causa della denervazione progressiva dei muscoli scheletrici è una carenza della proteina “survival motor neuron” (SMN), che è vitale per i motoneuroni. A causa di mutazioni o delezioni nel gene SMN1, nei pazienti con 5q-SMA viene prodotta troppo poca proteina SMN [8].
Il nusinersen contribuisce alla produzione di una proteina SMN più funzionale e quindi garantisce la sopravvivenza dei motoneuroni [9]. Questo può rallentare o addirittura arrestare il decorso della malattia. I pazienti beneficiano della conservazione o del miglioramento della funzione muscolare. L’efficacia di nusinersen è stata dimostrata per tutte le età e gli stati patologici: neonati con SMA 5q pre-sintomatica, bambini e adolescenti sintomatici e adulti [2-7].
I bambini con 5q-SMA beneficiano della terapia pre-sintomatica
Negli studi clinici, molti bambini con SMA 5q trattati con nusinersen sono stati in grado di raggiungere importanti tappe motorie non osservate nei pazienti non trattati con SMA 5q [2-4]. Questo ha dimostrato che la terapia precoce con SPINRAZA può consentire uno sviluppo adeguato all’età nei bambini con 5q-SMA. La maggior parte dei pazienti con diagnosi genetica di 5q-SMA che sono stati trattati in modo presintomatico con nusinersen nello studio clinico NURTURE avevano raggiunto le tappe motorie appropriate alla loro età alla valutazione intermedia dello studio (Tab. 1) [10].
Tabella 1: Valutazione intermedia dello studio NURTURE a febbraio 2020; età media dei partecipanti allo studio 3,8 anni (n = 25) [10]
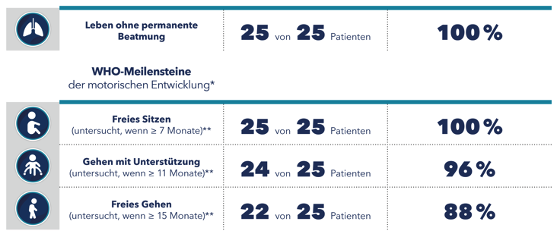





* Età in cui i bambini sani raggiungono normalmente queste pietre miliari.
** L’orario dell’esame rientrava nella finestra temporale specificata dall’OMS. [11]
Sono stati osservati miglioramenti significativi anche nelle funzioni bulbari, necessarie per la masticazione e la deglutizione [12]. Mentre molti pazienti non trattati con 5q-SMA si affaticano quando masticano, soffocano il cibo o richiedono un tubo di alimentazione [13-16], il trattamento pre-sintomatico con nusinersen nello studio NURTURE ha fatto sì che il 92% dei bambini continuasse a deglutire e l’84% riuscisse a gestire la situazione senza tubo di alimentazione [12]. Di conseguenza, i genitori dei bambini con 5q-SMA trattati con nusinersen non erano generalmente preoccupati per la deglutizione, l’alimentazione e il peso dei loro figli. [12].
L’efficacia di nusinersen è stata dimostrata anche negli adulti
Ampi dati provenienti da studi osservazionali in pazienti adulti con 5q-SMA mostrano che il trattamento con nusinersen può portare a miglioramenti significativi in tutte le scale di funzionalità motoria utilizzate (HFMSE, RULM, distanza del cammino di 6 minuti) [5-7].
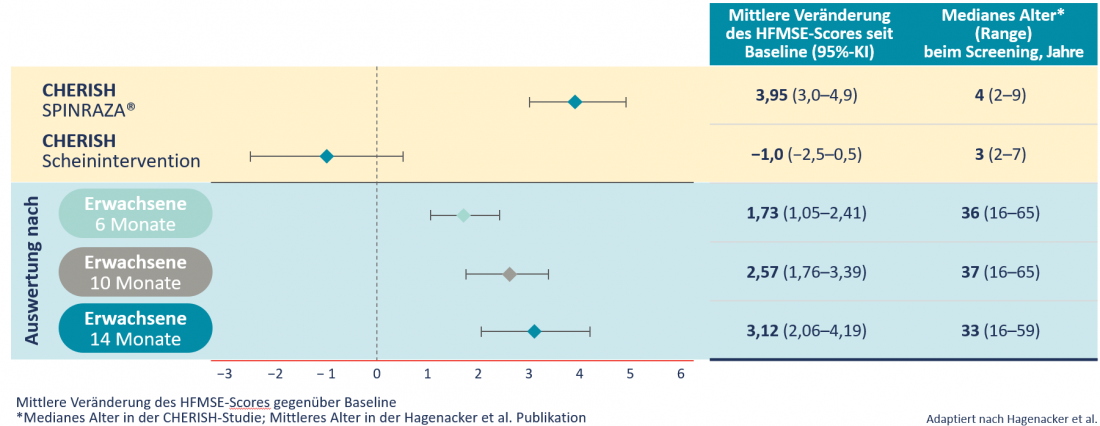
In uno studio prospettico multicentrico che ha coinvolto 139 pazienti di 10 centri clinici in Germania, un’alta percentuale di pazienti con 5q-SMA di tipo II o III ha mostrato miglioramenti clinicamente rilevanti nella funzione motoria. In tutti i momenti dello studio, i pazienti hanno ottenuto miglioramenti statisticamente significativi nel punteggio HFMSE in media. Questo è aumentato di 3,12 punti dopo 14 mesi. Nel corso naturale della malattia, tuttavia, il punteggio HFMSE diminuisce in media di 0,5-1,0 punti all’anno [6]. Un miglioramento comparabile del punteggio HFMSE è stato osservato negli adulti come nei bambini (Tab. 2) [6].
Tabella 2: Variazioni medie del punteggio HFMSE dal basale: Confronto tra 126 bambini con esordio tardivo della malattia 5q-SMA dello studio CHERISH e 173 pazienti adulti dello studio di Hagenacker et al. Pubblicazione [3,6].

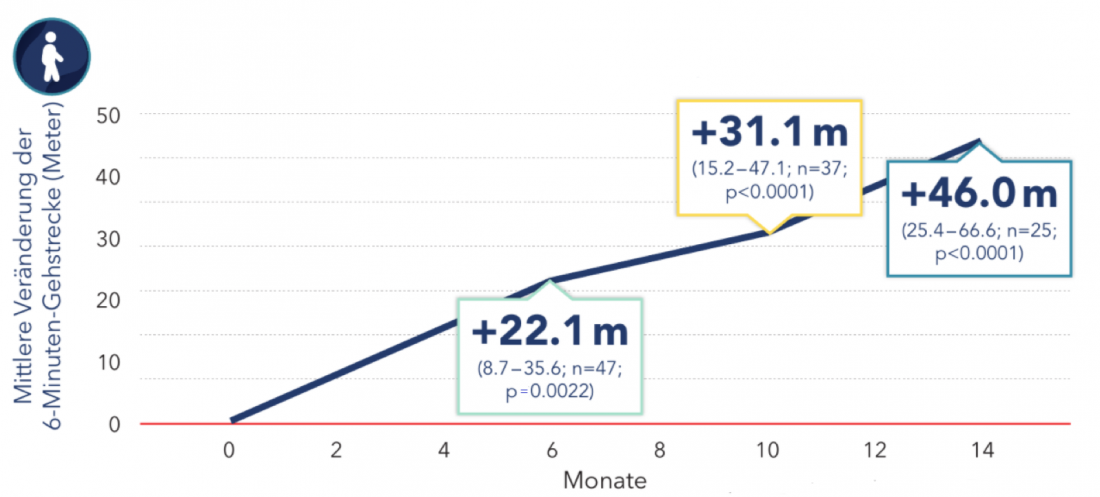
Il punteggio RULM, che misura la funzione dell’arto superiore, ha mostrato un miglioramento significativo di 1,09 punti in media dopo 14 mesi di studio. Inoltre, i pazienti sono riusciti a percorrere una media di 403 metri in 6 minuti. In media, erano in grado di camminare per 46 metri in più rispetto a prima dell’inizio della terapia (Fig. 2) [6].
L’età dei pazienti non ha influito sui risultati. Tuttavia, l’entità dei miglioramenti dipendeva dalla funzione motoria residua del paziente all’inizio dello studio. Più alto è il livello di funzione motoria residua prima dell’inizio della terapia, maggiore è l’effetto atteso della terapia con nusinersen [6].
Figura 2: Variazione della distanza di cammino di 6 minuti negli adulti con la terapia con nusinersen. I riquadri mostrano la media e l’IC al 95% [6]. Modificato secondo Hagenacker T et al. [6].
I pazienti vogliono partecipare alla vita normale
Molti pazienti adulti desiderano mantenere la loro forza in modo da potersi sedere, alzare e camminare in modo indipendente [17]. Le funzioni delle mani e delle braccia sono indispensabili per le attività quotidiane, come lavarsi o vestirsi in modo indipendente. La motricità fine gioca un ruolo importante anche nell’ambiente sociale dei pazienti, che si manifesta nell’uso di uno smartphone o di un computer portatile.
Tuttavia, nel decorso naturale della 5q-SMA, si verifica una debolezza muscolare progressiva e la perdita della funzione motoria [8]. Il trattamento con nusinersen può dare agli adulti con 5q-SMA una speranza per il futuro. In questo modo, i pazienti non solo possono ottenere una stabilizzazione a lungo termine dello status quo funzionale, ma molti di loro sperimentano miglioramenti rilevanti nelle funzioni motorie, hanno più forza nelle mani e nelle dita e possono alzarsi meglio, stare in piedi più a lungo e camminare di più [5-7].
Effetto mirato – Centrale al sistema nervoso centrale
In questo modo, Nusinersen si rivolge alla causa di 5q-SMA. Si lega reversibilmente al pre-mRNA del gene paralogico SMN2, che viene utilizzato per la formazione della proteina SMN nei pazienti con 5q-SMA. Questo sposta i fattori di splicing e l’esone 7 rimane nell’mRNA SMN2 maturo, in modo che si possa formare una proteina SMN più funzionale (Fig. 3) [1, 9].
Figura 3: Meccanismo d’azione mirato del nusinersen [9].

Il nusinersen viene somministrato per via intratecale attraverso una puntura lombare e quindi raggiunge direttamente il punto in cui dovrebbe agire: il sistema nervoso centrale [1]. L’applicazione intratecale fa sì che il nusinersen raggiunga direttamente il sito d’azione centrale, dove può esercitare il suo effetto mirato e specifico sul pre-mRNA del gene SMN2 [1]. L’effetto di nusinersen si manifesta rapidamente, già da 1 a 3 giorni dopo l’iniezione [18]. L’alta specificità di nusinersen e la sua applicazione mirata al sistema nervoso centrale hanno dimostrato di essere sicuri nell’uso a lungo termine e hanno anche portato a un effetto sostenuto sulla funzione motoria in un’ampia gamma di pazienti con SMA 5q [5-7,10,19-23].
Allo stesso tempo, l’applicazione intratecale presenta dei vantaggi in termini di aderenza. I dati attuali mostrano che la maggior parte dei pazienti riceve le dosi di nusinersen come previsto [24]. Per altre malattie, è stato dimostrato che la compliance è maggiore per le terapie somministrate in ambulatorio che per le terapie orali, giornaliere [25,26]. È quindi ragionevole supporre che, grazie alla somministrazione intratecale, i medici possano essere sicuri che i pazienti ricevano la giusta dose di nusinersen al momento giusto e che la loro salute e la risposta al trattamento possano essere monitorate di routine.
Non sono previsti effetti collaterali sistemici
Un vantaggio importante dell’uso intratecale di nusinersen è l’esposizione specifica al compartimento, che rende improbabili gli effetti collaterali sistemici. Ciò è stato confermato da studi clinici e reali. Mal di testa, mal di schiena e vomito sono gli eventi avversi più frequentemente osservati associati alla somministrazione intratecale [1]. Possono verificarsi poco dopo la somministrazione di nusinersen e sono in gran parte dovuti alla sindrome postpuntura che può verificarsi dopo la puntura lombare anche senza l’applicazione di sostanze medicinali [6]. Il profilo di sicurezza di nusinersen è ben documentato da 7 anni [19].
Può essere utilizzato anche per la scoliosi
Anche nei casi di scoliosi pronunciata o di altre gravi deformità spinali, che sono comuni nei pazienti SMA 5q, l’iniezione intratecale di nusinersen può generalmente avere successo, essere sicura e rapida [27]. Se necessario, l’iniezione nello spazio del liquor deve essere effettuata sotto controllo di imaging mediante tomografia computerizzata (TC) [27].
Conclusione
L’applicazione centrale di nusinersen fornisce un effetto mirato direttamente dove è necessario. L’efficacia di nusinersen è stata dimostrata in ampi studi clinici e in studi reali per tutte le età e gravità della SMA 5q [2-7]. Anche i pazienti adulti con 5q-SMA possono beneficiare della terapia e ottenere una stabilizzazione o un miglioramento clinicamente significativo della funzione motoria [5-7].
Il beneficio di nusinersen si riflette anche nella soddisfazione dei pazienti: in uno studio osservazionale prospettico su pazienti adulti condotto in Germania, il 95,7% ha riferito di essere soddisfatto di nusinersen – indipendentemente dall’età e dalla gravità della malattia [28].
Nel frattempo, esiste un’ampia esperienza nella pratica clinica quotidiana. Ad oggi, più di 11.000 pazienti in tutto il mondo sono stati trattati con nusinersen [29].
Letteratura
- Informazioni tecniche su SPINRAZA®, al mese di agosto 2019 (www.swissmedicinfo.ch)
- Finkel RS, Mercuri E, Darras BT, et al. Nusinersenrispetto al controllo Sham nell’atrofia muscolare spinale ad esordio infantile. N Eangl J Med. 2017;377:1723-32.
- Mercuri E, Darras BT, Chiriboga CA, et al. Nusinersen rispetto al controllo Sham nell’atrofia muscolare spinale ad insorgenza tardiva. N Engl J Med. 2018;378:625-35.
- De Vivo DC, Bertini E, Swoboda KJ, et al. Nusinersen iniziato nei bambini durante la fase presintomatica dell’atrofia muscolare spinale: risultati intermedi di efficacia e sicurezza dello studio di fase 2 NURTURE. Disordine neuromuscolare. 2019;29:842-56.
- Walter MC, Wenniger S, Thiele S, et al. Sicurezza ed effetti del trattamento di Nusinersen negli adulti di lunga data con 5q-SMA di tipo 3 – Uno studio prospettico osservazionale. J Neuromuscul Dis. 2019;6:453-65.
- Hagenacker T, Wurster CD, Günther R, et al. Nusinersen negli adulti con atrofia muscolare spinale 5q: uno studio di coorte osservazionale non interventistico, multicentrico. Lancet Neurol. 2020;19:317-25.
- Maggi L, Bello L, Bonanno S, et al. Sicurezza del nusinersened effetti sulla funzione motoria nell’atrofia muscolare spinale adulta di tipo 2 e 3. J Neurol Neurosurg Psychiatry. 2020;91(11):1166-74.
- Lunn MR, Wang CH. Atrofia muscolare spinale. Lancet. 2008;371:2120-33.
- Goodkey K, Ashley T, Maruyama R, et al. Nusinersen nel trattamento dell’atrofia muscolare spinale. Metodi Mol Biol. 2018; 1828: 69-76.
- Swoboda KJ, Kirschner J, Finkel RS, et al; Gruppo di studio NURTURE. Effetto del nusinersen nei neonati che iniziano il trattamento in una fase presintomatica della SMA: risultati di NURTURE. Conferenza virtuale Cure SMA 2020; 8-12 giugno 2020; https://curesma2020.biogenscicomm.com/curesma2020/sma/swoboda/#home. Recuperato nel settembre 2021.
- Gruppo di studio multicentrico di riferimento sulla crescita dell’OMS. Studio sullo sviluppo motorio dell’OMS: finestre di raggiungimento per sei tappe dello sviluppo motorio lordo. Acta Paediatr Suppl. 2006; 450: 86 – 95.
- Swoboda KJ, Sansone VA, De Vivo DC, et al. Funzione di deglutizione conservata nei bambini che hanno iniziato il trattamento con nusinersen nella fase presintomatica della SMA: risultati dello studio NURTURE. Presentato alla Conferenza clinica e scientifica MDA 2021, 15-18 marzo 2021.
- Van der Heul AMB, Wijngaarde CA, Wadman RI, et al. Problemi bulbari auto-riferiti da bambini e adulti con atrofia muscolare spinale. J Neuromuscul Dis. 2019;6:361-8.
- Finkel RS, McDermott MP, Kaufmann P, et al. Studio osservazionale dell’atrofia muscolare spinale di tipo I e implicazioni per gli studi clinici. Neurologia. 2014;83:810-7.
- Van der Heul AMB, Cuppen I, Wadman RI, et al. Problemi di alimentazione e deglutizione nei bambini con atrofia muscolare spinale di tipo 1: uno studio osservazionale. J Neuromuscul Dis. 2020;7:323-30.
- Choi YA, Suh DI, Chae JH, et al. Traiettoria del cambiamento dello stato di deglutizione nell’atrofia muscolare spinale di tipo I. Int J Pediatr Otorinolaryngol. 2020;130:109818.
- Burbridge C, Kelly K, Garcia L, et al. PND74 Mappatura di un’esplorazione qualitativa del cambiamento significativo nell’atrofia muscolare spinale di tipo II o III con la Hammersmith Functional Motor Scale Expanded (HFMSE). Valore nella salute. 2019; 22, Suppl 2, p284.
- Mazur C, Powers B, Zasadny K, et al. La farmacologia cerebrale degli oligonucleotidi antisenso intratecali rivelata attraverso l’imaging multimodale. JCI Insight. 2019;4:e129240.
- Claborn MK, Stevens DL, Walker CK, et al. Nusinersen: un trattamento per l’atrofia muscolare spinale. Ann Pharmacother. 2019; 53(1): 61-69.
- Castro D, Finkel RS, Farrar MA, et al. Nusinersen nell’atrofia muscolare spinale infantile: risultati del trattamento a lungo termine dello studio di estensione SHINE in aperto. Neurologia. 2020; 94(15):1640.
- Chiriboga CA, et al. Trattamento a lungo termine con nusinersen: risultati dello studio shine nell’atrofia muscolare spinale ad insorgenza tardiva. Presentato all’AAN 2020; 25. aprile-1. maggio 2020; https://www.neurologylive.com/view/nusinersen-shows-efficacy-in-infantile-and-lateonset-spinal-muscular-atrophy; Recuperato nel settembre 2021.
- Acsadi G, Crawford TO, Müller-Felber W, et al. Sicurezza ed efficacia del nusinersen nell’atrofia muscolare spinale: lo studio EMBRACE. Nervo muscolare. 2021;63:668-77.
- Duong T, Wolford C, McDermott, MP, et al. Trattamento con Nusinersen negli adulti con atrofia muscolare spinale. Neurol Clin Practice. 2021; 11(3): e317-27.
- Paradis A, et al. Esperienza di Nusinersen nell’atrofia muscolare spinale ad esordio tardivo. Presentato al WMS 2020.
- Seal BS, Anderson S, Shermock KM, et al. Fattori associati ai tassi di aderenza alla terapia antitumorale orale e endovenosa nei pazienti con cancro al colon metastatico assicurati commercialmente. J Manag Care Spec Pharm. 2016;22:227-35.
- Moran K, Null K, Huang Z, et al. Analisi retrospettiva dei reclami che confronta indirettamente l’aderenza ai farmaci e la persistenza tra i biologici per via endovenosa e le terapie orali a piccole molecole nelle malattie infiammatorie intestinali. Terapia avanzata. 2019;36:2260-72.
- Cordts I, Lingor B, Friedrich P, et al. Somministrazione di nusinersen intratecale in pazienti adulti affetti da atrofia muscolare spinale con anatomia spinale complessa. Ther Adv Neurol Disord 2020; 13: 1756286419887616
- Meyer T, Maier, A, Uzelac Z, et al. Aspettative di trattamento e percezione della terapia in pazienti adulti con atrofia muscolare spinale che ricevono nusinersen. Eur J Neurol. 2021; 28(8): 2582-95.
- Nuovi dati a Cure SMA 2021; Biogen, https://investors.biogen.com/news-releases/news-release-details/new-data-cure-sma-2021-highlight-long-term-efficacy-spinrazar; Ultimo accesso: settembre 2021
Riassunto delle informazioni sul prodotto SPINRAZA® Z: Una fiala contiene 12 mg di nusinersen in 5 ml di liquido cerebrospinale artificiale. I: Trattamento dell’atrofia muscolare spinale (SMA) associata a 5q D: Applicazione intratecale mediante puntura lombare (LP). 4 Dosi di saturazione di 12 mg (5ml) per applicazione nei giorni 0, 14, 28, 63; terapia di mantenimento ogni 4 mesi 12 mg (5ml). Spinraza deve essere somministrato solo in centri neuromuscolari ospedalieri e specializzati. È obbligatorio che il personale medico curante abbia esperienza nella diagnosi e nel trattamento dei pazienti con atrofia muscolare spinale e nell’esecuzione della LP. KI: Ipersensibilità al principio attivo o agli eccipienti. VM: Non ci sono dati sulla sicurezza a lungo termine. Rischio di effetti collaterali associati alla LP. Difficoltà di LP in pazienti molto giovani/con scoliosi. Esame delle piastrine e della coagulazione prima e regolarmente durante la terapia. Monitoraggio delle proteine dell’urina prima e regolarmente durante la terapia. ECG prima di iniziare e regolarmente durante la terapia. Possibile neurotossicità a dosi elevate e/o a lungo termine. Nei pazienti con perdita di coscienza, considerare un’indagine per l’idrocefalo. S: Non consigliato durante la S. UW: Forma infantile: Infezioni respiratorie, rinofaringiti, infezioni del tratto urinario, infezioni dell’orecchio, influenza, stipsi, flatulenza, perdita di peso, eruzioni cutanee. Insorgenza successiva della malattia: febbre, mal di testa, vomito, epistassi, congestione delle vie respiratorie, allergia stagionale, mal di schiena, caduta. Possibile riduzione della crescita. L’incidenza degli anticorpi anti-farmaco (ADA) è bassa; non è stato rilevato alcun impatto apparente dello sviluppo di ADA sulla risposta clinica, sugli eventi avversi o sul profilo farmacocinetico di nusinersen. Postmarketing: Infezioni gravi come meningite, idrocefalo comunicante, meningite asettica, ipersensibilità (ad esempio angioedema, orticaria, rash). IA: Nessuna interazione con il CYP450, interazione dovuta al legame competitivo con le proteine plasmatiche, effetto competitivo o inibizione dei trasportatori bassa. Elenco A. Le informazioni professionali complete sono pubblicate su www.swissmedicinfo.ch. Biogen Switzerland AG, 6340 Baar. Stato delle informazioni: agosto 2019. Biogen-29360_09.2020
Biogen Svizzera AG
Neuhofstrasse 30
6340 Baar
www.biogen.ch
Biogen-128051_09.2021