L’approvazione dell’anticorpo anti-CCR4 mogamulizumab consente ai pazienti con linfoma cutaneo a cellule T (CTCL) dei sottotipi micosi fungoide (MF) e sindrome di Sézary (SS) di ricevere per la prima volta un intervento efficace non chemioterapico dopo una precedente terapia sistemica. L’opzione terapeutica innovativa è stata in grado di mostrare una sopravvivenza libera da progressione significativamente migliore e una risposta a lungo termine nei comparti del sangue e della pelle rispetto alla terapia comparativa.
Il linfoma cutaneo a cellule T (CTCL) è caratterizzato dalla migrazione di cellule T degenerate nella pelle [3]. La malattia, rara ma grave, può colpire la pelle, il sangue, i linfonodi e i compartimenti degli organi interni [4,5]. I sottotipi più frequenti osservati sono MF e SS, come ha sottolineato il Prof. Dr. med. Reinhard Dummer, Zurigo, [3,5–7]. Sono tipiche le macchie e le placche rosse, che mostrano somiglianze con altre malattie della pelle e di conseguenza sono spesso attribuite alla psoriasi o all’eczema [8]. Pertanto, ci vogliono in media da due a sette anni prima della diagnosi – un tempo prezioso in cui la malattia può progredire [8]. Questo perché anche nelle fasi iniziali, fino al 34% dei pazienti con MF va incontro a progressione della malattia [7]. Nello stadio avanzato, solo il 52% delle persone colpite sopravvive più di cinque anni [9].
Elevata richiesta di una terapia efficace
La diagnosi più precoce possibile di CTCL è fondamentale per avviare una gestione terapeutica efficace. Oltre all’aumento del rischio di mortalità, i pazienti soffrono anche di una forte riduzione della qualità della vita, secondo l’esperto [10]. L’obiettivo della terapia deve quindi essere la remissione nei comparti interessati, il sollievo dai sintomi e la minimizzazione della progressione della malattia [11].
Approvato l’anticorpo anti-CCR4
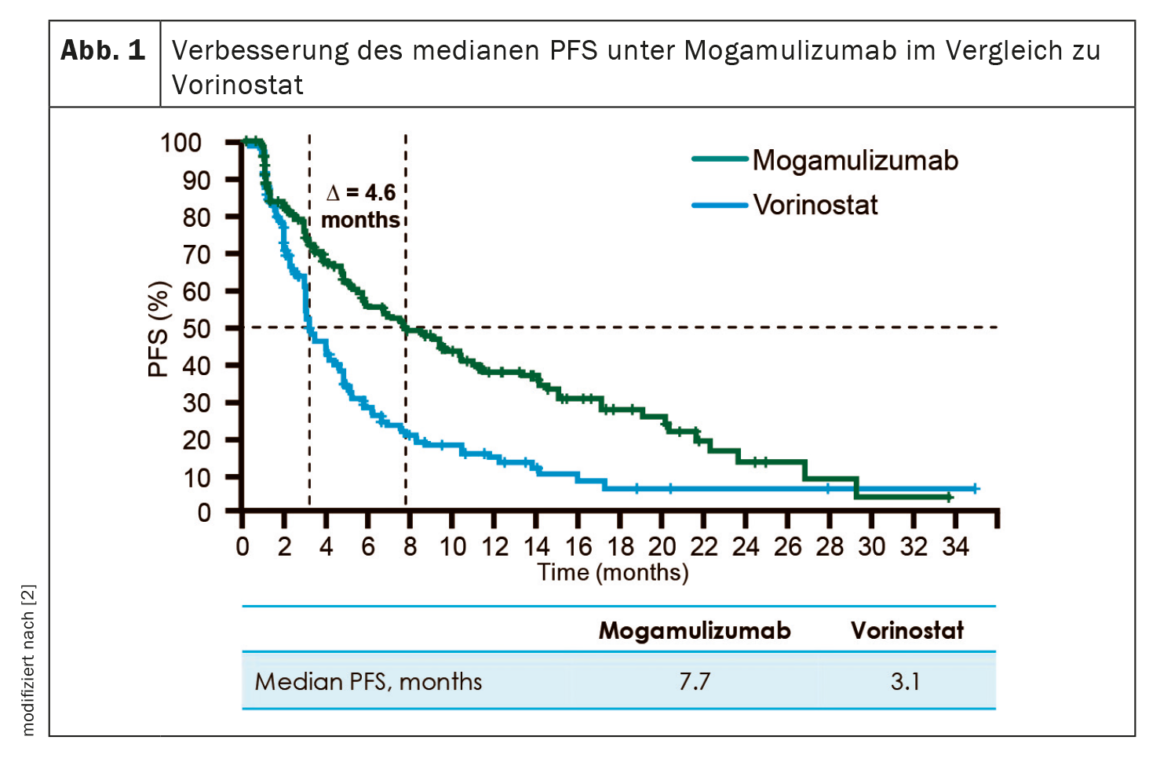
Con mogamulizumab (Poteligeo®), è stata approvata in Svizzera la prima terapia anticorpale per i pazienti adulti affetti da CTCL con MF o SS che hanno ricevuto almeno una precedente terapia sistemica [1]. L’approvazione si basa sui risultati dello studio di fase III MAVORIC [2]. Randomizzati in un rapporto 1:1, 372 pazienti hanno ricevuto o mogamulizumab 1,0 mg/kg i.v. settimanalmente per i primi 28 giorni e il giorno 1 e il giorno 15 nei cicli successivi, oppure vorinostat 400 mg al giorno (non approvato in Svizzera). Come ha spiegato la Prof.ssa Emmanuella Guenova, Losanna, MD, mogamulizumab ha prolungato la PFS mediana di oltre il doppio (7,7 mesi vs. 3,1 mesi) rispetto a vorinostat (Fig. 1) [2]. Inoltre, la terapia con anticorpi ha determinato una risposta complessiva più elevata, soprattutto nei comparti della pelle (41,9% contro 15,6%) e del sangue (66,9% contro 18,4%) [1]. La durata mediana della risposta è stata di 20,6 e 25,5 mesi, rispettivamente [2]. Inoltre, è stato raggiunto un miglioramento della qualità di vita nell’80% delle persone colpite nell’11° ciclo di terapia [12]. Nel complesso, il trattamento con mogamulizumab è stato ben tollerato e ha mostrato un profilo di sicurezza gestibile [2,13]. Le reazioni avverse più comunemente segnalate sono state le reazioni correlate all’infusione (30%) e l’eruzione cutanea da farmaco (21,5%) [1].
Fonte: Kyowa Kyrin
Letteratura:
- Poteligeo® SmPC, da maggio 2022 a
www.swissmedicinfo.ch. - Kim YH, et al: Mogamulizumab versus vorinostat nel linfoma cutaneo a cellule T precedentemente trattato (MAVORIC): uno studio internazionale di fase 3, in aperto, randomizzato e controllato. Lancet Oncol 2018; 19(9): 1192-1204.
- Nicolay JP, et al: CCR4 nel linfoma cutaneo a cellule T: bersaglio terapeutico di un driver patogeno. Eur J Immunol 2021; 51: 1660-1671.
- Organizzazione Nazionale per i Disturbi Rari: Database delle Malattie Rare: Linfomi Cutanei a Cellule T. Disponibile all’indirizzo: https://rarediseases.org/rare-diseases/cutaneous-t-cell-lymphomas (ultimo accesso 04.11.2022).
- Krejsgaard T, et al. Infiammazione maligna nel linfoma cutaneo a cellule T – un’acquisizione ostile. Semin Immunopathol 2017;39(3): 269-282.
- Dippel E, et al: S2k – Linea guida – Linfomi cutanei (ICD10 C82 – C86) Stato: 30.06.2021. Disponibile su: www.awmf.org/uploads/tx_szleitlinien/032-027l_S2k_Kutane_Lymphome_2021-12.pdf (ultimo accesso 04.11.2022).
- Agar N, et al.: Esiti di sopravvivenza e fattori prognostici nella micosi fungoide/sindrome di Sézary: validazione della proposta di stadiazione rivista della Società Internazionale per i Linfomi Cutanei/Organizzazione Europea per la Ricerca e il Trattamento del Cancro. J Clin Oncol. 2010;28(31): 4730-4739.
- Fondazione CL: Guida per il paziente. Disponibile su: www.clfoundation.org/sites/default/files/2018-04/a_patients_guide.pdf (ultimo accesso 04.11.2022)
- Scarisbrick JJ, et al: Cutaneous Lymphoma International Consortium Study of Outcome in Advanced Stages of Mycosis Fungoides and Sézary Syndrome: Effect of Specific Prognostic Markers on Survival and Development of a Prognostic Model. J Clin Oncol 2015; 33(32): 3766-3773.
- Demierre MF, et al. Impatto significativo del linfoma cutaneo a cellule T sulla qualità di vita dei pazienti: risultati di un sondaggio della National Cutaneous Lymphoma Foundation del 2005. Cancro 2006; 107(10): 2504-2511.
- Shalabi D, et al: Evasione immunitaria e attuali strategie di immunoterapia nella micosi fungoide (MF) e nella sindrome di Sézary (SS). Chinese Clin Oncol 2019; 8(1): 11.
- Porcu P, et al: Effetto sulla qualità della vita dell’anticorpo monoclonale anti-CCR4 Mogamulizumab rispetto a Vorinostat nei pazienti con linfoma cutaneo a cellule T. Clin Lymphoma Myeloma Leuk. 2021; 21(2): 97-105.
- Afifi S, et al. Valutazione della sicurezza farmacologica di mogamulizumab per il trattamento del linfoma cutaneo a cellule T. Expert Opin Drug Saf. 2019; 18(9): 769-776.
InFo ONCOLOGIA & EMATOLOGIA 2023; 11(2): 19