Secondo la linea guida della Società Europea di Cardiologia (ESC), aggiornata lo scorso anno, l’insufficienza cardiaca viene classificata in base alla frazione di eiezione ventricolare sinistra in HFrEF, HFmrEF e HFpEF. Per quanto riguarda la terapia farmacologica, recentemente è stata raccomandata una terapia combinata precoce con ACE-i, ARNI, MRA e SGLT-2-i per tutti i pazienti. Il fatto che i pazienti con HFpEF possano trarre beneficio anche dalla terapia con gli inibitori SGLT-2 è dimostrato in particolare dai dati di nuovi studi clinici pubblicati poco dopo la pubblicazione della linea guida.
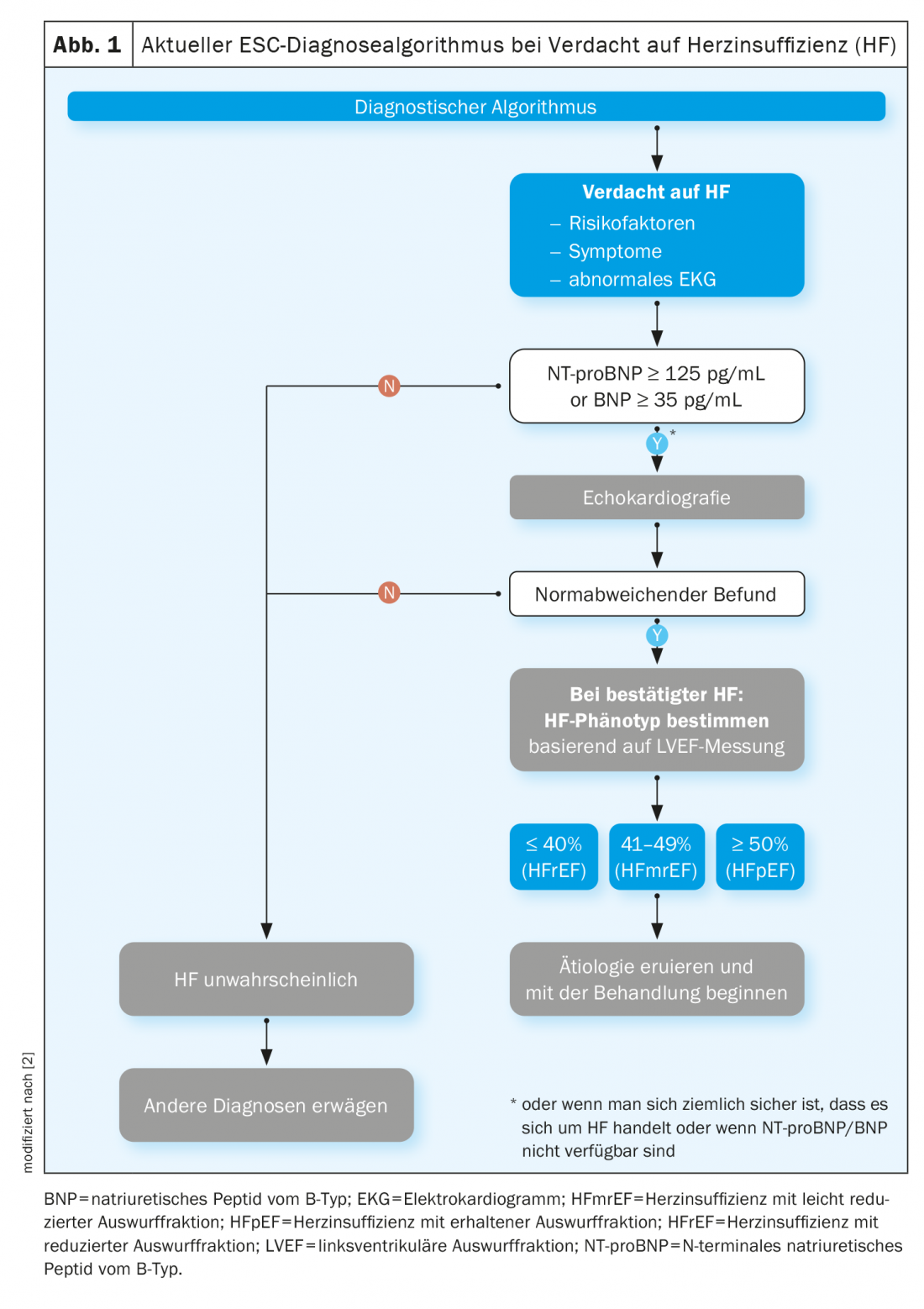
L’insufficienza cardiaca è una sindrome clinica causata da cambiamenti strutturali e funzionali del cuore ed è associata a una riduzione della frazione di eiezione o a un aumento delle pressioni di riempimento, sia a riposo che durante l’esercizio. La diagnosi di insufficienza cardiaca richiede la presenza di sintomi e di prove oggettive di disfunzione cardiaca (Fig. 1). I segni clinici tipici sono respiro corto, affaticamento e gonfiore alle caviglie. Dopo la diagnosi iniziale, i pazienti con insufficienza cardiaca vengono ricoverati in media una volta all’anno [9]. In relazione agli sviluppi demografici e all’aumento delle comorbidità, gli esperti ritengono che il numero di ricoveri ospedalieri potrebbe aumentare in modo significativo [7,8]. La fibrillazione atriale, l’elevato BMI e i livelli elevati di HbA1c o il basso tasso di filtrazione glomerulare (eGFR) sono forti predittori di ospedalizzazione [10]. “Il nostro obiettivo deve essere quello di identificare i pazienti in una fase precoce, per poter prevenire la progressione verso un’insufficienza cardiaca grave”, ha spiegato la Prof.ssa Sabine Genth-Zotz, MD, Chief Physician, Marienhaus Klinikum Mainz [1].
Qual è l’algoritmo diagnostico consigliato?
Per prima cosa, occorre fare un’attenta anamnesi medica. L’attuale linea guida ESC indica che la presenza di insufficienza cardiaca è più probabile nei pazienti con una storia di infarto miocardico, o in quelli con ipertensione arteriosa, malattia coronarica, diabete mellito, abuso di alcol o malattia renale cronica. È fondamentale chiedere informazioni sulla resistenza fisica e su eventuali episodi di affanno. Nell’esame clinico che segue l’anamnesi, occorre prestare particolare attenzione all’edema e all’auscultazione del cuore e dei polmoni (ritmo di galoppo? segni di congestione?), come sottolinea il Prof. Genth-Zotz. Il passo successivo nell’algoritmo diagnostico dell’ESC è un elettrocardiogramma (ECG). Un risultato ECG non rilevante rende improbabile la presenza di un’insufficienza cardiaca [5]. Anomalie normali come la fibrillazione atriale, le onde Q, l’ipertrofia ventricolare sinistra e un complesso QRS dilatato, invece, aumentano la probabilità della presenza di insufficienza cardiaca. In questo caso, sono indicate ulteriori indagini, come illustrato nella Figura 1 . Cosa deve essere registrato dalla diagnostica di laboratorio? La linea guida raccomanda elettroliti, urea sierica, creatinina e un emocromo completo. Ai fini della diagnosi differenziale, possono essere utili anche i test di funzionalità epatica e tiroidea. Secondo l’attuale linea guida ESC, i peptidi natriuretici svolgono un ruolo molto importante [2]. Se il valore di NT-proBNP è superiore a 125 pg/ml, è necessario effettuare un’ulteriore diagnosi; lo stesso vale per il BNP ≥35 pg/ml. Se i valori misurati sono inferiori, la probabilità di insufficienza cardiaca è bassa, aggiunge il Prof. Genth-Zotz. Se non è possibile misurare i peptidi natriuretici, il relatore raccomanda di procedere direttamente all’ecocardiografia [1].
Si tratta di HFrEF, HFmrEF o HFpEF?
Secondo l’ESC, se l’ecocardiografia rivela risultati patologici, l’insufficienza cardiaca (HF) può essere suddivisa in queste tre entità in base alla frazione di eiezione:
- HFrEF (“HF con frazione di eiezione ridotta”): LVEF ≤40 %
- HFmrEF (“HF con frazione di eiezione lievemente ridotta”): LVEF 41-49%
- HFpEF (“HF con frazione di eiezione preservata”): LVEF ≥50%
Le analisi del registro a lungo termine dell’ESC dei pazienti ambulatoriali con insufficienza cardiaca mostrano che il 60% è affetto da HFrEF, il 24% da HFmrEF e il 16% da HFpEF [6]. Tra i pazienti con HFmrEF si trovano spesso maschi più giovani. La malattia coronarica è presente in circa la metà dei casi, ma le comorbidità non cardiache sono rare. Il trattamento dei pazienti HFmrEF è strutturato in modo molto simile a quello dei pazienti HFrEF. L’HFpEF, invece, tende a essere una popolazione di pazienti speciale, per lo più anziani, spesso donne, e spesso con comorbidità non cardiovascolari (ad esempio, diabete, insufficienza renale).
Cambio di paradigma: quattro pilastri della terapia farmacologica
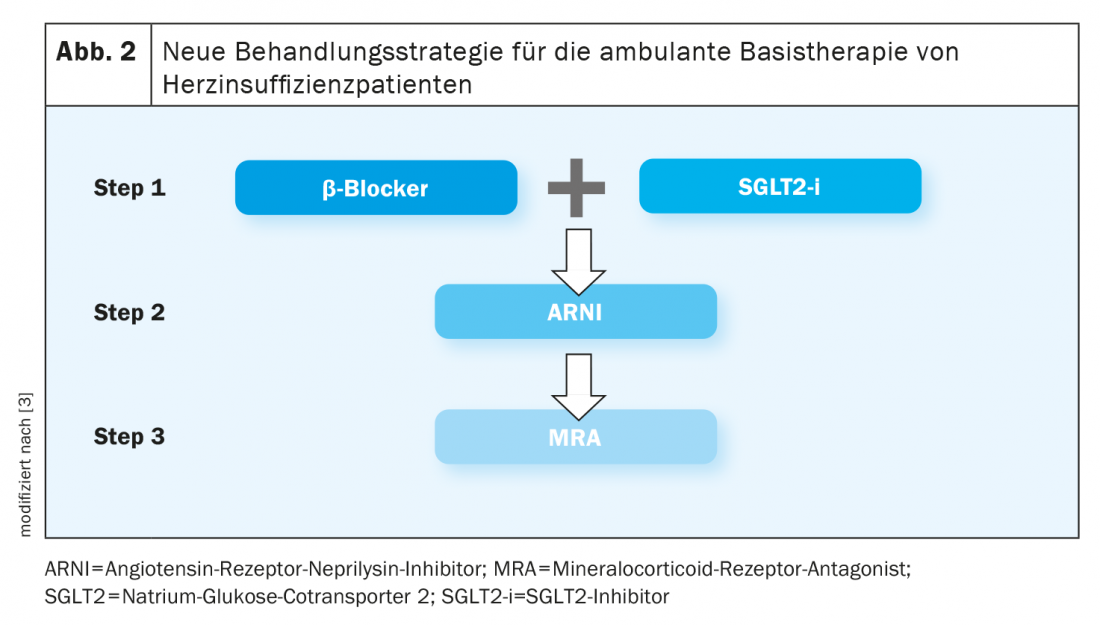
Il trattamento farmacologico suggerito dalla linea guida si basa sulla classificazione terminologica di HFrEF, HFmrEF o HFpEF [2]. Una nuova raccomandazione prevede che tutti i pazienti con insufficienza cardiaca ricevano inizialmente un ACE-inibitore (ACE-I), un inibitore della neprilisina del recettore dell’angiotensina (ARNI), un betabloccante, un antagonista del recettore mineralcorticoide (MRA) e un inibitore SGLT2 (SGLT2-i) (Fig. 2). Idealmente, tutti questi farmaci dovrebbero essere somministrati entro quattro settimane. Tuttavia, poiché il periodo di ricovero in ospedale è di solito di soli 4-5 giorni, i medici in genere danno una raccomandazione ai medici incaricati del trattamento ambulatoriale di follow-up su cosa dovrebbe essere titolato e a quale dose, spiega il relatore. Nei pazienti dopo uno scompenso cardiaco, bisogna essere particolarmente attenti alla titolazione e, in presenza di comorbilità, è molto importante un attento monitoraggio.
SGLT-2-i: adatto alla maggior parte dei pazienti – anche nell’HFpEF
Gli aspetti da considerare nei pazienti con ipotensione sono stati formulati da McMurray e Packer in un articolo pubblicato nel 2021 [3]. Di conseguenza, i pazienti con una pressione arteriosa<100 mmHg, possono essere avviati alla terapia con un bloccante del recettore dell’angiotensina. Inoltre, l’uso degli inibitori SGLT-2 è innocuo da questo punto di vista. “Abbiamo visto in diversi studi che la riduzione della pressione sanguigna con l’inizio di un inibitore SGLT-2 è solo molto marginale”, spiega il Prof. Genth-Zotz [1]. Che anche i pazienti con HFpEF traggano beneficio da questa opzione terapeutica è dimostrato dai risultati dello studio EMPEROR-Preserved, pubblicato poco dopo l’emanazione della linea guida ESC [4]. Questo dimostra che empagliflozin può ridurre efficacemente il rischio di ricovero ospedaliero legato all’insufficienza cardiaca nei pazienti con HFpEF. “Nell’insufficienza cardiaca, indipendentemente dalla frazione di eiezione, possiamo usare empagliflozin: molto semplicemente in una dose di 10 mg una volta al giorno”, riassume il relatore [1].
Ciò che va sempre tenuto presente, a prescindere da questo, sono i diuretici – questi giocano un ruolo nella maggior parte dei pazienti, soprattutto nello scompenso, ma: “Se il paziente è ricompensato, bisogna sempre assicurarsi di ridurre i diuretici, anche in ambito ambulatoriale”, sottolinea il Prof. Genth-Zotz [1]. Inoltre, non bisogna trascurare la questione se ci sono altri cambiamenti fisiopatologici che possono essere affrontati, come il blocco di branca del fascio sinistro. E se i pazienti hanno un’insufficienza della valvola mitrale di grado elevato o una stenosi della valvola aortica, anche questo dovrebbe essere trattato, e lo stesso vale per la rivascolarizzazione nella malattia coronarica grave, spiega il relatore.
Congresso: DGIM Internistenkongress
Letteratura:
- “Aggiornamento delle linee guida: cosa c’è di nuovo nell’insufficienza cardiaca”, Prof. Dr. med. Sabine Genth-Zotz, 128. Congresso della Società tedesca di medicina interna (DGIM), 30.04.2022
- McDonagh TA, et al.: Gruppo di documenti scientifici ESC: Linee guida ESC 2021 per la diagnosi e il trattamento dell’insufficienza cardiaca acuta e cronica: elaborate dalla Task Force per la diagnosi e il trattamento dell’insufficienza cardiaca acuta e cronica della Società Europea di Cardiologia (ESC). Con il contributo speciale della Heart Failure Association (HFA) dell’ESC. Eur J Heart Fail 2022; 24(1): 4-131.
- McMurray JJV, Packer M: Come dovremmo ordinare i trattamenti per l’insufficienza cardiaca e la frazione di eiezione ridotta: una ridefinizione della medicina basata sull’evidenza. Circolazione 2021; 143(9): 875-877.
- Anker SD, et al; Investigatori dello studio EMPEROR-Preserved. Empagliflozin nell’insufficienza cardiaca con frazione di eiezione conservata. N Engl J Med 2021; 385(16): 1451-1461.
- Mant J, et al: Revisione sistematica e meta-analisi dei dati dei singoli pazienti sulla diagnosi di insufficienza cardiaca, con modellazione delle implicazioni delle diverse strategie diagnostiche nell’assistenza primaria. Health Technol Assess 2009; 13:1-207, iii.
- Chioncel O, et al: Epidemiologia ed esiti a un anno nei pazienti con insufficienza cardiaca cronica e frazione di eiezione conservata, media e ridotta: un’analisi del registro a lungo termine dell’ESC Heart Failure. Eur J Heart Fail 2017; 19: 1574-1585.
- Savarese G, Lund LH: Il peso dell’insufficienza cardiaca sulla salute pubblica globale. Card Fail Rev 2017; 3: 7-11.
- Al-Mohammad A, et al: Gruppo di sviluppo delle linee guida sullo scompenso cardiaco cronico. Diagnosi e gestione degli adulti con insufficienza cardiaca cronica: sintesi della guida NICE aggiornata. BMJ 2010; 341: c4130.
- Barasa A, et al: Insufficienza cardiaca nei giovani adulti: tendenze ventennali nell’ospedalizzazione, nell’eziologia e nella mortalità in Svezia. Eur Heart J 2014; 35: 25-32.
- Mosterd A, Hoes AW: Epidemiologia clinica dell’insufficienza cardiaca. Cuore 2007; 93: 1137-1146.
PRATICA GP 2022; 17(7): 30-32