Le moderne opzioni terapeutiche immunomodulanti consentono una riduzione dei sintomi significativamente più forte e più rapida rispetto al passato. Per controllare il rischio di riattivazione di una precedente infezione da epatite, è necessario effettuare i test appropriati.
L’epatite B (HBV) è una delle malattie infettive più comuni. Se non viene trattata, sono possibili gravi complicazioni come l’insufficienza epatica. Di solito si tratta di una malattia virale acuta, ma esistono anche decorsi cronici. Una revisione pubblicata su JAAD nel 2019 raccomanda lo screening di tutti i pazienti affetti da psoriasi prima di iniziare la terapia sistemica, includendo i seguenti parametri: Anticorpi contro il nucleo dell’epatite B (anti-Hbc), antigene di superficie dell’epatite B (HbsAg) e anticorpi contro l’HCV (anti-HCV) [1].
La profilassi come fattore importante
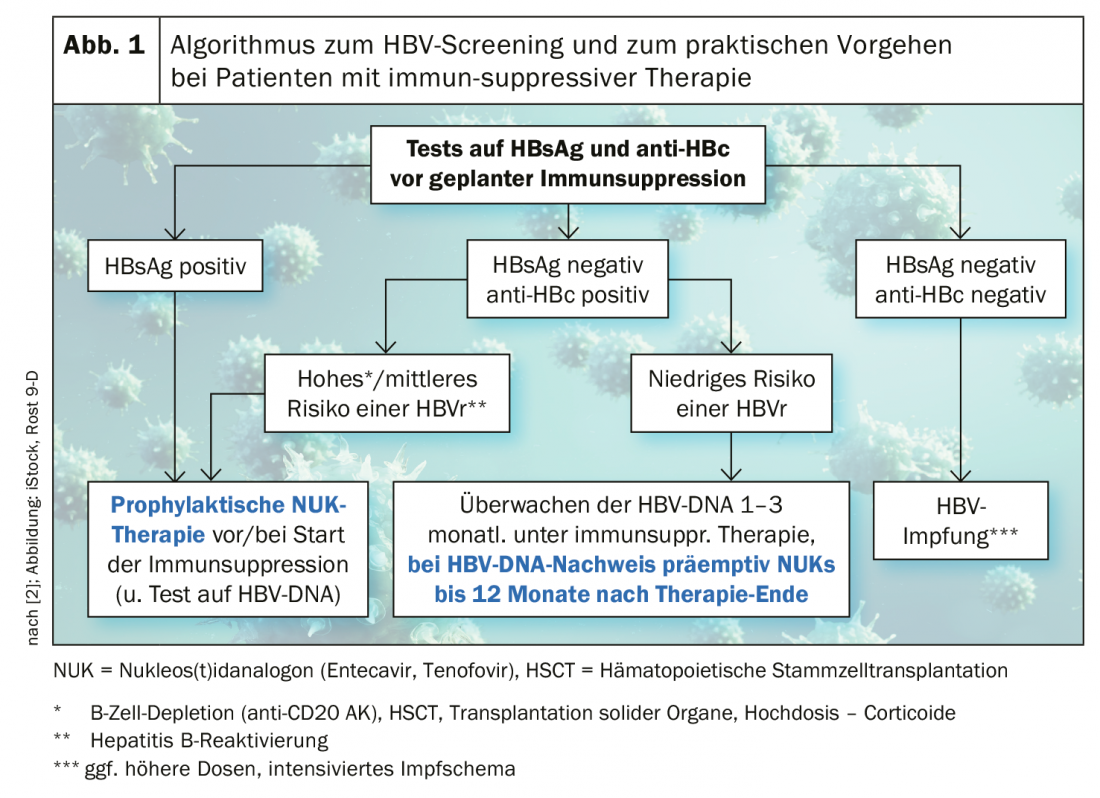
Per i soggetti HbsAg+ o ad alto/medio rischio di riattivazione dell’epatite B (HBVr), si suggerisce una terapia profilattica con un analogo del nucleos(t-id) (entecavir, tenofovir) prima/al momento di iniziare la terapia sistemica. Se il rischio è basso, il monitoraggio dell’HBV DNA è sufficiente. Se ci sono risultati negativi per HBsAg e anti-HBc, la vaccinazione è il miglior metodo preventivo [2,3]. I risultati sui profili di rischio specifici dei singoli principi attivi in relazione all’HBVr variano.
Per quanto riguarda il metotrexato (MTX), è noto che esiste un aumento del rischio di HBVr [1,4,5]. Non ci sono informazioni basate sull’evidenza su apremilast e dimetil fumarato. Per quanto riguarda gli inibitori del TNF-alfa, in uno studio è stato riscontrato che il 39% dei pazienti positivi ai marcatori dell’HBV presentava una ricomparsa dell’HBV DNA nel siero, dimostrando che il tasso di riattivazione era diverse volte più alto nei soggetti anti-HBc+ rispetto ai portatori di HBsAg+ [6]. I dati empirici sugli antagonisti dell’interleuchina sono piuttosto limitati finora. In uno studio prospettico di coorte su ustekinumab, è stato dimostrato che l’HBVr si manifesta relativamente raramente con questo inibitore dell’IL12/23 [7]. I dati si basano su un campione di 93 pazienti trattati con ustekinumab per 24 ± 12 mesi tra il 2011 e il 2016. Al basale, tutti i soggetti sono stati sottoposti a test sierologici e ogni anno è stato eseguito un test HBV DNA. Nei 54 soggetti di che erano portatori di HBV inattivo o guarito o che avevano un riscontro isolato di anti-HBC+, la riattivazione virologica si è verificata solo in 3 pazienti di .
| Messaggio da portare a casa Diverse linee guida internazionali raccomandano lo screening dell’epatite prima di iniziare la terapia sistemica della psoriasi [4]. A seconda dei risultati, si può prendere in considerazione la vaccinazione o la profilassi antivirale. Le terapie sistemiche che interferiscono con il sistema immunitario possono essere associate al rischio di riattivazione di precedenti infezioni da epatite. I dati empirici sui profili di rischio dei singoli principi attivi sono ancora limitati. Monitorando regolarmente i valori epatici, si può controllare questo fattore e, se necessario, avviare misure appropriate. |
Il monitoraggio dei valori epatici è essenziale
Secondo l’attuale linea guida S3 dell’AWMF, le terapie sistemiche per la psoriasi dovrebbero essere evitate durante l’epatite B acuta, fino a quando l’infezione non sarà tenuta sotto controllo dalla terapia antivirale [4].
Sebbene non esista un vaccino contro l’epatite C (HCV), il 90% delle persone trattate può essere curato con farmaci antivirali [8]. Il metotrexato è controindicato nell’HCV a causa del suo potenziale epatotossico e della tendenza a promuovere la replicazione virale [4]. Bonifati et al. raccomandano di monitorare i valori epatici e la carica virale dell’HCV ogni 3-6 mesi e, se necessario, di considerare la collaborazione interdisciplinare con l’epatologia [9].
Letteratura:
- Kaushik SB, Lebwohl MG: Psoriasi: quale terapia per quale paziente: J Am Acad Dermatol 2019; 80(1): 43-53.
- Zachoval R: Prevenzione della riattivazione dell’epatite B, Hepatitis &more 1/2017.
- Lockwood SJ, Prens LM, Kimball AB: Karger Compass Dermatol 2017; 5: 195-199. DOI: 10.1159/000481335, www.karger.com/Article/Pdf/481335
- AWMF 2017, www.awmf.org/uploads/tx_szleitlinien/013-001l_S3_Therapie_Psoriasis-vulgaris_2017-12.pdf
- Patterson AT: JAAD 2020; 82(2): 532.
- Perez-Alvarez R, et al: Medicine (Baltimore) 2011; 90: 359-371.
- Ting S-W, Chen Y-C, Huang Y-H. Clin Drug Investig 2018, doi:10.1007/s40261-018-0671-z.
- Ufficio federale della sanità pubblica Svizzera (UFSP): www.bag.admin.ch
- Bonifati C, Lora V, Graceffa D, Nosotti L: World J Gastroenterol 2016; 22: 6444-6455.
- EADV: Kirby B: Trattamento della psoriasi, presentazione di diapositive, Professor Brian Kirby, MD FRCPI, Congresso EADV, Madrid, 12.10.2019.
PRATICA DERMATOLOGICA 2020; 30(3): 26