Negli ultimi anni, la comprensione molecolare sempre migliore delle malattie maligne ha aperto strade per strategie di trattamento mirate. L’analisi del genoma del tumore sta diventando sempre più importante per consentire ai pazienti l’accesso ad agenti attivi efficaci individualmente. Il potenziale dell’oncologia di precisione è ancora lontano dall’essere esaurito. Ma ci sono anche delle sfide da superare.
I termini “terapia personalizzata” o “terapia di precisione” sono stati usati sempre più spesso di recente. Allo stesso tempo, all’inizio non è stato possibile stabilire definizioni chiare. Di norma, si parlava allora di farmaci con una struttura molecolare bersaglio nelle cellule tumorali. Tuttavia, con la crescente comprensione della base cellulare delle malattie ematologiche e l’avanzamento dell’analisi del genoma, l’oncologia di precisione presuppone oggi una terapia basata sulla caratterizzazione molecolare del singolo tumore. L’obiettivo è un trattamento più efficace e meglio tollerato [1].
Terapia individuale basata sul profilo del tumore
Nel percorso verso l’oncologia di precisione, sono necessarie l’interpretazione e la classificazione delle alterazioni genetiche tumorali riscontrate, la derivazione dei possibili effetti sulla biologia delle cellule tumorali e l’assegnazione di possibili bersagli terapeutici, che portano alla preparazione di un referto patologico molecolare [2]. La pianificazione della terapia basata esclusivamente sull’istologia era ieri. Nel frattempo, le entità vengono abbandonate sempre più spesso e l’attenzione si sposta sul profilo individuale del tumore. Questo sviluppo è stato reso possibile in parte dai miglioramenti del sequenziamento ad alto rendimento. Nel frattempo, le analisi delle mutazioni possono essere effettuate su un gran numero di geni con uno sforzo tecnicamente elevato, ma giustificabile dal punto di vista temporale e finanziario [1,2].
Tuttavia, le strategie terapeutiche basate sui risultati dell’analisi molecolare del tumore devono affrontare sfide particolari, poiché i singoli approcci terapeutici non possono mai essere basati sull’evidenza, né possono essere mappati in studi clinici completi. Pertanto, molte decisioni terapeutiche vengono prese sulla base di analogie, razionali biologici o piccole serie di casi. Tuttavia, la stessa alterazione genomica può avere valori diversi come bersaglio terapeutico nel contesto di malattie diverse – un’altra sfida per il medico. Pertanto, per implementare l’oncologia di precisione in modo significativo e di successo, sono necessari un’attenta selezione dei pazienti e l’accesso ai farmaci mirati.
Trattamento mirato delle malattie ematologiche
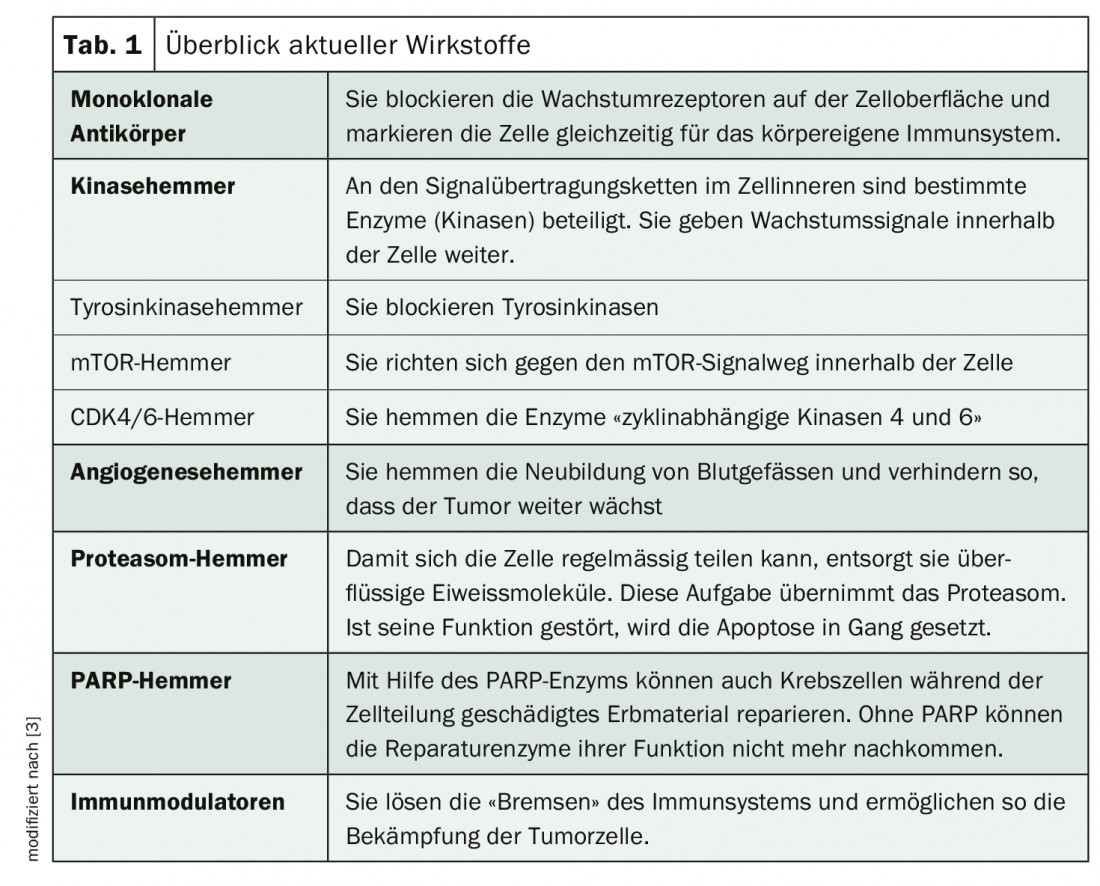
Le terapie biologiche molecolari sono dirette contro i ligandi, i recettori per queste sostanze messaggere sulla superficie cellulare o contro le vie di segnalazione nelle cellule stesse. Influenzano la crescita del tumore o dei vasi sanguigni sopprimendo i segnali di crescita, interrompendo l’alimentazione del tumore, bloccando lo smaltimento dei rifiuti della cellula o impedendo i meccanismi di riparazione della cellula tumorale [3]. Gli immunomodulatori assumono un ruolo speciale. Potenziano la risposta immunitaria antitumorale e migliorano la funzione immunitaria innata e adattativa (Tab. 1) [4–6]. Le opzioni terapeutiche possono essere utilizzate sia come monoterapia che in combinazione con la chemioterapia o la radioterapia.
Letteratura:
- Holch JW, Westphalen CB, et al: Dtsch Med Wochenschr 2017; 142(22): 1676-1684.
- www.klinikum-grosshadern.de/CCCLMU-Krebszentrum-Muenchen/download/inhalt/TZM-News-MTB.pdf (ultimo accesso 17.07.2020)
- www.krebsinformationsdienst.de/service/iblatt/iblatt-zielgerichtete-krebstherapien.pdf (ultimo accesso 17.07.2020)
- Quach H, et al: leukemia 2010; 24(1): 22-32.
- Davies FE, et al: Blood 2001; 98(1): 210-216.
- www.therapyselect.de/de/blog/zielgerichtete-krebstherapie-targeted-therapy-das-wichtigste (ultimo accesso 17.07.2020)
InFo ONCOLOGIA ED EMATOLOGIA 2020; 8(4): 19