Il carcinoma a cellule renali è uno dei tumori maligni più comuni negli adulti. In termini di opzioni di trattamento farmacologico, negli ultimi anni questa entità tumorale ha subito un cambiamento più rapido rispetto a quasi tutte le altre malattie maligne. Nel frattempo, l’attenzione non si concentra solo sulla terapia mirata per il carcinoma a cellule renali avanzato, ma anche sui trattamenti combinati.
Il cancro al rene è il terzo tumore urologico più comune. Ogni anno, quasi 1000 persone in Svizzera sviluppano un tumore renale maligno [1]. La maggior parte dei tumori appartiene istologicamente ai carcinomi renali a cellule chiare, che – a seconda del sottotipo – hanno una prognosi leggermente migliore rispetto al carcinoma renale non a cellule chiare [2]. Negli stadi avanzati, tuttavia, la prognosi è sfavorevole per la maggior parte delle persone colpite: tre quarti di loro hanno un rischio medio-alto che la malattia non si arresti [3]. Il panorama terapeutico del carcinoma a cellule renali metastatico è cambiato in modo significativo grazie alle numerose nuove approvazioni. Alle terapie mirate si sono aggiunti gli inibitori del checkpoint immunitario, che ora possono essere utilizzati anche in combinazione [4].
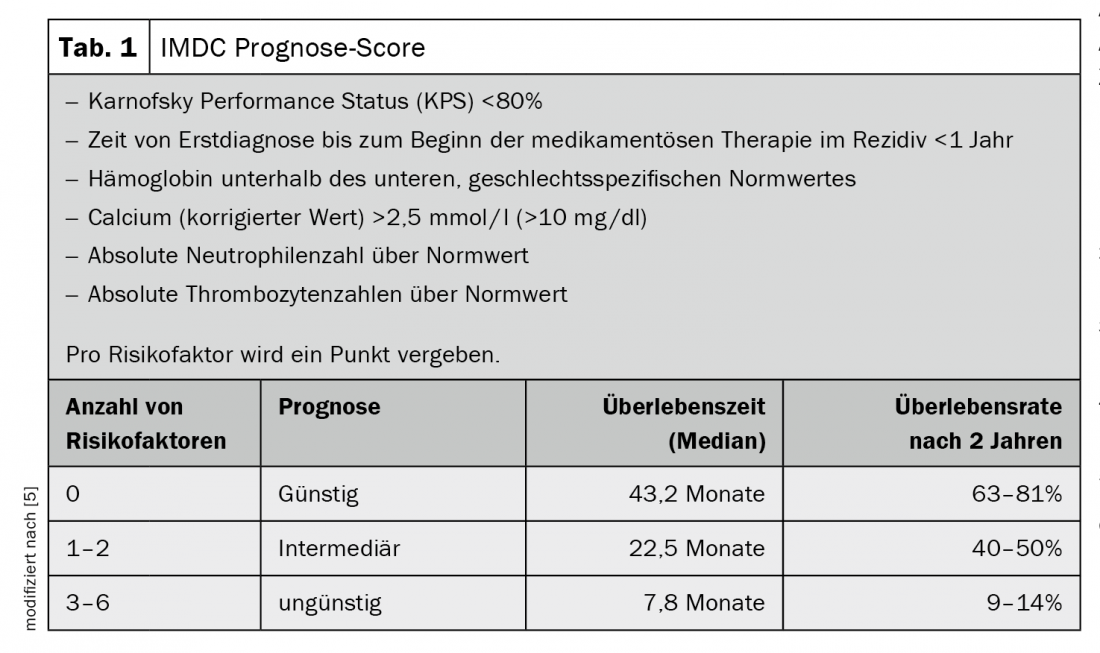
Negli ultimi anni si è affermata la terapia mirata con inibitori della tirosin-chinasi, inibitori di mTOR o anticorpi. In particolare, l’inibizione del VEGFR (recettore del fattore di crescita endoteliale vascolare) è l’opzione standard per i pazienti con prognosi favorevole, i cui tumori non possono essere operati o che hanno sviluppato metastasi [5]. (Tab. 1). Il primo inibitore del checkpoint, che ha come bersaglio la proteina di superficie PD-1, è stato approvato come terapia di seconda linea dopo il fallimento di una terapia precedente. Di recente, il doppio blocco del checkpoint immunitario è diventato possibile anche in un uso più precoce. È stata approvata la terapia combinata dell’inibitore del checkpoint nivolumab con l’anticorpo ipilimumab diretto contro il CTLA-4. Rispetto alla terapia mirata, il doppio blocco del checkpoint mostra vantaggi nei pazienti con rischio basale intermedio o sfavorevole. Dopo 18 mesi, il 75% delle persone colpite era ancora vivo e la sopravvivenza globale mediana non è stata raggiunta durante il periodo di osservazione dello studio. Nel 9% delle persone trattate con immunoterapia, la malattia ha risposto completamente al trattamento, il che significa che il tumore inizialmente non era più rilevabile dopo la terapia [3]. Tuttavia, la possibilità di ottenere una risposta ottimale e una remissione duratura con i nuovi farmaci è accompagnata da un alto tasso di effetti collaterali. Il loro trattamento richiede un team interdisciplinare ben coordinato [4].
Il futuro: le terapie combinate
Un nuovo modo di trattamento immuno-oncologico del tumore renale consiste nel combinare le sostanze mirate di provata efficacia con gli inibitori del checkpoint, ancora relativamente nuovi. In America, è già stata approvata la nuova modalità d’azione costituita, ad esempio, dall’inibitore della tirosin-chinasi axitinib con pembrolizumab (anticorpo anti-PD-1) o axitinib con l’anticorpo anti-PD-L1 avelumab. In Europa, l’approvazione è molto attesa.
Letteratura:
- www.krebsliga.ch/ueber-krebs/zahlen-fakten/-dl-/fileadmin/downloads/sheets/zahlen-krebs-in-der-schweiz.pdf (ultimo accesso 15.30.2020)
- www.krebsinformationsdienst.de/fachkreise/nachrichten/2019/fk17-nierenkrebs-immuntherapie-kombination.php (ultimo accesso 15.30.2020)
- Motzer RJ, Nizar M, Tannier MD, et al: Nivolumab più ipilimumab rispetto a sunitinib nel carcinoma a cellule renali avanzato. N Engl J Med 2018; 378: 1277-1290.
- Zschäbitz S, Ivanyi P, Delecluse S: Rivoluzione nella terapia sistemica del carcinoma a cellule renali metastatico. Il Nefrologo 2020; 15: 12-19.
- Ivanyi P, Grünwald V: Terapia sistemica del carcinoma a cellule renali. Oncologo 2019; 25: 517-522.
- Heng DYC, Xie W, Regan MM, et al: Convalida esterna e confronto con altri modelli del modello prognostico dell’International Metastatic Renal-Cell Carcinoma Database Consortium: uno studio basato sulla popolazione. Lancet Oncol 2013; 14: 141-148.
InFo ONCOLOGIA ED EMATOLOGIA 2020; 8(2): 23