La Società Europea per la Nutrizione Clinica e il Metabolismo (ESPEN) definisce la ME come uno stato nutrizionale in cui le carenze energetiche, proteiche e di micronutrienti portano a un’alterazione della composizione corporea (massa muscolare ridotta) e a una riduzione della funzione fisica e mentale. Nei Paesi industrializzati, un paziente su tre è a rischio di ME o presenta una ME manifesta al momento del ricovero in ospedale. La ME viene descritta come “una delle cause nascoste più importanti dell’aumento dei costi dell’assistenza sanitaria”.
Ippocrate di Kos, il padre della medicina moderna, attribuiva grande importanza all’alimentazione già nel IV secolo a.C.: “[…] che il tuo cibo sia la tua medicina e la tua medicina il tuo cibo”. Oggi, gli effetti clinici negativi della malnutrizione associata alla malattia (ME) sono ben studiati: degenza ospedaliera più lunga, qualità di vita inferiore, tassi di morbilità e mortalità più elevati. La ME viene descritta come “una delle più importanti ragioni nascoste dell’aumento dei costi nel sistema sanitario” [Neue Zürcher Zeitung, 11.06.2002].
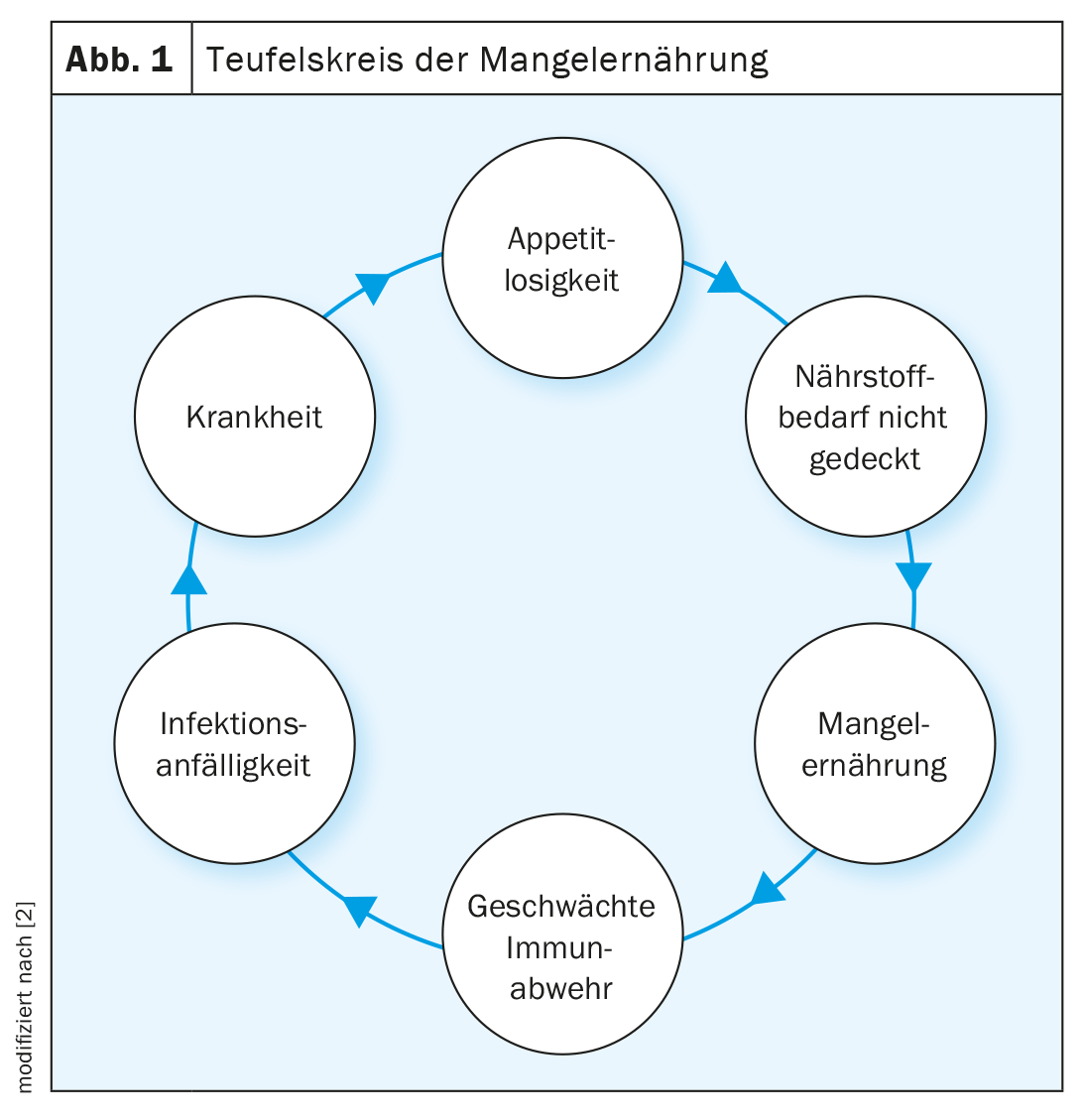
La Società Europea di Nutrizione Clinica e Metabolismo (ESPEN) definisce la ME come uno stato nutrizionale in cui le carenze energetiche, proteiche e di micronutrienti portano ad un’alterazione della composizione corporea (massa muscolare ridotta) e ad una riduzione della funzione fisica e mentale [1]. Nei Paesi industrializzati, un paziente su tre è a rischio di ME o presenta una ME manifesta al momento del ricovero in ospedale. Questi pazienti di solito continuano a perdere peso nel corso del ricovero, il che peggiora il loro stato nutrizionale. I molteplici fattori che influenzano questa perdita di peso progressiva e indesiderata includono la perdita di appetito, lo stato infiammatorio, il catabolismo proteico, la disfunzione ormonale, il disturbo gastrointestinale, l’inattività fisica e la stanchezza psicologica (Fig. 1). In media, il 2% della popolazione anziana è malnutrito e il 24% è a rischio di ME. Nelle persone fragili, la prevalenza era significativamente più alta, rispettivamente del 9% e del 45% [3]. La perdita di appetito è una risposta fisiologica alla malattia acuta, ma può portare a deficit energetici e proteici potenzialmente drastici. La ME e la malattia si influenzano a vicenda, per cui da un lato la malattia può provocare la ME e dall’altro la ME può influenzare negativamente il decorso della malattia. In combinazione con una risposta allo stress endocrino e infiammatorio, le carenze energetiche, proteiche e di micronutrienti possono portare alla perdita di massa muscolare e di forza e alla riduzione della funzionalità corporea, soprattutto nei malati cronici. Nelle malattie acute, invece, la perdita di appetito può agire come meccanismo protettivo e aumentare l’autofagia (il meccanismo dell’organismo per eliminare gli organelli cellulari danneggiati e i prodotti tossici), che può favorire il recupero. Quindi, la soppressione dell’autofagia da parte della terapia nutrizionale nella malattia acuta produce effetti potenzialmente negativi. Tuttavia, nei pazienti cronicamente malati, questo meccanismo protettivo fisiologico può portare alla ME associata alla malattia. Nei pazienti con malattie croniche multiple di lieve gravità e deterioramento dello stato nutrizionale, una terapia nutrizionale adeguata ha un effetto positivo sull’esito clinico. Questi pazienti possono avere un metabolismo e un utilizzo dei nutrienti più efficiente, grazie alla bassa resistenza all’insulina, rispetto ai pazienti malati acutamente [4]. Per migliorare i risultati clinici e aumentare il benessere, è necessario implementare una terapia nutrizionale personalizzata e individuale. Gli aspetti importanti sono la tempistica della terapia nutrizionale, il modo in cui viene somministrata, nonché la quantità e la scelta dei nutrienti.
Situazione attuale delle prove
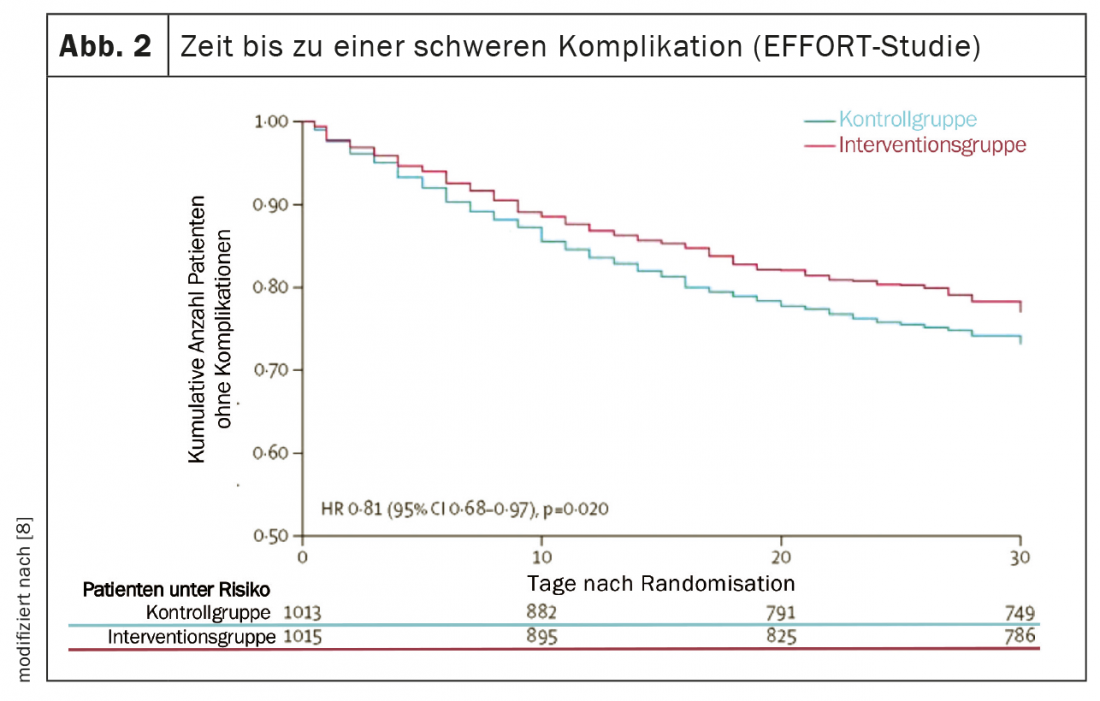
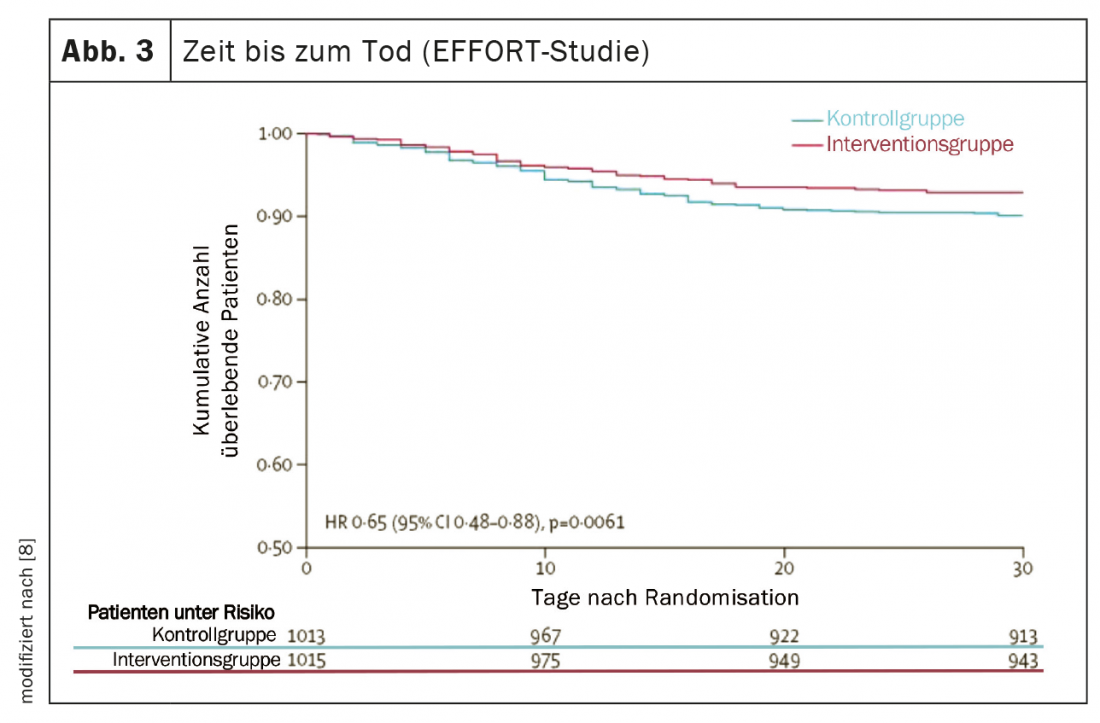
Negli ultimi cinque anni, diversi studi di alta qualità hanno fornito nuove conoscenze importanti che hanno fatto progredire in modo significativo la medicina nutrizionale e hanno tradotto i risultati della ricerca nutrizionale nella pratica [5]. Lo studio PREDIMED (Prevención con Dieta Mediterránea) ha fornito una solida evidenza che una dieta mediterranea integrata con olio extravergine di oliva o noci miste ha ridotto il rischio di malattie cardiovascolari e metaboliche di circa il 30% in cinque anni [6]. Due studi randomizzati controllati multicentrici hanno dimostrato l’elevata efficacia di un’adeguata terapia nutrizionale nei pazienti malnutriti sia in ospedale che dopo la dimissione [7,8]. In primo luogo, lo studio NOURISH (Nutrition effect On Unplanned Readmissions and Survival in Hospitalized patients), controllato con placebo, condotto su 652 anziani malnutriti, ha dimostrato che l’integrazione orale ad alto contenuto proteico può ridurre significativamente la mortalità a 90 giorni, con un Number Needed to Treat (NNT) di 20 [7]. D’altra parte, lo studio EFFORT (Effect of early nutritional support on Frailty, Functional Outcomes and Recovery of malnourished medical patients Trial), condotto su 2028 pazienti ricoverati affetti da malnutrizione in otto ospedali svizzeri, ha dimostrato l’efficacia di una terapia nutrizionale personalizzata e controllata da un algoritmo. Rispetto alla nutrizione ospedaliera standard, la terapia nutrizionale mirata a raggiungere gli obiettivi proteici ed energetici ha ridotto significativamente il tasso di complicanze gravi (NNT=25) e il tasso di mortalità (NNT=37) (Figg. 2 e 3). Inoltre, le menomazioni funzionali si sono verificate con una frequenza significativamente inferiore e la qualità della vita è migliorata in modo significativo [8]. Una recente meta-analisi, che ha incluso questi due studi, ha concluso che una terapia nutrizionale adeguata nei pazienti malnutriti riduce il rischio di mortalità e di riospedalizzazioni elettive di circa il 25% [5].
Gestione della nutrizione
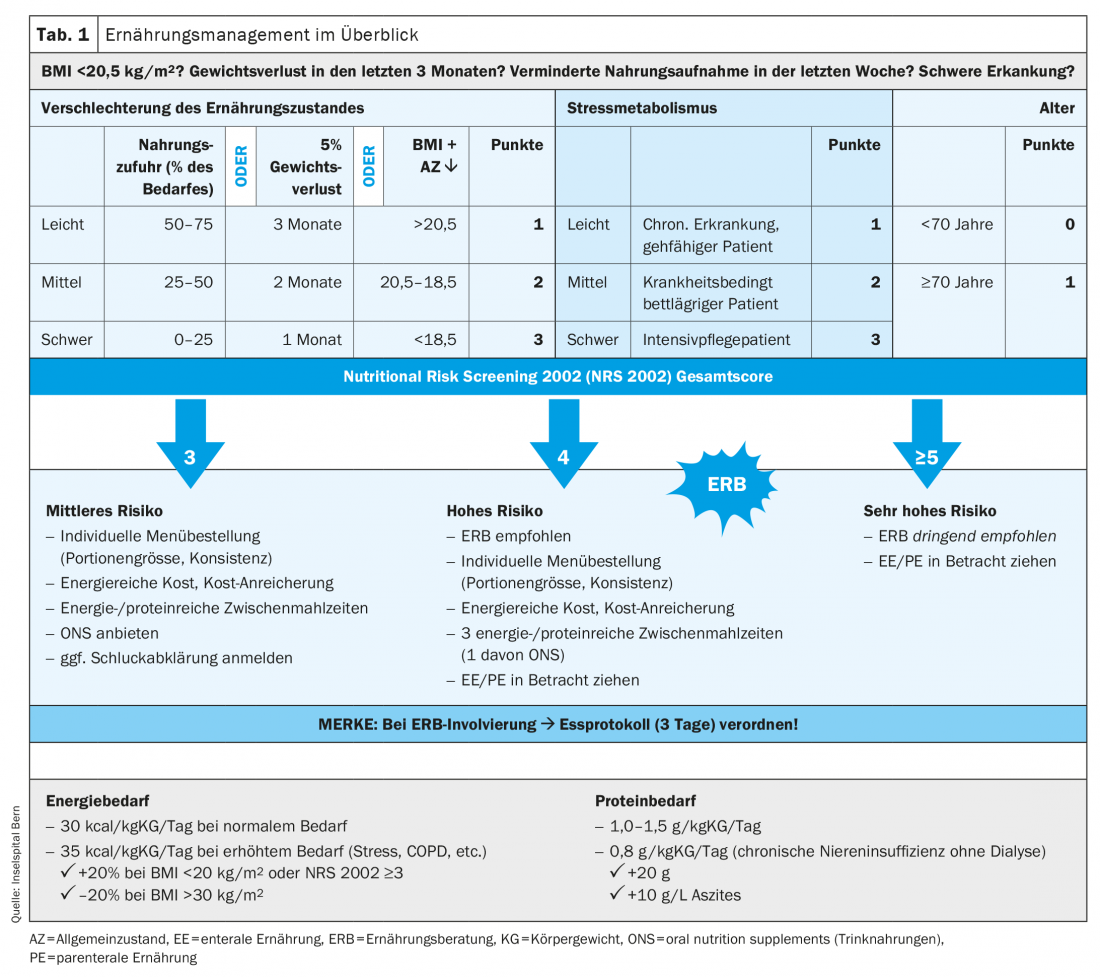
L’obiettivo della terapia nutrizionale è mantenere o migliorare lo stato nutrizionale e la qualità della vita attraverso la somministrazione adeguata di nutrienti. Per evitare un deterioramento dello stato nutrizionale, è necessaria una gestione nutrizionale rapida e funzionante (Tab. 1). Alla luce della crescente necessità di terapia nutrizionale in ambito ambulatoriale – un numero maggiore di pazienti anziani, polimorfi e bisognosi di cure – ha senso sviluppare un ambito di cura specializzato per la terapia nutrizionale in stretta collaborazione con un infermiere esperto. L’impiego di professionisti della salute in ruoli di pratica avanzata, soprattutto nella gestione della nutrizione, è a nostro avviso promettente. Hanno competenze cliniche approfondite e agiscono in base alle prove scientifiche attuali. In questo modo, possono consigliare, trattare o accompagnare in modo indipendente i pazienti con quadri clinici complessi. Questo porta a uno sviluppo efficiente e sostenibile della terapia nutrizionale.
Screening e valutazione in ambito ambulatoriale: sono necessarie procedure standardizzate per avviare una terapia nutrizionale tempestiva e adeguata. Dovrebbe essere condotto uno screening sistematico del rischio di ME, seguito da una valutazione nutrizionale completa, che porti allo sviluppo di un piano nutrizionale personalizzato. Lo screening per determinare il rischio di ME è il primo passo per identificare o, nel migliore dei casi, prevenire il deterioramento dello stato nutrizionale in una fase precoce. Lo screening deve identificare in modo rapido e sensibile le persone che hanno bisogno di una valutazione nutrizionale.
Lo screening deve essere effettuato con strumenti convalidati. ESPEN raccomanda lo Screening del rischio nutrizionale 2002 (NRS 2002), Scheda. 2). Può essere eseguito in pochi minuti e attualmente è il miglior strumento di screening validato [9,10]. È stato sviluppato nel 2002 dal gruppo di Jens Kondrup ed è uno dei più utilizzati negli ospedali di tutto il mondo. Consiste in un pre-screening con 4 domande. Se si risponde positivamente a una domanda, è necessario effettuare lo screening NRS 2002. Prende in considerazione la valutazione dello stato nutrizionale (0-3 punti), la gravità della malattia (0-3 punti) e l’età (1 punto se ≥70anni). I punti vengono sommati a un punteggio totale, dove ≥3punti indicano un rischio di ME o ME manifesta ed è indicata una valutazione nutrizionale.

La valutazione nutrizionale è una procedura completa per la valutazione oggettiva dello stato nutrizionale. Include l’anamnesi, gli esami fisici, le misure antropometriche (peso, altezza, BMI), i test funzionali, la qualità della vita, l’attività fisica e i valori di laboratorio. In pratica, si può effettuare una valutazione semplificata basata su peso, altezza, BMI e parametri soggettivi che si correlano allo stato nutrizionale secondo la letteratura, come l’appetito, il benessere generale e il rendimento. Il modo più semplice per registrare i parametri soggettivi è con una scala analogica visiva, simile alla registrazione del dolore (scala 1-10).
Piano nutrizionale: In linea con lo sviluppo della medicina personalizzata, il piano nutrizionale viene sempre adattato alle esigenze individuali. Queste esigenze dipendono in gran parte dallo stato nutrizionale valutato nella valutazione, con la malattia di base, la storia del peso, l’appetito e l’attuale assunzione di cibo che sono determinanti. Anche problemi come disturbi della masticazione, odinofagia, disfagia, xerostomia, disgeusia, mucosite/soor, nausea/emesi, costipazione/diarrea o dolore giocano un ruolo importante nel piano nutrizionale. Devono essere presi in considerazione altri aspetti come le abitudini alimentari, le preferenze/avversioni, la situazione psicosociale e l’attività fisica. La conduzione di un diario alimentare per 3-5 giorni è molto utile per registrare in modo semi-quantitativo la quantità di cibo consumato e per conoscere in dettaglio le abitudini alimentari (per i pazienti ricoverati, si può utilizzare anche il modello della tabella dei piatti). Prima della terapia nutrizionale, la terapia farmacologica deve essere ottimizzata, ad esempio antiemesi fissa, misure lassative, risciacquo della bocca, sostituto della saliva, bloccante acido, ecc.
Fabbisogno di energia, proteine e liquidi: la determinazione del fabbisogno energetico è un punto centrale della valutazione nutrizionale. Il consumo totale di energia è composto dal consumo di energia a riposo, dalla termogenesi indotta dal cibo e dall’energia consumata durante l’attività fisica. Il fabbisogno energetico totale può essere calcolato utilizzando una formula specifica per età, sesso e peso, che tenga conto anche dei fattori di attività e di stress (ad esempio, la formula di Harris-Benedict [11]). Nella vita pratica di tutti i giorni, può essere stimato approssimativamente utilizzando una formula semplificata basata sul peso, come segue: 30-35 kcal/kg/giorno; più 20% per un NRS 2002 ≥3o un IMC <20 kg/m2; meno 20% per un IMC >30 kg/m2 [12]. Una dieta completa ed equilibrata per i pazienti malnutriti dovrebbe coprire il 40-60% del fabbisogno energetico con carboidrati, il 10-20% con proteine e il 30-40% con grassi.
Il fabbisogno proteico per gli individui sani è generalmente di 0,8 g/kg/giorno. Nell’insufficienza renale cronica, l’apporto di proteine deve essere ridotto a 0,6 g/kg/giorno, a meno che non venga effettuata la dialisi. Nei pazienti anziani (>65 anni) con insufficienza renale cronica, l’apporto proteico è di 0,8 g/kg/giorno. In caso di dialisi, il fabbisogno proteico è lo stesso del caso normale e c’è un fabbisogno aggiuntivo di circa 20 g di proteine dopo la dialisi (perdita dialitica). I pazienti perdono circa 10 g di proteine per litro di ascite durante la paracentesi [4]. Per i pazienti malnutriti con malattie acute o croniche, le raccomandazioni per l’assunzione di proteine sono di 1,0-1,5 g/kg/giorno [13]. Non ci sono raccomandazioni specifiche per i pazienti polimorfi con insufficienza renale cronica. La nostra esperienza clinica dimostra che questa popolazione richiede circa 1 g/kg/giorno [8]. È necessario definire un obiettivo individuale per ogni paziente, poiché altri fattori come l’ipermetabolismo possono alterare il fabbisogno proteico (ad esempio, fattori di stress aggiuntivi come la BPCO o la malattia tumorale sottostante).
In generale, occorre garantire un’assunzione di liquidi sufficiente e adeguata. La regolazione del fluido deve (i) compensare la perdita impercettibile (500-1000 ml), (ii) fornire acqua ed elettroliti sufficienti, (iii) mantenere lo stato normale dei compartimenti dei fluidi corporei; e (iv) Fornire acqua sufficiente per consentire ai reni di espellere i prodotti di scarto (500-1500 ml). Il fabbisogno medio è di 30-35 ml di acqua/kg/giorno, 1 mmol di sodio/kg/giorno e 1 mmol di potassio/kg/giorno. La linea guida per l’assunzione totale di acqua è di >2 litri al giorno (circa 1,1 ml di acqua per kcal), di cui circa 1,4 litri dovrebbero essere consumati sotto forma di bevande. In caso di indicazioni particolari, è possibile bere quantità che si discostano da questo valore guida e sono determinate dal medico [14]. Le cause della carenza di liquidi o della disidratazione sono molteplici e di solito si basano su un’assunzione di liquidi troppo scarsa combinata con una perdita di liquidi eccessiva. Tra le eziologie più comuni vi sono le malattie con diarrea, vomito o febbre (per ogni grado superiore a 37 °C, l’organismo ha bisogno di circa 300 ml di liquidi in più al giorno), l’assunzione di diuretici o lassativi, la disfagia, la riduzione della sensazione di sete, le temperature esterne molto calde e il lavoro o lo sport fisicamente faticoso (fabbisogno supplementare di 0,5-1,0 litri di acqua per ogni ora di attività intensa). Qualsiasi prescrizione di liquidi deve coprire non solo il fabbisogno giornaliero di mantenimento, ma anche le perdite anomale. In caso di perdite dal tratto gastrointestinale, ad esempio a causa di una fistola o di un’aspirazione nasogastrica, la prescrizione di liquidi deve includere il fabbisogno giornaliero di mantenimento più una sostituzione equivalente di acqua ed elettroliti.
Fabbisogno di micronutrienti: nei pazienti polimorfi malnutriti, il fabbisogno di micronutrienti può aumentare a causa della ridotta assunzione di cibo o a causa della malattia. I micronutrienti devono essere integrati e/o sostituiti in base alla dose giornaliera raccomandata. Il fabbisogno giornaliero di micronutrienti è considerato soddisfatto se l’alimentazione tramite sondino enterale è di almeno 1500 ml al giorno. Le soluzioni nutritive parenterali non contengono vitamine e oligoelementi e devono essere integrate ulteriormente [4].
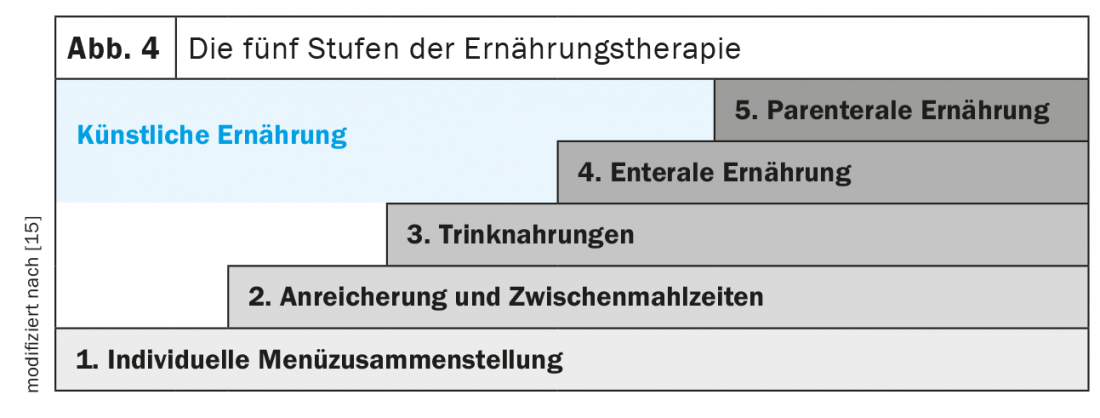
Le cinque fasi della terapia nutrizionale (Fig. 4) : Il primo passo è informare i pazienti sull’alimentazione ricca di energia e proteine, nonché sui ritmi dei pasti (pasti frequenti durante la giornata), affrontare eventuali problemi esistenti che impediscono un’adeguata assunzione di cibo e valutare le misure di ottimizzazione. La nutrizione orale con alimenti naturali energetici e ricchi di proteine dovrebbe essere la prima scelta della terapia nutrizionale. Comprende l’adattamento della consistenza del cibo (temperatura, sapore, consistenza, colore), le preferenze individuali, la scelta di alimenti poco odorosi, l’adattamento delle porzioni, nonché la preparazione blanda dei pasti e l’uso di ausili (cucchiaio, tazza, tettarella, ecc.). Inoltre, i pasti possono essere arricchiti con alimenti naturali come olio vegetale di alta qualità, burro, panna, formaggio cagliato, formaggio grattugiato, uova o con prodotti speciali come proteine o carboidrati in polvere (maltodestrina). Gli spuntini supplementari ad alta densità energetica (ad esempio, frullati fatti in casa, tartine, creme) possono essere inclusi nel programma giornaliero.
La fase successiva è la somministrazione di alimenti commerciali completamente bilanciati, che possono essere serviti in modo accattivante e creativo. Già nel 1990, lo studio di Delmi et al. ha dimostrato che la somministrazione serale di un alimento da bere completamente bilanciato (20 g di proteine, 254 kcal) ha aumentato l’assunzione di energia del 23% e l’assunzione di proteine del 62% nei pazienti geriatrici con frattura del collo del femore. Questo intervento ha ridotto in modo significativo i tassi di complicanze, la durata della degenza in ospedale e nelle unità di riabilitazione e la mortalità [16]. Ulteriori studi hanno dimostrato che la somministrazione complementare di mangimi sip come spuntino non riduce l’appetito, ma provoca un aumento significativo dell’assunzione totale di energia e proteine. Diversi studi e meta-analisi hanno dimostrato che l’alimentazione sip può preservare la massa muscolare e migliorare la qualità della vita, oltre a ridurre significativamente i tassi di complicanze, mortalità e riospedalizzazione [7,8,17–21]. Nel complesso, diversi studi, che si basano principalmente su analisi retrospettive dei costi, indicano che l’uso di alimentazione sip in ambito ambulatoriale comporta un beneficio economico complessivo. Questo è spesso associato a risultati clinicamente rilevanti, che indicano un rapporto costo-efficacia [22].
Se la nutrizione orale è insufficiente (<75% del fabbisogno energetico e proteico) o non è possibile, si deve prendere in considerazione la nutrizione enterale e, se necessario, quella parenterale. La nutrizione enterale è preferibile nei pazienti con un tratto gastrointestinale parzialmente funzionante, per il minor rischio di complicanze infettive e non infettive. Entrambe le diete artificiali e invasive devono essere complementari e non competitive. Se non ci sono esigenze particolari, si consiglia di iniziare con un’alimentazione in provetta o una soluzione nutritiva standard. Se necessario, esiste un’ampia gamma di prodotti più specifici per entrambe le diete.
L’apporto energetico e proteico dovrebbe essere valutato circa 2-3 volte alla settimana per i pazienti malati acuti, a seconda delle risorse di personale disponibili, e ogni due-quattro settimane per i pazienti malati cronici nello studio medico di base, come parte di una rivalutazione. A seconda del decorso, si dovranno definire ulteriori obiettivi e interventi nutrizionali e, se necessario, adottare ulteriori misure terapeutiche. Il contatto regolare medico-paziente e i contatti con il consulente nutrizionale o gli infermieri esperti offrono una buona opportunità per rivedere le raccomandazioni terapeutiche e migliorarne l’attuazione.
Alimentazione per stati patologici specifici: nei pazienti con insufficienza renale, spesso è necessario limitare l’assunzione di potassio e fosfato. I pazienti con insufficienza cardiaca possono trarre beneficio dalla restrizione di sodio e acqua o dall’integrazione regolare di tiamina e ferro in alcuni casi. Esiste una debole evidenza per l’uso di specifici integratori nutrizionali orali o soluzioni nutrizionali enterali nei pazienti polimorfi. Arginina, glutammina e beta-idrossi-beta-metilbutirrato (HMB) possono essere utilizzati nei pazienti con ulcere da pressione. Una miscela di fibre solubili e insolubili può essere utilizzata nei pazienti malati cronici che vengono alimentati con la nutrizione enterale e soffrono di diarrea o costipazione, le complicazioni più comuni della nutrizione enterale. Occorre prestare particolare attenzione allo stato di idratazione, poiché la disidratazione può portare alla stitichezza [4].
Tempistica della terapia nutrizionale: si raccomanda l’inizio precoce della terapia nutrizionale (in ospedale entro 48 ore dal ricovero) per prevenire il deterioramento dello stato nutrizionale e funzionale e la sarcopenia. Sebbene la durata ottimale della terapia nutrizionale non sia ancora chiara, le prove attuali raccomandano il trattamento oltre la dimissione dall’ospedale [13].
Monitoraggio della terapia nutrizionale: i team di nutrizione clinica esperti (in ambito ospedaliero) e i consulenti nutrizionali o gli infermieri esperti (in ambito ambulatoriale) devono rivedere l’indicazione, la via di somministrazione, i rischi, i benefici e gli obiettivi della terapia nutrizionale a intervalli regolari. La durata di questo intervallo dipende dal paziente e dai parametri da monitorare (ad esempio, parametri nutrizionali, antropometrici, biochimici, condizioni cliniche) e può essere prolungata se le condizioni del paziente migliorano con la terapia nutrizionale. Per esempio, si raccomanda di monitorare l’assunzione di nutrienti attraverso la nutrizione orale, enterale o parenterale in regime di ricovero o quando si inizia una terapia artificiale, inizialmente ogni giorno e due volte alla settimana quando la condizione è stabile (per esempio, quando c’è un alto rischio di sviluppare una sindrome da refeeding). Allo stesso modo, i parametri di laboratorio (ad esempio, potassio, magnesio, fosfato, sodio, urea, creatinina) devono essere monitorati quotidianamente all’inizio, e successivamente 1-2 volte alla settimana. Oltre ai parametri utilizzati per monitorare la risposta alla terapia nutrizionale, gli indici funzionali (ad esempio, la forza di chiusura del pugno) devono essere raccolti regolarmente per valutare altri esiti clinici (ad esempio, la sopravvivenza, la qualità della vita) [4]. Gli intervalli tra le visite di follow-up nel settore ambulatoriale sono significativamente più lunghi rispetto al settore ospedaliero.
Sensibilizzazione sulla prevenzione, l’identificazione e il trattamento della malnutrizione.
La ME dovrebbe essere affrontata più spesso nell’educazione e nella formazione del personale medico, sia negli ospedali che nel settore ambulatoriale. La consapevolezza della ME deve essere aumentata e la gestione della nutrizione deve essere vista come parte del trattamento medico multimodale. La ME è ancora troppo spesso non identificata, sotto-diagnosticata e di conseguenza non trattata.
Sono necessari protocolli e responsabilità chiaramente definiti per affrontare questo problema sia in ambito ospedaliero (al momento del ricovero) sia in ambito ambulatoriale (durante le consultazioni iniziali/di follow-up). Questo inizia con l’introduzione di uno screening nutrizionale sistematico, seguito da una valutazione nutrizionale rapida e semplice per i pazienti a rischio. Uno studio recente ha dimostrato che circa l’80% degli ospedali e delle case di cura in Svizzera non ha implementato un processo di screening sistematico per il rischio di ME e che solo il 25% degli ospedali sottopone i pazienti a screening se sospettano un problema. Inoltre, il 56% delle strutture controlla l’assunzione di cibo e il 50% monitora e documenta lo stato nutrizionale dei pazienti [23].
Poiché l’eziologia della ME è spesso multifattoriale (dalla depressione alla perdita di appetito, fino all’incapacità di alimentarsi), occorre garantire una comunicazione e una collaborazione ottimali tra l’équipe di trattamento ospedaliero, l’équipe/rete di trattamento ambulatoriale (medico di famiglia, Spitex, assistenza domiciliare, consulenza nutrizionale, ecc. Questo permette di affrontare i potenziali problemi in modo efficiente ed efficace.
La ME è un problema comune anche in ambito ambulatoriale. Il ruolo dei medici di base e degli infermieri esperti, degli specialisti in ambito privato, dei nutrizionisti e degli infermieri è fondamentale per individuare precocemente i segni della ME (pre-screening/screening NRS 2002) e per trattarli in modo appropriato. La terapia nutrizionale viene di solito iniziata durante il ricovero ospedaliero e proseguita in regime ambulatoriale e rivista regolarmente. Sulla base di molti anni di esperienza clinica e dei risultati dello studio EFFORT, è ora in programma lo studio di follow-up “Effect of Nutritional Therapy on Frailty, Functional Outcomes and Recovery of Undernourished Medical Patients at Discharge Trial” (EFFORT II), in ambito ambulatoriale – uno studio svizzero che si occupa di avviata dallo sperimentatore, studio controllato multicentrico non commerciale randomizzato, che inizierà nella seconda metà del 2021. L’obiettivo generale di questo studio è dimostrare il beneficio duraturo della terapia nutrizionale domiciliare personalizzata in termini di mortalità, complicanze gravi, riospedalizzazioni non elettive e funzionalità secondo un algoritmo di implementazione rispetto alla nutrizione abituale nei pazienti polimorfi malnutriti.
Conclusione
Una terapia nutrizionale appropriata e personalizzata ha dimostrato di essere un’opzione di trattamento molto efficace nella prevenzione e nella terapia della ME. Riduce in modo significativo i tassi di morbilità e mortalità. Inoltre, migliora significativamente la qualità della vita e la funzionalità fisica. In considerazione della complessità della ME e per poter ottenere un successo terapeutico a lungo termine degli interventi nutrizionali, è necessario integrare misure aggiuntive come l’attività fisica e il supporto psicologico regolare, nel senso di un approccio terapeutico multimodale. Durante i contatti regolari con i pazienti, si dovrebbero chiedere i problemi nutrizionali e raccogliere semplici dati antropometrici. È importante incorporare le nuove conoscenze presentate in questa revisione nella pratica clinica, per garantire che i pazienti ricevano un’assistenza ottimale, di alta qualità e sicura.
Messaggi da portare a casa
- La malnutrizione è comune e associata a un aumento della morbilità e della mortalità.
- È fondamentale identificare precocemente i pazienti malnutriti con un semplice strumento di screening (NRS 2002).
- La terapia nutrizionale deve essere pianificata, implementata, monitorata e regolata regolarmente.
- Interventi nutrizionali mirati e adeguati sono efficienti e riducono i tassi di complicanze e mortalità.
- Una gestione della nutrizione funzionante è orientata agli obiettivi e garantisce un’elevata qualità del trattamento.
Letteratura:
- de van der Schueren MAE, Soeters PB, Reijven PLM, et al: Diagnosi della malnutrizione – Screening e valutazione. In: Sobotka L, Allison SP, Forbes A, Meier RF, Schneider SM, Soeters PB, et al: Fondamenti di nutrizione clinica. 5 ed. Praga: Galén 2019; 18-27.
- Schindlegger W: Cause dell’anoressia in età avanzata. Journal of Nutritional Medicine (Issue for Switzerland) 2001; 3(3): 20-23.
- Guigoz Y: La revisione della letteratura sul Mini Nutritional Assessment (MNA) – Cosa ci dice? La rivista di nutrizione, salute e invecchiamento 2006; 10(6): 466-485; discussione 85-87.
- Reber E, Gomes F, Bally L, et al: Gestione nutrizionale dei pazienti medici ricoverati. Giornale di medicina clinica 2019; 8(8).
- Gomes F, Baumgartner A, Bounoure L, et al: Associazione del supporto nutrizionale con i risultati clinici tra i pazienti medici ricoverati che sono malnutriti o a rischio nutrizionale: una revisione sistematica aggiornata e una meta-analisi. JAMA network open 2019; 2(11): e1915138.
- Estruch R, Ros E, Salas-Salvado J, et al: Prevenzione primaria delle malattie cardiovascolari con una dieta mediterranea integrata con olio extravergine di oliva o noci. The New England journal of medicine 2018; 378(25): e34.
- Deutz NE, Matheson EM, Matarese LE, et al: Riammissione e mortalità in adulti malnutriti, anziani, ricoverati in ospedale e trattati con un integratore alimentare orale specializzato: uno studio clinico randomizzato. Nutrizione clinica 2016; 35(1): 18-26.
- Schuetz P, Fehr R, Baechli V, et al: Supporto nutrizionale personalizzato in pazienti medici a rischio nutrizionale: uno studio clinico randomizzato. Lancet 2019; 393(1088): 2312-2321.
- Kondrup J, Allison SP, Elia M, et al: Linee guida ESPEN per lo screening nutrizionale 2002. Nutrizione clinica 2003; 22(4): 415-421.
- Kondrup J, Rasmussen HH, Hamberg O, Stanga Z: Screening del rischio nutrizionale (NRS 2002): un nuovo metodo basato sull’analisi di studi clinici controllati. Nutrizione clinica 2003; 22(3): 321-336.
- Harris JA, Benedict FG: Uno studio biometrico del metabolismo basale umano. Atti dell’Accademia Nazionale delle Scienze degli Stati Uniti d’America 1918; 4(12): 370-373.
- Reber E, Strahm R, Bally L, et al: Efficacia ed efficienza dei team di supporto nutrizionale. Giornale di medicina clinica 2019; 8(9).
- Gomes F, Schuetz P, Bounoure L, et al: Linee guida ESPEN sul supporto nutrizionale per i pazienti polimorbidi di medicina interna. Nutrizione clinica 2018; 37(1): 336-353.
- Padhi S, Bullock I, Li L, Stroud M: Terapia con fluidi per via endovenosa per gli adulti in ospedale: sintesi della guida NICE. BMJ 2013; 347: f7073.
- Aubry E, Mareschal J, Gschweitl M, et al: Fatti di gestione della nutrizione clinica – un sondaggio online. Current Nutritional Medicine 2018; 42(06): 452-460.
- Delmi M, Rapin CH, Bengoa JM, et al: Integrazione alimentare nei pazienti anziani con frattura del collo del femore. Lancet 1990; 335(8696): 1013-1016.
- Norman K, Pirlich M, Smoliner C, et al: Costo-efficacia di un intervento di 3 mesi con integratori nutrizionali orali nella malnutrizione correlata alla malattia: uno studio pilota controllato e randomizzato. European journal of clinical nutrition 2011; 65(6): 735-742.
- Stratton RJ, Elia M: Una revisione delle recensioni: Un nuovo sguardo alle prove per gli integratori nutrizionali orali nella pratica clinica. Nutrizione clinica 2007; 2(1): 5-23.
- Istituto Nazionale per l’Eccellenza Sanitaria e Assistenziale. Supporto nutrizionale per gli adulti: supporto nutrizionale orale, alimentazione enterale con sondino e nutrizione parenterale (CG32)2006; ultimo aggiornamento 2017.
- Chew STH, Tan NC, Cheong M, et al: Impatto dell’integrazione nutrizionale orale specializzata sugli esiti clinici, nutrizionali e funzionali: Uno studio randomizzato, controllato con placebo, su adulti anziani che vivono in comunità e che sono a rischio di malnutrizione. Nutrizione clinica 2020.
- Milne AC, Avenell A, Potter J: Meta-analisi: integrazione proteica ed energetica negli anziani. Annali di medicina interna 2006; 144(1): 37-48.
- Elia M, Normand C, Laviano A, Norman K: Una revisione sistematica dei costi e del rapporto costo-efficacia dell’uso di integratori alimentari orali standard in comunità e case di cura. Nutrizione clinica 2016; 35(1): 125-137.
PRATICA GP 2021; 16(4): 11-17











