Il trattamento della SM, la malattia autoimmune del sistema nervoso centrale che più comunemente porta alla disabilità in giovane età, ha fatto molti piccoli progressi e anche alcuni più grandi negli ultimi due decenni. Il panorama terapeutico è cambiato in modo significativo, tanto che oggi sono disponibili diverse opzioni terapeutiche con diversi meccanismi d’azione.
La sclerosi multipla non può ancora essere curata, nonostante i numerosi progressi terapeutici, ma spesso può essere controllata. Il trattamento della malattia autoimmune del sistema nervoso centrale, che il più delle volte porta alla disabilità nella giovane età adulta, ha fatto molti piccoli progressi e anche alcuni più grandi negli ultimi due decenni, e il panorama terapeutico è cambiato in modo significativo, in modo che ora sono disponibili diverse opzioni terapeutiche con diversi meccanismi d’azione. In questo modo, l’eterogeneità della malattia e le caratteristiche e le esigenze del singolo paziente possono essere affrontate meglio.
Dalla fine del 2020, in Svizzera è stato approvato un nuovo farmaco per il trattamento della sclerosi multipla recidivante-remittente (SMRR), che verrà esaminato in dettaglio in questo articolo ECM. Si tratta di ozanimod, un modulatore selettivo del recettore della sfingosina-1-fosfato (S1P) che si lega specificamente ai sottotipi 1 e 5 del recettore S1P. Di conseguenza, i linfociti vengono trattenuti nella periferia e non possono più intervenire nel processo infiammatorio del sistema nervoso centrale (SNC); inoltre, sono potenzialmente ipotizzabili ulteriori meccanismi di azione nel SNC. Il farmaco è approvato in Svizzera come terapia di prima linea per i pazienti adulti affetti da SMRR.
Il meccanismo d’azione di Ozanimod in breve
Nella SM, l’ingresso di alcune cellule infiammatorie attraverso determinate barriere nel sistema nervoso centrale (SNC) è un punto chiave che può essere influenzato con ozanimod. Ozanimod, come modulatore selettivo del recettore della sfingosina-1-fosfato (S1P), trattiene queste cellule infiammatorie negli organi linfoidi secondari (come i linfonodi o la milza). Il legame dell’ozanimod ai recettori S1P sui linfociti immaturi porta all’attivazione e all’internalizzazione di questi recettori. Di conseguenza, l’uscita dei linfociti dai linfonodi nel flusso sanguigno viene inibita, per cui il numero di linfociti nel sangue diminuisce e questi non possono più intervenire nel processo infiammatorio del SNC; sono ipotizzabili anche altri meccanismi d’azione diretti sul SNC, ad esempio sulla funzione delle cellule gliali.
Differenza rispetto ad altri modulatori del recettore S1P
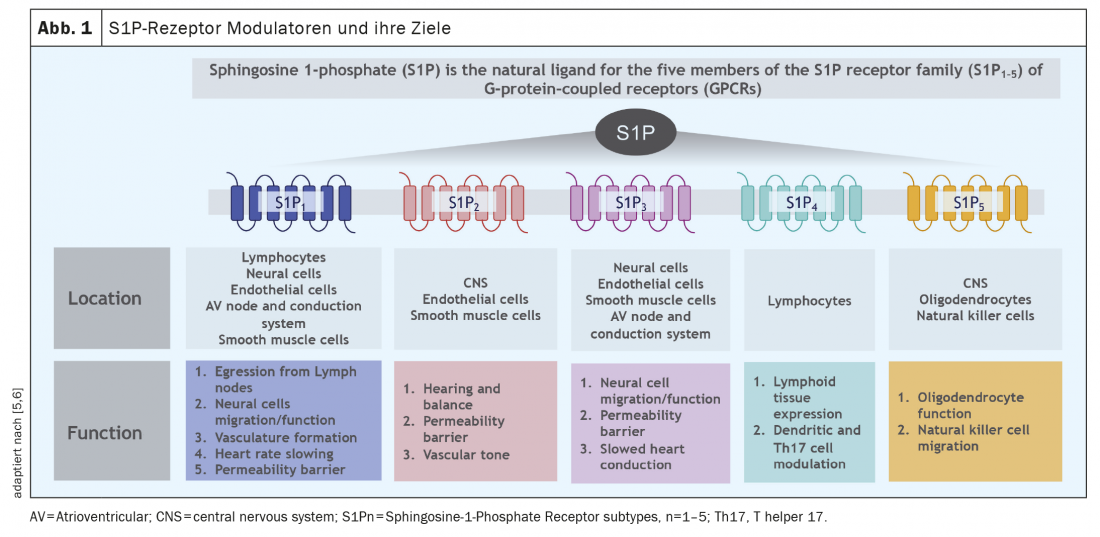
Oltre a ozanimod, ci sono altri due modulatori del recettore S1P nel panorama terapeutico svizzero della SM: Fingolimod e siponimod. Una caratteristica comune di queste sostanze è il legame con i recettori S1P, per cui esiste una selettività diversa per i singoli sottotipi di recettori a seconda della sostanza. Mentre ozanimod si lega in modo altamente selettivo alla sottofamiglia di recettori S1P1 e S1P5, fingolimod non si lega in modo selettivo a due recettori scelti, ma in modo più aspecifico a tutti e 5 i sottotipi di recettori S1P, al recettore S1P2 con bassa affinità (vedere sotto). Tuttavia, a seconda della cellula e del tessuto, i sottotipi dei recettori S1P sono espressi in modo diverso; una panoramica della distribuzione di questi recettori è riportata nella Figura 1. In sintesi, i recettori S1P1 si trovano principalmente sui linfociti, mentre il recettore S1P5 è espresso principalmente nel sistema nervoso centrale. Quindi, il legame selettivo con questi sottotipi di recettori ha anche un senso fisiopatologico. Come ozanimod, siponimod si lega selettivamente ai recettori S1P1 e S1P5, ma i farmaci differiscono nella farmacocinetica (ozanimod viene ampiamente degradato in 2 metaboliti attivi nel giro di poche ore) e forse anche nella selettività per i sottotipi recettoriali, dal momento che ozanimod si lega selettivamente in vitro con elevata affinità soprattutto ai recettori S1P1 e meno ai recettori S1P5 [1].
Punti finali di una terapia efficace per la SM
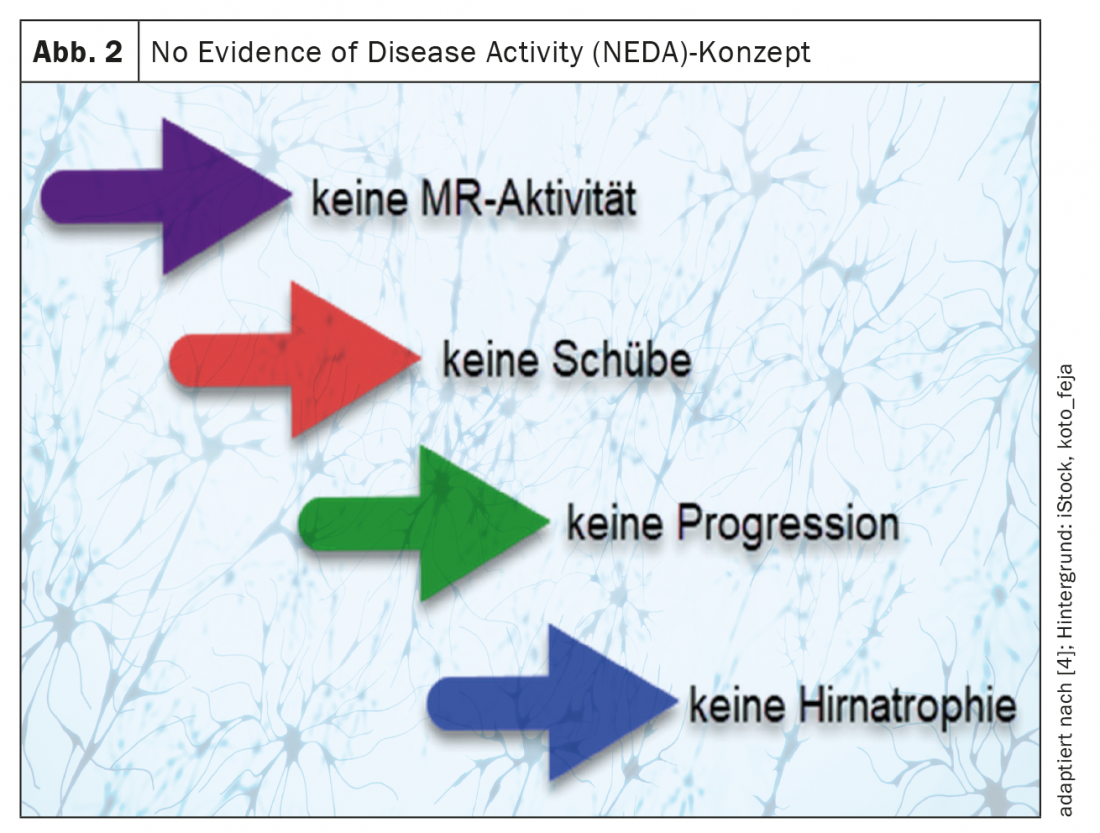
Oggi, grazie alle immunoterapie efficaci, è possibile fissare obiettivi terapeutici più elevati rispetto a quelli previsti qualche decennio fa. Un concetto comune, soprattutto negli studi terapeutici, è quello di “Nessuna evidenza di attività della malattia” (NEDA) [2,3].
Con la presente
- Nessuna attività di risonanza magnetica (lesioni iperintense T2 nuove e/o in espansione e/o lesioni T1 che assorbono il contrasto),
- nessun evento di spinta,
- nessuna progressione strisciante nella scala EDSS (Expanded Disability Status Scale) (“NEDA3”) [2–4] e spesso anche
- nessuna atrofia cerebrale definita come obiettivo della terapia (“NEDA 4”) (Fig. 2) [2– 5].
Tuttavia, a causa di difficoltà metodologiche e tecniche, la misurazione quantitativa dell’atrofia cerebrale non viene ancora eseguita regolarmente nella pratica clinica [10,11]. Inoltre, il concetto NEDA 3 è guidato principalmente dall’attività di imaging, che deve essere vista in modo critico da una prospettiva clinica. Nella pratica clinica quotidiana, finora l’attenzione si è concentrata sugli endpoint che possono essere regolarmente oggettivati senza grandi sforzi, come l’EDSS, ma si sta prestando maggiore attenzione anche ad aspetti come la cognizione o la fatica. Sempre più spesso, la risonanza magnetica (cranica) viene utilizzata come strumento sensibile per la valutazione dell’efficacia e della sicurezza. A medio termine, la misurazione quantitativa dell’atrofia cerebrale (ad esempio, grazie alla segmentazione automatizzata delle sezioni cerebrali mediante “machine learing”) probabilmente troverà sempre più spazio nella pratica clinica quotidiana [11].
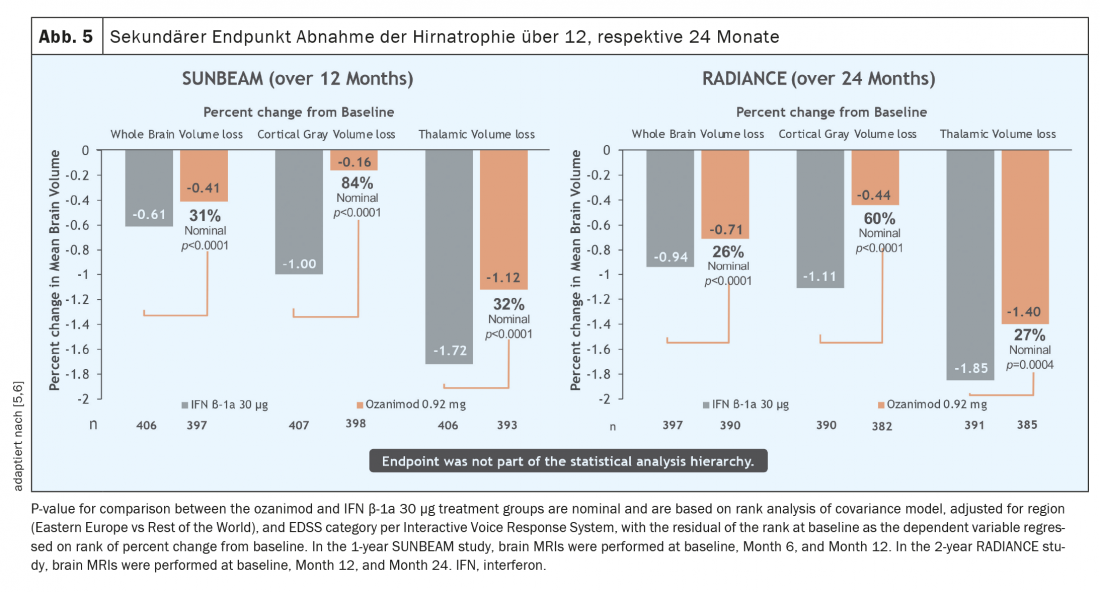
Per quanto riguarda i dati dello studio, anche la qualità dello studio è particolarmente importante. Con ozanimod, ad esempio, sono stati condotti in parallelo due diversi studi di grandi dimensioni. Se, come nel caso di ozanimod, entrambi gli studi giungono essenzialmente agli stessi risultati, si può ipotizzare una situazione di studio robusto. I due studi rilevanti per l’approvazione, RADIANCE [5] e SUNBEAM [6], sono studi di fase 3 multicentrici, in doppio cieco e a doppia manica, che confrontano ozanimod con il comparatore attivo interferone beta1a e differiscono principalmente per i diversi periodi di osservazione, rispettivamente di 24 e 12 mesi.
Efficacia di Ozanimod
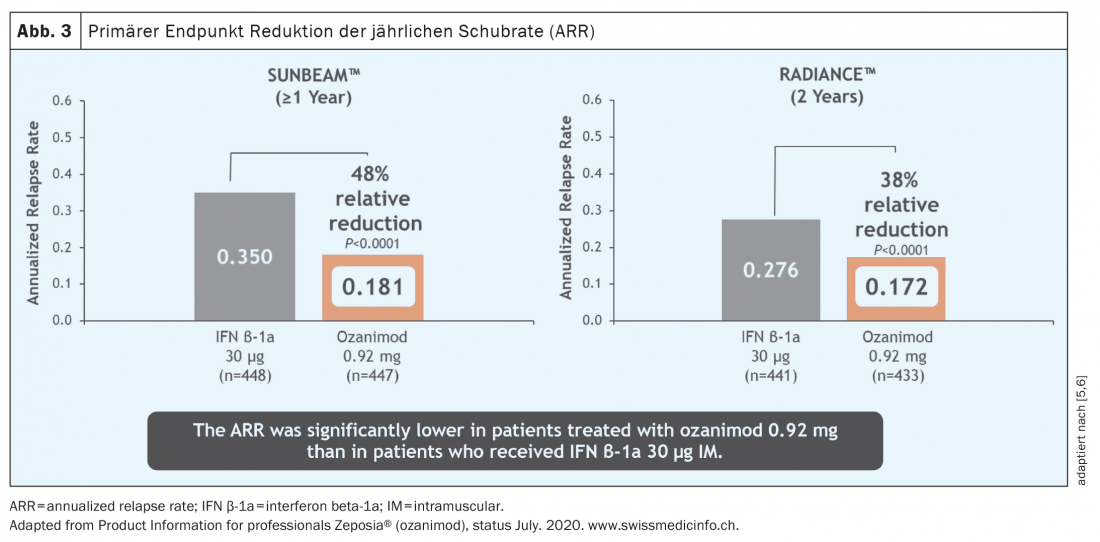
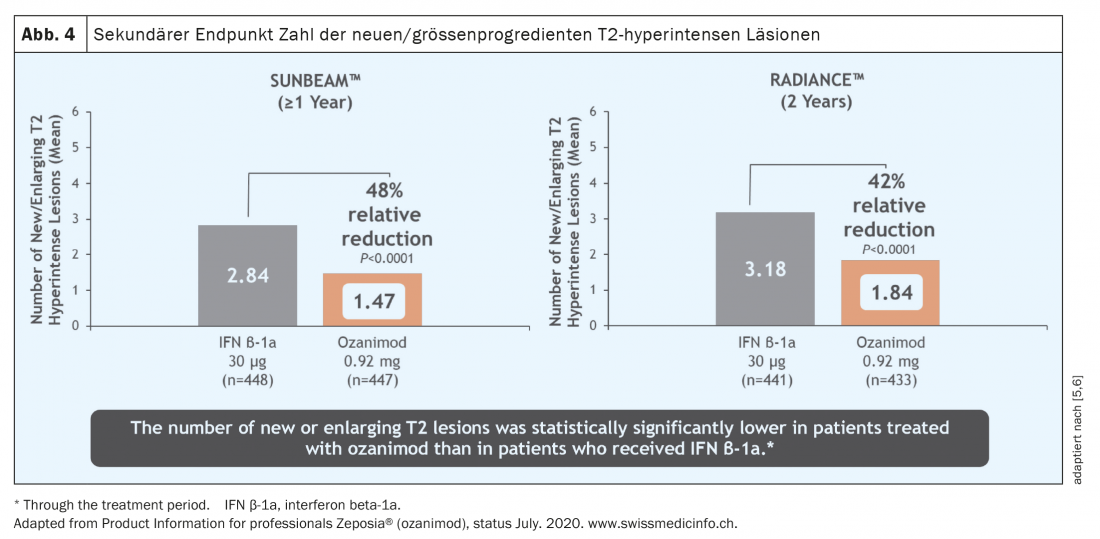
In un periodo di uno e due anni, il tasso di ricaduta è stato ridotto in modo significativo in una popolazione di pazienti che era attiva prima dell’inizio della terapia (Fig. 3) [5 – 7]. Va sottolineato che in questi studi ozanimod non è stato testato contro il placebo, ma contro un comparatore attivo (interferone beta-1A Avonex®), il che evidenzia l’efficacia clinica di ozanimod. Inoltre, è stata osservata una riduzione significativa dell’attività infiammatoria rilevabile a livello tomografico ( Fig. 4) . Tuttavia, nel periodo di studio relativamente breve di 12 e 24 mesi rispettivamente, non è stato possibile dimostrare alcun effetto sulla progressione della disabilità. Tuttavia, i dati iniziali della tomografia MR di entrambi gli studi hanno mostrato un effetto in termini di atrofia del cervello intero, atrofia talamica e atrofia corticale (Fig. 5) . I pazienti con Ozanimod hanno anche mostrato una maggiore velocità di elaborazione cognitiva rispetto al gruppo di confronto, fornendo una prima prova di un possibile effetto positivo anche sugli endpoint cognitivi. Quindi, oltre agli endpoint “classici” come il carico di lesioni T2 e gli eventi di ricaduta, gli studi cardine di ozanimod includevano anche endpoint “più recenti” come la cognizione e l’atrofia. Va notato, tuttavia, che in questi studi la misura dell’atrofia era solo un endpoint secondario e la velocità di elaborazione cognitiva era un endpoint esplorativo, per cui questi risultati devono essere considerati con alcune riserve. In questo caso, i dati a lungo termine porteranno risultati più precisi.
Effetti collaterali
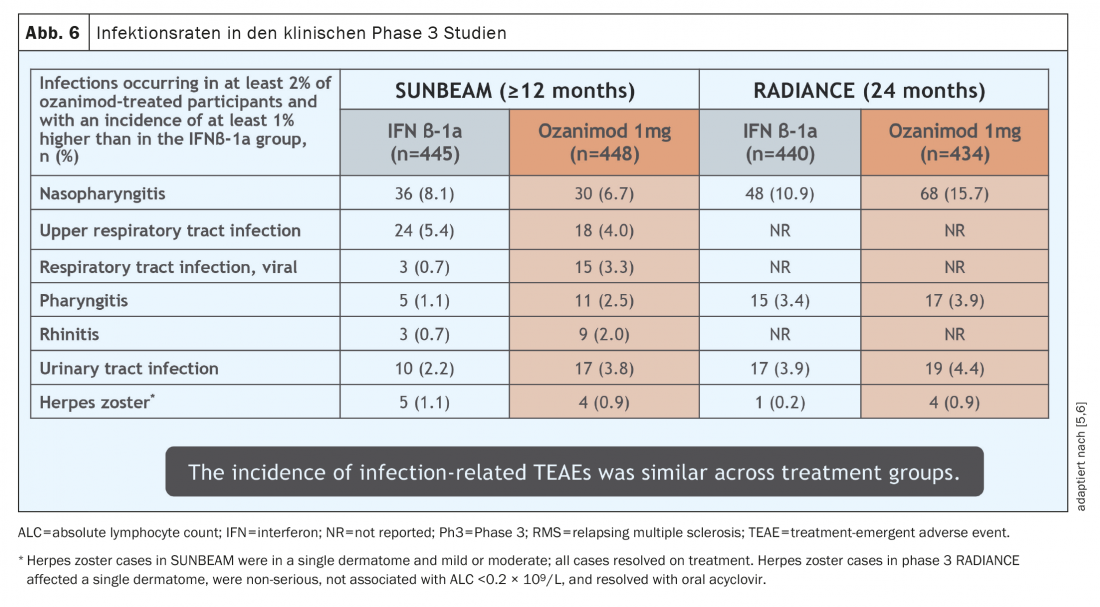
Gli effetti collaterali che si sono verificati negli studi di approvazione quando è stato assunto Ozanimod sono stati essenzialmente gli stessi di quelli sperimentati con altre sostanze che agiscono su SP1, presenti sul mercato da molti anni. L’effetto collaterale più frequente rilevato è stato un leggero aumento delle infezioni respiratorie e del tratto urinario (Fig. 6) . Queste infezioni hanno avuto un decorso lieve. In pochi casi (0,1- 0,3%), l’edema maculare si è verificato in pazienti con condizioni preesistenti (uveite, diabete mellito o malattie retiniche sottostanti/coesistenti) a maggior rischio, e l’herpes zoster è stato osservato nello 0,6%. Secondo il meccanismo d’azione, la riduzione dei linfociti nel sangue periferico è di circa il 45-50%, che tuttavia non rappresenta di per sé un effetto collaterale a causa del meccanismo d’azione di ozanimod con la ritenzione dei linfociti negli organi linfoidi secondari.Una linfopenia transitoria di grado 4 secondo CTCAE si è verificata nel 2,5-4,2% dei pazienti negli studi pivotal (<0,2 G/l), ma questi non sono stati associati a un aumento delle infezioni e non hanno portato all’interruzione della terapia. Non c’è ancora alcun segnale verso le malattie opportunistiche, ma sono necessari più dati e più lunghi per un’ulteriore valutazione. È importante notare che negli studi pivotal, i parametri epatici elevati (definiti come >3× il valore normale superiore) si sono verificati nel 5-6% dei pazienti, richiedendo l’interruzione della terapia nell’1,1% dei pazienti [5,6]. Va notato che nessuno di questi casi finora ha soddisfatto la legge di Hy, che descrive la probabilità che l’insufficienza epatica possa essere attribuita a un farmaco specifico [12].
Per minimizzare gli effetti collaterali cardiaci, ozanimod viene titolato gradualmente nell’arco di 7 giorni. Di conseguenza, si è verificata una tachicardia sinusale in 2 pazienti (0,5%) e una bradicardia sinusale in un paziente (0,2%) negli studi pivotal, motivo per cui è stato necessario interrompere la terapia in un paziente (0,2%).
Controindicazioni di Ozanimod
Le seguenti controindicazioni devono essere considerate prima di iniziare la terapia con ozanimod [adaptiert nach 8,9]:
- Ipersensibilità all’ozanimod o a uno qualsiasi degli altri ingredienti.
- Negli ultimi 6 mesi: Infarto miocardico, angina instabile, ictus, attacco ischemico transitorio, insufficienza cardiaca scompensata che richiede il ricovero in ospedale o Classe III/IV.
- Anamnesi o presenza attuale di blocco atrioventricolare (AV) di secondo grado (tipo II) o blocco AV di terzo grado o sindrome del nodo sinoatriale (eccezione: presenza di pacemaker funzionale).
- Apnea notturna grave non trattata
- Stato di immunodeficienza
- Aumento del rischio di infezioni opportunistiche, compresi i pazienti che stanno ricevendo una terapia immunosoppressiva o sono immunocompromessi.
- Infezioni attive gravi o infezioni croniche attive (ad esempio, epatite, tubercolosi).
- Malattia maligna attiva
- Grave insufficienza epatica (classe C di Child-Pugh)
- Edema maculare esistente
- Gravidanza
Altri aspetti della sicurezza [adaptiert nach 7,8]
Poiché gli studi pivotal hanno escluso i pazienti con pretrattamenti immunosoppressivi (fingolimod, natalizumab, alemtuzumab, cladribina, ocrelizumab, ciclofosfamide, mitoxantrone, irradiazione totale del corpo e trapianto di midollo osseo), ozanimod deve essere usato con cautela in questi pazienti.
Quando si interrompe la terapia con ozanimod, si deve considerare la possibilità di un grave peggioramento della malattia, poiché questo è stato riportato fino al 10% dei casi in seguito all’interruzione di un altro modulatore del recettore S1P [13]. Tuttavia, non è chiaro se questo valga anche per l’ozanimod, che ha un profilo recettoriale e una farmacocinetica diversi.
È inoltre importante evitare la co-somministrazione di ozanimod con gli inibitori della BCRP (Breast Cancer Resistance Protein) (come la ciclosporina), gli inibitori delle MAO (Monoaminoossidasi) (come la selegilina) e gli induttori e inibitori del CYP2C8 (Citocromo P2C8) (come la rifampicina) (come il gemfibrozil).
Nelle donne in età fertile, la gravidanza deve essere esclusa prima di iniziare la terapia e deve essere utilizzata una contraccezione efficace durante il trattamento con Zeposia e per 3 mesi dopo l’interruzione della terapia con Zeposia.
Monitoraggio prima e durante la terapia con ozanimod [adaptiert nach 8,9]
Prima di iniziare la terapia, tutti i pazienti devono sottoporsi al controllo dei parametri epatici e all’emocromo differenziale. Nelle donne in età fertile, si deve anche escludere la gravidanza e installare una contraccezione sicura (indicata fino a 3 mesi dopo l’interruzione della terapia).
Inoltre, lo stato di vaccinazione di tutti i pazienti deve essere aggiornato. I pazienti senza un’anamnesi di varicella confermata dal medico e senza una vaccinazione completa contro il VZV devono essere testati per gli anticorpi contro il VZV e vaccinati se non vengono rilevati anticorpi (attenzione: vaccino vivo; la vaccinazione deve essere completata almeno 1 mese prima dell’inizio della terapia). Non ci sono dati clinici relativi alla sicurezza e all’efficacia della vaccinazione durante la terapia con ozanimod. Per quanto riguarda la malattia COVID e la vaccinazione, nonostante le preoccupazioni teoriche dovute al meccanismo d’azione, ad oggi non ci sono segnali di sicurezza specifici per quanto riguarda l’ozanimod [14]. Secondo le linee guida svizzere e internazionali, la vaccinazione COVID è raccomandata nei pazienti che assumono Ozanimod [15,16]. I vaccini vivi attenuati devono essere evitati durante e fino a 3 mesi dopo la terapia con ozanimod e devono essere completati almeno 1 mese prima di iniziare la terapia.
Prima di iniziare la terapia, è necessario eseguire un ECG in tutti i pazienti per rilevare eventuali disturbi della conduzione. All’inizio della terapia, è necessario eseguire un monitoraggio cardiaco di sei ore con ECG in pazienti selezionati a rischio cardiaco. Questo è consigliato nei pazienti con FC a riposo <55 bpm, blocco AV di 2° grado [Mobitz Typ I] o st.n. Infarto miocardico prima di >6 mesi o insufficienza cardiaca indicata. Inoltre, i pazienti con St.n. arresto cardiaco, eventi cerebrovascolari prima di >6 mesi, ipertonia incontrollata, sincope ricorrente e bradicardia sintomatica, prolungamento significativo del QTc o trattamento con farmaci antiaritmici, deve essere effettuata una co-valutazione cardiologica per stabilire se la terapia con ozanimod può essere iniziata e come deve essere organizzato il monitoraggio. In tutti gli altri pazienti, a differenza di quanto accade con fingolimod, non è più necessario un monitoraggio cardiaco di sei ore. Tuttavia, si raccomanda un monitoraggio regolare della pressione arteriosa per tutti i pazienti in terapia.
Inoltre, il monitoraggio dei test di funzionalità epatica è indicato prima dell’inizio della terapia e nei pazienti senza sintomi dopo 1, 3, 6, 9 e 12 mesi (seguito da un monitoraggio periodico) [8]. Nell’ambito di questi controlli, è necessario effettuare anche un emocromo differenziale prima di iniziare la terapia e ogni 3 mesi per il primo anno, per non perdere una linfopenia eccessivamente grave (controlli periodici successivi).
I pazienti a rischio oftalmologico con fattori di rischio per l’edema maculare (uveite st.n., diabete mellito, malattie retiniche) devono essere regolarmente osservati dal loro oftalmologo prima e durante la terapia. In assenza di fattori di rischio per l’edema maculare, tuttavia, a differenza di fingolimod, non è necessaria una presentazione oftalmologica prima di iniziare la terapia.
In caso di infezioni gravi con ozanimod (che si sono verificate in meno dell’1% negli studi pivotal), si deve valutare l’interruzione della terapia. A causa del lungo tempo di eliminazione (soprattutto dei metaboliti attivi), il monitoraggio delle infezioni deve essere effettuato fino a 3 mesi dopo l’interruzione della terapia.
Procedura pratica per l’adattamento a Ozanimod [adaptiert nach 8,9]
Quando si passa dai farmaci immunosoppressivi a ozanimod, si deve tenere conto della durata d’azione e dei meccanismi d’azione di questi trattamenti, per evitare effetti immunosoppressivi additivi indesiderati. Per esempio, in caso di terapia precedente con farmaci che riducono i linfociti, aspetti che la conta dei linfociti si normalizzi prima di iniziare la terapia con Ozanimod. Si noti inoltre che negli studi pivotal, le terapie precedenti con fingolimod, natalizumab, alemtuzumab, anti-CD4, cladribina, rituximab, ocrelizumab, ciclofosfamide, mitoxantrone, irradiazione corporea totale e trapianto di midollo osseo sono state escluse in qualsiasi momento prima dell’ingresso del paziente nello studio clinico, e di conseguenza non sono disponibili dati clinici per questi gruppi di pazienti. Tuttavia, queste terapie precedenti non sono definite come controindicazioni alla terapia, per cui la terapia con ozanimod è certamente possibile anche dopo queste terapie precedenti, anche se la durata d’azione e i meccanismi d’azione delle terapie precedenti devono essere presi in considerazione per evitare effetti immunosoppressivi additivi non voluti. Il trattamento con ozanimod di solito può essere iniziato immediatamente dopo la sospensione degli interferoni o del glatiramer acetato, se i valori di laboratorio non sono rilevanti (soprattutto l’emocromo differenziale e i valori epatici).
All’inizio della terapia, è necessario un regime di titolazione della dose dal 1° al 7° giorno. Dopo la titolazione della dose di 7 giorni, la dose di mantenimento è di 0,92 mg per via orale una volta al giorno, assunta ininterrottamente a partire dal giorno 8. Le capsule di Ozanimod devono essere deglutite intere e possono essere assunte con un pasto o indipendentemente dai pasti. Se salta una dose di Ozanimod, la dose successiva prevista deve essere assunta il giorno successivo.
Il posto di Ozanimod nell’attuale panorama terapeutico della SM
Ozanimod è approvato in Svizzera per il trattamento di prima linea di pazienti adulti con SM recidivante-remittente e può essere prescritto solo da un consulente neurologo [17]. A differenza della Svizzera, l’ozanimod può essere utilizzato nell’area EMA solo in presenza di segni di attività della malattia (clinicamente o tomograficamente), mentre in Svizzera questo criterio non deve essere soddisfatto [8,18]. La popolazione dello studio comprendeva pazienti adulti affetti da SM-RR con malattia attiva e i criteri di inclusione richiedevano una ricaduta negli ultimi 12 mesi o una ricaduta negli ultimi 24 mesi con evidenza di una lesione con contrasto alla risonanza magnetica negli ultimi 12 mesi, oltre a un EDSS inferiore a 5,5. La maggior parte dei pazienti della popolazione di studio presentava già anomalie neurologiche (scala EDSS 2.5 – 2.7) (che, tuttavia, non è un prerequisito per la terapia con Ozanimod in Svizzera), l’età media era di circa 35 anni e ben due terzi dei partecipanti allo studio erano donne. Di conseguenza, la clientela idonea non è un gruppo di pazienti speciali altamente selezionati, ma piuttosto i pazienti che si incontrano ogni giorno nelle consultazioni. Il pre-trattamento con altri farmaci non esclude la terapia con Ozanimod (sebbene sia necessaria una maggiore vigilanza a seconda della terapia precedente). Gli studi post hoc non hanno individuato pazienti specifici che non hanno risposto al modulatore del recettore S1P, quindi ozanimod sembra essere un’opzione terapeutica per diversi profili di pazienti. Ozanimod è stato ben tollerato negli studi pivotal (e ora anche nei primi studi clinici), non ci sono effetti collaterali gastrointestinali significativi e la somministrazione orale una volta al giorno è anche semplice. Grazie a questi fattori, i pazienti possono integrare molto bene il trattamento nella loro routine quotidiana, per cui ci sono buone condizioni per un’elevata aderenza alla terapia.
Conclusione
Ogni nuova preparazione è una gradita aggiunta all’armamentario dei terapisti della SM. La SM non può essere curata, ma spesso può essere controllata. Tuttavia, non tutti i farmaci funzionano allo stesso modo per ogni paziente. Pertanto, è essenziale un approccio individuale alla persona interessata. In questo caso, Ozanimod è un altro tassello per fornire alle persone colpite una terapia personalizzata, efficace, sicura e ben tollerata.
Messaggi da portare a casa
- La sclerosi multipla non può ancora essere curata, nonostante i numerosi progressi, ma spesso può essere controllata.
- Ozanimod è un modulatore selettivo del recettore della sfingosina-1-fosfato (S1P) che si lega specificamente ai sottotipi 1 e 5 del recettore S1P.
- Legando ozanimod a questi recettori S1P, i linfociti non possono più interferire con il processo infiammatorio nel sistema nervoso centrale.
- Il preparato è stato approvato in Svizzera dalla fine del 2020 come terapia di prima linea per i pazienti adulti con sclerosi multipla recidivante-remittente (RRMS).
- Ozanimod viene assunto per via orale 1× al giorno e negli studi è stato ben tollerato senza effetti collaterali gastrointestinali significativi. Questi dati sono coerenti con le osservazioni iniziali della pratica clinica quotidiana.
Letteratura:
- Scott FL, Clemons B, Brooks J, et al: Ozanimod (RPC1063) è un potente agonista del recettore-1 della sfingosina-1-fosfato (S1P1) e del recettore-5 (S1P5) con attività modificante la malattia autoimmune. Br J Pharmacol. 2016;173(11): 1778-1792.
- Giovannoni G, Turner B, Gnanapavan S, et al: È giunto il momento di mirare all’assenza di attività di malattia evidente (NEDA) nella sclerosi multipla? Mult Scler Relat Disord. 2015 Jul;4(4): 329-333. doi: 10.1016/j.msard.2015.04.006. Epub 2015 May 8. PMID: 26195051.
- Ziemssen T, Derfuss T, de Stefano N, et al: Ottimizzare il successo del trattamento nella sclerosi multipla. J Neurol. 2016 Jun;263(6): 1053-1065. doi: 10.1007/s00415-015-7986-y. Epub 2015 Dec 24. PMID: 26705122; PMCID: PMC4893374.
- Kappos L, De Stefano N, Freedman MS, et al: Inclusione della perdita di volume cerebrale in una misura rivista di “nessuna evidenza di attività di malattia” (NEDA-4) nella sclerosi multipla recidivante-remittente. Mult Scler. 2016
- Cohen JA, Comi G, Selmaj KW; RADIANCE Trial Investigators, et al: Sicurezza ed efficacia dell’ozanimod rispetto all’interferone beta-1a nella sclerosi multipla recidivante (RADIANCE): uno studio multicentrico, randomizzato, di fase 3 della durata di 24 mesi. Lancet Neurol. 2019
- Comi G, Kappos L, Selmaj KW, SUNBEAM Study Investigators, et al: Sicurezza ed efficacia dell’ozanimod rispetto all’interferone beta-1a nella sclerosi multipla recidivante (SUNBEAM): uno studio multicentrico, randomizzato, di fase 3, della durata minima di 12 mesi. Lancet Neurol. 2019
- Cohen JA, Comi G, Arnold DL, RADIANCE Trial Investigators, et al: Efficacia e sicurezza di ozanimod nella sclerosi multipla: estensione in cieco della dose di uno studio randomizzato di fase II. Mult Scler. 2019
- Compendio dei medicinali della Svizzera, compendium.ch, a partire dal 01/2021.
- swissmedicinfo.ch, Stato 01/2021
- Rocca MA, Battaglini M, Benedict RH, et al: Quantificazione dell’atrofia della risonanza magnetica cerebrale nella SM: dai metodi all’applicazione clinica. Neurologia. 2017
- Sastre-Garriga J, Pareto D, Battaglini M, et al: Raccomandazioni di consenso MAGNIMS sull’uso delle misure di atrofia cerebrale e midollare nella pratica clinica. Nat Rev Neurol. 2020; 16(3): 171-182.
- Robles-Diaz M, Lucena MI, Kaplowitz N, Registro spagnolo DILI, et al.: Rete LatinDILI; Consorzio per la traduzione più sicura e veloce basata sull’evidenza. Uso della legge di Hy e di un nuovo algoritmo composito per prevedere l’insufficienza epatica acuta nei pazienti con lesioni epatiche indotte da farmaci. Gastroenterologia. 2014 Jul;147(1): 109-118.e5.
- Evangelopoulos ME, Miclea A, Schrewe L, et al: Frequenza e caratteristiche cliniche dei rimbalzi della sclerosi multipla dopo la sospensione di fingolimod. CNS Neurosci Ther. 2018 Oct;24(10): 984-986.
- Berger JR, Brandstadter R, Bar-Or A: COVID-19 e terapie modificanti la malattia della SM. Neurol Neuroimmunol Neuroinflamm. 2020 Maggio
- www.multiplesklerose.ch/de/aktuelles/detail/anti-sars-cov2-impfung-und-multiple-sklerose (recuperato il 08.03.2021)
- www.msif.org/news/2020/02/10/the-coronavirus-and-ms-what-you-need-to-know (recuperato il 08.03.2021)
- Elenco delle specialità Svizzera, Ufficio federale della sanità pubblica, www.spezialitätenliste.ch/ShowPreparations.aspx (recuperato il 08.03.2021)
- Agenzia europea dei medicinali, ema.europa.eu (recuperato il 08.03.2021)
InFo NEUROLOGIA & PSICHIATRIA 2021; 19(3): 12-18.