A gestão médica dos tumores cerebrais malignos, especialmente dos gliomas malignos, está orientada para a paliação devido aos curtos tempos de sobrevivência e à morbilidade que os acompanha. O edema cerebral vasogénico é tratado com corticosteróides; a dexametasona é a substância terapêutica padrão. A dexametasona é normalmente prescrita demasiadas vezes, durante demasiado tempo e em doses demasiado elevadas. A dose eficaz mais baixa deve ser titulada em consulta com o paciente e familiares. A terapia profiláctica anticonvulsiva na ausência de convulsões epilépticas não é indicada. Aspectos importantes da fase terminal devem ainda ser discutidos com todas as partes envolvidas na fase de comunicação preservada e registados com uma vontade viva.
Os tumores cerebrais do SNC estão divididos em gliomas de grau inferior (WHO grau I-II) e gliomas de grau superior (WHO grau III-IV). Estes incluem astrocitomas, oligodendrogliomas e as suas formas mistas, bem como, muito menos frequentemente, epenodímomas e outras variantes [1].
Os gliomas malignos caracterizam-se por um rápido crescimento tumoral e pela ocorrência de necrose. Estes surgem quando o fornecimento vascular ao tumor já não pode ser garantido. Em resposta à deficiência, citocinas vasculares e factores de crescimento (incluindo o factor de crescimento endotelial vascular, VEGF) são produzidos tanto por células neoplásicas como por células hospedeiras para restaurar a homeostase tecidual [2]. Os vasos de abastecimento de tumores de crescimento rápido são imaturos e permeáveis. Como resultado, as hemorragias desenvolvem-se no tumor e o edema cerebral vasogénico peritumoral é comum. Para além da destruição de células nervosas e tecido de suporte por infiltração maligna, o edema cerebral é um factor importante na morbidade e mortalidade dos gliomas.
Caracteristicamente, as células malignas obtêm a sua energia através da glicólise anaeróbica [3]. O lactato produzido acidifica o ambiente circundante para que os agentes quimioterápicos, anticonvulsivos e outros medicamentos possam penetrar mal nas regiões tumorais. A formação adicional de neurotransmissores excitatórios tais como o glutamato interfere com a função das células nervosas na região peritumoral e provoca sintomas neurológicos e convulsões epilépticas [4].
Iniciar os cuidados paliativos o mais cedo possível
Nos últimos anos, foram feitos progressos na terapia inicial multimodal, consistindo na máxima ressecção possível, radiochemoterapia pós-operatória e manutenção sistémica e terapia de recidiva. No entanto, a gestão médica, especialmente para gliomas malignos, está orientada para a paliação devido ao curto tempo de sobrevivência e à morbilidade que a acompanha. Por conseguinte, os princípios medicinais e não medicinais dos cuidados paliativos devem ser integrados no conceito terapêutico numa fase inicial [5]. O objectivo dos esforços terapêuticos deve ser o de preservar tanto quanto possível a qualidade de vida e a autonomia do paciente. Isto inclui a profilaxia e o tratamento da chamada toxicidade terapêutica e glioma-associada.
A seguir, o tratamento medicamentoso do edema cerebral e das convulsões epilépticas, bem como a gestão das perturbações da coagulação em tumores cerebrais são apresentados de um ponto de vista pragmático.
Edema cerebral perifocal
O edema cerebral vasogénico não é específico como reacção do SNC a um processo intracerebral crescente e ocorre tanto em processos malignos (gliomas, metástases cerebrais) como em inflamações (abcessos, doenças auto-imunes). Especialmente nos gliomas malignos, a quebra da barreira hemato-encefálica deve-se ao rápido crescimento de vasos tumorais imaturos [2]. Este é o pré-requisito anatómico para a fuga do meio de contraste aplicado por via intravenosa para o tumor cerebral. O crescimento tumoral e o edema vasogénico aumentam inicialmente a pressão intracraniana localizada, deslocando a matéria cerebral circundante e causando sintomas neurológicos focais. Se a pressão intracraniana aumenta, desenvolve-se uma deslocação da linha média e/ou um deslocamento dos lóbulos temporais através do tentorium para o caudal (hérnia transtemporal) (Fig.1). O aumento da pressão só pode ser compensado pela redução do volume de sangue intravascular, inicialmente venoso, mas mais tarde também arterial e do líquido cefalorraquidiano até que as reservas fisiológicas se esgotem. A congestão e hemorragia da saída venosa, a subperfusão arterial e as perturbações da circulação do líquido cefalorraquidiano, por sua vez, agravam o processo da doença.
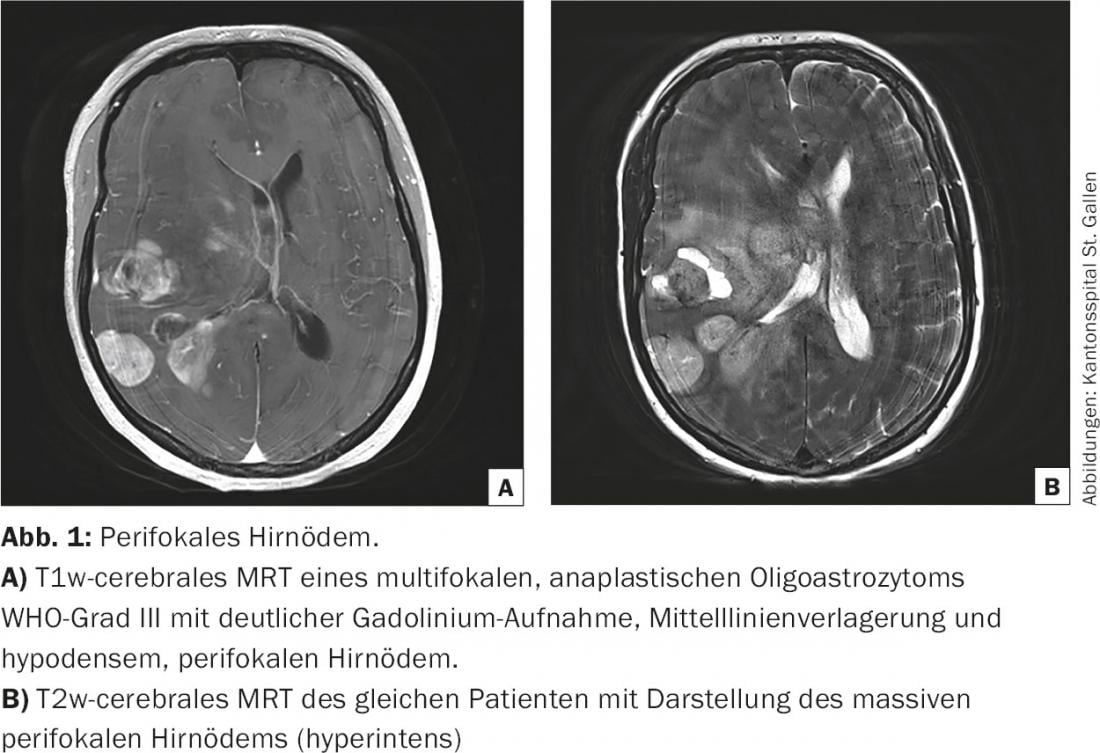
O edema peritumoral cerebral desempenha um papel importante tanto no diagnóstico inicial como no decurso da doença do tumor cerebral. Muitas vezes, os distúrbios neurológicos iniciais só são desencadeados pelo edema cerebral vasogénico e são rapidamente reversíveis (em 24 horas) pela administração de corticosteróides [6]. Os esteróides são utilizados como agente terapêutico diagnóstico para distinguir uma perturbação funcional (relacionada com a pressão) dos danos estruturais (infiltração, destruição). Isto ajuda na avaliação do risco-benefício de uma intervenção neurocirúrgica, especialmente na situação de recorrência. Na fase terminal da doença do tumor cerebral, o aumento da pressão intracraniana leva ao aumento da opacidade e finalmente à morte do paciente. Este processo de morte é predominantemente pacífico [7].
Gestão de edema cerebral vasogénico
Em contraste com o edema citotóxico cerebral, que é geralmente causado por hipoxia, o edema vasogénico cerebral é tratado com corticosteróides. A dexametasona é amplamente utilizada como uma substância terapêutica padrão na prática clínica diária. Tem uma longa meia-vida biológica, pode ser administrada por via oral e intravenosa, e proporciona um rápido alívio dos sintomas. O efeito é desdobrado através da modulação da expressão VEGF, efeitos anti-inflamatórios e a inibição da cascata de ácido araquidónico [8]. Contudo, com a terapia a longo prazo, são de esperar efeitos secundários consideráveis, por exemplo, a invalidação da miopatia esteróide proximal, hiperglicemia, hipalbuminemia, distúrbios electrolíticos, imunossupressão, distúrbios psiquiátricos, osteoporose e hemorragias cutâneas [8]. Portanto, a manipulação cuidadosa deste medicamento no tratamento de tumores cerebrais é crucial para não pôr substancialmente em perigo o estado de saúde do doente através de intervenções iatrogénicas(tab. 1).

A nossa experiência mostra que a dexametasona é prescrita com demasiada frequência, durante demasiado tempo e em doses demasiado elevadas. Recomendamos que a dose eficaz mais baixa seja titulada em consulta com o paciente e familiares, mesmo com o risco de agravamento temporário das queixas neurológicas (tab. 2 e 3) . Devido à longa meia-vida biológica, não há nenhum argumento racional para administrar dexametasona várias vezes ao dia. Uma única dose pela manhã é suficiente. A administração matinal é melhor tolerada (perturbações do sono, delírios nocturnos), reflecte a libertação fisiológica de corticosteróides endógenos e aumenta a aderência aos medicamentos. Os esteróides lipofílicos têm um potencial crítico de interacção com quimioterápicos, anticonvulsivos e anticoagulantes que é muito raramente considerado.

Ataques epilépticos
Em 20-40% dos doentes com tumor cerebral, as crises epilépticas levam ao diagnóstico de uma massa intracraniana. Um terço de todos os pacientes com tumor cerebral sofre de epilepsia estrutural, em que gliomas de baixo grau e tumores neurogénicos (por exemplo, gangliogliomas) são mais epilépticos do que gliomas malignos ou metástases [9]. No entanto, a terapia profiláctica anticonvulsiva não é indicada [10].
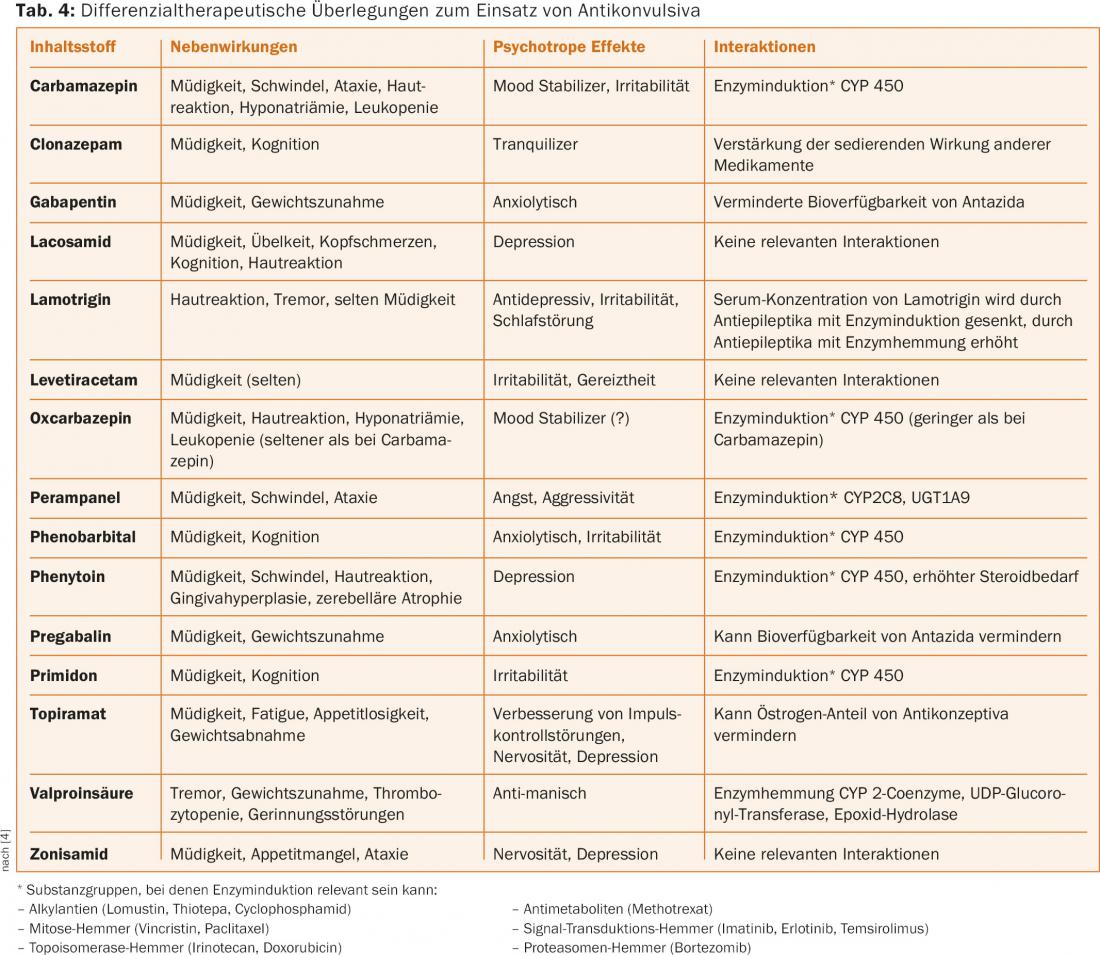
As crises epilépticas afectam a qualidade de vida devido ao aumento da probabilidade de ocorrência de crises inesperadas, apesar da terapia anticonvulsiva adequada. Isto tem consequências na autonomia do paciente (medo de convulsões), restringe a mobilidade (proibição de condução) e pode levar a lesões devido a quedas. Educar os afectados é importante nesta situação para contrariar o medo geralmente exagerado de ataques epilépticos. A ingestão regular de anticonvulsivos em doses terapêuticas, a selecção da preparação óptima para a terapia diferencial e a atenção às contra-indicações e interacções (www.cancerdrugs.ch) são determinantes importantes da terapia [10]. Uma terapia diferencial para o uso de anticonvulsivos pode ser encontrada no quadro 4. Evitar factores provocadores de convulsões, tais como privação do sono ou consumo excessivo de álcool, bem como uma boa adesão à medicação, fazem parte disto no lado do paciente. Devem ser evitados medicamentos que baixem o limiar de convulsões (por exemplo, bupropiona, clozapina e antibióticos beta-lactâmicos) e hiperglicemia excessiva.
A educação sobre as crises geralmente auto-limitadas e a prescrição de anticonvulsivos de acção rápida (Rivotril, Lorazepam, Dormicum) contribuem para a autonomia do paciente e para a redução da ansiedade. Igualmente importantes são as instruções sobre o que fazer em caso de ataque epiléptico (plano de tratamento, lista telefónica) e que actividades devem ser evitadas (escalar árvores, escalar escadas, tomar banho sozinho, mudar os bebés numa mesa em vez de no chão). Nem todas as crises epilépticas requerem uma visita ao departamento de emergência, onde o paciente tem de esperar muito tempo e são encomendadas imagens desnecessárias. Muitas vezes, uma consulta telefónica com o médico de família ou com um médico de serviço neurológico é suficiente para gerir a situação aguda. No entanto, as convulsões invulgares, a longa duração das convulsões, a inconsciência prolongada ou a agitação pós-parto devem dar razão para uma consulta médica a fim de não negligenciar a hemorragia tumoral, a progressão tumoral ou perturbações metabólicas (hipoglicemia, desequilíbrios electrolíticos).
Perturbações de coagulação
O risco de tromboembolismo venoso pós-operatório em doentes com tumor cerebral no primeiro ano é cumulativamente de 30% [11]. Os factores de risco são tumores cerebrais malignos, idade avançada, hemiparesia, grande volume de tumores e ressecção parcial de tumores. Como efeito paraneoplástico remoto, os gliomas malignos secretam substâncias vasoactivas (VEGF, factor de tecido) que desencadeiam distúrbios de coagulação, tais como trombose e embolia pulmonar [12]. Na avaliação do risco, a profilaxia e o tratamento de eventos tromboembólicos é sem restrições devido ao baixo risco de hemorragia intracerebral (cerca de 2%) [13]. Terapêuticamente, são utilizadas meias de compressão e heparinas de baixo peso molecular na fase pós-operatória imediata. Se for detectado tromboembolismo venoso, a anticoagulação parentérica ou oral é também indicada em doentes com tumor cerebral [11]. Isto também se aplica a doentes em terapia anti-angiogénica com bevacizumab [14].
Problemas especiais no fim da vida
Os pacientes com tumores cerebrais diferem de outros pacientes com tumores na fase de fim de vida pelo aparecimento de sintomas neurológicos específicos [15]. Entre estes incluem-se problemas de deglutição, perda de consciência, défices neurológicos progressivos, incontinência e dores de cabeça.
Em particular, as perturbações de comunicação e neurocognitivas interferem com a autonomia no fim da vida e levam os conceitos gerais de cuidados paliativos, que se baseiam frequentemente na expressão activa da vontade, aos seus limites. Por conseguinte, os aspectos importantes da fase terminal devem ainda ser discutidos com todas as partes envolvidas na fase de comunicação recebida e registados com uma directiva antecipada. Estes aspectos incluem decisões médicas como a alimentação artificial versus jejum para a morte, medidas de reanimação, terapia da dor e sedação, bem como necessidades espirituais, o local da morte, arranjos fúnebres e a organização de cuidados paliativos [5,16,17].
Em caso de perda de consciência, deve-se considerar criticamente a sensação de continuação da terapia medicamentosa através da aplicação de fluidos, corticosteróides, anticonvulsivos e profilaxia da trombose sob o aspecto de prolongar o sofrimento [7].
Literatura:
- Louis DN, et al: A classificação de 2007 da OMS de tumores do sistema nervoso central. Acta Neuropathol 2007; 114: 97-109.
- Wick W, et al: Situação actual e futuras direcções da terapia anti-angiogénica para gliomas. Neuro Oncol 2016; 18: 315-328.
- Woolf EC, Scheck AC: A dieta cetogénica para o tratamento do glioma maligno. J Lipid Res 2015; 56: 5-10.
- Hundsberger T, et al: Complicações neurológicas em doentes com cancro. Praxis 2014; 103: 1009-1016.
- Pace A, et al: Cuidados de apoio em neurooncologia. Curr Opinião Oncol 2010; 22: 621-626.
- Wolfson AH, et al: O papel dos esteróides na gestão do carcinoma metastático para o cérebro. Um ensaio-piloto em perspectiva. Am J Clin Oncol 1994; 17: 234-238.
- Bausewein C, et al.: Como é que morrem os pacientes com tumores cerebrais primários? Palliat Med 2003; 17: 558-559.
- Roth P, et al: Edema associado ao tumor em doentes com cancro do cérebro: patogénese e gestão. Perito Rev Anticancer Ther 2013; 13: 1319-1325.
- van Breemen MS, et al: Epilepsia em doentes com tumores cerebrais: epidemiologia, mecanismos, e gestão. Lancet Neurol 2007; 6: 421-430.
- Rossetti AO, Stupp R: Correlação do uso de anticonvulsivos indutores de enzimas com o resultado de pacientes com glioblastoma. Neurologia 2010; 74: 1329-1330.
- Perry JR, et al: Estudo de Fase II de temozolomida dose-intensa contínua em glioma maligno recorrente: Estudo RESCUE. J Clin Oncol 2010; 28: 2051-2057.
- Jenkins EO, et al: Tromboembolismo venoso em gliomas malignos. J de Trombose e Hemostasia 2010; 8: 221-227.
- Pan E, et al: Estudo Retrospectivo de Eventos de Hemorragia Tromboembólica Venosa e Intracerebral em Pacientes com Glioblastoma. Anticancer Research 2009; 29: 4309-4313.
- Nghiemphu PL, et al: Bevacizumab e quimioterapia para glioblastoma recorrente: uma experiência de uma única instituição. Neurologia 2009; 72: 1217-1222.
- Sizoo EM, et al: Sintomas e problemas na fase de fim de vida de doentes com glioma de alta qualidade. Neuro Oncol 2010; 12: 1162-1166.
- Koekkoek JA, et al: Sintomas e gestão de medicamentos na fase de fim de vida de doentes com glioma de alta qualidade. J Neurooncol 2014; 120: 589-595.
- Pace A, et al: Problemas de fim de vida em doentes com tumores cerebrais. J Neurooncol 2009; 91: 39-43.
- Kaal EC, Vecht CJ: A gestão do edema cerebral em tumores cerebrais. Curr Opinião Oncol 2004; 16(6): 593-600.
InFo NEUROLOGIA & PSYCHIATRY 2016; 14(4): 22-28