[1-3]O estudo comparativo SEQUENCE, recentemente publicado no New England Journal of Medicine (NEJM), comparou os dois inibidores da interleucina (IL)-23 e IL-12/-23, risankizumab (SKYRIZI®) e ustekinumab, em doentes com doença de Crohn (DC). [4-6] Foram agora apresentadas análises post-hoc suplementares na Semana Europeia Unida de Gastroenterologia (UEGW) deste ano, de 12 a 15 de outubro de 2024, em Viena. [4-6] Os resultados mostram, entre outras coisas, que o risankizumab atinge taxas de eficácia numericamente mais elevadas em comparação com o ustekinumab, independentemente da duração da doença, conduz a uma maior normalização dos biomarcadores e melhora significativamente a qualidade de vida.
No estudo SEQUENCE, mais de 500 doentes com DC com falha de tratamento foram aleatorizados para um ou mais inibidores do TNF e tratados de forma aberta durante 48 semanas com risankizumab (N=255) ou ustekinumab (N=265) [1]. < Ambos os objectivos primários foram alcançados: Com remissão clínica após 24 semanas (CDAI 150) O risankizumab foi não inferior ao ustekinumab (58,6 % vs. 39,5 %). < No que respeita ao segundo parâmetro de avaliação primário, a remissão endoscópica (SES-CD ≤ 4 e ≥ 2 pontos abaixo da linha de base) após 48 semanas, o risankizumab foi significativamente superior ao ustekinumab (31,8 % vs. 16,2 %, p 0,001) [1]. Além disso, a taxa global de eventos adversos emergentes do tratamento (TEAEs) foi baixa em ambos os grupos (27,9% vs. 21,9%) e não foram identificados novos sinais de segurança com o risankizumab em comparação com os estudos pivotais [1, 7, 8]. Análises post-hoc suplementares do estudo comparativo foram agora apresentadas na UEGW 2024.
Taxas de eficácia numericamente mais elevadas com o risankizumab, independentemente da duração da doença, com maior benefício após o início do tratamento o mais cedo possível [4]
O tratamento precoce com terapias avançadas, como os biológicos, pode retardar ou interromper a progressão da DC e, assim, melhorar a qualidade de vida dos pacientes e evitar complicações adicionais, como fístulas, hospitalização e cirurgia [9, 10].<2 Jahre, 2-5 Jahre, 5-10 Jahre,>A eficácia do risankizumab em comparação com o ustekinumab em doentes com diferentes durações de doença (10 anos) foi agora analisada numa análise post-hoc do estudo SEQUENCE [4]. O resultado: Independentemente do tempo que os doentes já tinham a doença, uma proporção numericamente maior alcançou a remissão clínica e endoscópica após 24 e 48 semanas com risankizumab, bem como a resposta endoscópica e a remissão clínica e endoscópica sem esteróides após 48 semanas [4]. Particularly in the endoscopic response at 48 weeks, more risankizumab patients reached the endpoint* compared to the ustekinumab group( <2 years: 52.8 % vs. 25,6 %, P < 0,05; 2-5 anos: 40,7 % vs. 12,9 %, P < 0,001; 5-10 anos: 46,3 % vs. 25,4 %, P < 0,05;>10 anos: 44,1 % vs. 23,6 %, P < 0,01). Os pacientes com risankizumab e uma duração da doença de ≤2 anos foram os que mais beneficiaram, o que apoia a intervenção precoce em pacientes com DC [4].

Fig 1: Taxas de normalização mais elevadas dos biomarcadores hs-CRP e FC com risankizumab. Análise post-hoc, todos os valores de p são nominais e não controlados por multiplicidade. FC = calprotectina fecal; PCR-hs = proteína C-reactiva de alta sensibilidade; Q8W = de 8 em 8 semanas; RZB = risankizumab; s.c. = subcutâneo; UST = ustekinumab. Adaptado de [5]
Os biomarcadores realçam a superioridade do risankizumab em comparação com o ustekinumab [5]
Na análise dos dados primários do estudo SEQUENCE, os doentes com risankizumab apresentaram uma maior redução da calprotectina fecal (CF) e da proteína C-reactiva (PCR) do que com ustekinumab [1]. [11] A CF e a PCR são os dois biomarcadores mais utilizados na DC e servem como marcadores objectivos da inflamação intestinal. [11] A normalização da FC e da PCR é, portanto, também recomendada como um objetivo de tratamento a médio prazo nas diretrizes STRIDE II. Uma análise post-hoc do estudo SEQUENCE apresentado na UEGW mostra que este objetivo é alcançável para mais doentes com risankizumab do que com ustekinumab: aqui, uma maior proporção de doentes com risankizumab com FC elevada (>1) alcançou a normalização da FC (>1):Em doentes com FC elevada (>250 mg/kg) ou PCR (>5 mg/L) no início do estudo, uma maior proporção de doentes com risankizumab alcançou a normalização do valor da PCR às semanas 24 e 48 e a normalização do valor da FC às semanas 8, 24 e 48 (p nominal < 0,01) (Fig. 1) [5]. Para além disso, mais doentes com risankizumab alcançaram a normalização dos biomarcadores em combinação com remissão clínica e resposta endoscópica do que os doentes que receberam ustekinumab (Fig. 2) [5].
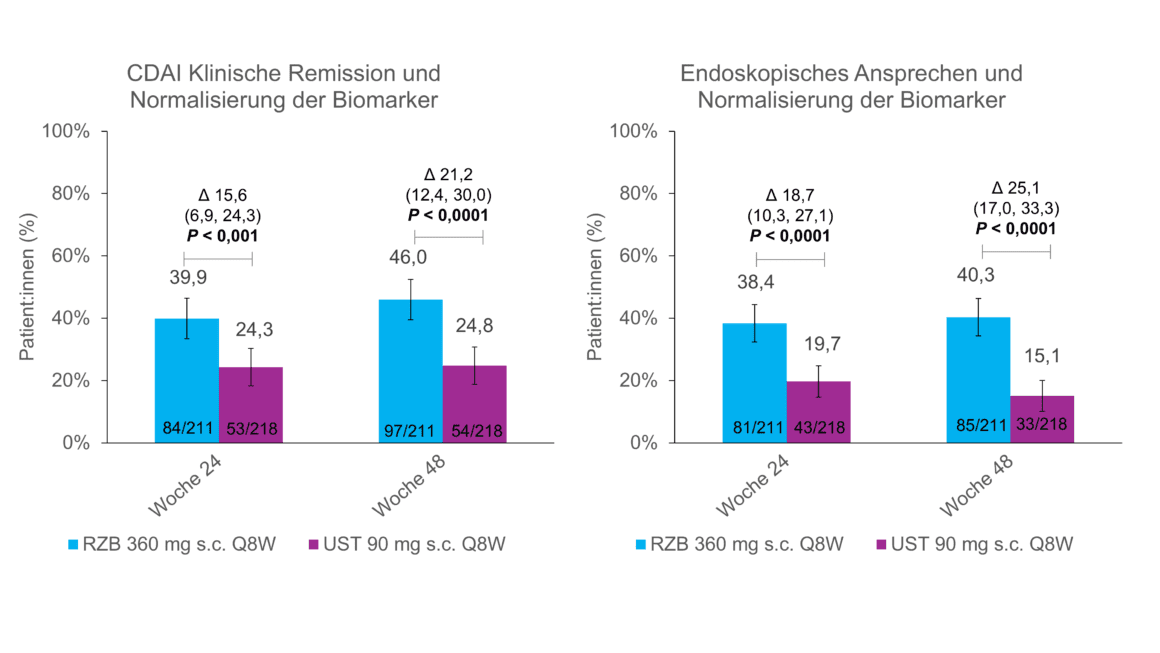
Fig. 2: Remissão clínica ou resposta endoscópica + normalização de biomarcadores mais frequente com risankizumab. Análise post-hoc, todos os valores de p são nominais e não controlados por multiplicidade. CDAI = Índice de Atividade da Doença de Crohn; Q8W = cada 8 semanas; RZB = risankizumab; s.c. = subcutâneo; UST = ustekinumab. Adaptado de [5]
Melhoria da qualidade de vida e dos sintomas psicológicos com risankizumab [6]
Uma outra análise post-hoc debruçou-se sobre a melhoria da qualidade de vida e analisou vários resultados relatados pelos doentes (PROs), como o IBDQ e o SF-36v2 [6]. Uma proporção significativamente maior de doentes tratados com risankizumab apresentou melhorias clinicamente significativas na remissão do IBDQ (semana 24: 52,5% vs. 30,9%; semana 48: 49,8% vs. 33,2%) e melhorias no SF-36v2 físico e mental em comparação com o grupo do ustekinumab [6]. Além disso, uma proporção significativamente menor de pacientes no grupo risankizumab relatou sintomas como fadiga, depressão ou ansiedade nas semanas 24 e 48 em comparação com os pacientes com ustekinumab [6].
Conclusão
[4-6]O estudo SEQUENCE é o primeiro estudo comparativo em DC a demonstrar a superioridade de um produto biológico em relação a outro produto biológico [1]. As análises post-hoc aprofundadas aqui apresentadas salientam agora também a maior eficácia do risankizumab em doentes com diferentes durações da doença, em termos de biomarcadores e qualidade de vida. Estes resultados realçam o potencial benefício da intervenção precoce com risankizumab para melhorar ainda mais o controlo da doença e a qualidade de vida dos doentes.
*Análise post-hoc, todos os valores de p são nominais e não controlados por multiplicidade.
Abreviaturas: CDAI = Índice de Atividade da Doença de Crohn; IBDQ = Questionário da Doença Inflamatória Intestinal; PRO = Resultado relatado pelo doente; SES-CD = Simple Endoscopic Score for Crohn’s Disease; SF-36v2 = Short Form-36versão 2; TEAE = Eventos adversos emergentes do tratamento.
Fonte:
Semana Europeia Unida de Gastroenterologia (UEGW) 2024, 12 a 15 de outubro de 2024, Viena (Áustria) Relatório: Dr. sc. nat. Stefanie Jovanovic
Breve informação técnica SKYRIZI® SKYRIZI

CH-SKZG-240100 11/2024 Este artigo foi produzido com o apoio financeiro da AbbVie AG, Alte Steinhauserstrasse 14, Cham.
Este artigo foi publicado em alemão.
Literatura
1 Peyrin-Biroulet, L., et al, Risankizumab versus ustekinumab para a doença de Crohn moderada a grave. N Engl J Med, 2024. 391(3): p. 213-223.
2. Resumo atual das caraterísticas do produto SKYRIZI® (risankizumab) Doença de Crohn em www.swissmedicinfo.ch.
3. Resumo atual das caraterísticas do produto do ustekinumab em www.swissmedicinfo.ch.
4 Peyrin-Biroulet, L., et al. Eficácia do Risankizumab Versus Ustekinumab por Duração da Doença em Doentes com Doença de Crohn Moderada a Grave: Uma Análise Posthoc do Estudo SEQUENCE de Fase 3 . PP0589. Poster apresentado na UEGW; Viena, 12-15 de outubro de 2024.
5 Colombel JF, et al: Inflammatory Biomarker Reduction and Improvement in Clinical and Endoscopic Outcomes With Risankizumab Versus Ustekinumab in Patients With Moderate to Severe Crohn’s Disease: A Posthoc Analysis From the Phase 3 SEQUENCE Study. PP0588. Poster apresentado na UEGW; Viena, 12 a 15 de outubro de 2024.
6 Loftus EV, et al: Melhoria da Qualidade de Vida Relacionada com a Saúde em Pacientes com Doença de Crohn Moderada a Grave Tratados com Risankizumab Versus Ustekinumab no Estudo SEQUENCE de Fase 3B. MP677. Poster apresentado na UEGW; Viena, 12-15 de outubro de 2024.
7 D’Haens, G., et al, Risankizumab as induction therapy for Crohn’s disease: results from the phase 3 ADVANCE and MOTIVATE induction trials. Lancet, 2022. 399(10340): p. 2015-2030.
8 Ferrante, M., et al, Risankizumab as maintenance therapy for moderately to severe active Crohn’s disease: results from the multicentre, randomised, double-blind, placebo-controlled, withdrawal phase 3 FORTIFY maintenance trial.Lancet, 2022. 399(10340): p. 2031-2046.
9 Danese, S., G. Fiorino, e L. Peyrin-Biroulet, Intervenção precoce na doença de Crohn: rumo a ensaios de modificação da doença. Gut, 2017. 66(12): p. 2179-2187.
10 Ben-Horin, S., et al, Efficacy of Biologic Drugs in Short-Duration Versus Long-Duration Inflammatory Bowel Disease: A Systematic Review and an Individual-Patient Data Meta-Analysis of Randomised Controlled Trials [Eficácia dos medicamentos biológicos na doença inflamatória intestinal de curta duração versus de longa duração: uma revisão sistemática e uma meta-análise de dados individuais de ensaios clínicos aleatórios ]. Gastroenterology, 2022. 162(2): p. 482-494.
11 Turner, D., et al, STRIDE-II: An Update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) Initiative of the International Organisation for the Study of IBD (IOIBD): Determining Therapeutic Goals for Treat-to-Target strategies in IBD. Gastroenterology, 2021. 160(5): p. 1570-1583.
As referências podem ser solicitadas por especialistas em medinfo.ch@abbvie.com.