A identificação e investigação de biomarcadores moleculares pode ajudar a decompor o fenótipo complexo da dermatite atópica em subfenótipos. Um objectivo a longo prazo desta investigação translacional é a estratificação e a selecção de doentes com base em biomarcadores de diagnóstico, prognóstico e previsão, como base para uma estratégia terapêutica individual optimizada.
Numerosas publicações recentes abordam o tema das abordagens de investigação translacional no contexto da dermatite atópica (DA). Incluindo um artigo de revisão publicado na Cellular & Molecular Immunology 2023 por Facheris et al. e uma revisão de Balato et al. publicada na Life 2022 [1,2]. Segue-se um resumo de algumas das principais conclusões abordadas no sítio [1,2].
Investigação translacional para abordagens terapêuticas personalizadas
Os recentes avanços na compreensão da patogénese da doença de Alzheimer revolucionaram a investigação translacional e conduziram a uma expansão exponencial do pipeline terapêutico [1]. Para além dos produtos biológicos já aprovados (Dupilumab, Tralokinumab) e dos inibidores JAK (Baricitinib, Upadacitinib, Abrocitinib), estão actualmente em desenvolvimento numerosas outras substâncias activas inovadoras, tais como produtos biológicos e “pequenas moléculas”, para a área de indicação da dermatite atópica. Estes incluem lebrikizumab (anti-IL13), nemolizumab (anti-31-R), tezepelumab (anti-TSLP), anti-Ox-40-Ak, bem como brepocitinib (inibidor tópico de TYK2/JAK1) e moduladores dos receptores de hidrocarbonetos arilo [1,2]. Com base no pressuposto de que as manifestações heterogéneas dos sintomas e a evolução da doença reflectem diferenças fundamentais a nível molecular, deverá ser possível, no futuro, identificar subgrupos de doentes com diferentes subtipos da doença e diferentes respostas a determinadas terapêuticas.
| Projectos de investigação translacional No projecto “BIOMAP “* (Biomarcadores na Dermatite Atópica e Psoríase) [14], as causas e os mecanismos da DA e da psoríase estão a ser investigados com o objectivo de identificar biomarcadores responsáveis pela variação no curso da doença. O projecto “CHAMP“$ (CHildhood Allergy and tolerance: bioMarkers and Predictors) [15] centra-se na investigação dos factores determinantes de várias doenças alérgicas (alergia alimentar, dermatite atópica, asma, febre dos fenos) desde o nascimento até à adolescência. É dada especial atenção aos factores que determinam a tolerância primária (=não ocorrência de doenças) e a tolerância adquirida (=remissão de doenças existentes). O projecto de estudo identificará biomarcadores clinicamente relevantes que possam ser utilizados para prever o início precoce, a progressão e a remissão. |
* Duração: 01.04.2019-31.03.2024 $ Duração: 2017-2022 |
DA: fisiopatologia multifactorial com predisposição genética
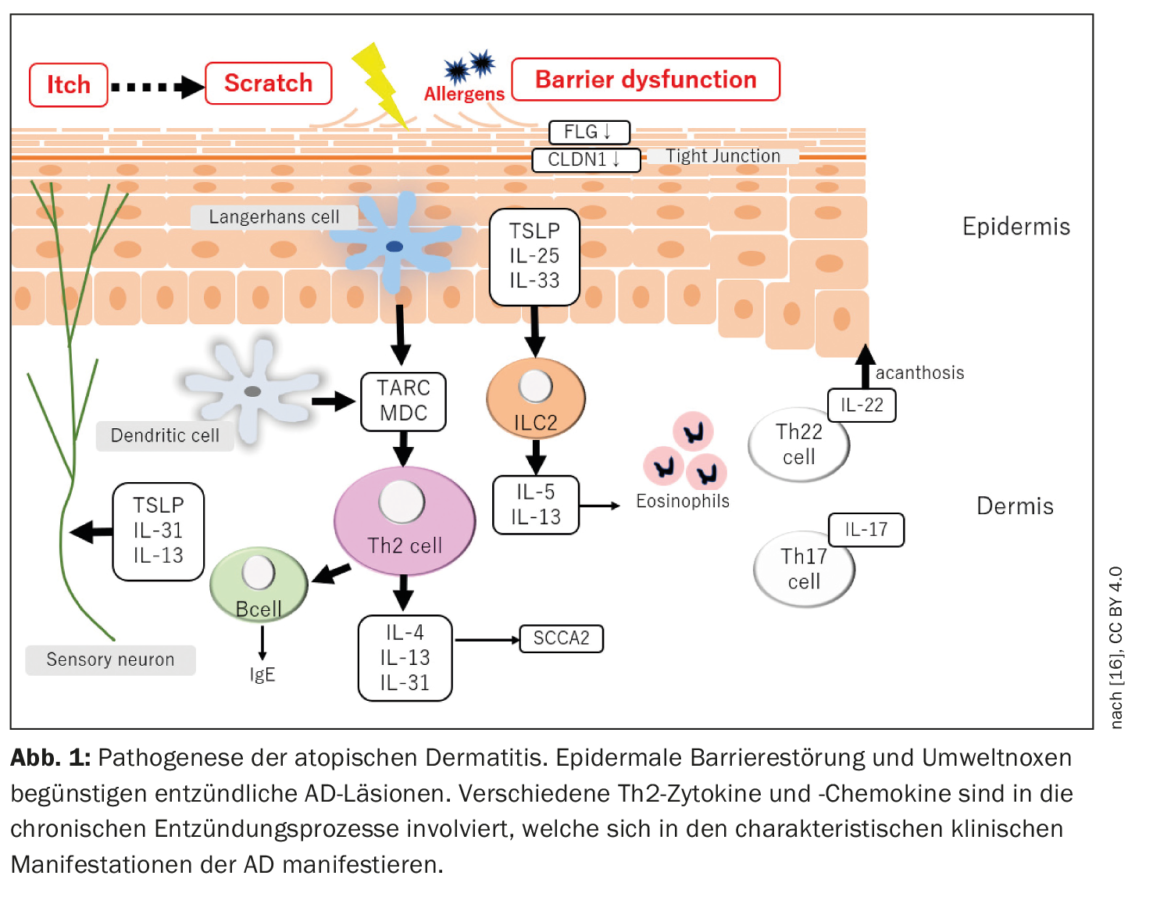
A dermatite atópica caracteriza-se por um curso recorrente crónico recidivante com início na primeira infância. As crises agudas são acompanhadas por lesões inflamatórias da pele e prurido intenso, pelo que a qualidade de vida dos doentes é consideravelmente afectada [3]. A fisiopatologia da DA é complexa (Fig. 1) : As interacções entre a função de barreira da pele comprometida e as respostas imunitárias modificadas contribuem para o desenvolvimento e manutenção da doença [2].
Sabe-se que uma predisposição genética é um pré-requisito para o desenvolvimento da DA. O factor de risco genético mais conhecido é uma mutação no gene FLG, que leva a uma expressão reduzida da filagrina na pele e a uma perturbação da barreira epidérmica associada [4]. Para além do FLG, foram identificados mais de 30 loci genéticos que estão associados à DA [5,6]. Além disso, as variantes no gene da IL-13 ou na região do receptor da IL-6, bem como várias variantes raras de codificação de proteínas, explicam quase 30% da susceptibilidade genética à DA [7]. A DA é considerada uma doença mediada por Th2, o que é apoiado por descobertas de níveis aumentados de mediadores Th2 e níveis diminuídos de IFN-γ no sangue de doentes com DA grave [1,8]. Vários estudos confirmaram que as lesões da DA são primariamente, mas não exclusivamente, mediadas por Th2 e associadas à produção excessiva de citocinas e quimiocinas Th2 importantes. No entanto, Th22 também parece estar envolvido, como reflectido por uma sobreprodução de IL-22, enquanto o envolvimento dos eixos Th1 e Th17 aparentemente varia dependendo do endofenótipo da DA [1].
A identificação de biomarcadores clinicamente relevantes continua a ser um desafio
Os projectos de investigação de biomarcadores clinicamente relevantes utilizam os mais recentes desenvolvimentos técnicos em medicina translacional com o objectivo a longo prazo de melhorar as opções de tratamento e a “gestão da doença”.
Um critério para os biomarcadores moleculares é o facto de serem detectados e medidos no sangue, noutros fluidos corporais ou em tecidos e poderem ser utilizados como indicadores de processos relevantes para a doença no organismo [9].
Actualmente, existem pelo menos 18 biomarcadores sanguíneos/séricos conhecidos associados à actividade da doença da DA, como os níveis de granulócitos eosinófilos, a desidrogenase láctica, a IgE total ou os níveis do receptor solúvel de IL-2 [10]. Além disso, várias quimiocinas# (CCL17, CCL18, CCL22, CCL26, CCL27) e interleucinas (IL-13, IL-22, IL-24, IL-25, IL-31, IL-33), bem como o “Thymic Stromal Lymphopoietint” (TSLP), a periostina e o antigénio-2 do carcinoma de células escamosas são considerados biomarcadores na DA [10]. O CCL18, o TSLP e o CCL26 foram associados à asma comórbida num estudo dinamarquês em crianças com DA [11]. Os investigadores estudaram quatro grupos de crianças dos 6 aos 12 anos de idade: (1) DA passada ou presente sem asma, (2) DA passada ou presente e asma actual, (3) asma actual sem DA. (4) controlos saudáveis. Foi realizado um ensaio clínico exploratório para investigar que biomarcadores estão associados à resposta ao tratamento da inibição do receptor-α da IL-4 pelo anticorpo monoclonal dupilumab na DA moderada a grave. Foi demonstrado que o dupilumab reduz a expressão aumentada de assinaturas Th2, tais como IL-13, IL-31, CCL17, CCL18, CCL22 e CCL26 no sangue e na pele lesionada da DA [12,13]. Balato et al. indicam que são necessários mais estudos para saber mais sobre possíveis associações destes biomarcadores com a doença e os resultados do tratamento na DA [2].
# As quimiocinas são um subgrupo das citocinas; são proteínas pequenas (8-10 kDa), quimiotacticamente activas (proteínas de sinalização).
Literatura:
- Facheris P, et al: A revolução translacional na dermatite atópica: a mudança de paradigma da patogénese para o tratamento. Cell Mol Immunol 2023,
https://doi.org/10.1038/s41423-023-00992-4,(último acesso em 24.02.2023). - Balato A, et al: O impacto da psoríase e da dermatite atópica na qualidade de vida: uma pesquisa bibliográfica sobre biomarcadores. Vida. 2022; 12(12): 2026.
- Arima K, et al: Carga da dermatite atópica em adultos japoneses: análise dos dados do Inquérito Nacional de Saúde e Bem-Estar de 2013. J Dermatol 2018; 45, 390-396.
- Irvine AD, et al: Mutações da filagrina associadas a doenças cutâneas e alérgicas. N Engl J Med 2011; 365: 1315-1327.
- Ellinghaus D, et al.: Estudo de genotipagem de alta densidade identifica quatro novos loci de susceptibilidade para dermatite atópica. Nat Genet 2013; 45: 808-812.
- Løset M, et al: Genética da dermatite atópica: da sequência de ADN à relevância clínica. Dermatologia 2019; 235: 355-364.
- Mucha S, et al.: As variantes de codificação de proteínas contribuem para o risco de dermatite atópica e para a expressão de genes específicos da pele. J Allergy Clin Immunol 2020, 145, 1208-1218.
- Gittler JK, et al: A activação progressiva de citocinas T(H)2/T(H)22 e de proteínas epidérmicas selectivas caracteriza a dermatite atópica aguda e crónica. J Allergy Clin Immunol 2012; 130: 1344-1354.
- Agência Europeia de Medicamentos (EMA). Qualificação de novas metodologias para o desenvolvimento de medicamentos. Regulamentação humana. Investigação e desenvolvimento. Pareceres e cartas de apoio sobre a qualificação de novas metodologias para o desenvolvimento de medicamentos. Disponível em linha: www.ema.europa.eu/en/glossary/biomarker,(último acesso em 24.03.2023).
- Nakahara T, et al: Exploração de biomarcadores para prever a melhoria clínica da dermatite atópica em pacientes tratados com dupilumab: um protocolo de estudo. Medicina 2020; 99: e22043.
- Basu MN, et al: Biomarcadores na asma no contexto da dermatite atópica em crianças pequenas. Pediatr Allergy Immunol 2022; 33: e13823.
- Guttman-Yassky E, et al: Dupilumab melhora progressivamente as anomalias sistémicas e cutâneas em pacientes com dermatite atópica. J Allergy Clin Immunol 2019; 143: 155-172.
- Hamilton JD, et al: Dupilumab melhora a assinatura molecular na pele de pacientes com dermatite atópica moderada a grave. J Allergy Clin Immunol 2014; 134: 1293-1300.
- Precision Medicine in Chronic Inflammation, www.precisionmedicine.de/fileadmin/user_upload/cluster/pmi/downloads/PMI-Magazin2021_digital_Doppelseiten.pdf,(último acesso em 24.03.2023)
- BMFB: CHAMP – Allergy and Tolerance in Childhood: Biomarkers and Predictors, www.gesundheitsforschung-bmbf.de/de/champ-allergie-und-toleranz-im-kindesalter-biomarker-und-pradiktoren-7268.php,(último acesso em 24.03.2023)
- Itamura M, Sawada Y: Envolvimento da Dermatite Atópica no Desenvolvimento de Doenças Inflamatórias Sistémicas. Revista Internacional de Ciências Moleculares. 2022; 23(21): 13445, www.mdpi.com/1422-0067/23/21/13445,(último acesso em 23.03.2023).
PRÁTICA DERMATOLÓGICA 2023; 33(2): 28-29