O tratamento da pitiríase rubra pilar pode ser um desafio. O arsenal terapêutico inclui corticosteróides tópicos, fototerapia ou terapias sistémicas clássicas como os retinóides ou os imunossupressores. Relatos de casos recentes e séries de casos de menor dimensão indicam que a utilização de produtos biológicos fora da indicação é uma opção de tratamento a considerar nos casos que não respondem à terapêutica convencional.
O tratamento da pitiríase rubra pilar (PRP) (caixa) é frequentemente difícil e moroso. Ainda não existe uma abordagem terapêutica universal para o PRP. Para além das preparações tópicas para aliviar os sintomas, a terapia sistémica é também utilizada para inibir a inflamação, sendo ambas as linhas de terapia frequentemente combinadas. No passado recente, foram publicados vários relatos de casos e pequenas séries de casos em que os produtos biológicos conduziram a um tratamento bem sucedido em doentes difíceis de tratar. Segue-se um resumo compacto de quatro casos da prática quotidiana.
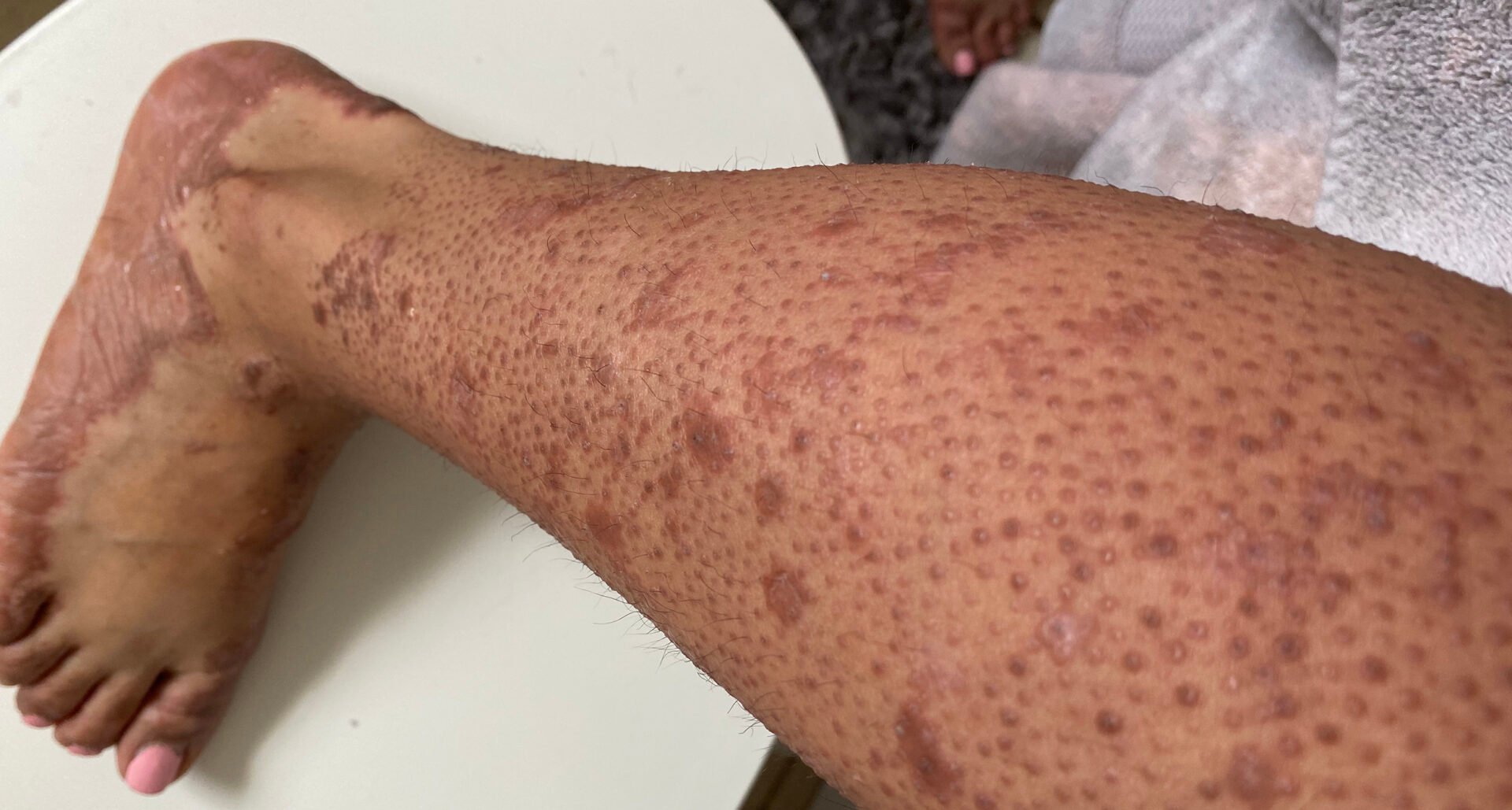
| A pitiríase rubra pilar (PRP) é uma dermatose inflamatória eritemato-escamosa de etiologia desconhecida, cujo diagnóstico se baseia nas características clínicas e histopatológicas clássicas. Sabe-se que pelo menos 6 subtipos ocorrem tanto em crianças como em adultos [3]. As características são pápulas foliculares e placas pequenas, escamosas e vermelho-alaranjadas. O PRP espalha-se normalmente a partir da face numa direção craniocaudal, deixando ilhas de pele clinicamente normais (nappes claires) no tronco e nas extremidades, incluindo as palmas das mãos e as plantas dos pés [4]. Até à data, não foi possível identificar marcadores serológicos ou imunohistoquímicos relevantes para o diagnóstico. O diagnóstico diferencial varia consoante o subtipo de PRP. Em geral, a PRP deve ser distinguida de outras doenças papuloescamosas, especialmente a psoríase. |
Ustekinumab para PRP em bebés e adultos
Na conferência DDG deste ano, foram apresentados dois relatos de casos em que a utilização de ustekinumab fora da indicação do medicamento se revelou eficaz [1]. O ustekinumab neutraliza as interleucinas IL-12 e IL-23, tendo assim um efeito imunossupressor e anti-inflamatório. No caso 1 , Almeida et al. de um bebé de seis meses de idade com lesões eritemato-escamosas que começaram na face e evoluíram para eritrodermia [1]. A histologia revelou dermatite psoriasiforme. Foi identificada uma mutação no gene CARD-14 (c.349 +2T>C), pelo que o quadro clínico foi classificado como erupção papuloescamosa associada ao CARD-14 (CAPE). O bebé não respondeu ao tratamento com metotrexato e acitretina. No entanto, foi obtida uma excelente resposta com a administração de ustekinumab adaptada ao peso.
No caso 2, os mesmos autores do estudo descreveram um adulto com PRP, que se manifestou por extensas lesões eritemato-escamosas e acentuação folicular [1]. Também neste caso, a histologia revelou uma dermatite psoriasiforme. O doente não respondeu nem ao metotrexato nem aos retinóides orais (isotretinoína), mas foi conseguida uma melhoria dos resultados com a utilização de ustekinumab.
Risankizumab em doentes com PRP de longa duração com mais de 55 anos
O caso 3 foi apresentado na conferência DDG do ano passado [2]. Este é um estudo de caso em que o tratamento com o inibidor da IL-23 risankizumab provou ser eficaz num doente a meio da idade adulta. A doente de 57 anos de idade, do sexo feminino, que sofria de pitiríase rubra pilar (PRP), tipo II segundo Griffith, há 38 anos, tinha sido tratada com glucocorticosteróides tópicos e tacrolimus durante vários anos no passado, mas tal não provocou qualquer melhoria clínica significativa. A terapia sistémica com retinóides foi pouco eficaz e causou efeitos secundários graves. O doente recusou outras terapias do sistema.
Após um esclarecimento pormenorizado, foi iniciada uma terapêutica off-label com o anticorpo Risankizumab IL-23 na dose aprovada para a psoríase em placas (150 mg s.c. nas semanas 0, 4 e depois de 12 em 12 semanas). Além disso, a terapia tópica existente com tacrolimus 0,1% foi continuada uma ou duas vezes por dia. Antes do início da terapêutica sistémica, surgiram em todo o tegumento placas grandes, confluentes, eritematosas, parcialmente liquenificadas, com descamação fina, lamelar e esbranquiçada. No meio, havia ilhas de pele saudável (nappes claires). A área facial apresentava eritema extenso com descamação e ectrópio em ambos os lados. As unhas das mãos e dos pés eram distróficas distalmente e apresentavam sulcos longitudinais. Negou prurido ou dor. Não tinha conhecimento de doenças concomitantes ou anteriores. Apenas quatro semanas após a primeira administração de risankizumab, verificou-se uma regressão clara dos achados cutâneos com uma redução das placas eritematosas e uma ausência quase completa de descamação, bem como um ectrópio menos pronunciado em ambos os olhos.
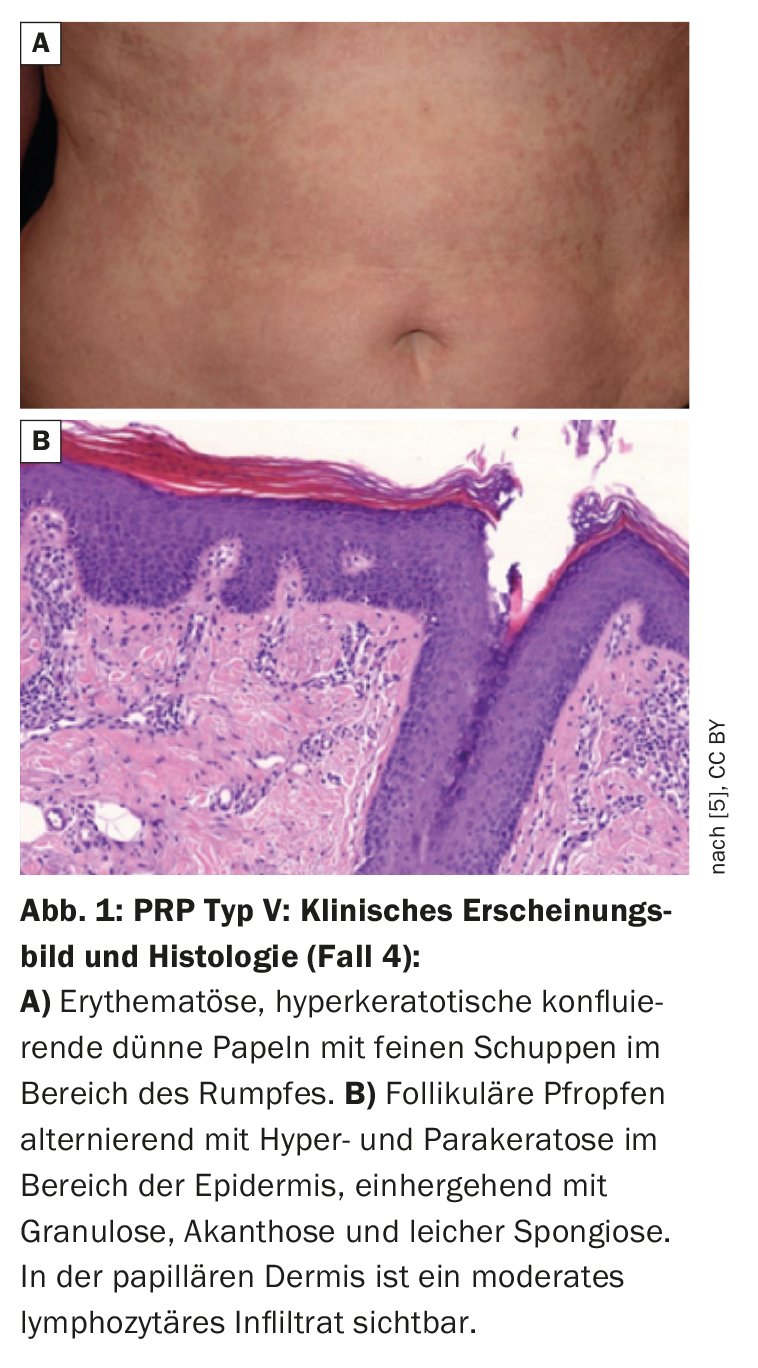
| Caso 4: Doente do sexo feminino, 61 anos, com PRP de tipo V e variantes CARD-14 A mulher apresentava eritrodermia generalizada com ligeiras infiltrações e escamas finas esbranquiçadas no tronco (Fig. 1). Os sintomas cutâneos apareceram pela primeira vez na infância e a doente foi submetida a tratamento dermatológico durante 28 anos. Foi encontrado um historial familiar – a sua filha e um neto tinham psoríase. As análises genéticas identificaram variantes do CARD-14 no doente com PRP. A sequenciação direta das regiões que codificam o CARD-14 levou à identificação de três variantes heterozigóticas missense: – c.1641G/C p.Arg547Ser (rs2066964) no exão 14 – c.2044C/T e p.Arg682Trp (rs117918077) no exão 17 – c.2458C/T p.Arg820Trp (rs11652075) no exão 20 As análises de previsão da patogenicidade utilizando uma ferramenta correspondente mostraram que a variante missense p.Arg682Trp é patogénica, enquanto as outras duas variantes são benignas. |
| de acordo com [5] |
Associação entre as variantes do gene CARD-14 e a PRP
Embora as características clínicas e histológicas da PRP e da psoríase sejam diferentes, existem, no entanto, sobreposições entre os dois quadros clínicos, por exemplo, na ativação do fator nuclear-kappa B (NF-κB) [3]. Em condições fisiológicas, esta cascata de sinalização é necessária para manter um equilíbrio imunológico na pele, mas quando (sobre)activada desempenha um papel central nas doenças inflamatórias da pele [3]. A proteína CARD-14, que está preferencialmente presente nos queratinócitos e nas células endoteliais dos vasos da pele, ativa o NF-κB [4]. As erupções papuloescamosas associadas ao CARD-14 (CAPE) estão associadas à psoríase, mas também ao tipo juvenil atípico de pitiríase rubra pilar (tipo V) [5–7]. Presume-se que certas mutações CARD-14 causam reacções inflamatórias que se desviam da norma, contribuindo assim para a etiopatogénese da PRP [5]. Entre outras coisas, foi demonstrado que a expressão excessiva de CARD-14 ativa a via IL-23/Th17 [6], o que pode explicar a resposta ao tratamento com ustekinumab e risankizumab descrita nos estudos de caso apresentados. A Figura 1 mostra os achados de PRP tipo V com variantes missense heterozigóticas nas regiões de codificação do CARD-14 (caixa) [5].
Literatura:
- De Almeida H, et al: Tratamento bem-sucedido com ustekinumab em dois casos de espetro de piriase rubra pilaris, P095. Conferência DDG 2023, volume de resumos, JDDG 2023; 21 Suppl 1: 1-177.
- Bätcher L, Homey B, Meller S: Controlo clínico da pitiríase rubra pilar por risankizumab, P002. Conferência DDG 2023, volume de resumos, JDDG 2022; Volume 20 (S1); 1-49.
- Brown F, Badri T. Pityriasis Rubra Pilaris. [Updated 2023 Jun 26]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing.
- Volc-Platzer B: Mutações CARD14 na pitiríase rubra pilar e a resposta terapêutica ao ustekinumab – uma hipótese. JDDG 2020, DOI: 10.1111/ddg.14218_g.
- Danis J, et al: Ativação do Fator Nuclear κB em um paciente com Pitiríase Rubra Pilaris Tipo V que abriga múltiplas variantes CARD14. Front Immunol 2018; 9: 1564. doi: 10.3389/fimmu.2018.01564, www.frontiersin.org/articles/10.3389/fimmu.2018.01564/full,(último acesso em 17 de outubro de 2023)
- Frare CP, et al: Erupção papuloescamosa associada ao CARD14 (CAPE) em pacientes pediátricos: Três casos adicionais e revisão da literatura. Pediatr Dermatol 2021; 38(5): 1237-1242.
- Fuchs-Telem D, et al: A pitiríase rubra pilaris familiar é causada por mutações no CARD14. Am J Hum Genet 2012; 91: 163-170.
PRÁTICA DE DERMATOLOGIA 2023; 33(5): 48-49
Imagem da capa: Kelly McGauran, wikimedia