Para além das doenças infecciosas, os problemas de pele são uma das razões mais frequentes para a consulta em consultórios de pediatria e de clínica geral, e os dermatologistas são também regularmente confrontados com doentes pediátricos. Que sinais de pele nos devem alertar? A mancha é realmente inofensiva ou faz parte de uma síndrome com problemas internos associados? Quantos diagnósticos são necessários? Este artigo destina-se a aguçar a visão de importantes manifestações cutâneas de doenças sistémicas na infância, com base em alguns sintomas clássicos e a apontar passos de diagnóstico sensatos.
“Mãos no balde-sinal
O adolescente na figura 1 mostrou pápulas transitórias, esbranquiçadas a translúcidas com rugas excessivas na zona da palma após breve contacto com água ou suor, acompanhadas de queimaduras desagradáveis e prurido.

Este fenómeno, resumido sob o termo “Rugas aquagenicas das palmas das mãos” (AWP), pode ser um sinal cutâneo específico de fibrose cística (FC) (prevalência 41-84%) ou de um estado heterozigoto portador do gene da FC [1]. Enquanto que o enrugamento palmar só ocorre após um tempo de contacto com a água de 11,5 minutos em indivíduos saudáveis, este fenómeno já pode ser observado após dois minutos em doentes com FC e após sete minutos em portadores heterozigóticos de FC [1]. AWP pode ser o primeiro sintoma de um fenótipo suave de FC em indivíduos de aparência de outro modo saudável [2]. Contudo, também pode ser observada de forma idiopática e transitória, especialmente em adolescentes.
Não se sabe quantas das pessoas afectadas por AWP têm na realidade uma mutação do gene CF.
“Racoon Eyes”

As lesões peri-oculares da pele, reminiscentes da visão de um “guaxinim” (guaxinim) com as suas marcações escuras características de espectáculo (Fig. 2) , fazem-nos pensar numa série de diagnósticos diferenciais sérios na infância e na infância:
- Neuroblastoma metástático (equimoses)
- Lúpus eritematoso neonatal (LNE)
- Base da fractura craniana, por exemplo, no abuso de crianças (equimose)
- Amiloidose (muito rara na infância).
A criança de três meses de idade, na figura 3, que nos foi encaminhada com a descrição de hemangioma de óculos, mostrou máculas periorbitárias, eritematosas, ligeiramente petequiais desde o nascimento, que eram principalmente compatíveis com o lúpus eritematoso neonatal (LNE) a partir dos diagnósticos diferenciais acima mencionados.

A detecção de anticorpos anti-Ro/SSA e anti-La/SSB na mãe e na criança confirmou rapidamente o diagnóstico suspeito. O envolvimento cardíaco, especialmente o bloqueio AV, que pode ocorrer em cerca de 10-20% das crianças com EMN, foi excluído por ecocardiografia e ECG. A maior parte no 6º-7º ano. As manifestações cutâneas típicas do NLE aparecem com a idade de duas semanas. As características são máculas e placas anulares, parcialmente policíclicas, eritematosas com predilecção pela cabeça e especialmente pela região periocular, semelhantes à imagem do lúpus eritematoso cutâneo subagudo (SCLE). A NLE mostra o curso típico de uma doença auto-imune de transmissão passiva. Com a decomposição dos auto-anticorpos maternos, a cura cutânea completa ocorre normalmente aos oito a doze meses de idade.
Em contraste com os sintomas cutâneos, o bloqueio AV completo fetal/congenital e a fibrose miocárdica como resultado da miocardite são, infelizmente, normalmente irreversíveis. Não é raro que isto exija um pacemaker permanente. O NLE é responsável por 80% de todos os blocos AV congénitos [3]. Uma vez que 20% dos irmãos subsequentes de uma doente com LES e 2% dos bebés de mulheres grávidas positivas anti-Ro/SSA (50% dos quais são assintomáticos!) estão em risco de LES, recomenda-se a monitorização ecocardiográfica fetal semanal entre 16 e 24 semanas de gestação [3]. Os recém-nascidos neste grupo de risco ou bebés com suspeita clínica de lúpus neonatal devem ser avaliados pela cardiologia pediátrica logo após o nascimento e acompanhados se forem encontradas anomalias. A relevância clínica da NLE reside assim na detecção precoce do seu envolvimento cardíaco.
Manchas vermelhas no rosto
As manchas vermelhas no rosto são comuns. Enquanto muitas lesões são inofensivas e regridem espontaneamente, é importante reconhecer e tratar prontamente as alterações persistentes e, portanto, esteticamente prejudiciais e aquelas com possíveis complicações funcionais.
Mais do que apenas um hemangioma?
Os hemangiomas infantis (IH) são os tumores benignos mais comuns na infância e ocorrem em até 5% das crianças. Caracterizam-se por um típico padrão de crescimento de rápida proliferação nos primeiros meses de vida, seguido de estabilização e lenta regressão a partir dos dois anos de idade. Assim, embora a maioria das IH não necessite de tratamento, deve ser dada atenção à possível deficiência funcional causada pelo crescimento expansivo, especialmente no caso de hemangiomas na região periorbital ou centrofacialmente, particularmente na face. Estes devem ser avaliados cedo, idealmente no início da fase de proliferação (com um a dois meses de idade) em centros especializados e tratados com bloqueadores beta sistémicos (propranolol). Além disso, é importante pensar nos problemas associados para além do hemangioma nas seguintes apresentações.
O hemangioma da barba: hemangiomas em forma de placa no queixo e no maxilar inferior (“região da barba”) e jugulum podem ser sinais de aviso de hemangiomas associados das vias aéreas superiores. Durante o acompanhamento de perto nos primeiros três meses de vida, deve ser dada especial atenção a sintomas como rouquidão, sintomas de garupa e estridor como sinais de um hemangioma subglótico. Em casos de suspeita clínica, a confirmação diagnóstica rápida por laringotraqueoscopia directa (a IRM não é a imagem de escolha!) e o início da terapia com propranolol e/ou terapia laser é de grande importância [5].
Síndrome de PHACES: Um hemangioma do tipo placa com mais de 5 cm de tamanho na cabeça ou pescoço pode ser indicativo de síndrome de PHACES (Tab. 1), que inclui uma vasta gama de malformações associadas, especialmente anomalias cardíacas, vasculares e cerebrais.

As raparigas são afectadas em 75% dos casos [7]. Em hemangiomas correspondentes (Fig. 4), pelo menos uma, mas geralmente várias manifestações extracutâneas de PHACES são encontradas em mais de 30% [7]. Para além de um exame oftalmológico e um esclarecimento cardiológico pediátrico, deve ser realizada uma angiografia de RM da cabeça e pescoço antes do início de um tratamento com beta-bloqueador normalmente necessário [7].
Mancha de vinho do porto com consequências: Enquanto os hemangiomas clássicos ainda não são visíveis ao nascimento ou são apenas visíveis como lesões precursoras discretas, as malformações capilares (CM = mancha de vinho do porto) já são visíveis como máculas eritematosas homogéneas no primeiro dia de vida. Com uma prevalência de 0,3%, são significativamente mais raros que o IH, crescem proporcionalmente com o corpo, persistem ao longo da vida e causam principalmente problemas estéticos [8]. Se a CM existir no rosto, aconselha-se precaução em algumas situações – para além da deficiência cosmética. Se as pálpebras (especialmente as superiores) forem afectadas, existe um risco significativo de glaucoma ipsilateral, que é uma emergência pediátrica. Um exame oftalmológico é portanto obrigatório nos primeiros dias de vida, tal como os controlos oftalmológicos regulares no decurso da vida. Se a região temporo-frontal (segmento V1) for incluída, deve ser considerada a possibilidade de síndrome de Sturge-Weber (tríade: CM fronto-temporal segmentar, glaucoma ipsilateral e angiomatose leptomeníngea) (Fig. 5), que não deve ser confundida com a síndrome de PHACES.

A síndrome de Sturge-Weber caracteriza-se clinicamente por epilepsia infantil difícil de tratar, possível paralisia e deficiência cognitiva. Além de uma rápida avaliação oftalmológica, recomenda-se a realização de uma ressonância magnética do crânio na infância.
A distinguir-se das manchas de vinho do porto no sentido mais estreito são as inofensivas “picadas de cegonha” que ocorrem em 50% dos recém-nascidos, as quais representam malformações funcionais, geralmente regressivas espontâneas, capilares. Estão sempre simetricamente distribuídos, na maioria das vezes na linha média do rosto e pescoço. O envolvimento frequente das pálpebras não está associado a um risco de glaucoma.
Erupção das fraldas – trivial?

A criança da Figura 6 tinha sofrido durante várias semanas de um exantema papuloso muito irritante, parcialmente petequial, na zona das fraldas e pequenas fissuras nas flexões, que continuaram a espalhar-se apesar das terapias anteriores. O diagnóstico diferencial de dermatoses de guardanapo é amplo (Tab. 2).

Se houver pápulas vermelhas-acastanhadas persistentes presentes e não houver resposta à terapia anti-inflamatória tópica, deve ser realizada uma avaliação adicional por biopsia. Na nossa criança, o diagnóstico de histiocitose de células de Langerhans (LCH) poderia ser confirmado histologicamente. Este é um importante diagnóstico diferencial na dermatite persistente dos guardanapos e eczema seborreico dos intertriginios em bebés e crianças pequenas. Uma pista clínica é o aspecto hemorrágico frequentemente observado das eflorescências e das hemorragias pontuais após o derrame.
A LCH é uma condição oncológica (incidência 0,4:100 000 crianças menores de 15 anos com um pico de idade nos primeiros 3 anos) com acumulação clonal e proliferação de células de Langerhans em vários órgãos (esqueleto 80% [Osteolysen], pele 25%, fígado, baço, medula óssea e gânglios linfáticos) [9]. Em casos de suspeita puramente radiológica de LCH (por exemplo, osteólises), vale a pena um exame dermatológico meticuloso, uma vez que mesmo um mínimo de descobertas cutâneas pode ser a chave para a confirmação histológica. Isto significa que uma biópsia arriscada dos órgãos internos ou do esqueleto pode ser dispensada. A classificação em LCH monossintomática (SS-LCH) com excelente prognóstico e LCH multissistémica (MS-LCH) com prognóstico muito variável é feita de acordo com um programa de exame normalizado. A terapia é realizada no âmbito do “LCH-IV international collaborative treatment protocol for Langerhans cell histiocytosis” (www.histiocytesocie ty.org) [9].
Pápulas comichosas
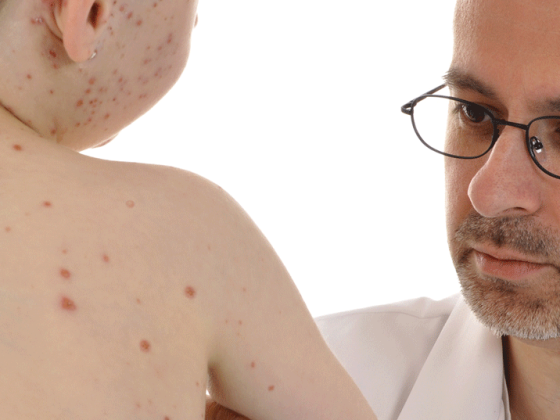
A menina de doze anos de idade da figura 7 tinha sofrido de pápulas comichão severa e extensoras no sentido de prurigo simplex subacuta durante seis semanas.

Não houve indicações anamnésticas para eczema atópico. Para além de uma linfadenopatia cervical e axilar, notou-se um LDH elevado com parâmetros laboratoriais que de outra forma não seriam notados. Histologicamente, a suspeita clínica e radiológica da doença de Hodgkin poderia ser confirmada. Prurigo simplex subacuta, que é regularmente visto em adultos (principalmente mulheres) sem uma causa interna identificável, é uma raridade nas crianças. normalmente só é de esperar em associação com dermatite atópica. Na situação aqui descrita, é indicada uma clarificação interna relativamente a uma doença hepática, nefrológica ou hemato-oncológica subjacente. A doença de Hodgkin é o representante clássico, é responsável por 5% das malignidades na infância e adolescência e muitas vezes (20-30%) apresenta sintomas cutâneos [11]:
- Prurigo simplex subacuta/eczema
- Erythema nodosum
- Infiltração cutânea específica da doença de Hodgkin: micose fungóide, CD30+ linfomas de células T.
Prurigo simplex acuta (estrophulus infantum) deve ser distinguido do prurigo simplex subacuta como uma reacção aguda a picadas repetidas de insectos na infância. A predominância de seropapulares é típica aqui.
Manchas brancas e castanhas no bebé e criança de tenra idade
Xantogranulomas e neurofibromatose juvenil: Múltiplos pontos de café-au-lait (número ≥6, tamanho >0,5 cm prepubertal) são um primeiro sinal bem reconhecido de neurofibromatose tipo 1 (NF1) na infância e primeira infância. Contudo, apenas 54% das crianças com NF1 satisfazem os critérios de diagnóstico clínico no primeiro ano de vida [12]. As crianças que possam ser afectadas devem ser submetidas a cuidadosos controlos de desenvolvimento pediátrico e a um exame oftalmológico inicial por volta dos doze meses de idade. A imagem cerebral é indicada em casos de perturbações visuais (glioma óptico) ou outras anomalias neurológicas. Uma análise genética não é necessária para o diagnóstico, mas pode ser útil em casos pouco claros. Se forem encontradas simultaneamente múltiplas manchas de café-au-lait e um ou mais xanthogranulomas juvenis (JXG) (Fig. 8), isto representa uma constelação de risco para a ocorrência de leucemia mielomonocítica juvenil (JMML). A JMML, que ocorre tipicamente na infância e infância, é significativamente mais comum em doentes com NF1 do que em crianças saudáveis. Se a JXG estiver presente ao mesmo tempo, o risco aumenta por um factor de 20-30 [13]. Com a ajuda de um acompanhamento atento e diagnóstico precoce, o prognóstico da JMML pode ser melhorado.
“Pontos brancos”: Ao avaliar as manchas brancas, é essencial distinguir as lesões hipopigmentadas das despigmentadas e as congénitas das manchas adquiridas. As máculas hipopigmentadas únicas e bem definidas, no sentido de um nevus depigmentosus, não são incomuns em bebés com 0,8% e em crianças mais velhas com até 5%, mas apenas 0,5% de todas as pessoas têm mais de dois desses spots [14]. Se forem encontradas mais de três destas folhas de cinza ou hipopigmentações semelhantes a confetis (Fig. 9), este é um possível primeiro sinal cutâneo de esclerose tuberosa (TS).

Nesta situação na primeira infância, os cuidadosos controlos de desenvolvimento pediátrico são primariamente importantes. Se ocorrerem anomalias neurológicas, é indicada uma avaliação neuropediatrica imediata. Até dois terços das crianças com TS têm mutações espontâneas, pelo que um historial familiar negativo não contesta este diagnóstico.
“Sinal de colarinho de cabelo”
Aplasia cutis congenita é uma aplasia congénita da pele e, no máximo, de estruturas mais profundas. As causas são múltiplas [15]. Se a aplasia cutânea estiver presente perto da linha média do crânio, pode ser uma expressão de disgrafia craniana oculta. Muitas vezes, em torno do cabelo aparece uma hipertricose muito característica de cabelos mais escuros e compridos, semelhante aos isobares no mapa meteorológico (Fig. 10), chamada “sinal de colarinho de cabelo”. Nesta situação, a imagem por sonografia ou melhor ressonância magnética do crânio é indicada, especialmente antes da intervenção cirúrgica [16].

Púrpura na infância
A partir do bem-estar completo, a criança da figura 11 desenvolveu placas purpúreas urticaria, parcialmente targetoid, nas extremidades bem como no rosto, compatíveis com edema hemorrágico agudo da infância (AHEI), também conhecido como a púrpura de Seidlmayer’s cocard purpura. A AHEI geralmente ocorre subitamente após infecções virais anteriores – tipicamente entre quatro meses e dois anos de idade – e cicatriza dentro de uma a três semanas sem consequências duradouras. Notável é a aparente contradição de manifestações de pele flagrantes, estado geral da criança sem alterações e, como regra geral, ausência de outras manifestações orgânicas. Se a apresentação for típica, o diagnóstico pode ser feito de forma puramente clínica e uma biópsia pode ser omitida.
A AHEI representa um subgrupo de Purpura Schönlein Hennoch (PSH) (Fig. 12)? Esta questão continua a ser controversa.

Em contraste com a AHEI, o curso da PSH caracteriza-se principalmente pelo possível envolvimento de órgãos (especialmente rins, intestinos e articulações). Na PSH, existe frequentemente dor abdominal com cólicas, pelo que uma possível intussuscepção ou hemorragia intestinal deve ser considerada e excluída por via sonográfica. Mesmo sem sinais iniciais de nefrite PSH, o acompanhamento clínico (medição da tensão arterial e estado da urina) é indicado durante pelo menos três a seis meses (uma ou duas vezes por semana no primeiro mês, depois uma vez por mês) [17]. Em casos de estado geral reduzido, febre alta, sinais acentuadamente aumentados de inflamação e parâmetros de coagulação anormais, o diagnóstico de PSH ou AHEI deve ser sempre questionado e o diagnóstico diferencial de púrpura fulminante (no contexto da sepse meningocócica) deve ser excluído.
Conclusão
Em resumo, esperamos ter dado aos leitores deste artigo algumas informações interessantes e práticas para a avaliação de crianças com manifestações dermatológicas. É claro que um artigo deste tipo só pode cobrir uma pequena selecção dos muitos sinais e sintomas excitantes da pele.
Literatura:
- Pride HB, et al: Journal of the American Academy of Dermatology 2013; 68(6): 885 e881-812; quiz 897-888.
- Weibel L, Spinas R: The New England journal of medicine 2012; 366(21): e32.
- Buyon JP, et al: Nature clinical practice Rheumatology 2009; 5(3): 139-148.
- Brown SJ, et al: Neonatal Lupus Erythematosus. In: Harper J, Oranje A, Prose N (eds.): Textbook of Pediatric Dermatology, 3rd edition, Vol. 1. Oxford: Blackwell Publishing 2011; p. 14.1-14.12.
- Weibel L: VASA Zeitschrift fur Gefässkrankheiten 2011; 40(6): 439-447.
- Theiler M, et al: J Dtsch Dermatol Ges 2013; 11(5): 397-405.
- Metry D, et al: Pediatrics 2009; 124(5): 1447-1456.
- Boon LM: Malformações vasculares. In: Harper J, Oranje A, Prose N (eds.): Textbook of Pediatric Dermatology, 3ª edição. Oxford: Blackwell Publishing 2011; 12.11-12.24.
- Minkoff M: Monatschr Kinderheilkd 2012; 160: 958-966.
- Lewis-Jones S: Erupção de fraldas. In: Lewis-Jones S (ed.): Paediatric Dermatology, Oxford: Oxford University Press 2010; 192-199.
- Rubenstein M, Duvic M: Revista internacional de dermatologia 2006; 45(3): 251-256.
- Boyd KP, et al: J Am Acad Dermatol 2009; 61: 1-14.
- Raygada M, et al:Pediatr. Blood Cancer 2010; 54: 173-175.
- Vanderhooft SL, et al: J Pediatr 1996; 129(3): 355-361.
- Frieden F: J Am Acad Dermatol 1986; 14(4): 646-660.
- Stevens CA: Am J Med Genet A 2008; 146A(4): 484-487.
- Scheer HS, Weibel L: JAMA 2013; 309(20): 2159-2160.
- Hospach T, Klaus G: Purpura Schönlein-Henoch. Guia do GKJ e DGKJ, Jan.2013, AWMF Online, www.awmf.org/uploads/tx_szleitlinien/027-064l_S1_Purpura_Schönlein_Henoch_2013-01.pdf
PRÁTICA DA DERMATOLOGIA 2013; 23(5): 4-8