“É mais importante saber que pessoa tem uma doença do que saber que doença uma pessoa tem” – esta frase é atribuída a Hipócrates, o que significa que o grego antigo já sabia da utilidade de uma terapia personalizada há cerca de 2400 anos. A medida em que tal abordagem pode também ajudar na reumatologia a identificar os doentes em risco de AR numa fase precoce e a tratá-los de forma orientada é o tema dos estudos actuais.
O conceito de medicina de “tamanho único”, ou seja, o curso padronizado da terapia independentemente das peculiaridades do respectivo paciente, naturalmente também traz sempre consigo uma proporção relativamente elevada de efeitos secundários (graves) e não-respondedores. Os efeitos da medicina personalizada, baseada no diagnóstico molecular (análise de biomarcadores) e estratificação dos doentes com base em biomarcadores, destinam-se a reduzi-los e a aumentar a taxa de respondedores.
A lista de medicamentos para os quais é obrigatório um teste genético na Alemanha estende-se por 29 páginas no website da Associação Alemã de Empresas Farmacêuticas Baseadas na Investigação (vfa). As doenças reumáticas ainda não fazem parte desta lista. Para o Prof. Dr. Andrea Rubbert-Roth da Clínica de Reumatologia do Hospital Cantonal de St. Gallen, esta é uma prova clara de que o tema da medicina personalizada ainda não foi capaz de se estabelecer no campo da reumatologia.
Sabe-se que, para além de factores ambientais como o fumo, pó e fibras têxteis, existe também uma susceptibilidade genética à artrite reumatóide (AR). Já em 2007, uma grande análise de dados com 14.000 doentes e 3.000 sujeitos de controlo em 7 doenças mostrou que no caso da AR com HLA e PTPN22, destacam-se dois genes. O Prof. Rubbert-Roth recordou a hipótese chamada Epitope Partilhado (SE), segundo a qual os alelos HLA-DRB1 associados à AR codificam uma sequência comum de aminoácidos na 3ª região hipervariável da cadeia DRβ1.
Os pacientes SE-positivos beneficiam mais
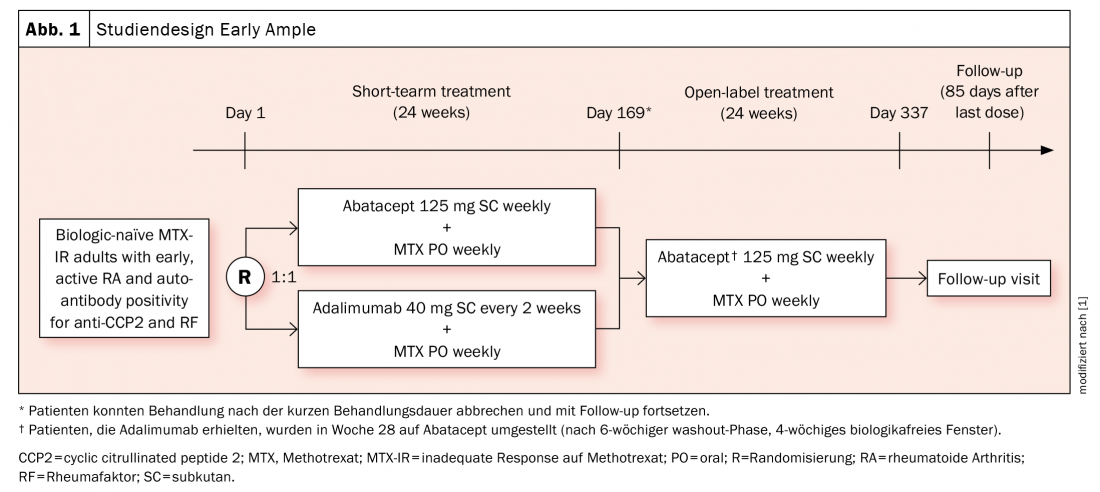
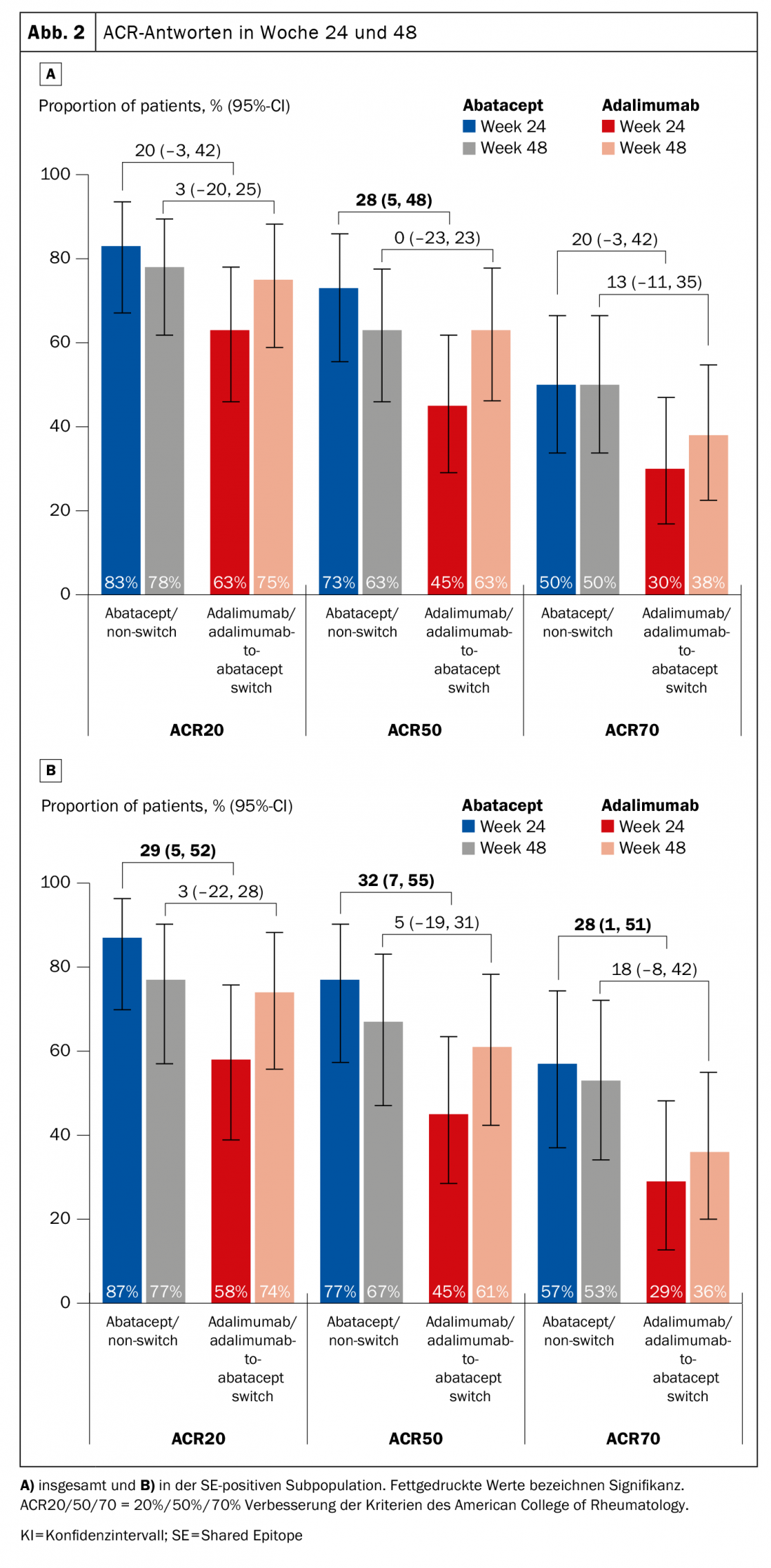
Avaliações anteriores deram indicações de que os pacientes HLA-DRB1-positivos respondem melhor à Abatacept (o que não significa que isto também não se possa aplicar a outros agentes, como salientou o perito). O estudo da fase 4 Early Ample [1], publicado em 2021, baseia-se nisto e divide os doentes com AR precoce biológica ingénua que não responderam adequadamente ao metotrexato (MTX) num braço abataceptor (n=39, dos quais 30 eram SE-positivos) e num braço adalimumab (n=40, dos quais 31 eram SE-positivos) (Fig. 1) . Os afectados tinham de ser CCP2 e o factor reumatóide positivo. Os assuntos foram aleatorizados para ABA ou ADA durante 24 semanas e depois todos mudaram para ABA. Foi demonstrado que os pacientes HLA-DRB1-positivos já tinham maiores probabilidades de conseguir um ACR20, -50 e -70 com abatacept após 24 e 48 semanas (Fig. 2A). O resultado foi ainda mais forte a favor da subpopulação SE+ (Fig. 2B).
Pode a AR ser evitada em doentes em risco?
Sabe-se que os doentes que ainda não têm sinovite clinicamente reconhecível, mas que já têm anticorpos CCP detectáveis, correm um risco acrescido de desenvolver AR. Se e como é possível impedir o desenvolvimento da AR neste grupo numa fase inicial é o tema do estudo ARIAA, apresentado no Congresso do ACR 2021 [2]. Os critérios de inclusão para este estudo de fase 2 foram a positividade ACPA (+/- RF), artralgias durante pelo menos 6 semanas, sinais de inflamação da mão dominante (sinovite, tenossinovite ou osteite) na RM mas sem inchaço clínico, e nenhuma terapia prévia com esteróides ou DMARD. 49 pacientes identificados desta forma foram tratados com abatacept durante um período de 6 meses contra placebo (n=49). Seguiu-se um período de acompanhamento de 12 meses sem tratamento.
O ponto final primário, melhoria em pelo menos um parâmetro de RM (pontuação RAMRIS), foi atingido: houve uma melhoria significativa em 61,2% dos pacientes no braço do abatacept (vs. 30,6% no placebo; p=0,0043). O grupo verum também teve um desempenho significativamente melhor nos pontos finais secundários de descontinuação prematura do estudo e progressão para AR clínica (descontinuação 14,3% vs. 42,9%; p=0,0032; progressão 8,2% vs. 34,7%; p=0,0025). O benefício para a Abatacept em relação ao placebo é, portanto, claramente visível e o Prof. Rubbert-Roth espera ter os outros resultados do seguimento a longo prazo apresentados na próxima EULAR. “Se os resultados fossem confirmados durante o período de seguimento, seria realmente espectacular”, conclui ela.
Mensagens Take-Home
- A implementação de novos conceitos de estudo, incluindo uma estratégia personalizada, pode também contribuir para optimizar a eficiência e segurança da terapia DMARD em reumatologia.
- Prova de princípio: Idealmente, os biomarcadores seriam facilmente acessíveis e fáceis de determinar no futuro.
- Este conceito também pode ser implementado para outras doenças reumatológicas? (por exemplo, assinatura de interferão em SLE)
Literatura:
- Rigby W, Buckner JH, Louis Bridges S, et al: os alelos de risco HLA-DRB1 para AR estão associados à resposta clínica diferencial a abatacept e adalimumab: dados de um estudo cabeça a cabeça, aleatório, mono-cego em AR autoanticorpo-positivo precoce. Arthritis Res Ther 2021; 23: 245; doi: 10.1186/s13075-021-02607-7.
- Rech J, et al: ACR 2021 [#0455].
InFo DOR & GERIATURA 2022; 4(1-2): 20-21