O estreitamento da válvula aórtica é o defeito mais comum da válvula adquirida e é corrigido por AKE ou TAVI. No entanto, apesar dos avanços na terapia, os problemas de ritmo ocorrem frequentemente. O que fazer?
Na Suíça, milhares de pacientes são submetidos anualmente à substituição cirúrgica da válvula aórtica (ACE) ou ao implante de válvula aórtica transcateter (TAVI). Na maioria dos casos, a indicação principal é a estenose da válvula aórtica calcária, que afecta 3-5% da população com mais de 75 anos de idade [1].
As taquiarritmias, particularmente a fibrilação atrial (FA) e as perturbações de condução atrioventricular (AV), especialmente o bloqueio de ramo esquerdo (LSB) e o bloqueio AV de grau superior, estão entre os problemas de ritmo mais comuns antes, durante e depois da cirurgia LCE ou TAVI. Estas arritmias aumentam tanto a morbilidade como a mortalidade, levam a estadias hospitalares prolongadas e aumentam os custos.
O impacto clínico destas arritmias em pacientes com vício da válvula aórtica é variado e o espectro de sintomas varia desde a completa ausência de sintomas e desconforto, a palpitações ocasionais, fadiga, tonturas, dispneia ou dores no peito, a insuficiência cardíaca grave clinicamente manifestada, síncope, choque cardiogénico e morte.
Fibrilação atrial – Procure e encontrará!
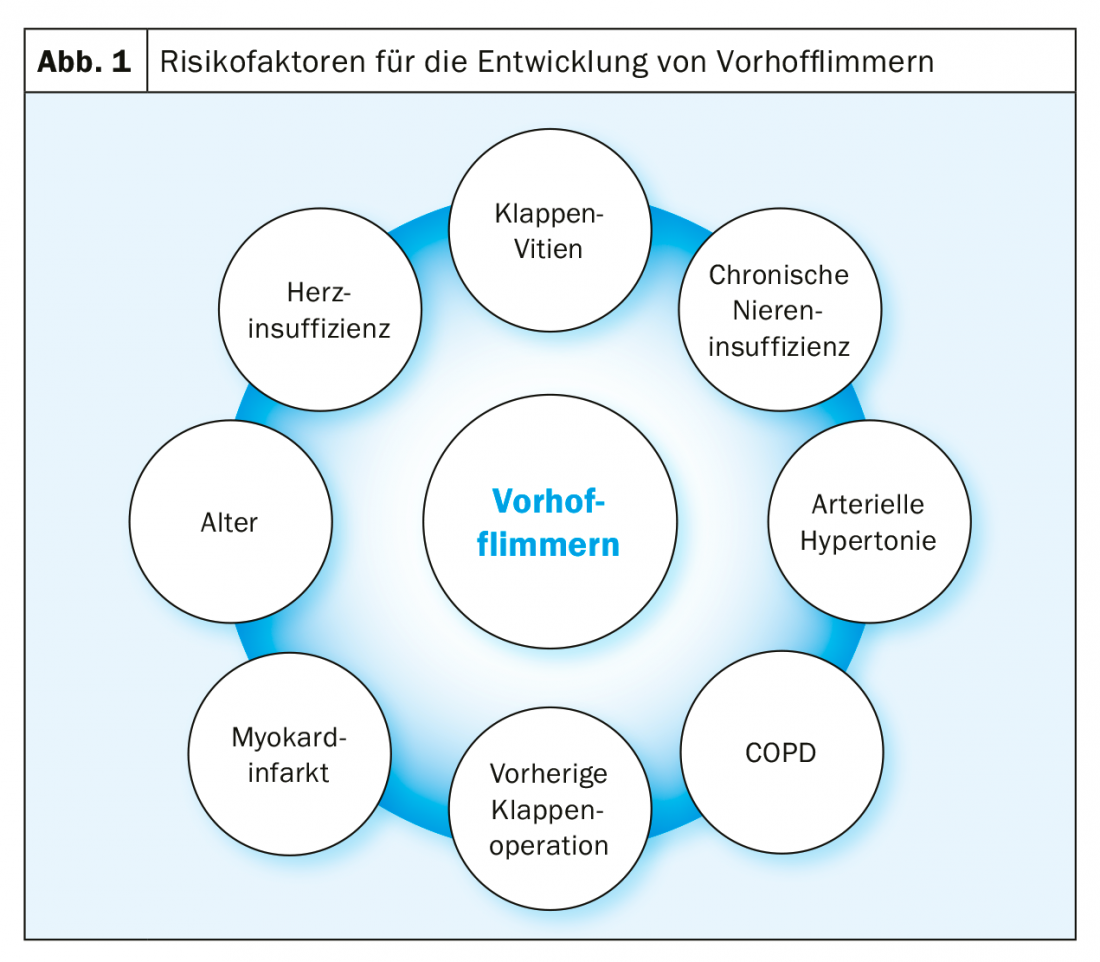
A fibrilação atrial é a arritmia cardíaca mais comum, com um aumento acentuado da prevalência com a idade: em pessoas com mais de 80 anos, a prevalência já é superior a 10% [1]. A prevalência é também aumentada em insuficiência renal, DPOC, insuficiência cardíaca, e em doentes após cirurgia valvar (Fig. 1) [2]. Em doentes com estenose valvar aórtica grave, esta prevalência aumenta de novo significativamente e, de acordo com a literatura, é de 8-13% antes da cirurgia AKE e 16-51% antes da TAVI [3].
Esta prevalência muito elevada de FVC na estenose grave da válvula aórtica deve-se, por um lado, à co-incidência de factores de risco para ambas as doenças: em geral, os doentes com estenose grave da válvula aórtica são, na sua maioria, muito idosos. Por outro lado, o próprio vício também conduz a alterações hemodinâmicas, que resultam numa carga de pressão no átrio esquerdo e em fibrose atrial esquerda consecutiva com alterações eléctricas dos átrios. Globalmente, esta transformação do substrato favorece a ocorrência de VHF (Fig. 2).
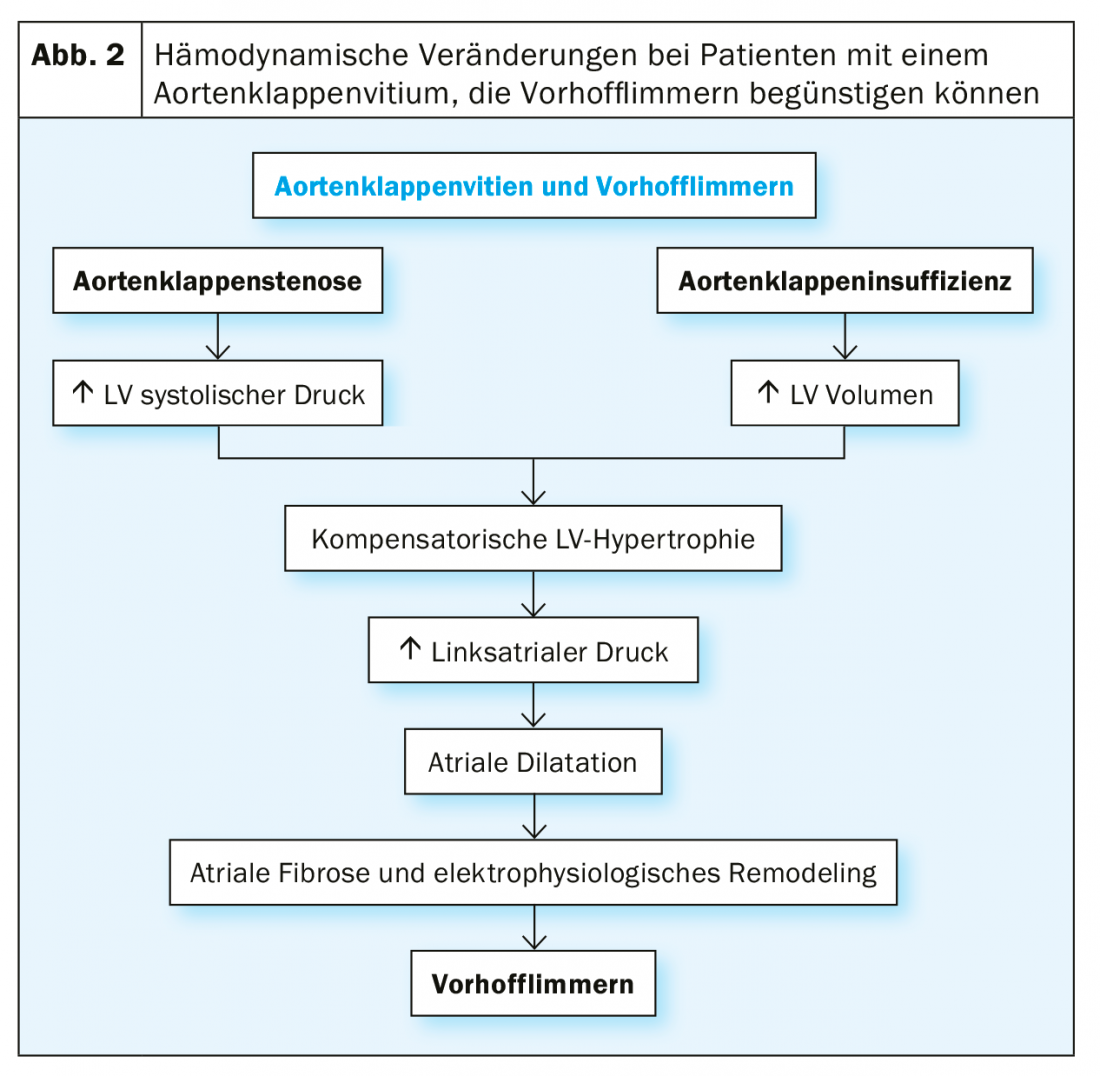
Especialmente em AKE cirúrgico, é gerado um estado hiperadrenérgico periintervencionista e uma resposta inflamatória cardíaca é induzida pelo trauma cirúrgico, que é considerado como parcialmente responsável pelo desenvolvimento de FCR periintervencionista.
Mesmo após a cirurgia AKE ou TAVI, VHF é a mais comum arritmia recém-diagnosticada. A incidência depende fortemente do método de rastreio utilizado: quanto maior for a monitorização do ritmo, mais frequentemente o FCR é encontrado.
Em geral, as taxas de incidência elevada de FCR são descritas após a cirurgia ACE e TAVI (31-64% e 4-32%, respectivamente) [4]. Um estudo recentemente publicado por Kalra et al, que analisou dados de 171.480 pacientes após LCE e TAVI cirúrgicos, encontrou uma taxa de incidência de FCR de aproximadamente 50% em ambos os grupos [2]. No importante ensaio NOTION, 52 pacientes foram continuamente monitorizados utilizando um gravador de eventos após a cirurgia AKE ou TAVI [4]. A incidência de VCVA foi de 100% após LCE cirúrgico e de 82% após TAVI. Após a cirurgia AKE, o novo diagnóstico de FA ocorreu nos primeiros 61 dias em todos os pacientes e após TAVI nos primeiros 41 dias. A carga de arritmia nas primeiras 2 semanas após a cirurgia AKE e TAVI foi significativamente mais longa (2,8%) nos pacientes após a cirurgia AKE em comparação com 0,04% após TAVI (p=0,01). No entanto, a carga de arritmia diminuiu significativamente após 3 meses em pacientes após a IFT cirúrgica [4].
É provável que muitos destes pacientes tivessem um FCR pré-existente mas assintomático. O sub-diagnóstico da FA assintomática é um problema geral e não afecta apenas pacientes com estenose grave da válvula aórtica.
Um novo diagnóstico de FCR após ACE ou TAVI cirúrgico leva a um prolongamento da hospitalização em comparação com pacientes sem FCR (9 vs. 6 dias para ambos os grupos; p<0,001) [2]. Nestes pacientes, também se pode observar um aumento significativo da mortalidade durante a hospitalização após a ECA e TAVI cirúrgica, em comparação com pacientes sem VCVA recém-diagnosticado. Além disso, a mortalidade de 1 ano de pacientes com FVC incisional após TAVI é significativamente aumentada em comparação com pacientes sem FVC recém-diagnosticado (31% vs. 14%; p<0,01) [5].
A anticoagulação oral para a profilaxia do tromboembolismo deve ser utilizada em todos os doentes com FCR e risco acrescido de tromboembolismo.
Perturbações da condução AV e requisitos do pacemaker
Os factores de risco mais importantes para as perturbações da condução AV são a idade, insuficiência cardíaca, doença coronária, hipertensão arterial e diabetes mellitus [6]. Não é, portanto, surpreendente que os distúrbios de condução AV sejam muito comuns nos doentes tipicamente bastante idosos com estenose grave da válvula aórtica: em 10-20% dos doentes que recebem uma AKE cirúrgica ou um TAVI, um pacemaker já foi implantado anteriormente [7]. Os factores de risco adicionais para perturbação da condução AV após TAVI são, em particular, o bloco de ramo direito completo e o bloco de 1º grau AV (Fig. 3).
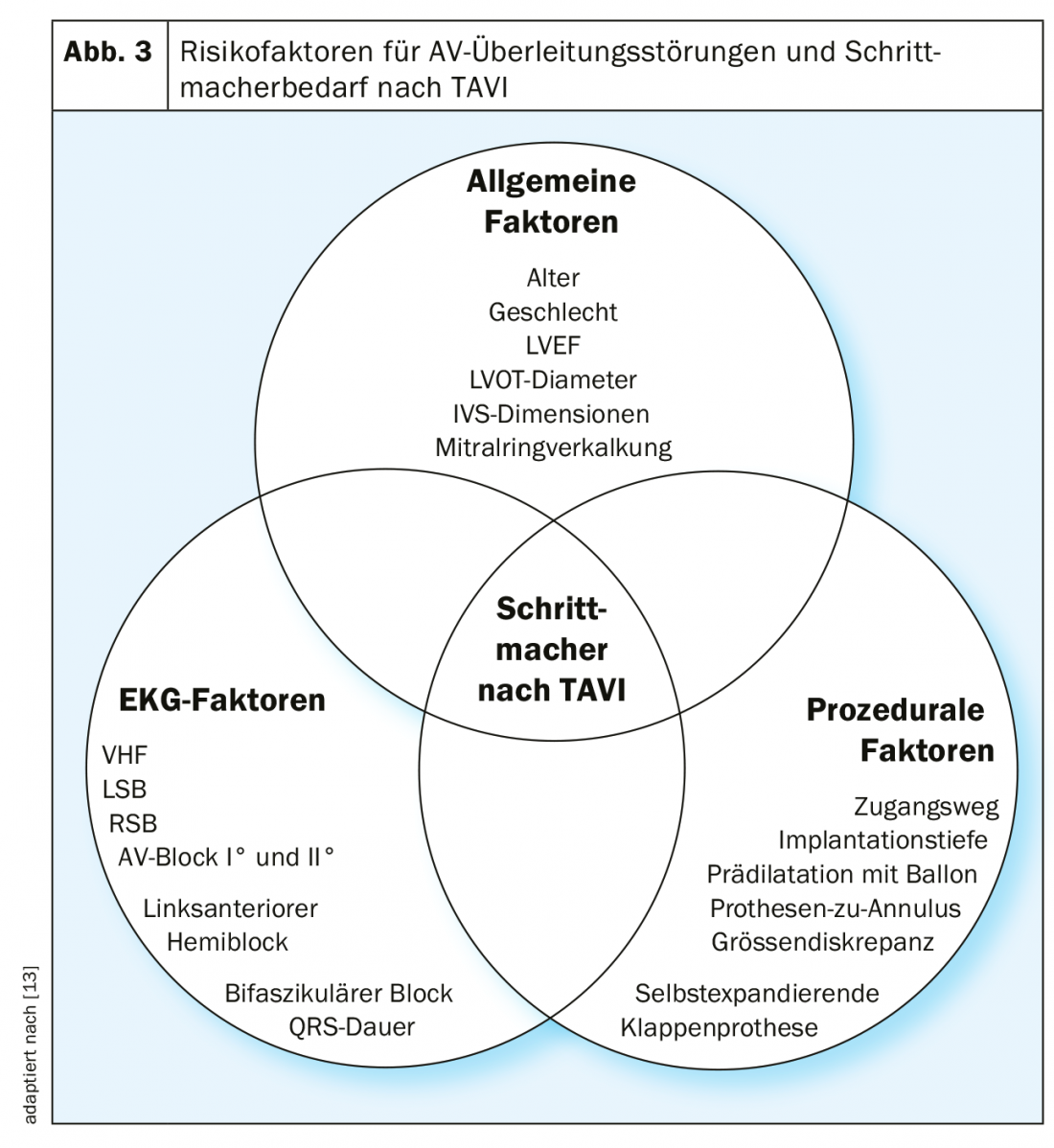
O desenvolvimento de perturbações da condução AV durante e após a cirurgia AKE ou TAVI também se deve à estreita relação anatómica da válvula aórtica com o sistema de condução. Assim, o fascículo esquerdo corre relativamente superficialmente directamente abaixo da válvula aórtica na via de saída do ventrículo esquerdo. A compressão mecânica desta região por uma válvula aórtica profundamente implantada durante TAVI, ou a lesão desta região durante AKE cirúrgica, resultará em bloco de ramo esquerdo ou mesmo bloco AV completo, este último especialmente na presença de bloco de ramo direito pré-existente.
Se estiver presente uma válvula aórtica bicúspide ou uma estenose da válvula aórtica gravemente calcificada, também se observa uma maior prevalência de anomalias de condução AV e requisitos de estimulação, devido à necessidade de desbridamento extensivo.
A incidência de defeitos de condução de AV após TAVI também depende do modelo de válvula implantada. Isto é geralmente mais elevado com próteses de válvula auto-expansíveis em comparação com modelos expansíveis por balão. O tamanho do anel da válvula aórtica em relação ao diâmetro da válvula protética também desempenha um papel, juntamente com a profundidade de implantação.
Os defeitos de condução atrioventricular ocorrem geralmente durante ou pouco depois da implantação da válvula, mas também podem ocorrer alguns dias após TAVI [8]. Este último torna a gestão destes pacientes difícil e leva a uma indicação muito mais liberal para o implante de marca-passo após TAVI, em comparação com a AKE cirúrgica. Em contraste, após a cirurgia AKE, no caso de um bloco AV completo, espera-se até uma semana e um pacemaker só é implantado se o bloco AV não recuperar.
A incidência de bloqueio de ramo esquerdo após cirurgia AKE é de 3-4% e a incidência de bloqueio AV completo persistente com necessidade de estimulação é de 3-12% [8,9]. Em contraste, a incidência de bloco de ramo esquerdo após TAVI é de 18-65% para válvulas protéticas auto-expansíveis e de 4-30% para válvulas protéticas balão-expansíveis [10]. Um pacemaker é reimplantado em 25-28% dos pacientes após TAVI com uma válvula protética auto-expansível e em 5-7% dos pacientes que receberam uma válvula protética balão-expansível [10].
É intuitivo assumir que o bloqueio completo do ramo esquerdo é prognosticalmente desfavorável devido à dissincronia ventricular associada, especialmente na presença de uma função ventricular esquerda concomitantemente afectada. Da mesma forma, o novo bloco iatrogénico do ramo esquerdo comporta um risco de progressão de perturbação da condução AV para completar o bloco AV.
Numa meta-análise, Regueiro et al. descrevem. em pacientes com novo bloco de ramo esquerdo após TAVI, uma taxa mais elevada de implante de marcapasso (RR 2,18; 95% CI, 1,28-3,70; p<0,01), mortalidade cardíaca mais elevada (RR 1,39, 95% CI, 1,04-1,86, p=0,03) e um efeito negativo na função da bomba ventricular esquerda no primeiro ano após TAVI, em comparação com os pacientes sem novo bloqueio de ramo esquerdo. [11]. No entanto, os dados são contraditórios a este respeito: outra meta-análise, por exemplo, não conseguiu demonstrar o aumento da mortalidade em doentes com novo bloco de ramo esquerdo após TAVI [12].
Fornecer aos pacientes certos um pacemaker na altura certa depois de TAVI continua a ser um desafio clínico difícil.
Literatura:
- Go AS, Hylek EM, Phillips KA, et al: Prevalência de Fibrilação Atrial Diagnosticada em Adultos. Jama 2001; 285: 2370.
- Kalra R, Patel N, Doshi R, et al: Avaliação da Incidência da Fibrilação Atrial New-Onset após a Substituição da Válvula Aórtica. JAMA Intern Med 2019; 35294: 1-9.
- Tarantini G, Mojoli M, Urena M, Vahanian A: Fibrilação atrial em pacientes submetidos a implante de válvula aórtica transcatérmica: epidemiologia, tempo, preditores, e resultado. Eur Heart J 2017; 38: 285-293.
- Jørgensen TH, Thyregod HGH, Tarp JB, et al: Mudanças temporais de fibrilação atrial de novo início em pacientes aleatorizados para substituição da válvula aórtica cirúrgica ou transcatéter. Int J Cardiol Elsevier B.V.; 2017; 234: 16-21.
- Stortecky S, Buellesfeld L, Wenaweser P, et al: Fibrilação atrial e estenose aórtica. Circ Cardiovasc Interv 2013; 6: 77-84.
- Kerola T, Eranti A, Aro AL, et al: Factores de risco associados ao bloqueio atrioventricular. JAMA Netw aberto em 2019; 2: e194176.
- Franzone A, Windecker S: O Enigma da Implantação Permanente de Pacemaker após a Implantação da Válvula Aórtica Transcatheter. Circ Cardiovasc Interv 2017; 10: 1-4.
- Roten L, Stortecky S, Scarcia F, et al: Condução atrioventricular após implante de válvula aórtica transcatérmica e substituição cirúrgica da válvula aórtica. J Cardiovasc Electrophysiol 2012; 23: 1115-1122.
- Khounlaboud M, Flécher E, Fournet M, et al: Preditores e prognóstico do impacto do novo bloco de ramo esquerdo após substituição cirúrgica da válvula aórtica. Arch Cardiovasc Dis Elsevier Masson SAS; 2017; 110: 667-675.
- Auffret V, Puri R, Urena M, et al: Perturbações de condução após substituição da válvula aórtica transcatérmica: Estado actual e perspectivas futuras. Circulação 2017; 136: 1049-1069.
- Regueiro A, Altisent OAJ, Trigo M Del, et al: Impacto do novo bloco de ramo esquerdo e implante de marcapasso periprocedural permanente em resultados clínicos em pacientes submetidos a substituição da válvula aórtica transcatéter. Circ Cardiovasc Interv 2016; 9: 1-10.
- Ando T, Takagi H: O Impacto Prognóstico do Novo Bloco de Ramo Esquerdo Persistente após Implantação de Válvula Aórtica Transcatêter: Uma Meta-análise. Clin Cardiol 2016; 39: 544-550.
- Siontis GCM, Jüni P, Pilgrim T, et al: Predictors of Permanent Pacemaker Implantation in Patients With Severe Aortic Stenosis Undergoing TAVR. J Am Coll Cardiol Elsevier Inc; 2014; 64: 129-140.
CARDIOVASC 2019; 18(5): 10-12