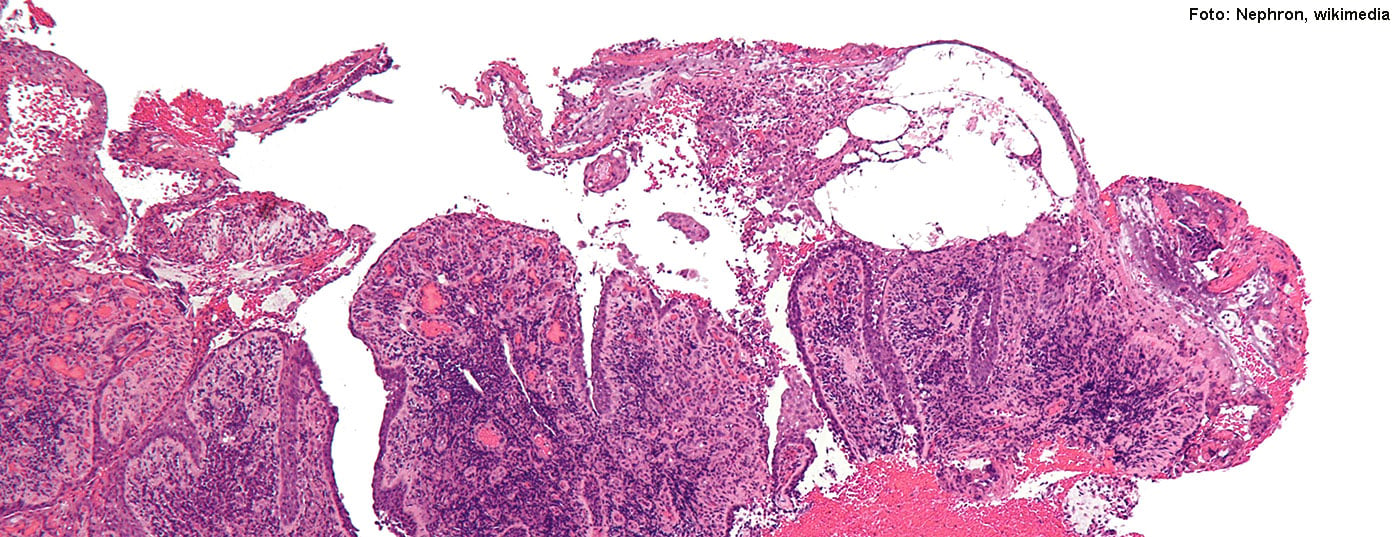
Nos últimos anos, foram feitos grandes progressos na investigação de terapias imunocelulares autólogas. O desenvolvimento de um receptor de antigénio quimérico (CAR) alvo específico contra o pemphigus vulgaris das células B autoreactivas patogénicas é um destes marcos.
As imunoterapias são uma técnica em que os linfócitos T são geneticamente modificados para que destruam selectivamente o material celular patogénico. O Dr. Christoph Ellebrecht, MD, Universidade da Pensilvânia (EUA) falou na reunião anual deste ano da Arbeitsgemeinschaft Dermatologische Forschung (ADF) [1] sobre as imunoterapias específicas de alvo CAR-T (“Chimeric antigen receptor T-cell therapy”) e CAAR-T (“Chimeric autoanticbody receptor T-cell therapy”) para a doença auto-imune pemphigus vulgaris (PV) rara, com bolhas e potencialmente fatal [2–4]. Vários estudos têm demonstrado que as células receptoras de antígenos quiméricos são eficazes como terapia específica de alvo (CAR-T) contra células B patogénicas em PV. O conceito da célula CAR-T tem sido investigado há várias décadas, principalmente no campo das terapias anticancerígenas, embora os desafios técnicos tenham atrasado a entrada no mercado (Fig. 1) . Em 2018, um produto CAR-T recebeu autorização de comercialização na Suíça na área da oncologia (tisagenlecleucel: para casos refractários de leucemia e linfoma de grandes células B) [5].
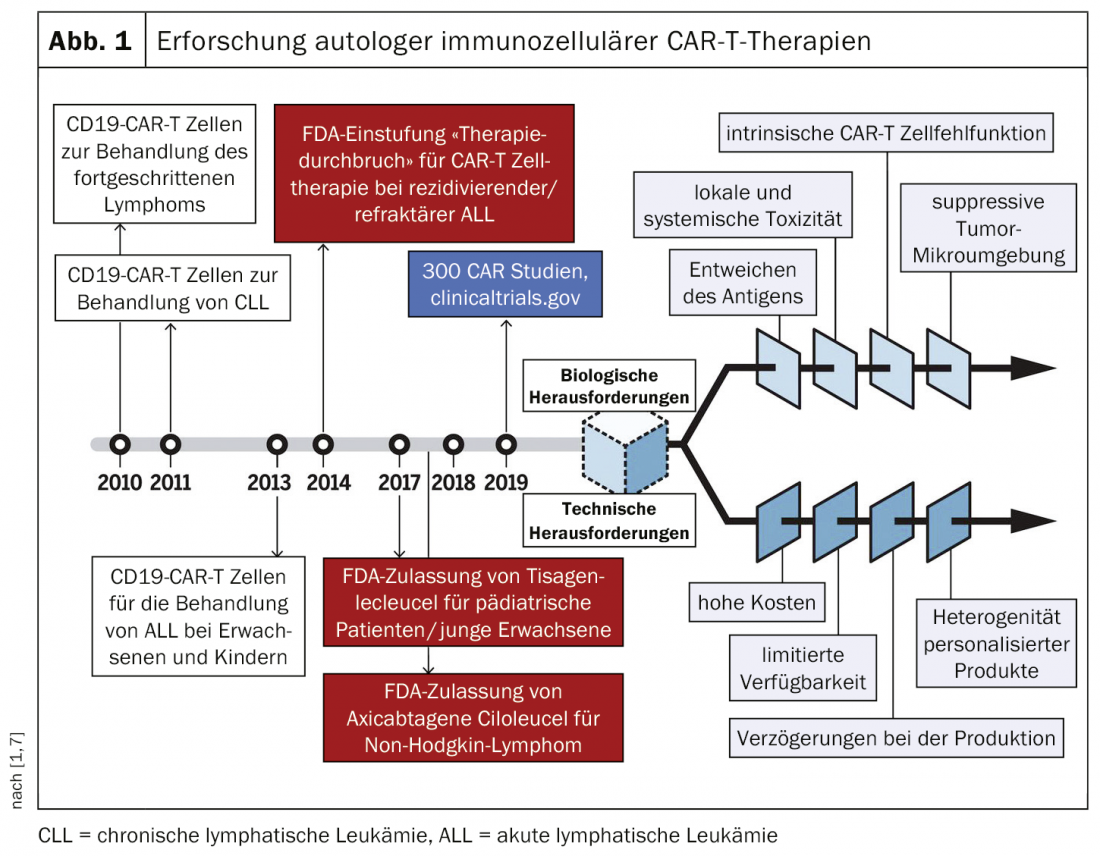
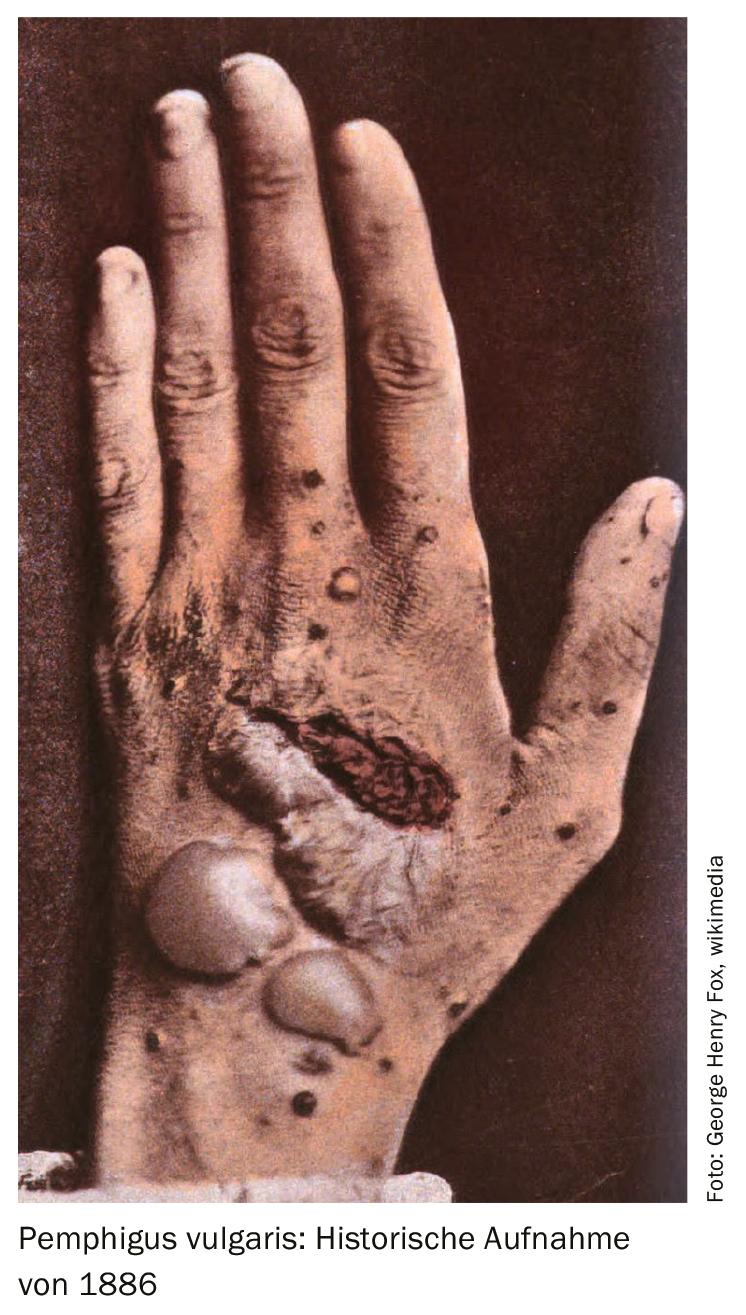
A terapia Anti-CD 20 só é geralmente eficaz a curto prazo
Se não for tratada, a PV é fatal após alguns anos devido à perda de líquidos e superinfecção através da barreira cutânea danificada. As opções de tratamento utilizadas até à data incluem corticosteróides sistémicos, azatioprina, micofenolato mofetil, ciclofosfamida, metotrexato. Em Março de 2019, o rituximab de anticorpos monoclonais recebeu autorização de comercialização na UE para formas moderadas a severas de PV; nos EUA, esta extensão de indicação já tinha sido concedida em 2018. O Rituximab é uma biologia que visa especificamente o CD20 ligando-se a este antigénio transmembrano localizado em linfócitos pré-B e B maduros. O orador explicou que o rituximab é uma estratégia terapêutica eficaz a curto prazo, mas que a taxa de recorrência é relativamente elevada. Em 95% dos casos, a actividade da doença pode ser controlada através da destruição de células B de memória, mas em 77%, a doença recai [6]. Sabe-se que as células B autoreactivas desempenham um papel fundamental no patomecanismo das recidivas.
CAR-T e CAAR-T em pemphigus vulgaris
Para tratar o PV sem causar imunossupressão generalizada, a equipa de investigação da Universidade da Pensilvânia desenvolveu um receptor de autoanticorpos quimérico artificial (CAAR) que exibe fragmentos do autoantigénio Dsg3 – os mesmos fragmentos aos quais os anticorpos causadores do PV e as suas células B se ligam tipicamente. As células B auto-reactivas desempenham um papel importante no patomecanismo da PV e a sua eliminação específica é um mecanismo de acção central desta estratégia de tratamento. Um desenho receptor comprovado na cultura de células foi também bem sucedido num modelo de rato para PV. Estudos in vivo mostraram que as células CAAR T reconhecem e eliminam especificamente as células B reactivas Dsg3 e não levam a uma toxicidade fora do alvo contra queratinócitos [1].
Em contraste com a terapia baseada em anticorpos, na qual uma dose definida é infundida, as células T CAAR podem expandir-se várias vezes in vivo e dar origem a células T que persistem durante décadas. Assim, só é preciso infundir as células T CAAR uma vez, elas matam todas as células pênfigo B e depois tornam-se inactivas. Se uma célula pênfigo B reaparecer a qualquer momento no futuro, as células CAAR T de memória podem voltar a aumentar e eliminá-la.
Um artigo de revisão publicado em 2018 por Siddiqi et al. [4] concorda que a CAR-T é uma abordagem de tratamento promissora da PV, mas os autores salientam que as actuais terapias CAR-T estão associadas a um risco relativamente elevado de síndrome de libertação de citocinas como um efeito secundário adverso, uma doença inflamatória sistémica potencialmente fatal.
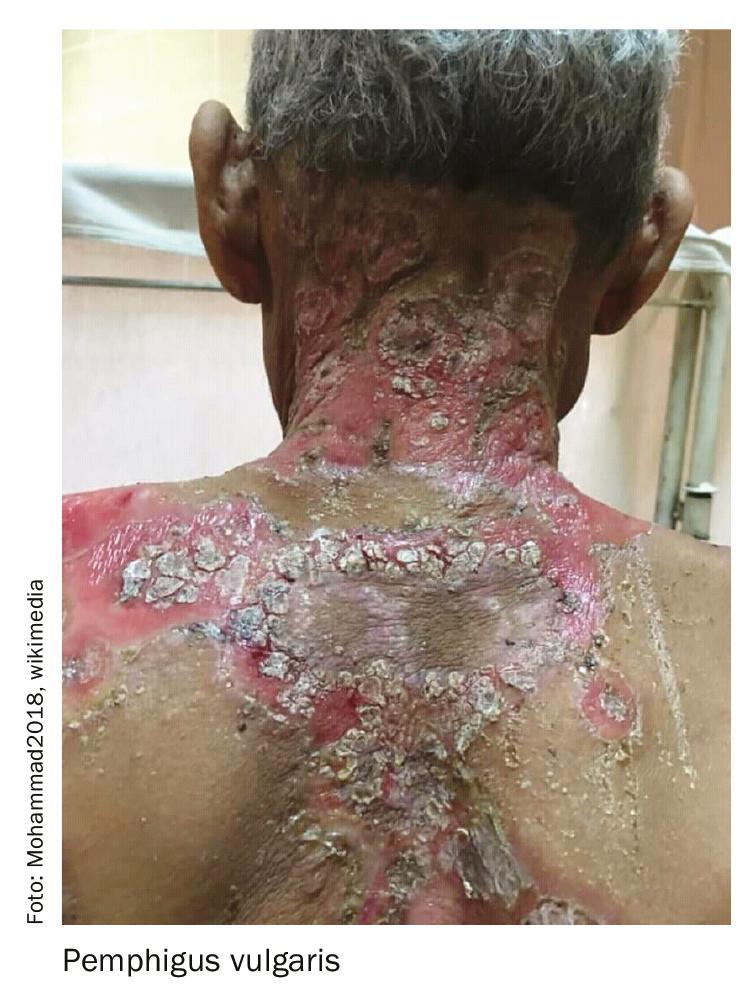
O desenvolvimento e aprovação no mercado de produtos CAR-T no campo da oncologia também está associado a obstáculos, mas algumas preparações estão agora disponíveis. O produto CAR-T tisagenlecleucel, aprovado na Suíça desde 2018 para o tratamento da leucemia linfoblástica aguda de células B refratária (adolescentes) e do linfoma de grandes células B refratária (adultos), é uma terapia autóloga e imunocelular do cancro que leva a uma reprogramação das próprias células T do paciente com um transgene que codifica um receptor de antigénio quimérico (CAR) de modo a identificar e eliminar as células CD19-expressoras [5].
Literatura:
- Ellebrecht CT: Go CAART – Imunoterapia para aplicações não cancerígenas, Christoph Ellebrecht, MD, residente em Dermatologia, Universidade da Pensilvânia, apresentação de slides 46ª Reunião Anual da Associação para a Investigação Dermatológica (ADF), 13-16 de Março de 2019, Munique.
- Ellebrecht CT, Payne AS: Definir o alvo para a terapia do pemphigus vulgaris. JCI Insight 2017; 2(5): e92021. https://doi.org/10.1172/jci.insight.92021.
- Ellebrecht CT, et al: Reengenharia de células T quiméricas receptoras de antigénios para terapia orientada de doenças auto-imunes. Ciência 2016; 353(6295): 179-184. doi: 10.1126/science.aaf6756. Epub 2016 Jun 30.
- Siddiqi HF, Staser KW, Nambudiri VE: Técnicas de Pesquisa Tornadas Simples: Terapia com células T da CAR. Journal of Investigative Dermatology 2018; 138: 2501e2504. doi:10.1016/j.jid.2018.09.002. https://beaumont.cloud-cme.com/assets/beaumont/Presentations/14208/14208.pdf
- Compêndio: KYMRIAH, https://compendium.ch/prod/kymriah-zellsuspension-inf-los–nh-/de, acedido pela última vez a 15 de Julho de 2019.
- Joly P: rituximab de primeira linha combinado com prednisona de curto prazo versus prednisona apenas para o tratamento de pênfigo (Ritux 3): um ensaio randofmised prospectivo, multicêntrico, de grupo paralelo, de rótulo aberto. Lancet 2017; 389(10083): 2031-2040. doi: 10.1016/S0140-6736(17)30070-3. Epub 2017 Mar 22.
- Schultz L, et al: Conduzindo a tradução de células CAR T para a frente. Science Translational Medicine 2019; 11 (481), eaaw2127. DOI: 10.1126/scitranslmed.aaw2127
DERMATOLOGIE PRAXIS 2019; 29(4): 46-47 (publicado 28.8.19, antes da impressão).