A memória imunológica desempenha um papel importante na patogénese da psoríase. Cada vez mais, os investigadores estão a concentrar-se nas células T de memória residente de tecido (células TRM). Isto porque a retenção de células TRM em lesões psoriásicas saradas é uma explicação para a recorrência de lesões no mesmo local após a descontinuação da terapia sistémica.
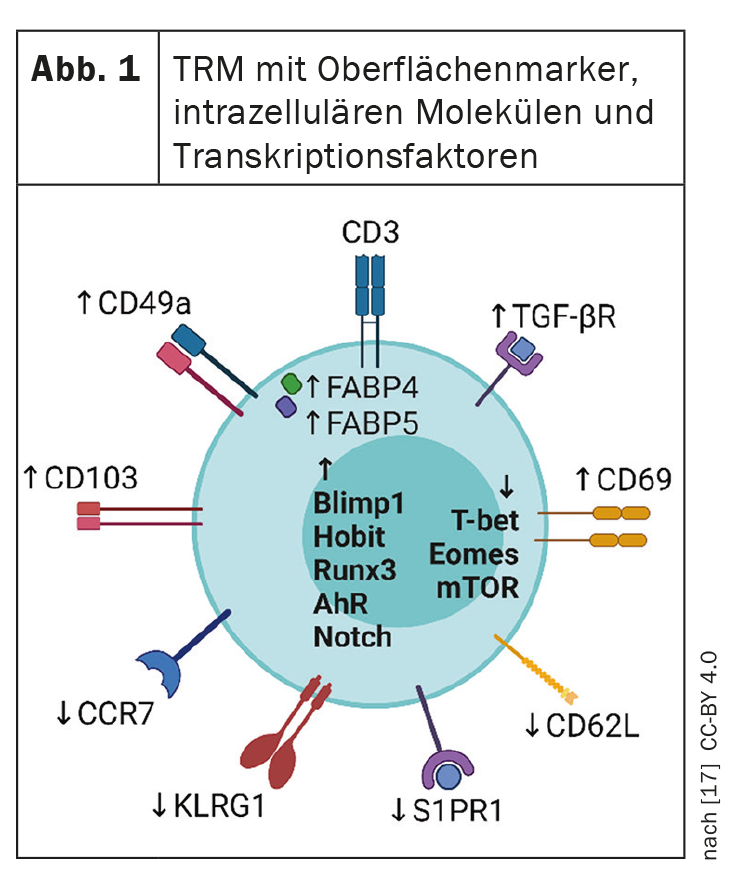
As terapias modernas altamente eficazes da psoríase sistémica convertem a pele lesional num estado sem manifestações clínicas visíveis. No entanto, uma vez terminada a terapia, as lesões psoriásicas da pele reaparecem frequentemente nas áreas anteriormente afectadas. Isto sugere que a actividade residual da doença persiste na área das lesões aparentemente curadas, predispondo os indivíduos afectados à recorrência [2]. As células t de memória residente de tecido (células TRM) (Fig. 1) fazem parte do sistema imunitário adaptativo e armazenam informação sobre antigénios com os quais o sistema imunitário foi anteriormente confrontado. As células TRM desempenham provavelmente um papel fundamental na reactivação da inflamação latente e, por conseguinte, no decurso a longo prazo da doença (caixa) .
Células CD8+ TRM como biomarcadores da actividade psoriásica?
Uma questão actual é saber se se pode livrar da psoríase através de uma abordagem de “golpe duro e precoce”, explicou o Prof. Wolf Henning Boehncke, MD, Hôpitaux Universitaires de Genève [1]. Vários estudos estão a investigar se a intervenção precoce com produtos biológicos pode ter um efeito duradouro no curso da psoríase e prevenir o desenvolvimento da artrite psoriásica ou o comprometimento cumulativo do curso de vida (CLCI) [3–7]. Outra questão é se as células TRM podem ser usadas como biomarcador da actividade psoriásica, diz o Prof. Boehncke [1]. Num artigo de revisão publicado em 2022 por Puig et al. é apresentado o estado actual dos conhecimentos [8]. As células TRM podem ser divididas em subconjuntos CD8+ e CD4+. As células CD8+ TRM são localizadas na epiderme onde desempenham um papel crucial nas respostas imunitárias, as células CD4+ TRM são menos bem caracterizadas e podem estar envolvidas na imunidade protectora contra infecções bacterianas e micóticas na pele [9,10]. A maioria das células CD8+ TRM expressam o marcador de células CD103. CD103 é o subunidade αE-subunidade de αEβ7. E-cadherin é um ligante para a integrina αE(CD103)β7. As interacções Integrin- [11,12]-E-cadherin desempenham um papel na organização do epitélio da pele psoriásica, bem como na localização específica dos órgãos dos linfócitos T na epiderme αEβ7 .
|
Os psoriásicos têm mais células CD8+ TRM mesmo em pele nãoesional As células CD8+ TRM produzem as citocinas pró-inflamatórias IL-17 e IL-22 no estado activo, exprimem o receptor IL-23 e são reactivadas pela IL-23. Vo et al. relatou que as células CD8+ TRM são enriquecidas tanto em pele lesional como não lesional de doentes psoriásicos em comparação com a pele normal [15]. Isto sugere que estas células TRM promovem a reactivação da inflamação latente e, portanto, a recorrência das lesões. Por conseguinte, os novos tratamentos para a psoríase que visam alcançar a remissão sustentada da doença devem visar o esgotamento das células patogénicas CD8+ TRM, os investigadores concluem [16]. |
Relevância para a modificação a longo prazo do curso da doença
No futuro, espera-se que os biólogos sejam capazes de modificar de forma sustentável a fisiopatologia da psoríase através da modulação das células TRM. As evidências iniciais sugerem que a inibição da IL-23 inibe a activação das células TRM e, por conseguinte, previne a inflamação sistémica a longo prazo. No estudo ECLIPSE, uma análise das biópsias de lesões psoriásicas mostrou que o número de células CD8+ TRM em eflorescências foi reduzido para o nível de pele não-lesional após 24 semanas de tratamento com guselkumab [13,14]. O estudo GUIDE está a investigar a hipótese de que o tratamento precoce com guselkumab pode reduzir a acumulação de células TRM na pele e assim influenciar positivamente o curso a longo prazo da doença [18].
Congresso: Skin Inflammation & Psoriasis International Network
Literatura:
- “Patogenética: psoríase vs dermatite atópica”, Sessão Plenária 4, Prof. Dr. Wolf Henning Boehncke, SPIN, Congresso da Rede Internacional de Inflamação da Pele & Psoríase, 07.07.2022.
- Clark RA: J Invest Dermatol 2011; 131: 283-285.
- Gisondi P, et al: Expert Rev Clin Immunol 2020; 16: 591-598.
- Gisondi P, et al: Ann Rheum Dis 2022; 81: 68-73.
- Acosta Felquer ML, et al: Ann Rheum Dis. 2021 Ann Rheum Dis 2022; 81(1): 74-79.
- von Stülpnagel CC, et al: J Eur Acad Dermatol Venereol 2021; 35: 2166-2184.
- Iversen L, et al: J Eur Acad Dermatol Venereol 2018; 32: 1930-1939.
- Puig L, et al: Br J Dermatol 2022; 186(5): 773-781.
- Chen L, Shen Z: Cell Mol Immunol 2020; 17: 64-75.
- Ho AW, Kupper TS: Nat Rev Immunol 2019; 19: 490-502.
- Watanabe R, et al: Sci Transl Med 2015; 7:279ra39.
- Pauls K, et al: J Invest Dermatol 2001; 117: 569-575.
- Warren RB, et al: J Eur Acad Dermatol Venereol 2021; 35: 919-927.
- Mehta H, et al: J Invest Dermatol 2021; 141: 1707-1718.
- Vo S, et al: Br J Dermatol 2019; 181:410-12.
- Armstrong AW, et al: Br J Dermatol 2020; 182: 1484-1487.
- Vu TT, et al: J Clin Med 2021; 10(17): 3822.
- Eyerich K, et al: BMJ Open 2021; 11(9): e049822
DERMATOLOGIE PRAXIS 2022; 32(4): 20 (publicado 21.8.22, antes da impressão).