A colite ulcerosa é uma doença inflamatória crónica do intestino de etiologia desconhecida. A apresentação clínica é diarreia mucopurulenta sangrenta com tenesmo que a acompanha e raramente incontinência fecal. As recaídas são classificadas de acordo com a sua propagação e gravidade. O diagnóstico requer uma combinação de resultados clínicos, laboratoriais, radiológicos, endoscópicos e histológicos. As preparações tópicas e sistémicas 5-ASA estão disponíveis terapeuticamente. Na ausência de eficácia, podem ser administrados também esteróides, medicamentos imunomoduladores ou anticorpos TNF-alpha. Uma recaída grave deve ser tratada como um paciente internado. Após a remissão ter sido alcançada, é indicada a terapia de manutenção permanente da remissão.
A colite ulcerosa (CU) é uma doença inflamatória crónica do intestino. Caracteriza-se por uma inflamação crónica e recaída da mucosa do cólon. A causa exacta não é conhecida: É uma desordem do sistema imunitário que ocorre em certas constelações genéticas (são agora conhecidas mais de 160 variações genéticas), dietéticas e ambientais [1].
Espalhar
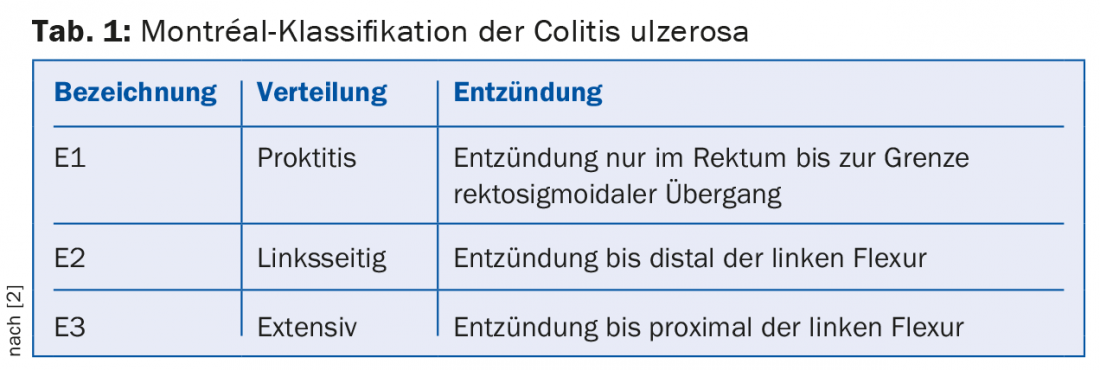
CU afecta tipicamente a mucosa do cólon, começando distalmente com uma propagação contínua proximal. Casos especiais são o envolvimento do íleo terminal (chamado “backwash ileitis”), uma inflamação que é adicionalmente isolada em torno da saída do apêndice na CU do lado esquerdo (“remendo cecal”), e a variante de exclusão do recto. A directriz ECCO de 2012 recomenda a classificação de CU de acordo com a classificação de Montreal de acordo com a propagação da inflamação [2]: Se a inflamação é limitada ao recto, chama-se proctite ulcerosa (E1); se se espalha para a flexão esquerda, há CU do lado esquerdo (E2); se há actividade da doença proximal à flexão esquerda, há CU extensa (E3, pancreatite). (Tab.1).
As manifestações extraintestinais ocorrem em aproximadamente 30% dos doentes em vários órgãos (pele, olhos, articulações, fígado), em parte paralelas à actividade da doença de CU, em parte independentes desta [3] (Tab. 2).

Epidemiologia
A incidência na Europa Ocidental é de 11/100.000. É mais elevada nas nações industrializadas e em latitudes mais elevadas, e tem vindo a aumentar nas últimas décadas. Nutrição, higiene e uso de antibióticos são postulados como causas possíveis, presumivelmente com uma influência resultante sobre o microbioma [4]. Um estudo italiano no âmbito dos cuidados primários encontrou uma prevalência de 97/100.000 [5]. A idade média de início é de 30-49 anos. A primeira manifestação da doença ocorre em 25% dos casos antes dos 25 anos de idade. Mulheres e homens adoecem com aproximadamente a mesma frequência.
Previsão
Em 80% dos casos, a doença progride em recidivas, 50% têm inicialmente uma ligeira recidiva. Por outro lado, pouco menos de 20% dos pacientes têm de ser hospitalizados inicialmente, metade dos quais têm de ser colectomizados apesar da terapia com esteróides intravenosos. Uma idade mais jovem de início está associada a mais recaídas e actividade mais severa. O risco de desenvolvimento de carcinoma colorrectal é significativamente aumentado na CU esquerda e extensa e é ainda aumentado pela presença simultânea de colangite esclerosante primária.
Factores de risco
Uma história familiar da doença aumenta o risco: para filhos de alguém com CU, o risco é de 2% [1]. Além disso, uma recente infecção por salmonela ou campylobacter e um elevado padrão de higiene na infância são factores de risco. O baixo abuso de nicotina e o estatuto após apendicectomia para apendicectomia são protectores [2].
Clínica
Num episódio agudo, a pessoa afectada sofre de diarreia sangrenta e mucosa, muitas vezes também à noite, com cólicas abdominais (tenesmus) e urgência. Por vezes, a incontinência fecal também ocorre. Dependendo da gravidade do episódio, pode ocorrer anemia com fraco desempenho, taquicardia, febre, mal-estar e anorexia. Se não houver sintomas clínicos e a mucosa tiver cicatrizado endoscopicamente, a isto chama-se remissão profunda. A gravidade de uma recaída é dividida em suave, moderada e grave de acordo com Truelove e Witts (Tab. 3) [6]. Um episódio grave é quando há mais de seis movimentos intestinais sangrentos por dia e sinais de toxicidade sistémica. Os doentes com recaídas graves devem ser tratados como doentes internados.

Diagnósticos
O diagnóstico da UC baseia-se numa combinação de história, clínica, testes químicos laboratoriais, incluindo testes de fezes, resultados endoscópicos, resultados histológicos e possivelmente resultados radiológicos. Os valores de inflamação (PCR, leucócitos) e trombocitose fornecem informações sobre a actividade inflamatória da UCC. O valor da hemoglobina pode indicar anemia, o estado do ferro uma deficiência em ferro ou inflamação crónica. As enzimas hepáticas elevadas podem indicar colangite esclerosante primária. Está excluída uma causa infecciosa de diarreia utilizando amostras de fezes para protozoários, helmintos e agentes patogénicos bacterianos, incluindo Clostridium difficile. A síndrome do intestino irritável pode ser largamente descartada inicialmente por uma calprotectina patologicamente elevada nas fezes [7]. A calprotectina, juntamente com o PCR, leucócitos, hemoglobina e plaquetas, também pode ser utilizada como parâmetro de progressão para monitorizar a actividade das UCs [2,8]. Um abdómen CT pode ser útil para excluir complicações tais como megacólon tóxico, perfuração, peritonite transmigratória, abcesso ou estenose com carcinoma num episódio grave ou abdómen peritoniano e para diferenciar a diverticulite.
A Ileocolonoscopia com múltiplas biopsias continua a ser o componente mais importante do diagnóstico. Por um lado, o diagnóstico pode muitas vezes ser feito com base em alterações histológicas típicas e, por outro lado, as complicações infecciosas podem ser excluídas (por exemplo, colite do citomegalovírus). (Fig. 1). Há frequentemente um atraso no diagnóstico: Na coorte suíça IBD, a UC foi diagnosticada após uma mediana de quatro meses, com 75% dos doentes diagnosticados no prazo de doze meses [9]. Em Itália, o tempo médio entre o aparecimento dos sintomas e o diagnóstico no contexto do GP foi de 14 meses [5].

Terapia da recidiva aguda
A terapia de indução de remissão depende da propagação anatómica e da gravidade do actual episódio de CU [10,11]:
- Um episódio leve a moderado de proctite ulcerosa (E1) é tratado principalmente com salicilato tópico de 5-amino (5-ASA) (supositórios 1 g/dia). Se não houver resposta, a budesonida tópica é suplementada (espuma rectal 2 mg/dia). Se a actividade inflamatória persistir sob esta, deve ser iniciada a terapia oral com 5-ASA (>2 g/dia) ou esteróides (Fig. 2).
- Um episódio ligeiro a moderado de colite do lado esquerdo (E2) é inicialmente tratado com uma combinação de oral e tópico 5-ASA. Em vez de supositórios, deve ser utilizada espuma ou enemas (2-4 g/d cada), pois estes, ao contrário dos supositórios, atingem a mucosa até à flexão esquerda. A administração única diária de 5-ASA é equivalente a várias vezes a administração diária. Se ineficaz, a terapia com esteróides tópicos (por exemplo, espuma de budesonida) deve ser adicionada primeiro antes da terapia com esteróides orais. A dose inicial da terapia oral é de 40 mg com reduções de dose semanais de 5 mg (duração total de aproximadamente 8 semanas) (Fig. 2).
- A CU extensa (E3) deve ser inicialmente tratada com uma combinação de 5-ASA oral e tópica para uma actividade suave a moderada. Os esteróides orais estão disponíveis como uma escalada da terapia.
- Um episódio grave de CU é considerado potencialmente fatal e deve ser tratado como um doente internado. A avaliação interdisciplinar precoce em conjunto com o cirurgião visceral é importante. Inicialmente, complicações como o Clostridium difficile ou a colite do citomegalovírus devem ser excluídas. Se a administração intravenosa de metilprednisolona (60 mg/dia) não mostrar efeito dentro de aproximadamente três dias (taxa de resposta de 67%), deve ser discutida a terapia de resgate com ciclosporina (2 mg/kg i.v. durante 8 dias, taxa de resposta de 84% e taxa de colectomia de 9%) ou um anticorpo TNF-alfa como o infliximab ou adalimumab ou colectomia. Infliximab leva a uma resposta clínica em 69,4% após oito semanas (remissão clínica 34,7% após 54 semanas) [12]. Adalimumab levou a uma resposta clínica em 50,4% dos pacientes (remissão clínica 17,3% às 52 semanas) após oito semanas no ensaio ULTRA-2 [13].

Terapia de remissão-preservação
Depois de se conseguir a remissão, recomenda-se sempre a terapia de manutenção da remissão. Isto depende da propagação, do curso anterior, da gravidade do último ataque e da medicação actual. Uma preparação 5-ASA é permanentemente recomendada como terapia de primeira linha: topicamente em E1 (possivelmente E2) com uma dose mínima de 3 g/semana e sistemicamente em E2 e E3 (dose mínima 1,2/d), sendo a combinação tópica e oral a mais eficaz. Se necessário, a azatioprina (dose alvo 2-2,5 mg/kg de peso corporal) ou 6-mercaptopurina (dose alvo 1-1,5 mg/kg de peso corporal) deve ser adicionada em casos de recidivas frequentes (>1×/ano), recidiva precoce, intolerância 5-ASA ou curso dependente de esteróides. Alternativamente, seria possível a terapia com um anticorpo TNF-alfa (infliximab, adalimumab, golimumab) ou com tacrolimus.
Mensagens Take-Home
- A colite ulcerativa é classificada de acordo com a propagação anatómica em proctite ulcerativa, colite ulcerativa do lado esquerdo e colite ulcerativa extensiva.
- As manifestações extraintestinais ocorrem em parte em paralelo com a actividade inflamatória do cólon e em parte independentemente dela.
- A classificação da gravidade de uma recaída baseia-se nos critérios da Truelove e do Witts.
- Uma recaída grave pode precisar de ser tratada como um paciente internado.
- Na remissão, a terapia de manutenção da remissão deve ser sempre realizada.
Literatura:
- Adams SM, et al: Colite ulcerosa. Am Fam Physician 2013; 87(10): 699-705.
- Dignass A, et al.: Segundo Consenso Europeu baseado em evidências sobre o diagnóstico e gestão da colite ulcerosa: Definições e diagnóstico. J Crohns Colitis 2012; 6(10): 965-990.
- Vavricka S, et al: Frequência e factores de risco para manifestações extraintestinais na coorte suíça de doenças inflamatórias intestinais. Am J de Gastroenterologia 2011; 106(1): 110-119.
- Talley NJ, et al: Uma revisão sistemática baseada em provas sobre terapias médicas para a doença inflamatória intestinal. Am J Gastroenterol 2011; 106(suppl 1): 2-25.
- Tursi A, et al.: Incidência e prevalência de doença inflamatória intestinal no contexto dos cuidados primários de gastroenterologia. Eur J Intern Med 2014; 24(8): 852-856.
- Truelove SC, et al: Cortisone in ulcerative colitis; relatório final sobre um ensaio terapêutico. Br Med J 1955; 2: 1041-1048.
- Manz M, et al: Valor da calprotectina fecal na avaliação de pacientes com desconforto abdominal: um estudo observacional. BMC Gastroenterol 2012; 12(5): 1471.
- Xiang JY, et al: Valor clínico da calprotectina fecal na determinação da actividade da doença na colite ulcerosa. Mundo J Gastroenterol 2008; 14(1): 53-57.
- Vavricka SR, et al: Avaliação sistemática dos factores de risco de atraso no diagnóstico de doenças inflamatórias intestinais. Inflamm Bowel Dis 2012; 18(3): 496-505.
- Dignass A, et al.: Segundo Consenso Europeu baseado em provas sobre o diagnóstico e gestão da colite ulcerosa: Gestão actual. J Crohns Colitis 2012; 6(10): 991-1030.
- Manz M, et al: Algoritmo de tratamento para a colite ulcerativa moderada a grave. Swiss Med Wkly 2011; 141: w13235.
- Rutgeerts P, et al: Infliximab para Indução e Terapia de Manutenção para Colite Ulcerosa. N Engl J Med 2005; 353(23): 2462-2476.
- Sandborn WJ, et al: Adalimumab induz e mantém a remissão clínica em doentes com colite ulcerosa moderada a grave. Gastroenterologia 2012; 142(2): 257-265.
PRÁTICA DO GP 2015; 10(4): 16-20