As estratégias terapêuticas actuais para a doença inflamatória intestinal (DII) atingiram um patamar em termos de taxas de resposta e/ou remissão alcançadas com um único agente terapêutico. Consequentemente, a terapia combinada avançada (ACT) surgiu como um novo conceito de tratamento. Um grupo de investigadores analisou estudos recentes que comparam as ACT com as monoterapias.
As terapias biológicas tornaram-se o padrão de cuidados para o tratamento da doença inflamatória intestinal (DII) ativa moderada a grave, incluindo a doença de Crohn (DC) e a colite ulcerosa (CU). Apesar destes avanços, as abordagens terapêuticas actuais para a DII estagnaram em termos de taxas de resposta e/ou remissão. O arsenal existente de terapias avançadas resulta em taxas de remissão clínica global de apenas cerca de 50%. Além disso, cerca de 50% dos doentes que inicialmente respondem à terapêutica biológica ou com pequenas moléculas perdem essa resposta ao longo do tempo. Consequentemente, os doentes com DII que não respondem ou que perderam a resposta a uma determinada terapêutica biológica têm de mudar para uma molécula diferente, reduzindo as suas hipóteses de alcançar a remissão da doença a longo prazo.
A nova abordagem da terapia combinada avançada ( ACT) surgiu como uma estratégia de tratamento promissora para a DII. Envolve a utilização de duas terapias específicas diferentes, biológicas ou de pequenas moléculas, com o objetivo principal de ultrapassar o patamar terapêutico. Recentemente, foram obtidos dados sobre o ACT no ensaio VEGA, controlado e aleatório: O Dr. Panu Wetwittayakhlang, do Departamento de Gastroenterologia e Hepatologia da Universidade Prince of Songkla, Hat Yai, Tailândia, e o Dr. Peter L. Lakatos, do Departamento de Gastroenterologia e Hepatologia do Centro de Saúde da Universidade McGill, Montreal, analisaram as evidências actuais (em fevereiro de 2024) sobre o ACT e o seu impacto na superação do limite terapêutico no tratamento da DII [1].
A combinação a curto prazo de dois medicamentos biológicos pode ajudar os doentes com CU a obter um melhor controlo da doença
No RCT VEGA de fase 2a, a eficácia da terapia de indução combinada com o inibidor seletivo da interleucina (IL)-23 guselkumab e o inibidor do TNF-alfa golimumab foi investigada em comparação com a monoterapia com guselkumab ou golimumab em doentes com CU moderada a gravemente ativa. Um total de 214 doentes que não tinham respondido à terapêutica anti-TNF e que não responderam ou não toleraram a terapêutica convencional foram aleatoriamente distribuídos por um dos seguintes tratamentos:
- Guselkumab 200 mg i.v. nas semanas 0, 4 e 8 (n=71),
- Golimumab 200 mg s.c. na semana 0, depois 100 mg s.c. nas semanas 2, 6 e 10 (n=72)
- ou uma combinação de 200 mg de guselkumab i.v. mais 200 mg de golimumab s.c. na semana 0; 100 mg de golimumab s.c. nas semanas 2, 6 e 10 e 200 mg de guselkumab i.v. nas semanas 4 e 8 (n=71).
Na fase de manutenção, os doentes no braço de combinação foram transferidos para monoterapia com guselkumab no início da semana 12.
Em doentes com CU não tratados biologicamente, o estudo indica uma maior taxa de remissão clínica e melhoria endoscópica no braço de combinação (terapia de indução com golimumab e guselkumab) vs. monoterapias com golimumab ou guselkumab. No entanto, os autores referem que o estudo VEGA não incluiu doentes com UC com exposição prévia ou insucesso a biológicos anteriores. Por conseguinte, existem ainda dados limitados de ensaios clínicos sobre a eficácia do ACT em doentes com CU refractários ao tratamento biológico. Os dados disponíveis sobre o ACT em doentes com doença de Crohn são também limitados, o que representa um desafio particular em doentes com doença complicada.
A terapêutica combinada conduziu a uma remissão clínica em 54,5% dos doentes
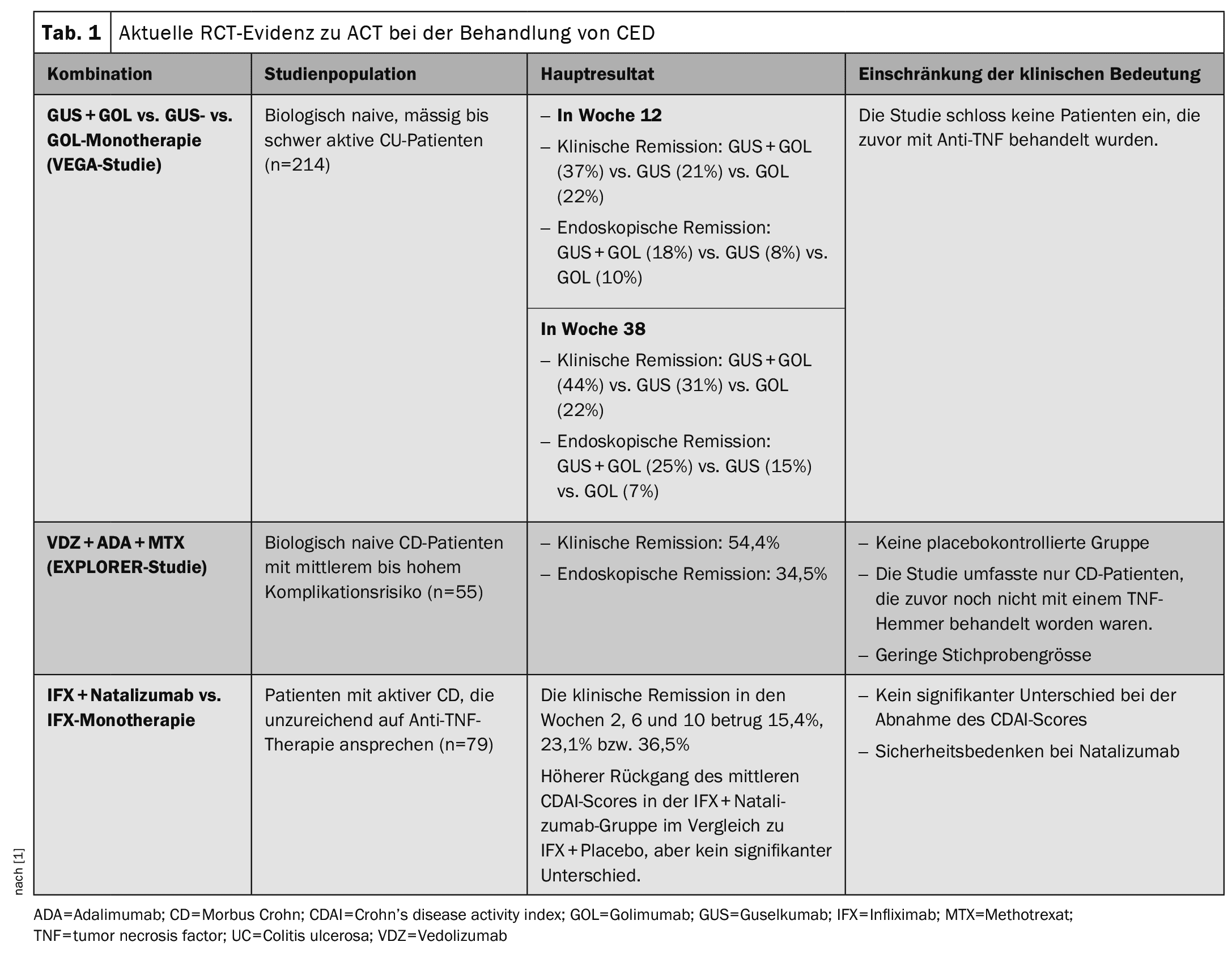
> >O estudo EXPLORER de fase 4, aberto, investigou a eficácia de uma terapêutica de combinação tripla de vedolizumab, adalimumab e metotrexato em doentes não tratados biologicamente com doença de Crohn (DC) de risco moderado a elevado, conforme determinado por uma pontuação endoscópica para DC (SES-CD) 7 (ou 4 para doença ileal isolada). Os doentes elegíveis com doença de Crohn foram considerados como tendo um risco médio a elevado de complicações. Foi efectuada uma análise interina de 55 doentes tratados com a terapêutica tripla (vedolizumab 300 mg i.v. no dia 1 e nas semanas 2 e 6 e depois de 8 em 8 semanas; adalimumab 160 mg s.c. no dia 2, 80 mg na semana 2 e depois 40 mg de 2 em 2 semanas até à semana 26; metotrexato 15 mg por via oral semanalmente até à semana 34). Após a tríplice e até à semana 34, cada doente recebeu monoterapia com vedolizumab até à semana 102. Na semana 26, observou-se resposta clínica e remissão endoscópica em 54,4% e 34,5%, respetivamente. Não se registaram sinais de segurança associados à terapêutica tripla. A evidência atual dos ensaios clínicos randomizados sobre ACT no tratamento da DII está resumida naTabela 1 .
O ensaio EXPLORER sugere a eficácia de uma combinação de vedolizumab, adalimumab e metotrexato para melhorar a resposta endoscópica e a remissão em doentes com DC sem tratamento biológico e com risco intermédio a elevado de complicações. No entanto, a falta de um braço controlado no estudo impede uma demonstração clara da eficácia terapêutica do ACT na DC, afirmaram os Drs. Wetwittayakhlang e Lakatos.
Evidências fracas de estudos do mundo real
Em termos de dados observacionais do mundo real, um grande estudo multicêntrico relatou 98 doentes que iniciaram uma terapêutica combinada para DII ativa (67%), doenças inflamatórias imunomediadas activas (DIMI) ou manifestações extra-intestinais (MIE, 22%) ou ambas (10%) após múltiplos biológicos terem falhado. A atividade da doença da DII melhorou clinicamente em 70% dos doentes e em 81% dos doentes com DIMI/EIM. Outro estudo retrospetivo relatou 92 doentes que receberam terapia biológica combinada para DII ativa ou EIM. As combinações mais comuns foram vedolizumab e ustekinumab (32%) ou vedolizumab e anti-TNF (31%). As taxas de resposta clínica aos 3 e 6 meses foram de 46% e 34%, respetivamente. Um estudo retrospetivo de Glassner et al. examinou 50 doentes com DII que foram tratados com várias combinações de terapêuticas biológicas ou de pequenas moléculas. Aproximadamente 50% receberam vedolizumab mais anti-IL-12 e IL-23 (ustekinumab) por atividade persistente da doença (n=47) ou doença reumatológica ou dermatológica concomitante (n=3). Ao fim de 4 meses, o número de doentes em remissão clínica (50% vs. 14%, p=0,0018) e ao fim de 8 meses em remissão endoscópica (34% vs. 6%, p=0,0039) era significativamente superior ao registado no início do tratamento.
Outra série de casos mostrou que a terapia biológica dupla foi segura e eficaz em 22 doentes com DC refractária grave que tinham recebido um total de 24 tratamentos biológicos duplos após múltiplas terapias biológicas falhadas. A resposta clínica e a remissão clínica foram observadas em 50% e 41% dos pacientes, respetivamente. A melhoria endoscópica e a remissão foram observadas em 43% e 26%, respetivamente. A presença de fístula perianal ativa diminuiu de 50% na linha de base para 33% após o tratamento. Do mesmo modo, a eficácia da combinação de tofacitinib com outras terapêuticas biológicas foi comunicada em dois estudos de coorte retrospectivos.
Uma meta-análise efectuada por Alayo et al. avaliou a eficácia do ACT com diferentes regimes de combinação. Nos doentes que receberam vedolizumab mais tofacitinib, as taxas combinadas de resposta clínica e remissão foram de 59,9% (IC 95% 37,2-80,8) e 47,8% (IC 95% 19,0-77,4), respetivamente. Para vedolizumab mais ustekinumab, as taxas combinadas de resposta clínica e remissão foram de 83,9% (IC 95% 66,4-96,8) e 47,0% (IC 95% 14,5-80,7), respetivamente. Os doentes que receberam vedolizumab mais anti-TNF tiveram taxas combinadas de resposta e remissão endoscópica/radiológica de 38,2% (IC 95% 19,5-58,4) e 18,0% (IC 95% 1,6-41,8), respetivamente. E nos doentes tratados com tofacitinib mais vedolizumab, as taxas correspondentes foram 46,2% (IC 95% 20,4-73,0) e 24,6% (IC 95% 6,4-47,6).
De acordo com o Dr. Wetwittayakhlang e o Dr. Lakatos, os estudos observacionais do mundo real são informativos, mas deixam em aberto a questão de saber se o ACT pode aumentar o teto terapêutico na DII nas complexidades de um contexto clínico da vida real, uma vez que a maioria dos doentes que recebem ACT não responderam ou responderam inadequadamente à terapêutica biológica. Por conseguinte, devem ser considerados os dados disponíveis mais fiáveis, principalmente de um número limitado de ensaios clínicos que envolveram doentes com ACT que ainda não tinham recebido agentes biológicos.
Opção terapêutica promissora para um controlo eficaz da doença
A ACT surgiu como uma potencial nova estratégia terapêutica destinada a melhorar a eficácia terapêutica e a ultrapassar o patamar observado com as terapêuticas atualmente disponíveis. Em doentes altamente selecionados com um fenótipo de doença de alto risco (como os doentes com envolvimento extenso do intestino delgado na doença de Crohn ou os doentes que não respondem a múltiplas terapêuticas), a utilização de ACT para o controlo precoce da doença pode ser útil para evitar a progressão da doença e as complicações. Durante a fase de indução, a co-indução simultânea com uma combinação de medicamentos biológicos ou de pequenas moléculas pode ser utilizada para maximizar o controlo da doença através de efeitos sinérgicos. Uma vez atingida a remissão da doença, a monoterapia com um dos agentes combinados pode ser utilizada para manter a remissão da doença.
Outro aspeto, segundo os autores, que deve ser considerado aquando da aplicação da estratégia ACT na prática clínica é o potencial para alterações nos sinais de segurança com a exposição prolongada a múltiplos imunossupressores. Embora as preocupações com a segurança não tenham sido um foco importante até à data, é importante reconhecer que os dados disponíveis provêm de pequenos estudos com períodos de acompanhamento limitados. Por conseguinte, são necessários mais estudos prospectivos de grande dimensão com períodos de seguimento mais longos para compreender plenamente a eficácia e a segurança desta estratégia. Permanecem também incertezas quanto ao facto de a combinação dever ser utilizada exclusivamente na fase de indução ou alargada à terapêutica de manutenção.
Os resultados actuais, como os do estudo VEGA, mostram que a combinação de novos produtos biológicos alcança uma eficácia terapêutica superior em doentes biologicamente ingénuos com CU moderada a gravemente ativa, tanto clínica como endoscopicamente, em comparação com a terapêutica monobiológica. No entanto, os dados são frequentemente limitados. Olhando para o futuro, estudos em curso como os ensaios DUET-CD e DUET-UC (que avaliam a combinação de guselkumab e golimumab em doentes com DII refractária) e o ensaio VICTRIVA (que avalia a combinação de vedolizumab e upadacitinib) prometem fornecer dados adicionais sobre a eficácia do ACT em doentes com doença de Crohn e colite ulcerosa que falharam a terapêutica biológica, concluiu o Dr. Wetwittayakhlang. Wetwittayakhlang e Dr. Lakatos.
Literatura:
- Wetwittayakhlang P, Lakatos PL: Terapia de combinação avançada: será a melhor forma de quebrar o teto terapêutico? Therapeutic Advances in Gastroenterology 2024; 17; doi: 10.1177/17562848241272995.
PRÁTICA DE GASTROENTEROLOGIA 2024; 2(2): 22-23