Um estudo recente investigou a concordância entre a variabilidade da frequência cardíaca derivada do sinal fotopletismográfico de um smartwatch disponível no mercado e a variabilidade da frequência cardíaca derivada do eletrocardiograma de alta resolução (padrão de ouro) em doentes com doenças cardiovasculares.
A variabilidade da frequência cardíaca (VFC) reflecte a variação dos intervalos entre os batimentos cardíacos e é uma ferramenta comprovadamente não invasiva para avaliar o estado funcional do sistema nervoso autónomo cardíaco [2]. A disfunção do sistema nervoso autónomo, frequentemente caracterizada por uma sobreactividade do sistema nervoso simpático e por uma retração vagal, desempenha um papel fundamental na patogénese de várias doenças cardiovasculares e cerebrovasculares e está, por conseguinte, associada a um pior prognóstico [3,4]. Assim, as medições da VFC têm sido propostas para a previsão do risco em doentes com doenças cardiovasculares, incluindo enfarte do miocárdio, insuficiência cardíaca crónica, diabetes mellitus, acidente vascular cerebral isquémico e outras [5–8].
A partir das medições tradicionais normalizadas da VFC no domínio do tempo e da frequência, foi desenvolvida uma variedade de medições não normalizadas [9], incluindo, entre outras, marcadores de complexidade de curto prazo [10], entropia [11], bem como a análise do gráfico de Poincare [12], capacidade de desaceleração (DC) [13] e turbulência da frequência cardíaca [14]. Embora algumas destas medidas tenham mostrado resultados promissores como preditores de risco em grandes ensaios clínicos, a VFC tem sido pouco utilizada na prática clínica.
Mesmo um registo de 5 minutos do eletrocardiograma (ECG) permite a análise da VFC [2]. No entanto, para efeitos de previsão de risco, a análise da VFC é normalmente realizada com registos de ECG mais longos, especialmente quando se avaliam os parâmetros da VFC que captam os componentes de baixa frequência da VFC. Isto pode limitar a aplicabilidade da VFC na vida quotidiana, especialmente se a VFC for utilizada como uma ferramenta de monitorização contínua num ambiente ambulatório. Com algumas limitações, a VFC também pode ser calculada a partir de registos de ondas de pulso fotopletismográficas (PPG) [15]. A crescente prevalência de dispositivos portáteis com sensores PPG integrados na população poderia, por conseguinte, tornar a análise da VFC baseada em PPG com dispositivos inteligentes disponíveis no mercado numa abordagem futura promissora. Dois pequenos estudos em populações saudáveis já demonstraram a viabilidade geral dos marcadores de VFC baseados em smartwatches [16,17]. No entanto, desconhece-se a exatidão da VFC baseada em PPG derivada de um smartwatch em populações maiores com doenças cardiovasculares ou cerebrovasculares que possam beneficiar da monitorização contínua do risco.
O objetivo de um estudo recente foi, por conseguinte, determinar a precisão dos marcadores de VFC normalizados e não normalizados calculados a partir de registos PPG de um smartwatch disponível no mercado, em comparação com as métricas de VFC derivadas do ECG num número relevante de doentes com doenças cardiovasculares e cerebrovasculares [1].
Conceção do estudo e participantes
O estudo incluiu três coortes diferentes que se apresentaram a um ambulatório de cardiologia entre junho de 2021 e julho de 2022: Doentes após enfarte do miocárdio com elevação de ST (coorte STEMI), doentes após AVC isquémico (coorte STROKE) e doentes sem doença cardiovascular estrutural conhecida (coorte CONTROL).
Os critérios de inclusão para a coorte STEMI foram os pacientes com um primeiro STEMI tratado com intervenção coronária percutânea primária nas 24 horas seguintes ao início dos sintomas. Os critérios de inclusão para a coorte STROKE foram os doentes com AVC isquémico agudo confirmado por tomografia computorizada ou ressonância magnética com início dos sintomas nos 30 dias anteriores à admissão hospitalar. A coorte CONTROL incluiu pacientes sem história conhecida de doença cardiovascular estrutural manifesta. Os critérios gerais de inclusão incluíram uma idade ≥18 anos e a presença de ritmo sinusal. Os doentes com batimentos ventriculares prematuros frequentes (>10% do total de batimentos) ou de má qualidade foram excluídos.
Gravações e processamento de sinais
O ECG e o PPG foram registados simultaneamente durante 30 minutos em todos os indivíduos. Os registos foram efectuados em condições normalizadas, em posição supina e com respiração espontânea. Os estímulos externos (ruídos, etc.) foram reduzidos ao mínimo e os doentes receberam instruções para relaxar.
Dos 282 indivíduos que tinham registos simultâneos de ECG e PPG, 263 indivíduos preencheram os critérios de inclusão e foram incluídos no estudo. Destes, 104 tiveram um STEMI, 129 tiveram um AVC e 30 pertenciam à coorte CONTROL. A idade média da coorte total era de 61 anos e 71 (27%) eram do sexo feminino. A mediana do tempo de registo foi de 32,1 minutos. Nas coortes STEMI e STROKE, os registos foram efectuados três dias e cinco dias após os eventos índice, respetivamente. As medidas de VFC foram significativamente mais baixas nas coortes de STEMI e STROKE em comparação com a coorte CONTROL (P <0,05 para todos, exceto DF-α2).
Avaliação da variabilidade da frequência cardíaca
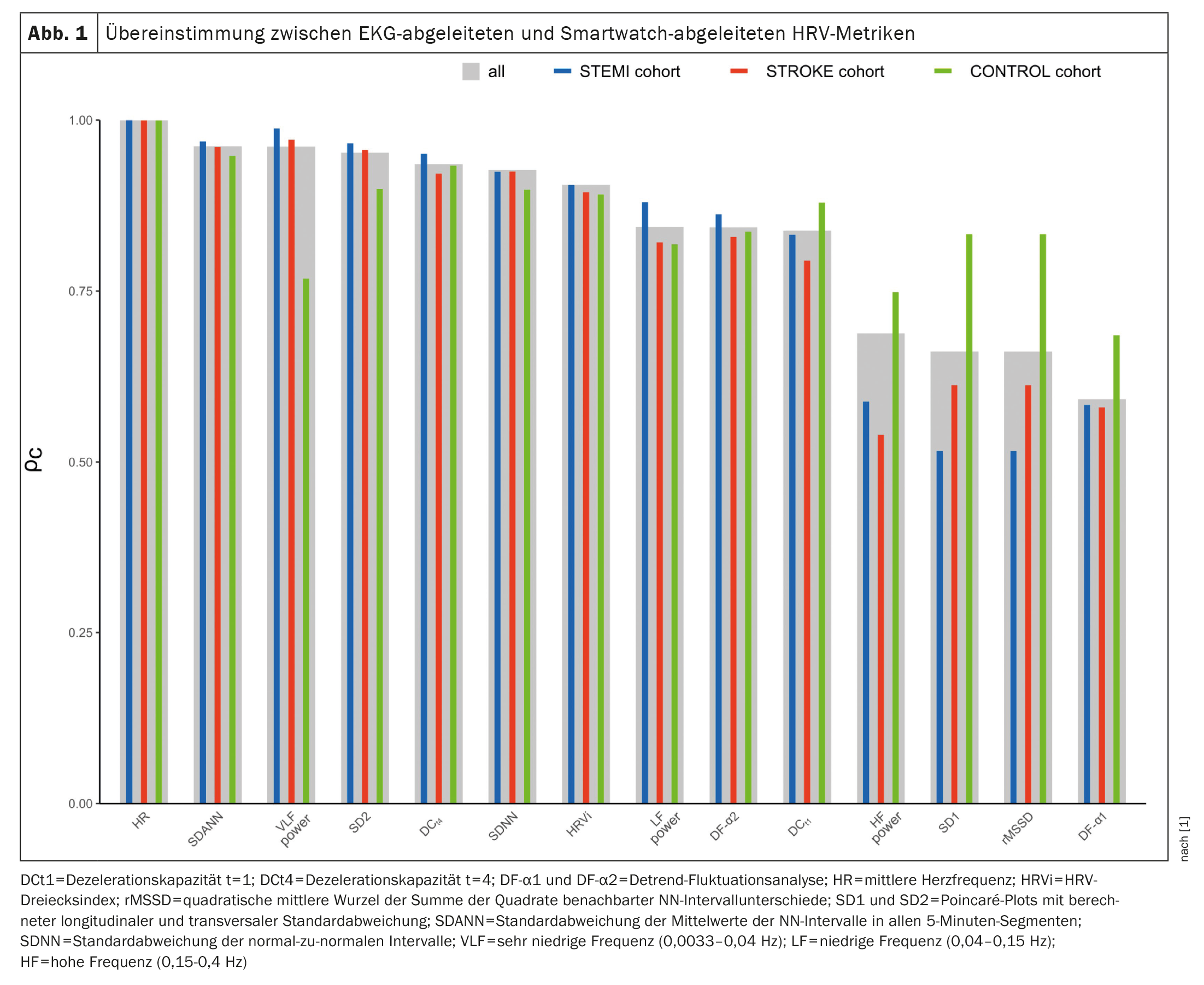
A concordância entre as medições do PPG e do ECG foi avaliada utilizando o coeficiente de correlação de concordância de Lin (ρc), o coeficiente de correlação intraclasse (ICC; modelo de efeitos mistos de duas vias), o erro absoluto médio (MAE), o erro percentual absoluto médio (MAPE) e gráficos de Bland-Altman com vieses calculados e limites de concordância (LoA). As concordâncias entre as métricas de VFC derivadas do ECG e do PPG são apresentadas na Figura 1 [1]. As concordâncias mais elevadas foram observadas para a frequência cardíaca média (ρc=0,9998), SDANN (ρc=0,9617), potência VLF (ρc = 0,9613) e SD2 (ρc=0,9523). Em contrapartida, SD1 (ρc=0,6617), rMSSD (ρc=0,6617) e DF-α1 (ρc=0,5919) apresentaram a menor concordância. Para a potência de RF, as concordâncias SD1, rMSSD e DF-α1 foram inferiores nas coortes STEMI e STROKE em comparação com os controlos. Para todos os outros marcadores, as concordâncias foram semelhantes entre as três coortes. Os coeficientes de correlação intraclasse variaram entre 0,6318 para DF-α1 e 0,9998 para a frequência cardíaca média. A concordância foi classificada como excelente para sete (50%), boa para três (21%), moderada para quatro (29%) e má para nenhum dos marcadores. Não foi possível observar qualquer desvio sistemático, com desvios próximos de zero em todas as análises. Foi encontrada uma concordância quase perfeita para VLF e SD2, enquanto DCt4, SDNN, SDANN, HRVi e DF-α2 apresentaram uma concordância considerável. Em contrapartida, apenas foi encontrado um baixo nível de concordância para rMSSD e SD1.
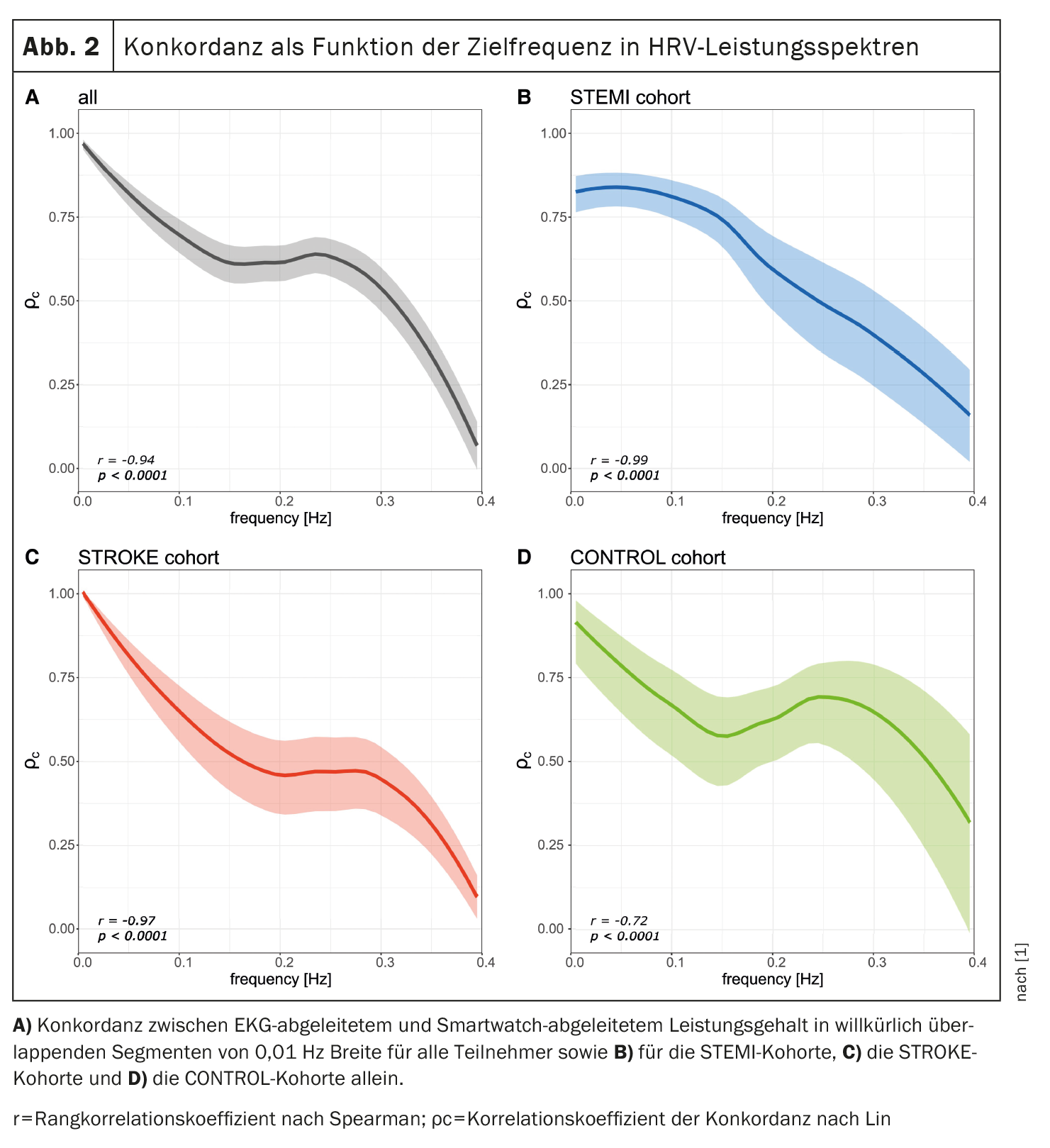
Além disso, a concordância entre o conteúdo de potência derivado do ECG e do PPG em bandas de frequência arbitrariamente sobrepostas foi calculada para avaliar uma possível relação entre a frequência espetral da VFC e a respectiva concordância. Como mostrado na Figura 2 [1], foi observada uma relação inversa entre a frequência espetral da VFC e a concordância entre as métricas de VFC derivadas do ECG e do PPG (r=-0,94, p<0,0001). Esta tendência foi observada nas três coortes.
Os parâmetros de FC derivados do smartwatch oferecem uma alternativa prática
Em resumo, o estudo fornece provas suficientes de que o cálculo dos marcadores de HRV a partir do sinal PPG de um smartwatch é possível em condições de repouso. A concordância entre a VFC derivada do smartwatch e a VFC derivada do ECG de alta resolução é excelente para parâmetros de baixa frequência, mas apenas moderada para métricas de alta frequência, especialmente em pacientes com doença cardio ou cerebrovascular conhecida. São necessários estudos futuros para validar estes resultados em situações reais.
Literatura:
- Theurl F, et al.: Smartwatch-derived heart rate variability: a head-to-head comparison with the gold standard in cardiovascular disease. European Heart Journal 2023; doi: https://doi.org/10.1093/ehjdh/ztad022.
- Task Force of the ESC: Heart rate variability standards of measurement, physiological interpretation, and clinical use. Circulation 1996; 93:1043-1065.
- Corr P, et al: Mechanisms Controlling Cardiac Autonomic Function and Their Relation to Arrhythmogenesis (Mecanismos que controlam a função autonómica cardíaca e a sua relação com a arritmogénese). Nova Iorque: Raven Press; 1986.
- Lown B, Verrier RL: Atividade neural e fibrilhação ventricular. N Engl J Med 1976; 294: 1165-1170.
- Kleiger RE, et al: Diminuição da variabilidade da frequência cardíaca e sua associação com o aumento da mortalidade após enfarte agudo do miocárdio. Am J Cardiol 1987; 59: 256-262.
- Adamson PB, et al: Avaliação autonómica contínua em doentes com insuficiência cardíaca sintomática: valor prognóstico da variabilidade da frequência cardíaca medida por um dispositivo de ressincronização cardíaca implantado. Circulation 2004; 110: 2389-2394.
- Gerritsen J, et al.: A função autonómica prejudicada está associada a um aumento da mortalidade, especialmente em indivíduos com diabetes, hipertensão ou história de doença cardiovascular: o estudo Hoorn. Diabetes Care 2001; 24: 1793-1798.
- Yperzeele L, et al: Variabilidade da frequência cardíaca e sensibilidade dos barorreceptores no AVC agudo: uma revisão sistemática. Int J Stroke 2015; 10: 796-800.
- Sassi R, et al: Advances in heart rate variability signal analysis: joint position statement by the e-Cardiology ESC Working Group and the European Heart Rhythm Association co-endorsed by the Asia Pacific Heart Rhythm Society. Europace 2015; 17: 1341-1353.
- Peng CK, et al.: Quantificação de expoentes de escala e fenómenos de cruzamento em séries temporais não estacionárias de batimentos cardíacos. Chaos 1995; 5: 82-87.
- Richman JS, Moorman JR: Análise de séries temporais fisiológicas utilizando a entropia aproximada e a entropia da amostra. Am J Physiol Heart Circ Physiol 2000; 278: H2039-H2049.
- Huikuri HV, et al: Anormalidades na dinâmica batimento a batimento da frequência cardíaca antes do início espontâneo de taquiarritmias ventriculares com risco de vida em pacientes com enfarte do miocárdio prévio. Circulation 1996; 93: 1836-1844.
- Bauer A, et al: Deceleration capacity of heart rate as a predictor of mortality after myocardial infarction: cohort study. Lancet 2006; 367: 1674-1681.
- Schmidt G, et al: Heart-rate turbulence after ventricular premature beats as a predictor of mortality after acute myocardial infarction. Lancet 1999; 353: 1390-1396.
- Vescio B, et al.: Comparação entre a deteção fotopletismográfica eletrocardiográfica e de pulso do lóbulo da orelha para avaliar a variabilidade da frequência cardíaca em indivíduos saudáveis em registros de curto e longo prazo. Sensores (Basileia) 2018; 18: 844.
- Hernando D, et al.: Validação do apple watch para medições da variabilidade da frequência cardíaca durante o relaxamento e o stress mental em indivíduos saudáveis. Sensores (Basileia) 2018; 18:2619.
- Miller DJ, Sargent C, Roach GD: Uma validação de seis dispositivos portáteis para estimar o sono, a frequência cardíaca e a variabilidade da frequência cardíaca em adultos saudáveis. Sensors (Basileia) 2022; 22: 6317.
CARDIOVASC 2023; 22(3): 46-48