Não só devido à sua elevada mortalidade, a endocardite infecciosa requer um tratamento abrangente. É necessária uma estreita cooperação interdisciplinar para alcançar os melhores resultados possíveis.
A endocardite infecciosa é uma doença complexa associada a uma elevada mortalidade. Uma estreita cooperação interdisciplinar, especialmente entre cardiologistas, infectologistas, radiologistas e cirurgiões cardíacos, é necessária para assegurar o melhor tratamento possível. A publicação de novos artigos, melhorias nas técnicas de imagem e discrepâncias entre as anteriores directrizes europeias e americanas levaram a que as directrizes europeias fossem actualizadas em 2015 [1]. Este artigo resume estas directrizes.
Prevenção
As indicações para a profilaxia da endocardite já eram restritas há alguns anos. As actividades diárias, tais como escovar os dentes, causam uma bacteremia repetitiva e fraca, que presumivelmente representa um risco mais elevado para o desenvolvimento de endocardite do que a bacteremia rara no decurso de uma intervenção (dentária) [2]. Assume-se, portanto, que a profilaxia de endocardite antibiótica só é capaz de prevenir um pequeno número de casos de endocardite, se houver algum. A profilaxia da endocardite é, portanto, agora apenas recomendada para pacientes com maior risco de aquisição e para um curso desfavorável de endocardite. Segundo as directrizes europeias, trata-se de doentes com válvulas protéticas ou com válvulas reconstruídas (se for utilizado material protético), doentes submetidos a endocardite ou doentes com cianose, cuidados paliativos ou viciação congénita corrigidos por material estranho (durante 6 meses após a intervenção) [1]. As directrizes suíças recomendam ainda a profilaxia para pacientes com um defeito do septo ventricular, um botalli de ducto persistente ou para pacientes com viciação valvar em corações transplantados. Enquanto as directrizes europeias prevêem apenas a profilaxia antes dos procedimentos dentários, na Suíça também se recomenda a profilaxia antes de certos procedimentos sobre as vias gastrointestinais, urogenitais e respiratórias [3].
Diagnóstico
Clínica, microbiologia (especialmente culturas de sangue) e ecocardiografia são as pedras angulares no diagnóstico da endocardite. Além disso, outras técnicas de imagem podem fornecer informações importantes.
Clínica: O quadro clínico da endocardite é variável e depende do a.o. Os resultados dependem do agente patogénico e das várias características do doente. O sintoma mais comum é a febre, que ocorre em até 90% dos casos. Um sopro cardíaco pode ser auscultado em até 85% dos casos. As complicações embólicas são encontradas em cerca de 25% dos doentes no momento do diagnóstico [1]. Os clássicos estigmas periféricos de origem vascular (por exemplo, lesões de Janeway, hemorragias de farpas) e imunológica (por exemplo, nódulos de Osler, manchas de Roth) tornaram-se mais raros, uma vez que são v.a. estão presentes nos casos subagudos e hoje em dia os pacientes tendem a apresentar-se na fase aguda da endocardite.
Microbiologia: Se houver suspeita de endocardite, pelo menos três pares de culturas de sangue devem ser colhidos de veias periféricas a intervalos de 30 minutos antes de se iniciar a antibioticoterapia. Em quase 1/3 dos casos de endocardite, estas culturas de sangue são negativas. A razão mais comum para isto é a terapia antibiótica anterior. Em tais situações, é indicado um período de tempo sem antibióticos com subsequente repetição da colheita de cultura de sangue, se justificável do ponto de vista clínico. Outras causas de hemoculturas iniciais negativas são fungos, e bactérias difíceis de cultivar ou intracelulares (por exemplo, Coxiella burnetii, Bartonella spp., Brucella spp.). No caso de hemoculturas iniciais negativas e suspeita persistente de endocardite, as culturas em meios especiais, exames serológicos ou testes de “reacção em cadeia da polimerase” podem contribuir para o diagnóstico [4]. Se for realizada uma cirurgia numa válvula infectada, o exame microbiológico do material ressecado é de importância diagnóstica.
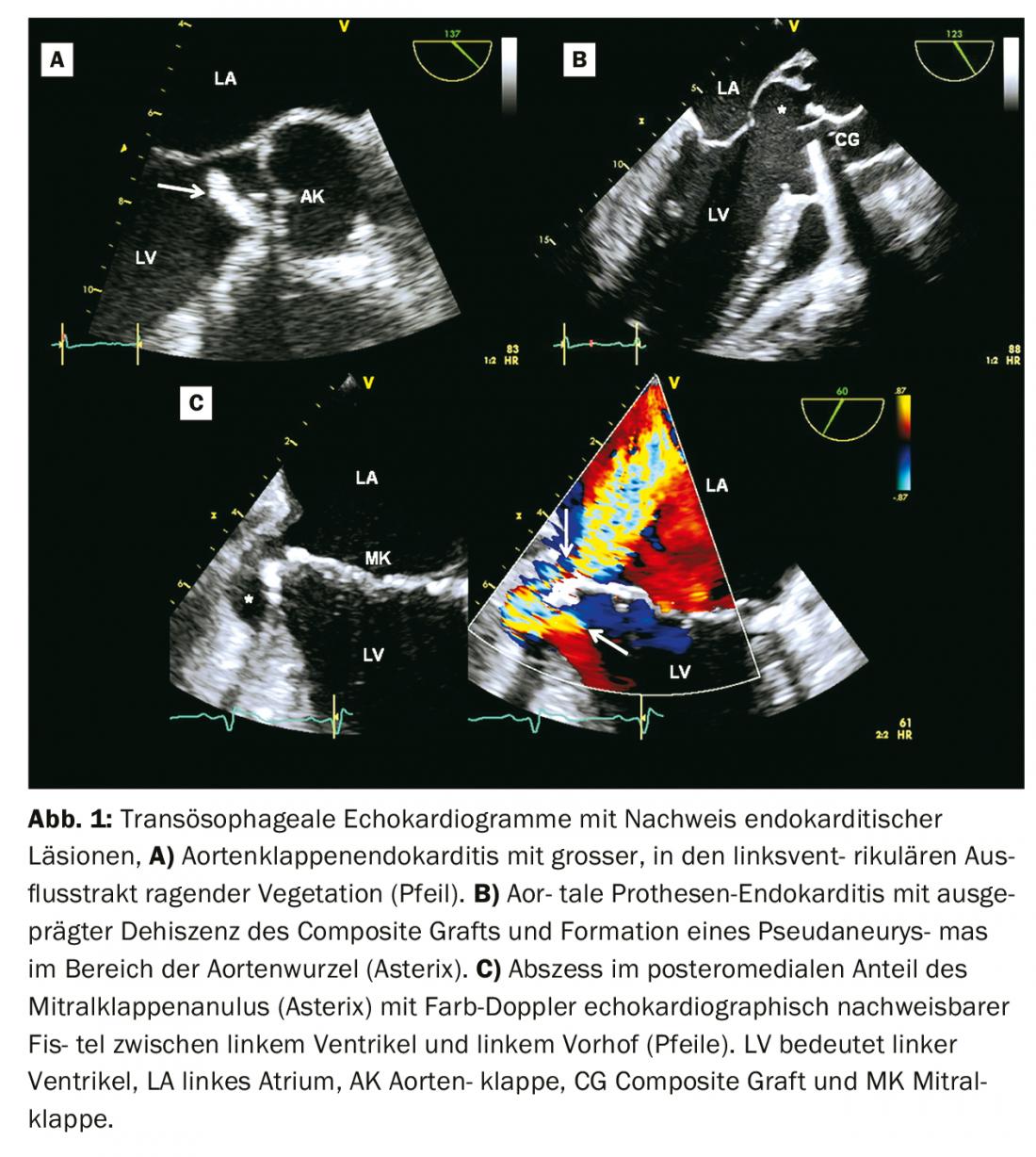
Ecocardiografia: A ecocardiografia é a imagem de eleição para a suspeita de endocardite [5]. Em regra, um ecocardiograma transtorácico (TTE) é realizado em primeiro lugar. Um ecocardiograma transoesofágico (ETE) é normalmente indicado como seguimento, excepto em casos de ETE negativo e clinicamente baixa suspeita de endocardite. De acordo com os critérios da Duke, bem como de acordo com os critérios de diagnóstico modificados das directrizes europeias, as vegetações, complicações paravalvulares (abcesso, pseudaneurismas, fístulas) ou uma nova deiscência de uma prótese valvar são considerados critérios ecocardiográficos principais para a endocardite (Fig. 1, Tab. 1) [1,6]. No esquema de diagnóstico modificado das directrizes europeias, as insuficiências de válvulas recentemente detectadas já não são consideradas um sinal de diagnóstico, enquanto que as perfurações e aneurismas de válvulas são considerados critérios principais (Tabela 1) [1].

A sensibilidade para o diagnóstico de vegetações usando TTE é de 70% para válvulas nativas e 50% para válvulas protéticas. Para o ETE, os valores correspondentes são 96 e 92%. A especificidade é de cerca de 90% para ambas as modalidades [5]. A sensibilidade para o diagnóstico de abcessos em TTE é de 50% e em TEE 90% [5].
Se a avaliação ecocardiográfica inicial não revelar quaisquer resultados diagnósticos e persistir uma elevada suspeita clínica de endocardite, recomenda-se uma repetição da TTE e TEE após 5-7 dias [1]. Além disso, devem ser consideradas imagens suplementares nestas situações, especialmente em casos ecocardiográficos difíceis, tais como pacientes com válvulas protéticas ou com dispositivos electrónicos intracardíacos.
Outras modalidades de imagem: A tomografia computorizada cardíaca (TC) pode ser útil no diagnóstico de complicações paravalvulares (Tab. 1) [1], especialmente na endocardite protética. A TC é também adequada para detectar complicações extracardíacas de endocardite (por exemplo, lesões isquémicas devido à embolização de uma vegetação, abcessos). A ressonância magnética (RM) é particularmente adequada para a detecção de lesões cerebrais. As lesões cerebrais são comuns e são geralmente embolicamente isquémicas por natureza. Mesmo pacientes neurologicamente inconspícuos apresentam lesões na ressonância magnética em pelo menos 50% dos casos [7]. No esquema de diagnóstico modificado das directrizes europeias, as lesões paravalvulares na TC cardíaca são consideradas critérios principais e as complicações vasculares detectadas por imagem (TC ou MRI) são consideradas critérios menores (Quadro 1) [1].
As técnicas de imagiologia nuclear, tais como o 18F-FDG PET/CT ou o leucócito SPECT/CT, também podem ser úteis em casos de diagnóstico difícil. De acordo com dados recentes, estes exames podem melhorar a precisão diagnóstica da endocardite em válvulas protéticas e dispositivos intracardíacos [8]. No entanto, ao avaliar por 18F-FDG PET/CT, a cirurgia de válvula deve ter tido lugar há pelo menos 3 meses, uma vez que a actividade metabólica não específica na área da prótese é possível pouco tempo após a cirurgia. SPECT/CT é mais específica do que 18F-FDG PET/CT na detecção de endocardite [9]; contudo, é uma tecnologia de imagem complexa e demorada.
No esquema de diagnóstico modificado das directrizes europeias, a detecção de actividade peri-protética anormal na imagiologia nuclear é considerada um critério importante (Tab. 1) [1].
Terapia
Terapia antibiótica: A terapia antibiótica é administrada por via intravenosa. A duração depende do agente patogénico e da complexidade da endocardite. Nas válvulas nativas, recomenda-se a terapia empírica inicial com amoxicilina 6 × 2 até se obterem resultados microbiológicos. g i.v., gentamicina 3 mg/kg i.v. e fluocloxacilina 6 × 2 g i.v. diariamente, em válvulas nativas e alergia à penicilina com vancomicina 2 × 15 mg/kg i.v. e gentamicina 3 mg/kg i.v. diariamente e para válvulas protéticas com vancomicina 2 × 15 mg/kg i.v., gentamicina 3 mg/kg i.v. e rifampicina 2 × 450 mg p.o. diariamente são recomendados [1].
Indicações cirúrgicas: A insuficiência cardíaca é a complicação mais comum e a causa de morte mais comum na endocardite [10]. A infecção com Staphylococcus aureus aumenta o risco de insuficiência cardíaca. Desde que não existam comorbilidades graves, é normalmente indicado um procedimento cirúrgico precoce (Tab. 2) [1].
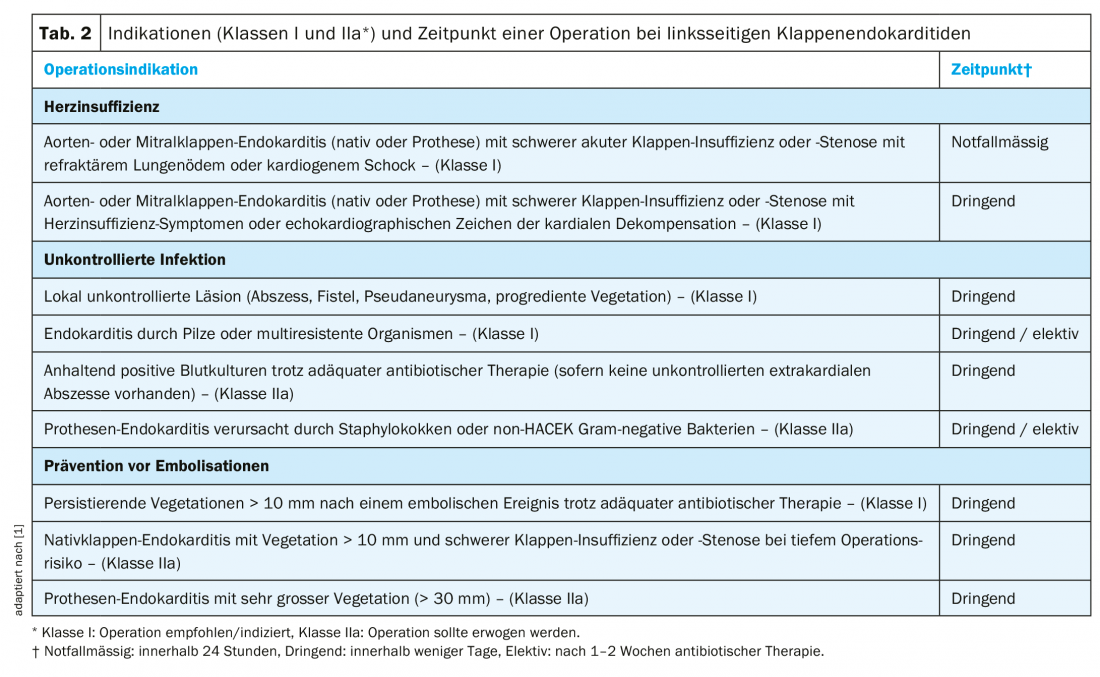
A segunda causa mais comum de intervenção cirúrgica para endocardite é e infecção não controlada (Tab. 2) [1,10]. Na maioria dos casos, isto deve-se a uma extensão paravalvular da infecção (abcesso, pseudoaneurisma, fístula). As indicações clínicas de uma complicação paravalvular são febre persistente ou novo bloqueio atrioventricular de início.
Outra complicação temida que pode levar à cirurgia das válvulas é a embolização sistémica da vegetação (Quadro 2) [1]. Os eventos embólicos ocorrem em 20-50% dos doentes com endocardite. Contudo, o risco de novos eventos sob terapia antibiótica adequada é menor (6-21%) e fortemente decrescente após a 1ª semana sob antibióticos [11,12]. O tamanho e a mobilidade da vegetação são factores de risco importantes para a embolização (Tab. 2) [1,11,12].
Complicações neurológicas: As complicações neurológicas sintomáticas ocorrem em cerca de 15-30% dos doentes com endocardite [13]. Um insulto cerebral está associado ao aumento da mortalidade. O diagnóstico rápido e o início de uma terapia antibiótica adequada são de grande importância para a prevenção de complicações neurológicas na endocardite [12]. Após um primeiro insulto isquémico, a cirurgia cardíaca necessária (Tab. 2) não está contra-indicada e não deve ser atrasada se o dano neurológico não for grave [14]. No caso de uma hemorragia cerebral relevante, por outro lado, pelo menos uma hemorragia deve ser tratada. esperar 1 mês antes de ser submetido a cirurgia cardíaca [15].
Infecção de dispositivos electrónicos intracardíacos: A endocardite associada a um pacemaker ou desfibrilador é frequentemente um desafio de diagnóstico e está associada a uma elevada mortalidade [1,16]. O tratamento envolve geralmente terapia antibiótica prolongada (geralmente 4-6 semanas) e remoção completa do corpo estranho [1]. Se possível, os eléctrodos devem ser removidos transvenalmente [17]. Ao implantar um dispositivo electrónico intracardíaco, recomenda-se a profilaxia antibiótica de rotina, geralmente com uma cefalosporina i.v. (que começa 1 hora antes da implantação, administrada durante 24-36 horas), [18].
Mensagens Take-Home
- A profilaxia da endocardite é agora apenas recomendada para doentes cardíacos de alto risco que se encontrem em maior risco de contrair endocardite e pela sua evolução desfavorável.
- A ecocardiografia é a imagem de eleição no diagnóstico da endocardite. Em primeiro lugar, é realizado um TTE; geralmente seguido por um TTE, excepto no caso de um TTE negativo e clinicamente baixa suspeita.
- Uma TC cardíaca, 18F-FDG PET/CT ou SPECT/CT pode ser útil como imagem complementar, especialmente se houver suspeita de endocardite protética ou associada a um dispositivo.
- Indicações para cirurgia são endocardite complicada com sinais de insuficiência cardíaca, infecção descontrolada ou risco de embolia sistémica
- O insulto cerebrovascular isquémico não é uma contra-indicação e não deve atrasar a cirurgia cardíaca necessária na ausência de danos neurológicos graves
- No caso de endocardite associada a dispositivos, recomenda-se a remoção do corpo estranho e a antibioticoterapia prolongada.
Literatura:
- Habib G, Lancellotti P, Antunes MJ, et al: 2015 ESC Guidelines for the management of infective endocarditis: The Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC). Endossado por: Associação Europeia de Cirurgia Cardio-Torácica (EACTS), a Associação Europeia de Medicina Nuclear (EANM). Eur Heart J 2015; 36: 3075-3128.
- Lockhart B, Brennan MT, Sasser HC, et al: Bacteremia associada à escova de dentes e à extracção dentária. Circulação 2008; 117: 3118-3125.
- Flückiger U, Jaussi A: Directrizes suíças revistas para a profilaxia da endocardite. Medicina Cardiovascular 2008; 11: 392-400.
- Raoult D, Casalta JP, Richet H, et al: Contribuição dos testes serológicos sistemáticos no diagnóstico de endocardite infecciosa. J Clin Micro- biol 2005; 43: 5238-5242.
- Habib G, Badano L, Tribouilloy C, et al: Recomendações para a prática da ecocardiografia em endocardite infecciosa. Eur J Echocardiogr 2010; 11: 202-219.
- Li JS, Sexton DJ, Mick N, Nettles R, Fowler VG Jr, Ryan T, et al. Modi- ficação proposta aos critérios do Duque para o diagnóstico de endocardite infecciosa. Clin Infect Dis 2000; 30: 633-638.
- Hess A, Klein I, Iung B, et al: Resultados de ressonância magnética cerebral em doentes neurologicamente assintomáticos com endocardite infecciosa. Am J Neuroradiol 2013; 34: 1579-1584.
- Pizzi MN, Roque A, Fernández-Hidalgo N, et al: Improving the Diagnosis of Infective Endocarditis in Prosthetic Valves and Intracardiac Devices With 18F-Fluorodeoxyglucose Positron Emission Tomography/Computed Tomography Angiography: Initial Results at an Infective Endocarditis Referral Center. Circulação 2015; 132: 1113-1326.
- Rouzet F, Chequer R, Benali K, et al: Desempenho respeitoso de 18F-FDG PET e cintilografia de leucócitos radiomarcados para o diagnóstico de endocardite da válvula protética. J Nucl Med 2014; 55: 1980-1985.
- Tornos P, Iung B, Permanyer-Miralda G, et al: Infective endocarditis in Europe: lessons from the Euro heart survey. Coração 2005; 91: 571-575.
- Vilacosta I, Graupner C, San Roman JA, et al: Risco de embolização após instituição de terapia antibiótica para endocardite infecciosa. J Am Coll Cardiol 2002;39: 1489-1495.
- Dickerman SA, Abrutyn E, Barsic B, et al: The relationship between the initiation of antimicrobial therapy and the incidence of stroke in infective endocarditis: an analysis from the ICE Prospective Cohort Study (ICE- PCS). Am Heart J 2007; 154: 1086-1094.
- Garcia-Cabrera E, Fernandez-Hidalgo N, Almirante B, et al: Complicações neurológicas da endocardite infecciosa: factores de risco, resultado, e impacto da cirurgia cardíaca: um estudo observacional multicêntrico. Circulação 2013; 127: 2272-2284.
- Kang DH, Kim YJ, Kim SH, et al: Cirurgia precoce versus tratamento convencional para endocardite infecciosa. N Engl J Med 2012; 366: 2466-2473.
- Yoshioka D, Sakaguchi T, Yamauchi T, et al: Impacto do tratamento cirúrgico precoce no resultado neurológico pós-operatório de endocardite infecciosa activa complicada por enfarte cerebral. Ann Thorac Surg 2012; 94: 489-495.
- Nof E, Epstein LM: Complicações dos implantes cardíacos: infecções dos dispositivos de manipulação. Eur Heart J 2013; 34: 229-236.
- Sohail MR, Uslan DZ, Khan AH, et al: endocardite infecciosa complicando o marcapasso permanente e a infecção por cardioversor-desfibrilador implantável. Mayo Clin Proc 2008; 83: 46-53.
- Klug D, Balde M, Pavin D, et al: Factores de risco relacionados com infecções de pacemakers implantados e cardioversores-desfibrilhadores: resultados de um grande estudo prospectivo. Circulação 2007; 116: 1349-1355.
CARDIOVASC 2019; 18(4): 4-7