Até agora, os testes moleculares no cancro do pulmão de células não pequenas (NSCLC) têm sido reservados principalmente para doentes em fase IV. No entanto, com a introdução de terapias específicas também em fases iniciais do tumor, isto poderá mudar em breve – uma grande oportunidade que, no entanto, também coloca muitos desafios para a prática clínica diária.
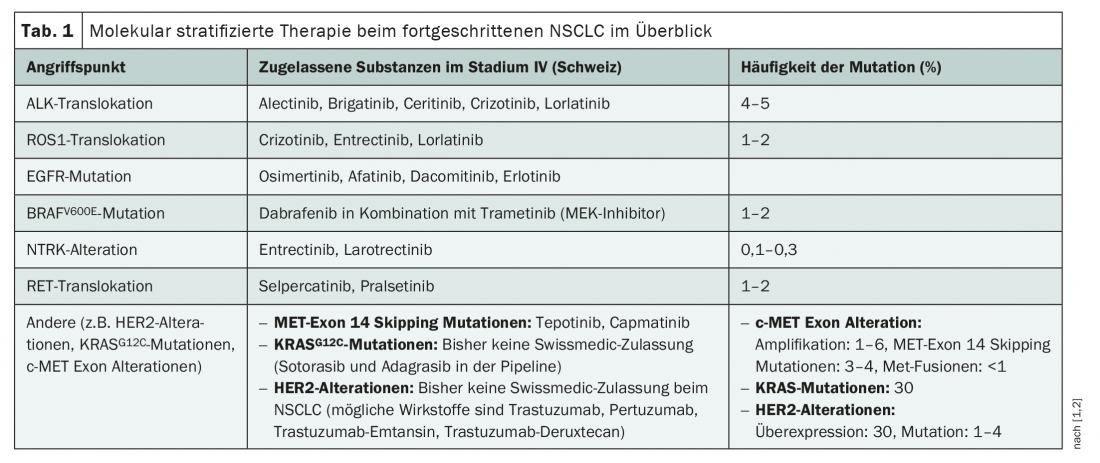
Com terapias que visam especificamente ROS1, ALK, EGFR, BRAF, mas também TRK e RET, já existem numerosas opções de tratamento direccionadas para o NSCLC (separador 1). Contudo, com excepção do osimertinibe inibidor do EGFR, estes só foram até agora aprovados na Suíça para o tratamento de tumores localmente avançados e metastáticos [1]. Assim, um diagnóstico de mutações relevantes para a terapia só é recomendado na fase IV antes do início da terapia de primeira linha [2]. Em qualquer caso, as translocações ALK, mutações BRAFV600E, mutações EGFR exon 18-21, fusões NTRK, translocações RET e translocações ROS1 devem ser registadas [2] – porque existem conceitos terapêuticos aprovados para estas alterações. No entanto, a terapia orientada no NSCLC está a sofrer rápidas mudanças, e com ela os testes moleculares. Por um lado, isto poderia ser expandido num futuro próximo com objectivos adicionais, uma vez que existem algumas substâncias novas no pipeline. Por outro lado, os fármacos oncológicos alvo estão cada vez mais a ser testados para uso neoadjuvante e adjuvante em fases iniciais do tumor – com sucesso, como evidenciado pela recente aprovação do osimertinib no contexto do adjuvante. A consequência lógica: a classificação dos tumores moleculares já poderia ser útil para os tumores da fase I-III.
Outros pontos de ataque à vista
Actualmente, para além das bem conhecidas, há muitas outras mutações do condutor em foco. Num futuro próximo, por exemplo, poderá haver aprovação de vários agentes-alvo dirigidos contra o HER2 ou KRAS, entre outros. Apenas em Abril e Junho deste ano, respectivamente, foram lançados no mercado suíço os inibidores altamente específicos MET capmatinib e tepotinib para o tratamento de NSCLC metastásico com um receptor MET tirosina quinase exon 14, saltando a mutação [1]. Esta alteração genética afecta até 3-4% dos pacientes NSCLC e está associada a um prognóstico desfavorável [2].
No ensaio VISION pivotal, que incluiu 152 pacientes na sua maioria pré-tratados com mutação MET exon 14 saltando, o tepotinib resultou numa taxa de resposta objectiva de 44,7% com uma sobrevida mediana sem progressão (PFS) de 8,9 meses [1]. No caso do capmatinibe, a taxa de resposta objectiva no ensaio pivotal GEOMETRY mono-1 foi de 67,9%, e a PFS mediana foi de 9,69 meses. Faltam ainda mais dados sobre a sobrevivência global e a comparação da eficácia com o tratamento padrão de imunochemoterapia. O que já é certo é que os testes para o MET exon 14 saltando mutações irão provavelmente expandir o padrão de diagnóstico no futuro.
As mutações KRAS e as aberrações HER2 também poderiam em breve ser acrescentadas ao diagnóstico molecular no NSCLC. Embora ainda não tenham sido aprovadas terapias específicas para estes alvos na Suíça, há muita coisa a acontecer na calha. Por exemplo, o soterasib e o adagrasib foram os primeiros inibidores KRASG12C a serem desenvolvidos e encontram-se actualmente em ensaios clínicos. Foi apresentado um pedido de autorização de introdução no mercado da UE para o soterasib e espera-se que seja ainda este ano, e a US Food and Drug Administration (FDA) já concedeu aprovação preliminar para o tratamento de pacientes pré-tratados com a mutação KRASG12C [3,4]. Cerca de 13% dos pacientes NSCLC poderiam beneficiar de um lançamento no mercado – é assim que a mutação KRASG12C é comum [3]. No ensaio fase II CodeBreak 100, 124 pacientes pré-tratados com mutação KRASG12C mostraram uma taxa de resposta de 37,1% ao sororasib com uma PFS mediana de 6,8 meses e uma OS mediana de 12,5 meses [5]. Em contraste com o KRAS, agentes como o trastuzumab, pertuzumab e o anti-corpo conjugado trastuzumab emtansine e trastuzumab deruxtecan já existem para visar o HER2. Embora a sua utilização esteja a ser investigada em alguns ensaios clínicos no NSCLC, não tem havido comparações directas com a imunochemoterapia nem aprovação Swissmedic para o NSCLC até à data [1,2].
Terapia adjuvante e neoadjuvante em transição
Para além de expandir a caracterização molecular do NSCLC, a sua importância em fases anteriores do tumor poderia também aumentar. Osimertinib faz o início. Este ano, o inibidor EGFR foi aprovado na Suíça para o tratamento adjuvante de pacientes com NSCLC não sequencial com EGFR exon 19 supressões ou exon 21 (L858R) mutações de substituição após ressecção tumoral completa [1]. Isto foi baseado no ensaio ADAURA, no qual a terapia adjuvante durante três anos nas fases II e IIIA após ressecção R0 levou a uma melhoria significativa na sobrevivência sem doenças em comparação com placebo (HR 0,17; p<0,001) [2]. A maioria dos participantes no estudo também recebeu quimioterapia adjuvante. A nova opção de tratamento adjuvante orientado significa esperança para os pacientes NSCLC com mutação EGFR – e requer uma selecção apropriada de pacientes.
É provável a aprovação de outros agentes-alvo no cenário adjuvante e neoadjuvante. Assim, tornam-se necessárias estratégias justas e uniformes de testes moleculares. Embora muitas directrizes ainda não incluam uma recomendação para análise molecular nas fases I-III do tumor, as directrizes do National Comprehensive Cancer Networks (NCCN) e o Asian Thoracic Oncology Research Group, as recomendações do Consenso Canadiano, as directrizes chinesas para o diagnóstico e tratamento do cancro do pulmão primário e o Consenso da Society for Translational Medicine recomendam pelo menos o teste EGFR. Isto faz sentido não só em vista da nova opção terapêutica, mas também porque as mutações EGFR são as chamadas mutações trunculares: Estão presentes desde o início, a sua prevalência dificilmente muda de fase para fase. Para além dos inibidores EGFR, inibidores ALK como o alectinibe estão actualmente a ser testados em neoadjuvant, adjuvant e terapia de manutenção do NSCLC. As directrizes ficarão provavelmente sempre um pouco atrás destes desenvolvimentos – e a sua implementação na prática clínica diária levará, por sua vez, algum tempo. Isto torna ainda mais importante avaliar cada paciente individualmente e, tendo em conta as numerosas novas possibilidades, pensar fora da caixa de estruturas entrincheiradas.
Fonte: Aggarwal C, et al.: Molecular testing in stage I-III non-small cell lung cancer: Approaches and challenges. Cancro do pulmão. 2021; 162: 42-53.
Literatura:
- Informação sobre drogas Swissmedic: www.swissmedicinfo.ch (último acesso em 25.11.2021).
- Griesinger F, et al: Directrizes da Onkopedia: Cancro do pulmão, célula não pequena (NSCLC). Estado Julho 2021. www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html (último acesso 25.11.2021).
- Whitlock Burton K: A FDA aprova o Sotorasib como primeira terapia orientada para NSCLC com mutações KRAS G12C. 03.06.2021. www.univadis.de (último acesso em 25.11.2021).
- DGHO: Pedido de amostras NUB Sotorasib 2021/2022. www.dgho.de (último acesso em 25.11.2021).
- Skoulidis F, et al: Sotorasib para Cancros Pulmonares com Mutação KRAS p.G12C. New England Journal of Medicine. 2021; 384(25): 2371-2381.
InFo ONcOLOGIA & HaEMATOLOGIA