“Quanto mais baixo melhor” – a abordagem de baixar os níveis de colesterol tanto quanto possível em doentes em risco cardiovascular é mais relevante do que nunca, de acordo com a actualização das directrizes suíças AGLA e as novas directrizes ESC/ESA. De facto, uma redução do LDL-C em 1 mmol/l reduz o risco de eventos cardiovasculares em um quinto. No entanto, tais reduções de LDL são difíceis em alguns pacientes. Além disso, surgem as questões: Quando consultar o especialista e quando fazer um trabalho genético?
“Quanto mais baixo melhor” – a abordagem de baixar os níveis de colesterol tanto quanto possível em doentes em risco cardiovascular é mais relevante do que nunca, de acordo com a actualização das directrizes suíças AGLA e as novas directrizes ESC/ESA. De facto, uma redução do LDL-C em 1 mmol/l reduz o risco de eventos cardiovasculares em um quinto. No entanto, tais reduções de LDL são difíceis em alguns pacientes. Além disso, surgem as questões: Quando consultar o especialista e quando fazer um trabalho genético?
A dislipidemia é uma das principais causas de doenças cardiovasculares. O enfoque é particularmente no colesterol LDL (“colesterol lipoproteico de baixa densidade”). Vários estudos realizados nas últimas décadas mostram claramente que a redução das concentrações de LDL-C está associada a um menor risco de eventos cardiovasculares [1,2]. As causas da dislipidemia são múltiplas. Segundo a Fundação Suíça para o Coração, a hipercolesterolemia familiar (FH) afecta cerca de uma em cada 200 pessoas neste país [3]. Por exemplo, cerca de 30% dos pacientes mais jovens com doença coronária (CHD) ou enfarte do miocárdio têm FH [4]. Além disso, sabe-se que o estilo de vida e doenças como o hipotiroidismo, doenças hepáticas, obesidade, insuficiência renal crónica, diabetes mellitus insuficientemente controlada ou os efeitos secundários de certos medicamentos (por exemplo, antivirais) têm por vezes uma influência considerável nas alterações do metabolismo das gorduras. Estes factores de risco significam que hoje em dia cerca de uma em cada três pessoas na Suíça tem um perfil lipídico desfavorável [5].

Embora tenham passado apenas alguns anos desde a publicação das últimas directrizes da Sociedade Europeia de Cardiologia (ESC) e da Sociedade Europeia de Aterosclerose (EAS) sobre o tratamento da dislipidemia em 2016, um grande número de novas descobertas científicas e o desenvolvimento de novas opções terapêuticas tornaram necessária a actualização das directrizes [6]. Estas novas “Orientações ESC/EAS para a gestão das dislipidemias” apresentadas em 2019 foram revistas e adaptadas no ano seguinte pelo Grupo de Trabalho sobre Lípidos e Aterosclerose (AGLA), com vista à sua aplicação na Suíça [7,8]. O objectivo deste resumo é informar os médicos de clínica geral sobre as directrizes actualizadas e ajudá-los a decidir quando encaminhar que pacientes para um especialista.
Avaliação de risco
Não há dúvida de que níveis elevados de choles-te-rin estão associados ao aumento do risco cardiovascular. A avaliação dos factores de risco é uma componente central do cálculo do risco. Por exemplo, não só o nível de lípidos é decisivo, mas também a duração da exposição [6]. De acordo com as directrizes ESC/EAS, são classificadas quatro categorias de risco diferentes, nomeadamente muito alto, alto, moderado e baixo risco (visão geral 1).
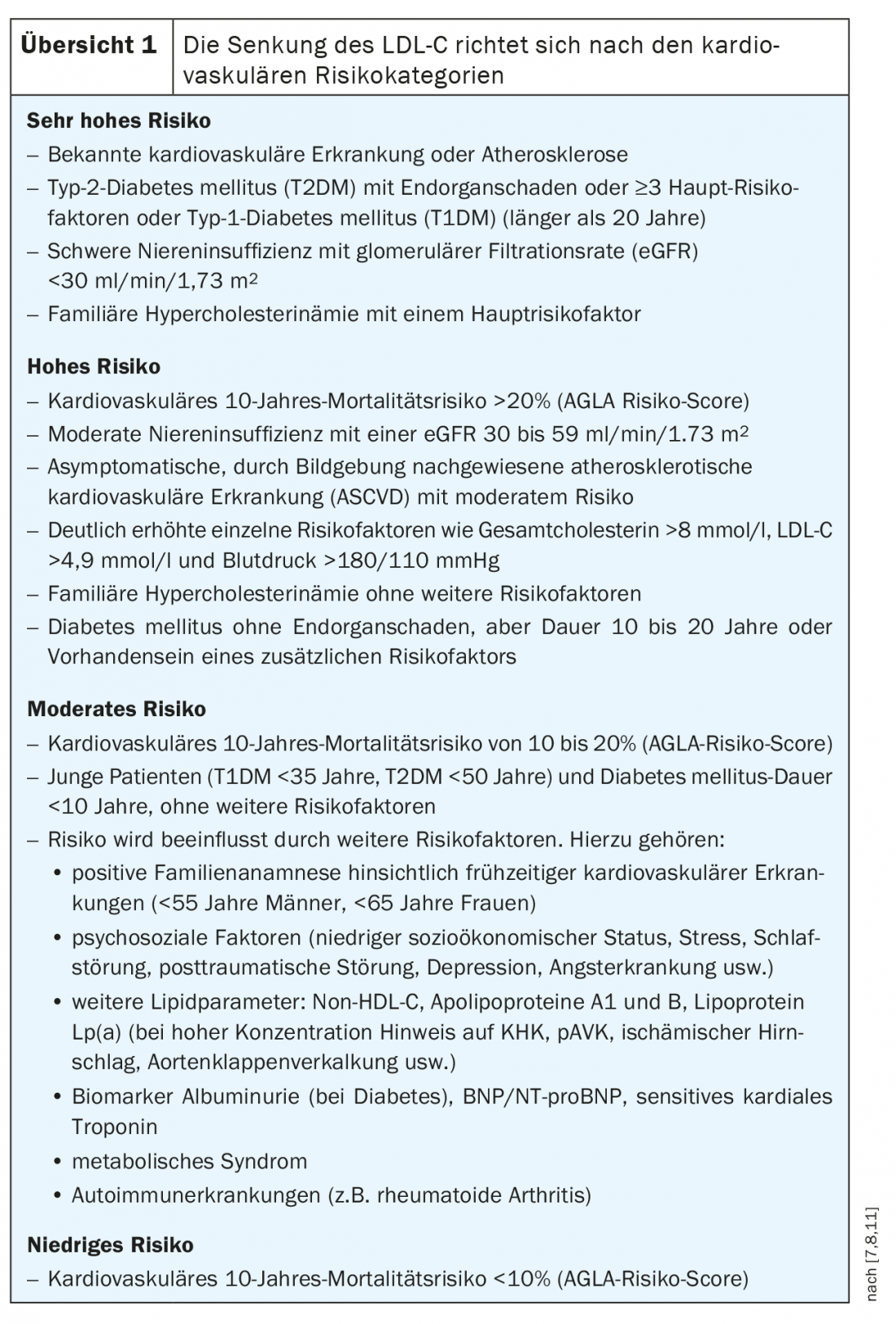
Na Suíça, foi criada a calculadora de risco AGLA para o cálculo do risco individual. Pode ser utilizado em linha para calcular facilmente o risco absoluto durante dez anos de um evento coronário fatal ou de um enfarte do miocárdio não fatal (www.agla.ch/de/rechner-und-tools/agla-risikorechner) [8]. A calculadora AGLA tem em conta parâmetros tais como idade, história familiar, tabagismo, tensão arterial, colesterol LDL, colesterol HDL ou níveis de triglicéridos. No entanto, a actividade física, radioterapia, etc., não são tidas em conta.
O ESC/EAS-SCORE também pode ser utilizado para estimar o risco de 10 anos de mortalidade cardiovascular (www.scores.bnk.de/esc.html). A Suíça é considerada uma região com baixo risco cardiovascular, pelo que é utilizada a “variante de baixo risco ESC-SCORE”.
Para a prevenção primária, a AGLA recomenda a avaliação inicial do risco em homens assintomáticos com mais de 40 anos de idade e mulheres com mais de 50 anos. Se o risco for baixo, deve ser reavaliado de cinco em cinco anos, e se o risco for moderado, deve ser reavaliado de dois em dois ou de cinco em cinco anos. Para as pessoas que já apresentam um risco elevado ou muito elevado na avaliação inicial, não é necessária uma estimativa com uma calculadora de risco, uma vez que estes pacientes são automaticamente classificados como pacientes de alto risco. Isto aplica-se a:
- Doenças cardiovasculares documentadas (por exemplo, enfarte do miocárdio ou síndrome coronária aguda, 2-doenças com pelo menos uma oclusão da artéria coronária). 50% de estenose na TC cardíaca, acidente vascular cerebral isquémico, doença arterial periférica (DVPA) ou história de revascularização coronária/arterial).
- Diabetes mellitus com danos nos órgãos terminais, longa duração da doença ou pelo menos 3 factores de risco
- insuficiência renal moderada a grave (grau KDIGO ≥3)
- Factores de risco individuais pronunciados (LDL-C >4,9 mmol/l, colesterol total >8 mmol/l, pressão arterial >180/110 mmHg)
- hipercolesterolemia familiar
- Forte aumento da lipoproteína Lp(a)
Modificadores de risco
Para pacientes com risco baixo e especialmente moderado, foram recentemente introduzidos critérios adicionais de avaliação de risco como potencial instrumento complementar. Estes “modificadores de risco” podem ajudar a ajustar a estimativa do risco cardiovascular. Os pacientes que se encontram efectivamente numa categoria de risco inferior podem então ser colocados num nível de risco mais elevado. Tais modificadores incluem:
- Privação social, stress psicossocial, esgotamento vital, doenças psiquiátricas graves
- Imagem cardiovascular não invasiva: Medição da pontuação da artéria coronária de cálcio (CAC) na TC cardíaca (pontuação CAC, pontuação Agatston), sonografia da artéria femoral e artéria carótida para detecção da placa (IIbB).
- História familiar positiva de doença cardiovascular precoce (homens <55 anos, mulheres <60 anos).
- Iactividade física, obesidade (medida pelo índice de massa corporal ou medida da circunferência abdominal).
- Doença inflamatória imunológica crónica mediada
- Tratamento para a infecção pelo VIH
- Fibrilação atrial
- Hipertrofia ventricular esquerda
- Insuficiência renal crónica
- Síndrome da apneia obstrutiva do sono
- Fígado gordo não-alcoólico
- Lipoproteína Lp(a)
Valores-alvo LDL-C
Existe uma associação significativa entre a redução do colesterol LDL e a redução do risco cardiovascular [10]. Por esta razão, as novas orientações do CES (e correspondentemente as actuais orientações do AGLA) foram além das recomendações das orientações anteriores ao formularem os novos objectivos de redução do LDL-C. Em princípio, o LDL-C deve ser baixado o mais baixo possível (“quanto mais baixo, melhor”), especialmente no caso de alto e muito alto risco. Quanto maior for o risco cardiovascular, mais baixos serão os valores-alvo (Tab. 1) .
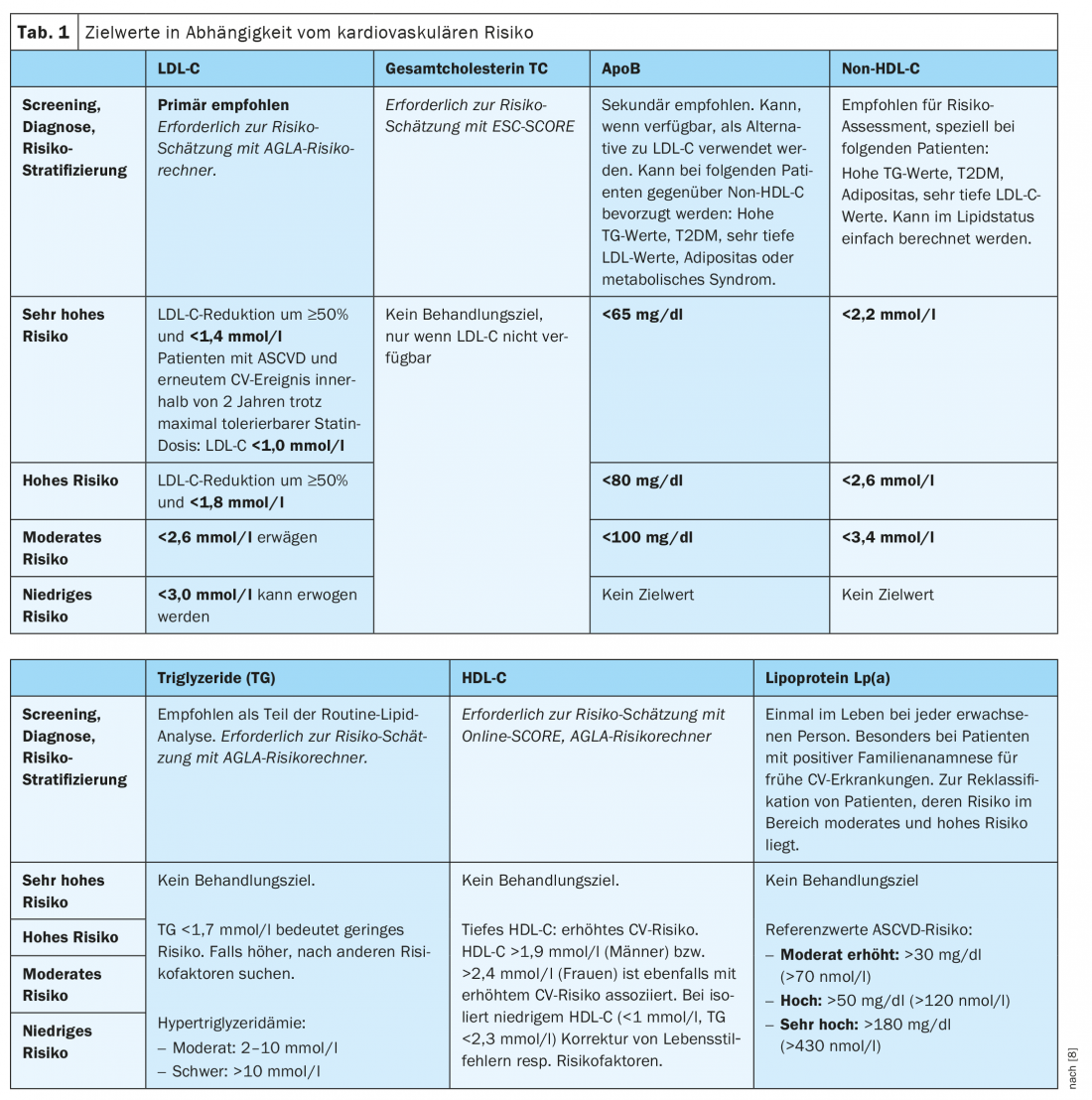
Os doentes com risco muito elevado devem visar uma redução de 50% do LDL-C e um valor-alvo de LDL-C de <1,4 mmol/l. Além de uma redução de 50%, recomenda-se um valor-alvo de <1,8 mmol/l para risco elevado e <2,6 mmol/l para risco moderado. Finalmente, um nível de baixo risco de <3,0 mmol/l pode ser visado. Os pacientes com FH com ASCVD ou outro factor de risco são considerados de risco muito elevado (ver abaixo). De acordo com a AGLA, o estado lipídico do plasma sem jejum é suficiente para avaliação na maioria dos casos. No entanto, a recolha de sangue em jejum é recomendada nas seguintes situações:
- Síndrome metabólico
- Triglicéridos sem jejum >5 mmol/l
- Conhecida hipertriglicéridosemia
- Após a hipertrigliceridemia induzida pela pancreatite
- Antes de iniciar a terapia medicamentosa com hipertrigliceridemia grave como um possível efeito secundário
- Se forem necessárias análises adicionais que tenham de ser determinadas em jejum, por exemplo, glicose em jejum, monitorização de medicamentos terapêuticos
Hipercolesterolemia familiar
Se o perfil lipídico mostrar perturbações significativas, FH pode também estar presente. As pessoas afectadas por colesterol LDL geneticamente elevado têm um risco cardiovascular muito maior do que os pacientes com LDL adquirido ao mesmo nível [8]. Por exemplo, em FH, o risco de 10 anos de enfarte do miocárdio sem tratamento é superior a 50%. Indicações de FH para adultos são CHD em homens com menos de 55 anos ou mulheres com menos de 60 anos. Além disso, recomenda-se uma clarificação para níveis elevados de colesterol, nomeadamente um colesterol total de ≥8mmol/l ou LDL ≥5.0 mmol/l ou triglicéridos ≥5.0 mmol/l (crianças/adolescentes correspondentemente mais baixos). A aterosclerose prematura ou, nos menores de 45 anos, os xantomas tendinosos ou arcus cornealis, bem como a hiperlipidemia genética noutros membros da família, poderiam também indicar FH. Se houver suspeita de FH, isto deve ser esclarecido de acordo com os “Dutch Lipid Clinic Network Criteria” (www.agla.ch/de/rechner-und-tools/agla-fh-rechner). Se a suspeita for confirmada, deve ser tratada como “alto risco” e com um factor de risco adicional como “muito alto risco”. A FH deve ser diagnosticada clinicamente se possível e confirmada geneticamente, e o rastreio familiar dos doentes com FH é indicado. Se a mutação for detectada, a aderência à terapia é muitas vezes melhorada.
Terapia
O tratamento da dislipidemia depende do risco cardiovascular global e dos valores-alvo de LDL para os pacientes com base nisso. A base de tal terapia é uma mudança no estilo de vida, especialmente com ajustamento dietético, redução do consumo de álcool, mais exercício, perda de peso e cessação do tabagismo. Se a redução lipídica for necessária para além de atingir o objectivo terapêutico de acordo com a categoria de risco, as estatinas são os fármacos de primeira escolha. Isto significa: Na primeira fase, são utilizadas estatinas altamente eficazes na dose máxima tolerável. Se os valores alvo ainda não forem atingidos, recomenda-se a combinação com o inibidor de absorção do colesterol ezetimibe. Se houver uma intolerância à estatina, o ezetimibe também deve ser considerado. Um inibidor PCSK9 pode ser utilizado para além de ezetimibe.
Se os pacientes com risco muito elevado não atingirem o seu objectivo terapêutico apesar da dose máxima de estatina mais ezetimibe, podem ser tratados adicionalmente com um inibidor PCSK9 na prevenção primária. Uma combinação com um tal anticorpo PCSK9 também pode ser considerada para doentes com risco muito elevado na prevenção secundária, nomeadamente quando o objectivo terapêutico não é atingido apesar da estatina máxima tolerável mais ezetimibe. Para pacientes com FH em risco muito elevado e tratamento falhado com a maior dose de estatina mais ezetimibe, sugere-se também uma combinação com um inibidor PCSK9. No futuro, outras substâncias tornar-se-ão disponíveis, tais como o ácido bempedóico (inibidor da liase do citrato de ATP, apenas eficaz no fígado), Inclisiran (uma molécula de siRNA que inibe os anticorpos PCSK9) ou ANGPTL3 em doentes com triglicéridos elevados.
Os medicamentos mais importantes para a redução de lipídios
Com terapia intensiva com estatinas, é possível reduzir as concentrações de LDL em mais de 50%, e com terapia moderada em mais de 30 a 50%. A intensidade desta redução depende, por um lado, das estatinas utilizadas (atorvastatina, rosuvastatina e pitavastatina são consideradas estatinas potentes) e, por outro lado, da dosagem e da predisposição genética do doente. Por exemplo, uma grande meta-análise mostrou que a redução do LDL-C em 1 mmol/l reduz o risco relativo de eventos cardiovasculares em 22% ao longo de cinco anos [2]. Os estatinas também reduzem os triglicéridos em 10 a 20%, mas aumentam o HDL apenas ligeiramente (1 a 10%). A concentração de Lp(a), por outro lado, não é, ou é apenas muito ligeiramente influenciada. Os efeitos secundários do tratamento com estatina podem incluir miopatia, miosite e rabdomiólise. Tais sintomas musculares normalmente começam algumas semanas após o início da terapia. Além disso, especialmente em pacientes mais idosos, o risco de desenvolvimento de diabetes mellitus tipo 2 é ligeiramente aumentado com doses elevadas de estatinas [11]. Se o risco de hemorragias também aumenta ligeiramente, ainda não foi provado sem margem para dúvidas. Aconselha-se cautela com as interacções. Algumas estatinas reagem com certos medicamentos, tais como imunossupressores, inibidores da protease HIV, macrolídeos, antifúngicos azole, benzodiazepinas ou antagonistas do cálcio.
Os inibidores de absorção do colesterol são também ferramentas importantes para a redução da gordura no sangue. Ezetimibe bloqueia a absorção do colesterol no intestino, baixando os níveis de LDL em cerca de 18,5%. Ezetimibe actua via Niemann-Pick proteína C1 (NPC1L1), mas não reduz a absorção de alimentos lipossolúveis.
Os triglicéridos também são reduzidos, nomeadamente em 8%, enquanto que há um aumento mínimo no HDL [12]. A combinação de ezetimibe com estatinas tem demonstrado reduzir ainda mais os eventos cardiovasculares. Os efeitos secundários mais comuns de uma tal terapia combinada são dores de cabeça, dores musculares e um aumento das transaminases GOT e GPT.
A redução da concentração de PCSK9 (proteína convertase subtilisina/kexina tipo 9) promove a expressão dos receptores LDL e, portanto, a absorção de LDL pelas células hepáticas. Isto leva a uma redução significativa dos níveis de LDL-C de cerca de 60%, em combinação com a dose máxima de estatinas em até 73% [6]. A concentração de triglicéridos e Lp(a) também é reduzida em cerca de um quarto, enquanto o nível HDL aumenta ligeiramente. Os inibidores PCSK9 (evolocumab, alirocumab) mostram uma redução significativa do risco cardiovascular devido a estes efeitos. São indicados na Suíça para pacientes com risco cardiovascular muito elevado cujas alterações alimentares e tratamento LDL com estatinas na dose máxima tolerada (com ou sem ezetimibe) não conduziram à consecução dos valores-alvo. Além disso, a pressão arterial deve ser controlada e, no caso da diabetes mellitus, o valor de HbA1c deve ser <8% e a abstinência de nicotina deve ser procurada. A obtenção de uma consulta da seguradora de saúde sobre os custos é obrigatória.
Para prevenção secundária, são elegíveis para tratamento com inibidores PCSK9: pacientes de alto risco com eventos cardiovasculares isquémicos ateroscleróticos e um LDL-C de >2,6 mmol/l, adultos com FH heterozigótico e – para evolocumab – adultos e adolescentes com 12 anos ou mais com FH homozigótico. Na prevenção primária, os inibidores PCSK9 são indicados em doentes adultos e adolescentes de alto risco com 12 anos ou mais com FH heterozigotos graves ou homozigotos e um LDL-C de >5,0 mmol/l. Há também uma indicação para pacientes com FH heterozigótico grave, um LDL-C de >4,5 mmol/l e pelo menos um dos seguintes factores de risco: diabetes mellitus, Lp(a) >120 nmol/l ou hipertensão grave.
O diagnóstico e prescrição inicial, bem como os controlos regulares, devem ser efectuados por um especialista FMH em angiologia, diabetologia/endocrinologia, cardiologia, nefrologia, neurologia ou por especialistas designados em hipercolesterolemia. O tratamento com inibidores PCSK9 só deve ser continuado se for bem sucedido. Isto significa que, num check-up dentro de seis meses após o início do tratamento, o LDL-C deveria ter sido reduzido em pelo menos 40% do valor de base sob a terapia de redução de lípidos maximamente intensificada ou um valor LDL de <1,8 mmol/l deveria ter sido alcançado. Isto não se aplica a pessoas com FH homozigotos.
Mensagens Take-Home
- O LDL-C é uma das principais causas para o desenvolvimento de doenças cardiovasculares.
- Em pacientes com risco cardiovascular muito elevado, a terapia intensiva deve visar uma redução de 50% no CLDL e um valor-alvo de CLDL de <1,4 mmol/l; em pacientes de alto risco, uma redução de 50% e um valor-alvo de <1,8 mmol/l também deve ser visado. Deve-se notar que a duração da exposição à hipercolesterolemia é também crucial.
- Se os níveis alvo não forem atingidos com estatinas e ezetimibe na dose máxima tolerável durante pelo menos três meses, os inibidores PCSK9 devem ser utilizados em doentes com risco cardiovascular muito elevado.
- Os doentes com hipercolesterolemia familiar e pelo menos um factor de risco cardiovascular são considerados de alto risco. Devem também ser tratados intensivamente (estatinas, ezetimibe e inibidores PCSK9) com um LDL-C >5,0 mmol/l ou >4,5 mmol/l mais outros factores de risco.
- O encaminhamento para um especialista deve ser feito se a terapia intensiva com LDL falhar, para pacientes de alto ou muito alto risco, ou para pacientes com hipercolesterolemia familiar, ou se determinados factores de risco cardiovascular estiverem presentes.
- No caso da hipercolesterolemia familiar, o rastreio familiar é obrigatório e recomenda-se a clarificação genética.

Literatura:
- Carballo D, Mach F: Redução intensiva do colesterol LDL e inibição da inflamação para reduzir ainda mais o risco cardiovascular. Medicina Cardiovascular 2018; 21(12): 310-315.
- Baigent C, et al.: Colaboração de Trialistas de Tratamento do Colesterol: Eficácia e segurança de uma redução mais intensiva do colesterol LDL: uma metanálise dos dados de 170.000 participantes em 26 ensaios aleatorizados. Lancet 2010; 376: 1670-1681.
- www.swissheart.ch/de/herzkrankheiten-hirnschlag/erkrankungen/familiaere-hypercholesterinaemie.html.
- Rodondi N: Os pacientes devem ser examinados para a hipercolesterolemia familiar no consultório médico? Swiss Med Forum 2014; 14(19): 377.
- www.swissheart.ch.
- Riesen WF et al: Novas directrizes para a dislipidemia ESC/EAS. Swiss Medical Forum 2020; 20(9-10): 140-148.
- Mach F, et al: 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. European Heart Journal 2019; doi: 10.1093/eurheartj/ehz455.
- AGLA: Prevenção da Aterosclerose Foco na Dislipidemia 2020; www.agla.ch.
- Weingärtner O, et al: Comentário sobre as directrizes ESC/EAS (2019) sobre o diagnóstico e tratamento das dislipidemias. Cardiologista 2020; 14: 256-266.
- McCormack T, et al: Níveis muito baixos de LDL-C podem proporcionar com segurança um benefício cardiovascular clínico adicional: as provas até à data. Int J Clin Pract 2016; 70(11): 886-897; doi: 10.1111/ijcp.12881.
- Sattar N, et al: Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials. 2010 Fev 27; 375(9716): 735-742.
- Pandor A, et al: monoterapia Ezetimibe para a redução do colesterol em 2.722 pessoas: revisão sistemática e meta-análise de ensaios controlados aleatórios. J Intern Med 2009; 265(5): 568-580; doi: 10.1111/j.1365-2796.2008.02062.x.
PRÁTICA DO GP 2021; 16(10): 9-13