Até 30 por cento das pessoas afectadas pela psoríase vulgar também têm artrite. A terapia da artrite psoriásica depende do tipo de manifestação. Para tal, estão disponíveis várias substâncias imunomoduladoras, que são utilizadas por fases.
A artrite psoriásica (PsA), pela sua natureza progressiva e destrutiva, pode levar a limitações significativas na função e qualidade de vida. Em 1964, a PsA foi reconhecida como uma doença por direito próprio pela Associação Americana de Rheumatismo.
20-30% dos doentes afectados pela psoríase vulgar também sofrem de artrite. A incidência é de cerca de 3-8/100.000 [1]. PsA ocorre normalmente durante ou após o envolvimento cutâneo. Contudo, pode também manifestar-se antes da psoríase cutânea ou mesmo sem psoríase (psoríase senoidal). Neste caso, o diagnóstico é feito com base no padrão de infestação e nas alterações radiológicas típicas. A gravidade da psoríase cutânea não está correlacionada com o envolvimento das articulações.
Clínica
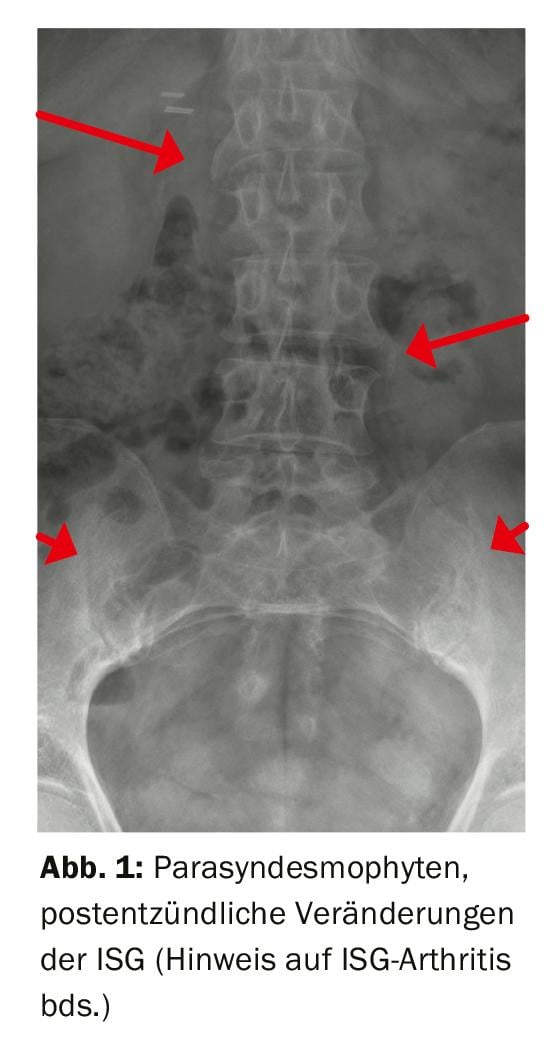
O quadro de PsA é muito heterogéneo e é classificado por Moll e Wright [2] em cinco formas, variando desde a poliartrose simétrica, a oligartrose assimétrica que afecta algumas articulações, até à rara artrite mutilante. Uma afecção isolada das articulações interfalangeais distais (DIP), frequentemente acompanhada por uma afecção psoriásica das unhas, ou uma afecção por radiação em que MCP, PIP e DIP dos dedos das mãos ou dos pés individuais são afectados, é particularmente típica e pode ser facilmente distinguida de uma artrite reumatóide para ser considerada como um diagnóstico diferencial. No entanto, em casos de envolvimento transversal das articulações DIP, a diferenciação da poliartrose dos dedos (artrose de Heberden) pode ser difícil. Em 20% dos doentes, é detectada uma afecção axial, frequentemente uma artrite unilateral de uma articulação sacroilíaca ou uma espondilite (Fig. 1), o que explica a classificação da PsA como um tipo de espondilo-artrose. Outras manifestações típicas de doenças músculo-esqueléticas em PsA são os enthesitides (inflamação dos tendões e ligamentos) e os dactilídeos (inflamação tipo salsicha dos dedos das mãos ou dos pés individuais). As manifestações extra-articulares incluem a uveíte e a doença inflamatória intestinal. Mais de metade dos doentes com psA são afectados por pelo menos uma comorbidade, doença cardiovascular mais comum, síndrome metabólica, e depressão e distúrbios de ansiedade. A inflamação sistémica, mediada por células inflamatórias e citocinas, incluindo TNFα, leva a uma aterosclerose prematura através de uma inflamação vascular ligeira. Outras doenças associadas incluem a osteoporose e a esteatose hepática [3].
PsA está associado a genótipos complexos, com uma predisposição genética mais forte em PsA do que em psoriasis vulgaris. Os desencadeadores da doença podem ser factores ambientais (especialmente o tabagismo), stress, obesidade ou trauma. Este último é conhecido como o fenómeno de Köbner na psoríase vulgaris. De acordo com um estudo, o trauma local precede o desenvolvimento da artrite psoriásica em quase 25% dos pacientes [4]. O eixo IL23/IL17 desempenha um papel importante na patogénese da artrite psoriásica, com células auxiliares tipo 17 T produzindo citocinas pró-inflamatórias através da indução de IL23.
Diagnósticos
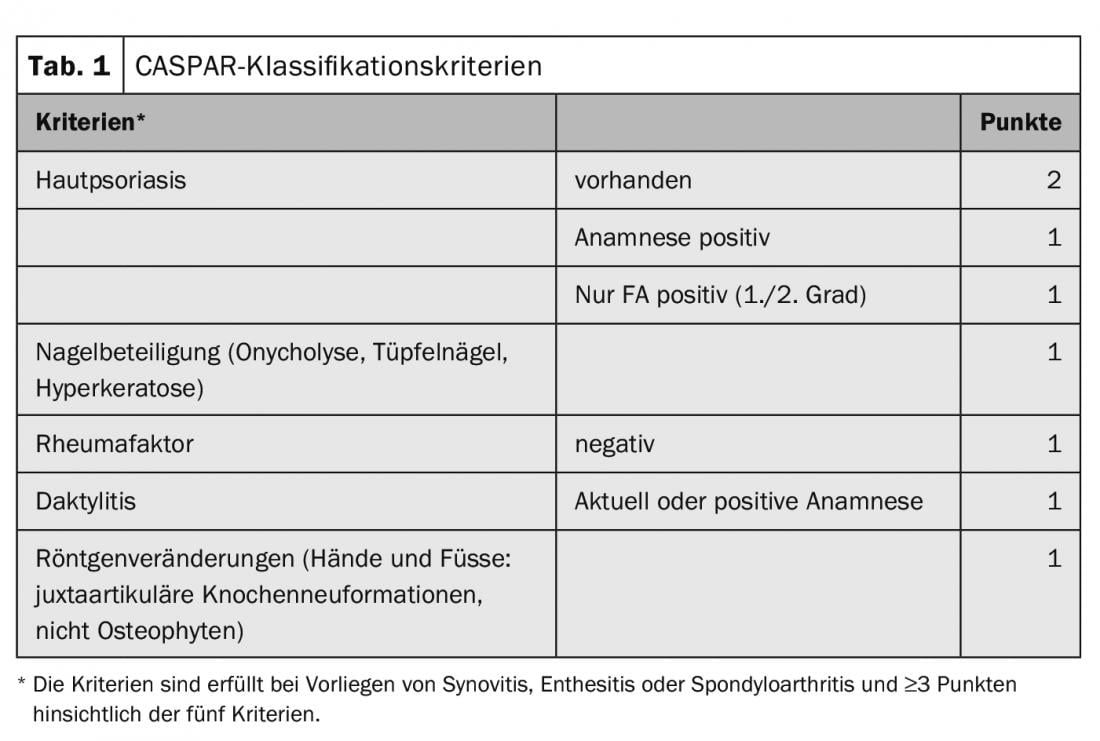
O diagnóstico precoce é importante para assegurar um tratamento atempado para prevenir sequelas e consequências socioeconómicas associadas. Um dos biomarcadores mais fortes para o desenvolvimento da PsA é a psoríase prevalecente. A pele e as unhas devem, portanto, ser examinadas de perto, não apenas nos locais típicos de predilecção, tais como os lados extensores das articulações afectadas: a linha do cabelo, os canais auditivos, o umbigo, a fenda da nádega, etc., devem também ser verificados. Observa-se uma forma especial de pustolosis palmo-plantar, especialmente na síndrome SAPHO, que está relacionada com a artrite psoriásica. Os critérios de classificação CASPAR (Tab. 1) [5] fornecem orientações para a realização de um diagnóstico.
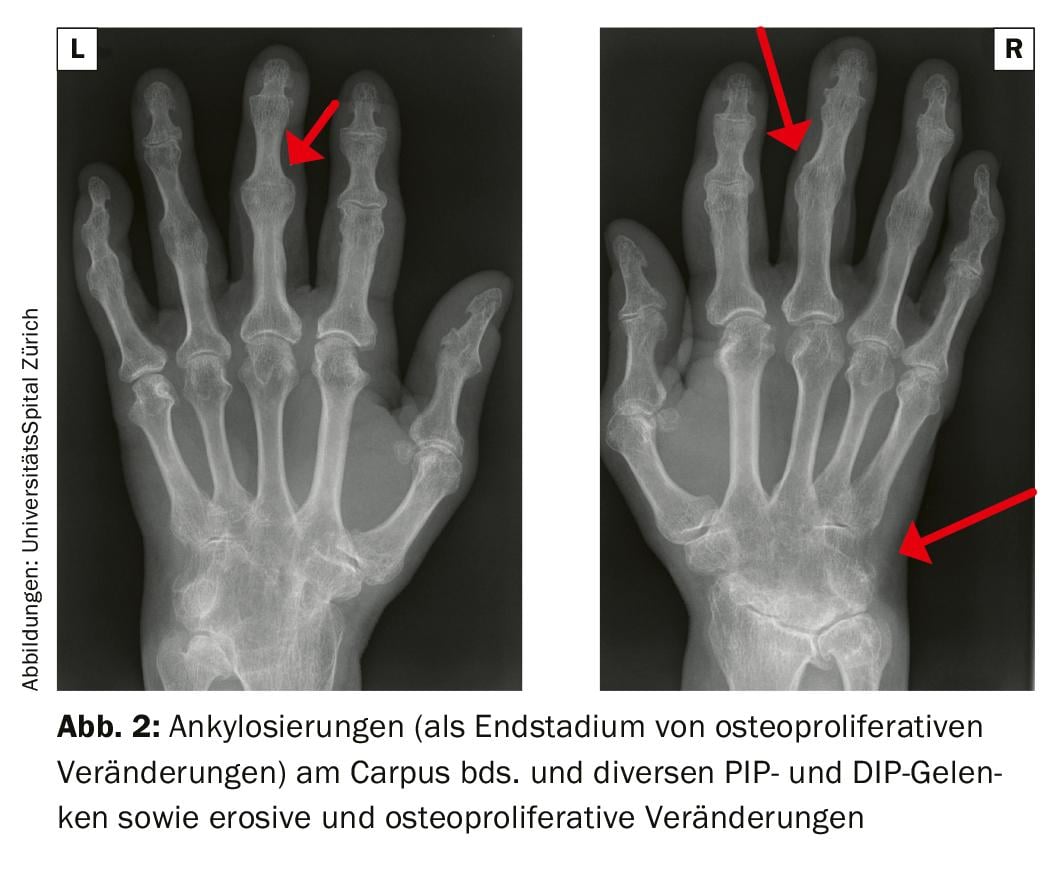
O quadro misto de erosões e neoplasias ósseas periosteais é típico na imagiologia. Na forma mutilante, podem ocorrer alterações até à acroosteólise (dissolução óssea dos elos do dedo do pé ou do pé) ou formações típicas de lápis na tampa devido à osteólise que aguça a falange média (Fig. 2 e 3) . As radiografias convencionais das mãos e dos pés, bem como da coluna e da pélvis, são recomendadas para determinar o local com uma pergunta sobre a destruição/osteoproliferações. A sonografia e, em alternativa, a ressonância magnética do esqueleto axial são adequadas para o diagnóstico alargado, por exemplo para diferenciar da artrite reumatóide, e para verificar a actividade da doença. No laboratório de reumatismo, são de esperar factores de reumatismo negativos, os anticorpos CPP podem ser positivos de baixo ponto. Uma característica genética positiva do HLA-B27 está associada ao envolvimento axial e à uveíte.
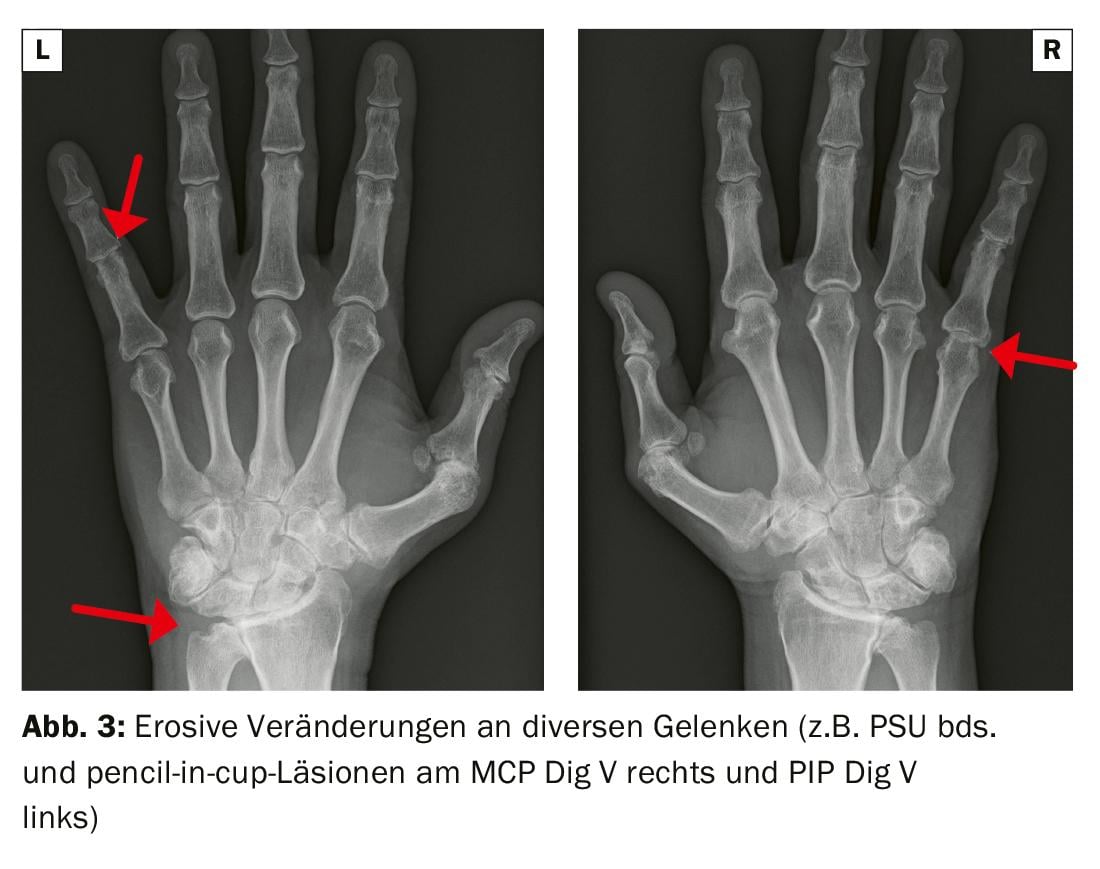
No entanto, nem todas as queixas músculo-esqueléticas na psoríase vulgar podem ser atribuídas per se à artrite psoriásica. Os diagnósticos diferenciais são outras doenças do grupo da espondilartrose, artrite reumatóide, artrite cristalina ou doenças degenerativas [6].
Terapia
Os conceitos de terapia orientada (“treat to target”) com controlo apertado que foram testados em artrite reumatóide também provaram ser válidos e eficazes em PsA para alcançar a remissão ou, se não possível, a actividade mínima da doença (MDA). Isto é medido através da pontuação da actividade, que é composta por vários paramaters, tais como actividade da doença, valores de inflamação e estado. Na prática clínica, os escores DAS 28 [7] e ASDAS [8] são particularmente comuns. Quanto mais cedo a terapia puder ser iniciada, mais cedo será alcançada uma remissão (“janela de oportunidade”).
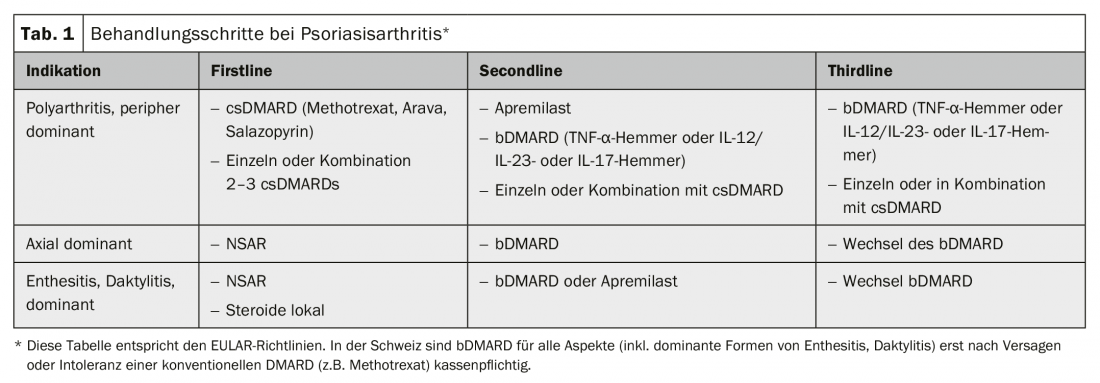
Estão disponíveis orientações terapêuticas actualizadas a partir de 2015 na Liga Europeia Contra o Reumatismo (EULAR) e no Grupo de Investigação e Avaliação da Psoríase e Artrite Psoriática (GRAPPA) [9]. As directrizes foram resumidas de uma forma simplificada nos quadros 2 e 3. A terapia é baseada no tipo de manifestação do PsA e é progressivamente alargada em função da gravidade da condição e da resposta à terapêutica imunomoduladora anterior. As recomendações das duas directrizes diferem ligeiramente, com a EULAR a considerar principalmente os aspectos reumatológicos e a GRAPPA a considerar tanto os aspectos reumatológicos como dermatológicos.
Os AINE são prescritos na fase inicial para dores articulares sem inchaço e sem envolvimento axial, e como terapia adjuvante quando necessário. Os esteróides são utilizados principalmente como terapia adjuvante localmente injectados e oralmente apenas de forma muito cautelosa.
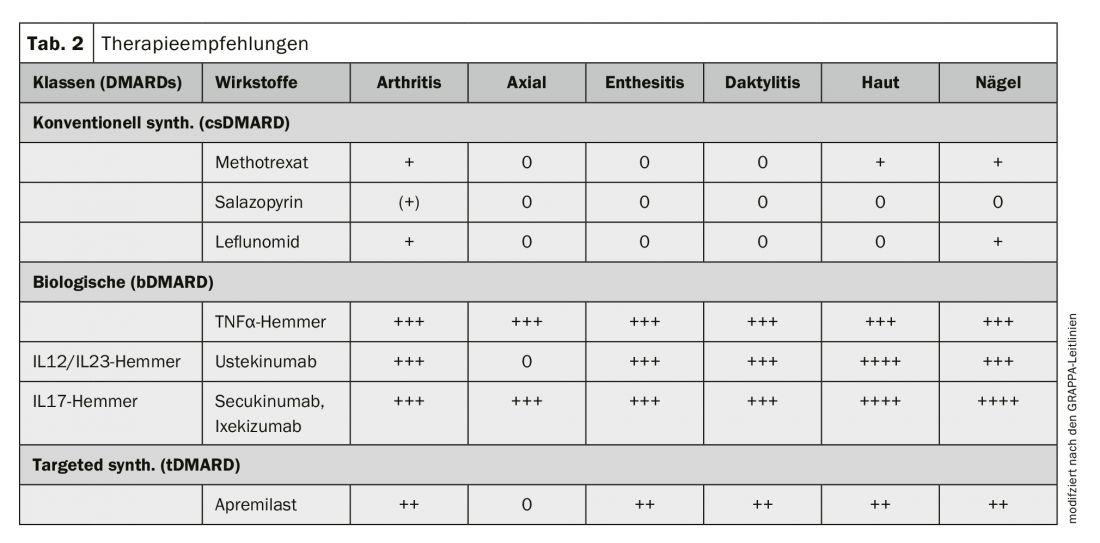
Os medicamentos anti-reumáticos modificadores da doença estão divididos em diferentes grupos. As preparações mais antigas e mais baratas – as chamadas substâncias modificadoras de doenças sintéticas convencionais – tais como metotrexato (de preferência subcutâneo), leflunomida (oralmente) ou sulfasalazina (oralmente) são utilizadas em primeiro lugar nos sinovírus, mas não são eficazes nas afecções axiais, entesitides e dactilídeos. Aqui, e em caso de falha de csDMARD, principalmente DMARD biológicos, são utilizados os inibidores TNFα (etanercept; adalimumab; golimumab; certolizumab pegol, todos s.c.; infliximab, por infusão) ou os novos inibidores da IL17 (secukinumab; ixekizumab, ambos s.c.) e inibidores da IL12/IL23 (ustekinumab, s.c. ou i.v.). Se o efeito estiver ausente ou for insuficiente, ou se o efeito for perdido, os bloqueadores TNFα ou classes de substâncias são alterados. O mais recente apremilast sintético de DMARD, uma terapia em comprimidos, é eficaz para a artrite, entesitides e dactilídeos, embora menos eficaz do que os biológicos. Além disso, não foi possível mostrar um efeito sobre a infestação do esqueleto axial.
Quaisquer comorbidades são também tidas em conta na escolha de uma terapia. TNFα inibidores, por exemplo, estão contra-indicados na esclerose múltipla, os inibidores da IL17A podem desencadear recaídas da doença de Crohn. Mais informações sobre as terapias e os necessários esclarecimentos preliminares e vacinas recomendadas sob imunossupressão podem ser encontradas no compêndio de medicamentos ou no website da Sociedade Suíça de Reumatologia (a partir de 6.12.18). Em desenvolvimento para o tratamento da artrite psoriásica estão o inibidor guselkumab IL23, já aprovado na Suíça para o tratamento da psoríase vulgar, o receptor A inibidor brodalumab IL17 e vários inibidores de Janus kinase. Entre outras coisas, espera-se a indicação de expansão do tofacitinibe, que já é utilizado em reumatologia para o tratamento da artrite reumatóide. Existem estudos sobre bimekizumab, um inibidor duplo de IL17A e IL17F (bimekizumab), sobre inibidores duplos de TNF-α e IL17A, bem como sobre compostos completamente novos [10].
Mensagens Take-Home
- 20-30% das pessoas afectadas pela psoríase vulgar também sofrem de artrite. A gravidade da infestação da pele não está correlacionada com a da infestação das articulações.
- Existem diferentes tipos de manifestações de artrite psoriásica tanto no esqueleto periférico como no axial. Também ocorrem padrões de infestação extra-articular, por exemplo, uveíte.
- A terapia da artrite psoriásica depende do tipo de manifestação. Estão disponíveis várias substâncias imunomoduladoras, que são utilizadas em fases.
Literatura:
- Stolwijk C, et. al: Epidemiologia da espondiloartrose. Rheum Dis Clin North Am 2012; 38(3): 441-476.
- Moll JM, Wright V: Artrite psoriásica. Semin Arthritis Rheum 1973; 3(1): 55-78.
- Husni ME: Comorbidades na artrite psoriásica. Rheum Dis Clin North Am 2015; 41(4): 677-698.
- Goupille P, Soutif D, Valat JP: artrite psoriásica precipitada por trauma físico. J Rheumatol 1991; 18(4): 633.
- Taylor W, et al: Critérios de classificação para a artrite psoriásica: desenvolvimento de novos critérios a partir de um grande estudo internacional. Arthritis Rheum 2006; 54(8): 2665-2673.
- Van den Bosch F, Coates L: Gestão clínica da artrite psoriásica. Lancet 2018; 391(10136): 2285-2294.
- Prevoo ML, et al: Pontuações de actividade de doença modificadas que incluem vinte e oito contagens conjuntas. Desenvolvimento e validação num estudo prospectivo longitudinal de pacientes com artrite reumatóide. Arthritis Rheum 1995; 38(1): 44-48.
- van der Heijde D, et al: ASDAS, uma pontuação de actividade altamente discriminatória da ASAS em doentes com espondilite anquilosante. Ann Rheum Dis 2009; 68(12): 1811-1818.
- Gossec L, et al: Management of psoriatic artritis in 2016: a comparison of EULAR and GRAPPA recommendations. Nat Rev Rheumatol 2016; 12(12): 743-750.
- Elalouf O, Chandran V: Nova terapêutica na artrite psoriásica. O que está a ser preparado? Curr Rheumatol Rep 2018; 20(7): 36.
PRÁTICA DA DERMATOLOGIA 2019; 29(5): 20-22