Estão disponíveis classes de medicamentos com diferentes mecanismos de acção para o tratamento da diabetes tipo 2. No entanto, a presença de insuficiência renal ou cardíaca, doença cardiovascular ou deficiência de insulina influencia significativamente a terapia.
Na Suíça, cerca de 5% da população tem diabetes, sendo a proporção mais elevada nos homens (5,5%) do que nas mulheres (3,9%) [1]. Cerca de 90% das pessoas afectadas sofrem de diabetes tipo 2 (T2D) [2]. Em comparação com a população em geral, a prevalência desta condição é particularmente elevada em pessoas com insuficiência cardíaca e é de cerca de 40% em pessoas hospitalizadas com insuficiência cardíaca [3]. Isto deve-se, entre outras coisas, à sobreposição de factores de risco, fisiopatologia e comorbidades [3]. Uma característica central comum de ambas as doenças é que são frequentemente acompanhadas por deficiências da função renal [3]. Assim, o T2D e a insuficiência cardíaca estão associados ao desenvolvimento e agravamento da doença renal crónica, o que por sua vez contribui para um mau prognóstico [3]. Devido à associação entre T2D, insuficiência cardíaca e disfunção renal, há uma necessidade crescente de agentes anti-hiperglicémicos com propriedades cardio e nefroprotectoras [3].
Classes de medicamentos disponíveis e recomendações SGED
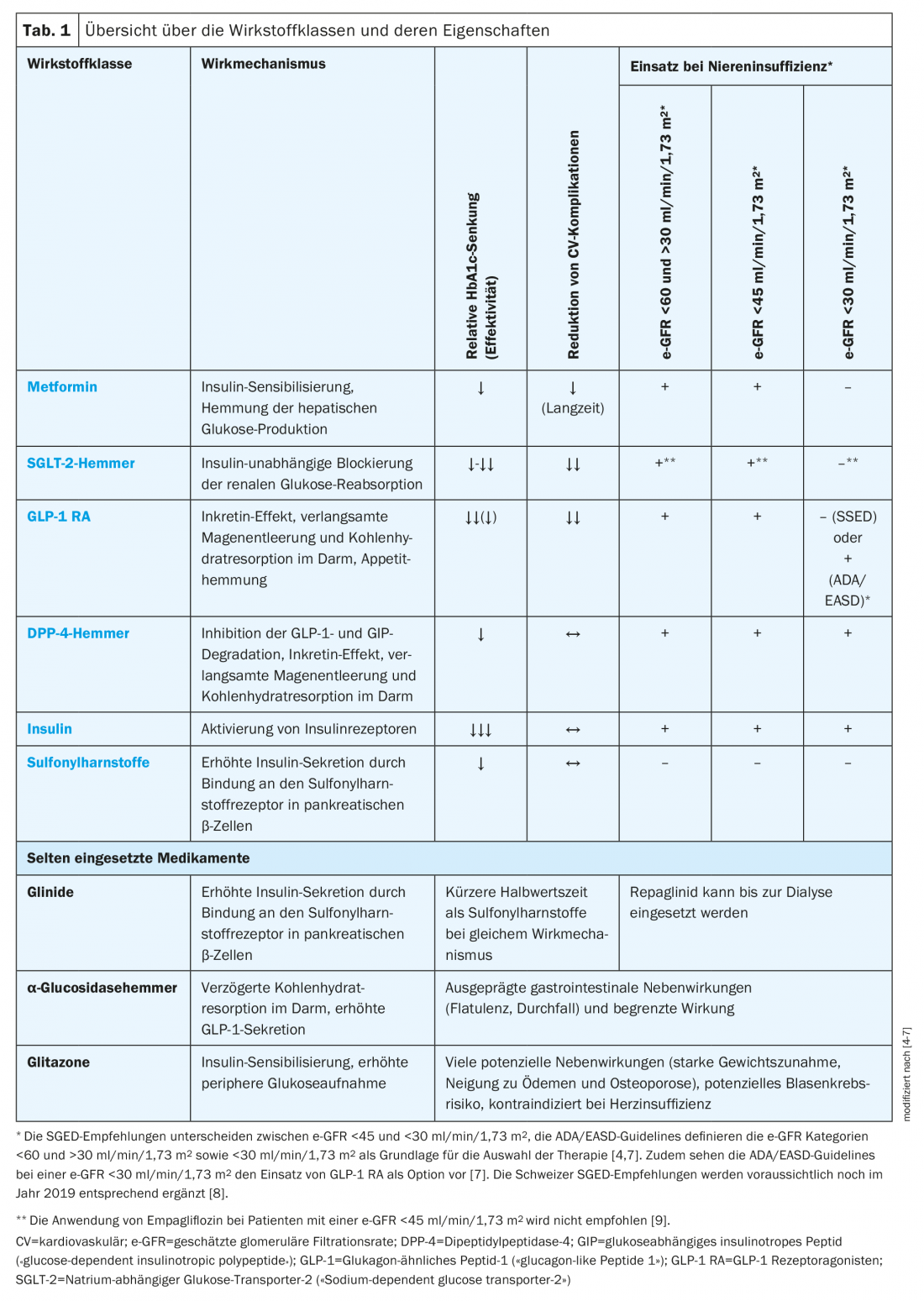
Estão disponíveis várias classes de medicamentos com diferentes mecanismos de acção para o tratamento do T2D (Tab. 1) . De acordo com as recomendações da Sociedade Suíça de Endocrinologia e Diabetologia (SGED), a metformina é geralmente o medicamento de primeira linha de escolha, com o qual os outros medicamentos disponíveis podem ser combinados precocemente, tendo em conta o seu mecanismo de acção e efeitos secundários [4]. Contudo, vários outros factores, tais como a presença de insuficiência renal, doença cardiovascular, insuficiência cardíaca ou deficiência de insulina, podem limitar a escolha da terapia [4].
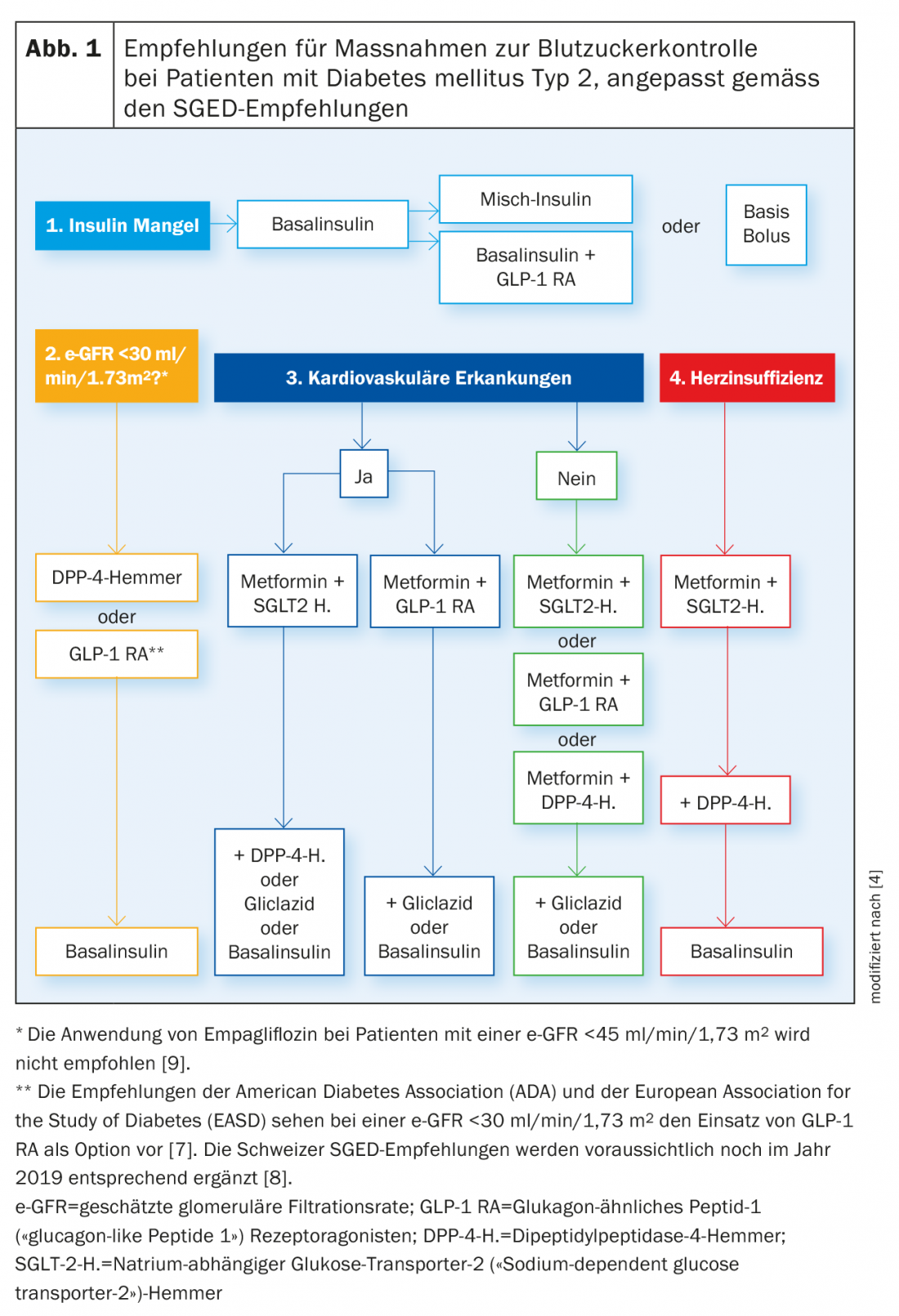
Segundo as recomendações do SGED, a insulina basal é o tratamento de escolha para a deficiência de insulina, seguido de insulina mista ou de insulinas co-formuladas, insulina basal em combinação com um agonista receptor de peptídeo 1 tipo glucagon (GLP-1 RA) ou uma terapia básica com bolus.
Nos doentes com insuficiência renal, a gama de medicamentos que podem ser utilizados é também significativamente limitada. Embora as sulfonilureias de acção prolongada não possam ser utilizadas em doentes com insuficiência renal moderada (taxa de filtração glomerular estimada, e-GFR <60 mas >30 ml/min/1,73m2), em insuficiência renal grave (e-GFR <30 ml/min/1,73 m2), só podem ser considerados inibidores do peptídeo dipeptidil peptidase-4 (DPP-4), agonistas do peptídeo tipo glucagon 1 receptor (GLP-1 RA)1 e insulina [4,7]. O ajuste da dose é necessário para todos os inibidores de DPP-4 excepto linagliptin, e todos os inibidores de DDP-4 excepto saxagliptin podem ser utilizados até à diálise. Se o tratamento não conduzir à realização da meta individual de HbA1c no prazo de três meses, a insulina basal deve ser administrada.
No que diz respeito ao risco cardiovascular, existem também diferenças entre as classes de medicamentos. Por exemplo, a metformina em utilização a longo prazo e na presença de doença cardiovascular, os inibidores de glicose-2 (SGLT-2) dependentes do sódio e a AR GLP-1 estão associados a uma redução das complicações cardiovasculares e mesmo da mortalidade por todas as causas [4]. De acordo com as recomendações do SGED, a metformina deve portanto ser utilizada em primeiro lugar em pessoas com doenças cardiovasculares, com combinação precoce com um inibidor SGLT-2 ou um GLP-1 RA indicado. Se o objectivo individual de HbA1c não for alcançado, a combinação de metformina mais inibidor SGLT-2 pode ser suplementada com um inibidor DPP-4, gliclazida ou insulina basal. Com tratamento inicial com metformina mais inibidores de DPP-4, a gliclazida ou insulina basal são possíveis como medicamentos adicionais.
Em pessoas sem doença cardiovascular, é possível o tratamento com metformina em combinação com um inibidor SGLT-2, GLP-1 RA ou inibidor DPP-4. Esta última pode ser suplementada com gliclazida ou insulina basal, se necessário.
Se a insuficiência cardíaca estiver presente, o tratamento com metformina mais inibidor SGLT-2 é indicado em primeiro lugar. Se necessário, um inibidor DPP-4 também pode ser utilizado no curso seguinte. Se isto não conduzir ao sucesso do tratamento desejado, deve ser utilizada insulina basal (Fig. 1) [4].
Foco coração
Inibidores SGLT-2: Para além do seu efeito anti-hiperglicémico primário, os inibidores SGLT-2 têm várias propriedades que podem influenciar favoravelmente o prognóstico cardiovascular [10]. Assim, os efeitos positivos sobre eventos cardiovasculares têm sido demonstrados em vários estudos de resultados cardiovasculares em pacientes com T2D. No estudo EMPA-REG OUTCOME em doentes com doença cardiovascular estabelecida, a empagliflozina foi superior ao placebo em termos do ponto final cardiovascular composto primário (dados agrupados, Separador. 2). Além disso, a empagliflozina reduziu a mortalidade cardiovascular, a mortalidade por todas as causas (FC 0,68; 95% CI 0,57-0,82; p<0,001) e o risco de hospitalização por insuficiência cardíaca (FC 0,65; 95% CI 0,50-0,85; p=0,002) [10,11]. No ponto final composto de hospitalização ou morte por insuficiência cardíaca, a empagliflozina também mostrou um efeito positivo (HR 0,61; 95% CI 0,47-0,79; p<0,001) [12]. Com base nestes dados, a empagliflozina é indicada pelo Swissmedic “para a prevenção de eventos cardiovasculares em pacientes com diabetes mellitus tipo 2 e que já manifestam doenças cardiovasculares” [9].
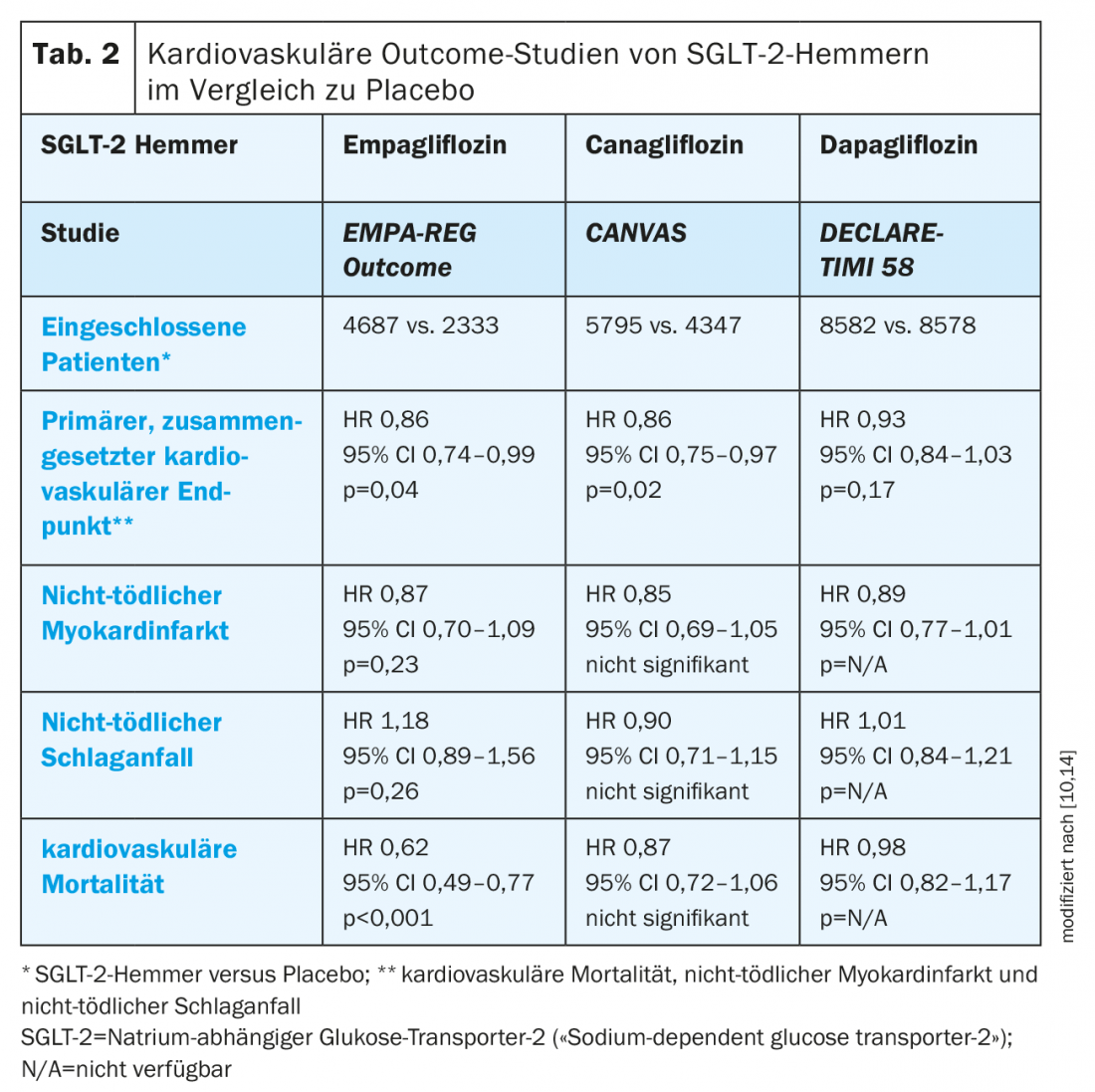
O Canagliflozin também mostrou uma redução do parâmetro cardiovascular composto primário em pacientes com doenças cardiovasculares ou factores de risco associados no programa de ensaio do CANVAS, mas não conseguiu atingir uma significância em termos de mortalidade cardiovascular [10,13]. Além disso, foi observado um risco acrescido de amputações [13].
Os dados recentemente apresentados do ensaio DECLARE-TIMI 58 mostraram uma redução estatisticamente significativa das hospitalizações por insuficiência cardíaca em doentes com doenças cardiovasculares ou factores de risco associados à toma de dapagliflozina (2,5% vs. 3,3% com placebo; p<0,005), e no ponto final composto de hospitalização devido a insuficiência cardíaca ou morte cardiovascular (4,9% vs. 5,8% com placebo, p=0,005). Além disso, o dapagliflozin alcançou a não-inferioridade mas não superioridade ao placebo em termos de eventos cardiovasculares importantes. Em contraste com a canagliflozina, não foi observado qualquer risco acrescido de amputações com dapagliflozina [14]. Deve também notar-se que os pacientes do estudo DECLARE-TIMI 58 apresentaram valores significativamente melhores de e-GFR em comparação com os estudos EMPA-REG Outcome e CANVAS devido a diferentes critérios de exclusão, o que contribuiu para a menor mortalidade no estudo DECLARE-TIMI 58 [11,13,14].
GLP-1 RA: O estudo ELIXA demonstrou a não-inferioridade da lixisenatite RA GLP-1 versus placebo em relação ao parâmetro cardiovascular composto primário, mas nenhum efeito positivo no resultado cardiovascular (separador. 3) [15].
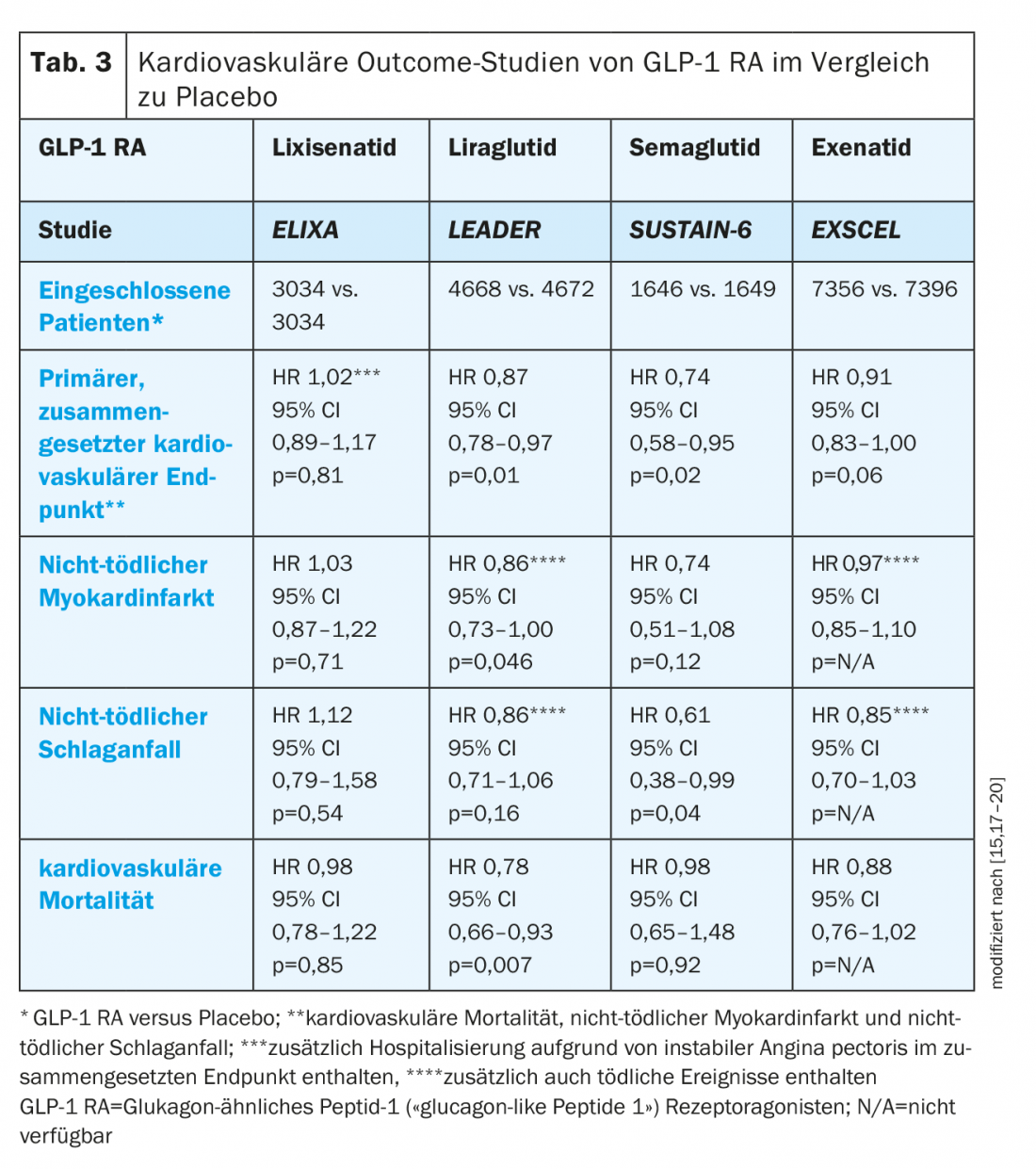
Em contraste, o ensaio LEADER demonstrou tanto a não-inferioridade do liraglutido ao placebo como uma redução significativa da mortalidade cardiovascular em doentes com doenças cardiovasculares ou factores de risco associados. A mortalidade por todas as causas foi também significativamente reduzida, enquanto não houve diferença na hospitalização por insuficiência cardíaca [15]. Com base nestes dados, o liraglutido é indicado pelo Swissmedic para a “prevenção de eventos cardiovasculares em pacientes com diabetes mellitus tipo 2 e que já manifestam doenças cardiovasculares” [16].
A não-inferioridade do semaglutido ao placebo foi confirmada no MACE de 3 pontos e foi demonstrada uma possível superioridade (MACE de 3 pontos: redução de 26%; p<0,001 para a não-inferioridade; p=0,02 para a superioridade), embora o estudo não tenha sido concebido para avaliar a superioridade. Além disso, foi observada uma redução significativa do AVC não fatal e do enfarte do miocárdio, mas nenhum efeito sobre a mortalidade cardiovascular ou de todas as causas foi observado [17].
O tratamento uma vez por semana com exenatide foi não-inferior ao placebo no ensaio EXSCEL, mas não mostrou diferenças na mortalidade cardiovascular, incidência de enfarte do miocárdio não fatal ou AVC, e hospitalização por insuficiência cardíaca [15,17–20].
Inibidores DPP-4: Em estudos preliminares, foram observados efeitos cardíacos e vasculares positivos dos inibidores DPP-4 e os primeiros resultados do estudo das fases II e III indicaram uma redução dos eventos cardiovasculares por estes compostos [10]. Os ensaios de resultados cardiovasculares demonstraram a não-inferioridade da alogliptin, saxagliptin, sitagliptin e linagliptin ao placebo (Tabela 4) . É de notar que os pacientes incluídos nestes ensaios já estavam a receber o padrão de cuidados relativamente à gestão do T2D e à gestão do risco cardiovascular [10].
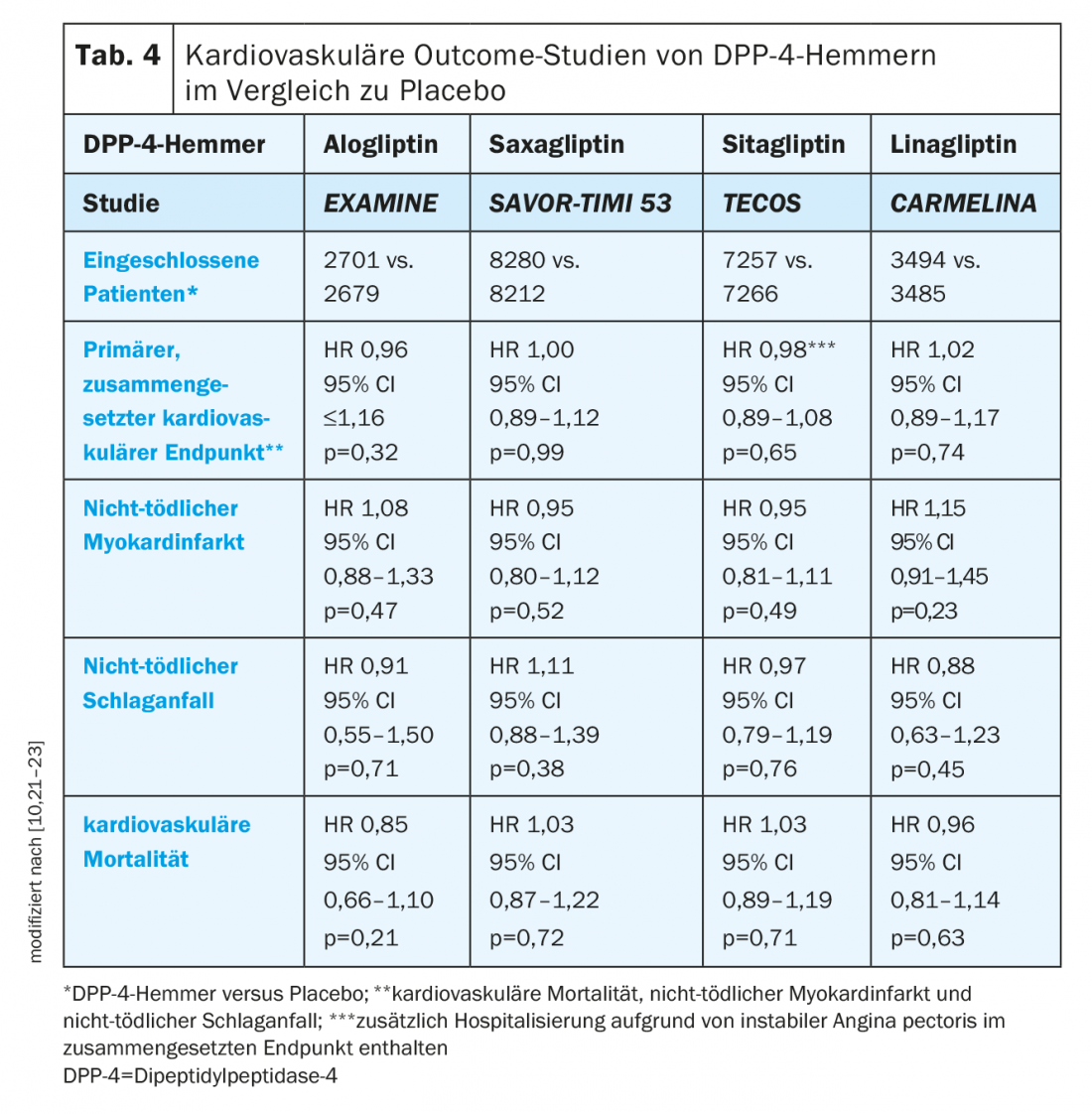
Uma questão em aberto relativamente ao uso de inibidores DPP-4 é a sua influência na ocorrência de insuficiência cardíaca. No ensaio EXAMINE, houve uma tendência não significativa para uma maior taxa de hospitalização devido à insuficiência cardíaca com alogliptin (1,07; 95% CI 0,79-1,46; p=0,657) [10,24]. Contudo, uma análise post-hoc não encontrou qualquer efeito sobre o ponto final composto de morte cardiovascular e hospitalização por insuficiência cardíaca (HR 1,00; 95% CI 0,82-1,21) [24].
No ensaio SAVOR-TIMI 53, foram hospitalizados significativamente mais pacientes do grupo saxagliptin com insuficiência cardíaca do que com placebo (3,5% vs. 2,8%; HR 1,27; 95% CI 1,07-1,51; p=0,007) [22]. O risco de insuficiência cardíaca foi mais elevado em pacientes T2D com níveis elevados de peptídeo natriurético, insuficiência cardíaca anterior ou doença renal crónica na linha de base [25].
Em contraste com dois estudos anteriores, no estudo TECOS a taxa de hospitalização não diferiu entre os grupos sitagliptin e placebo (HR 1,00; 95% CI 0,83-1,20; p=0,98) [10,26].
Linagliptin também não levou a um aumento da taxa de hospitalização devido à insuficiência cardíaca no estudo CARMELINA (HR 0,90; 95% CI 0,74-1,08; p=0,2635) [21].
Rim de foco
Os inibidores SGLT-2: Empagliflozina, bem como canagliflozina e dapagliflozina mostraram potenciais propriedades nefroprotectoras nos respectivos estudos de resultados, em que as populações de doentes diferiram nos vários estudos (Tab. 5) [3]. Enquanto os estudos EMPA-REG Outcome e CANVAS incluíram doentes com um e-GFR de pelo menos 30 ml/min/1,73 m², o estudo DECLARE-TIMI 58 incluiu apenas doentes com um e-GFR >60 ml/min/1,73 m² [11,13,14].
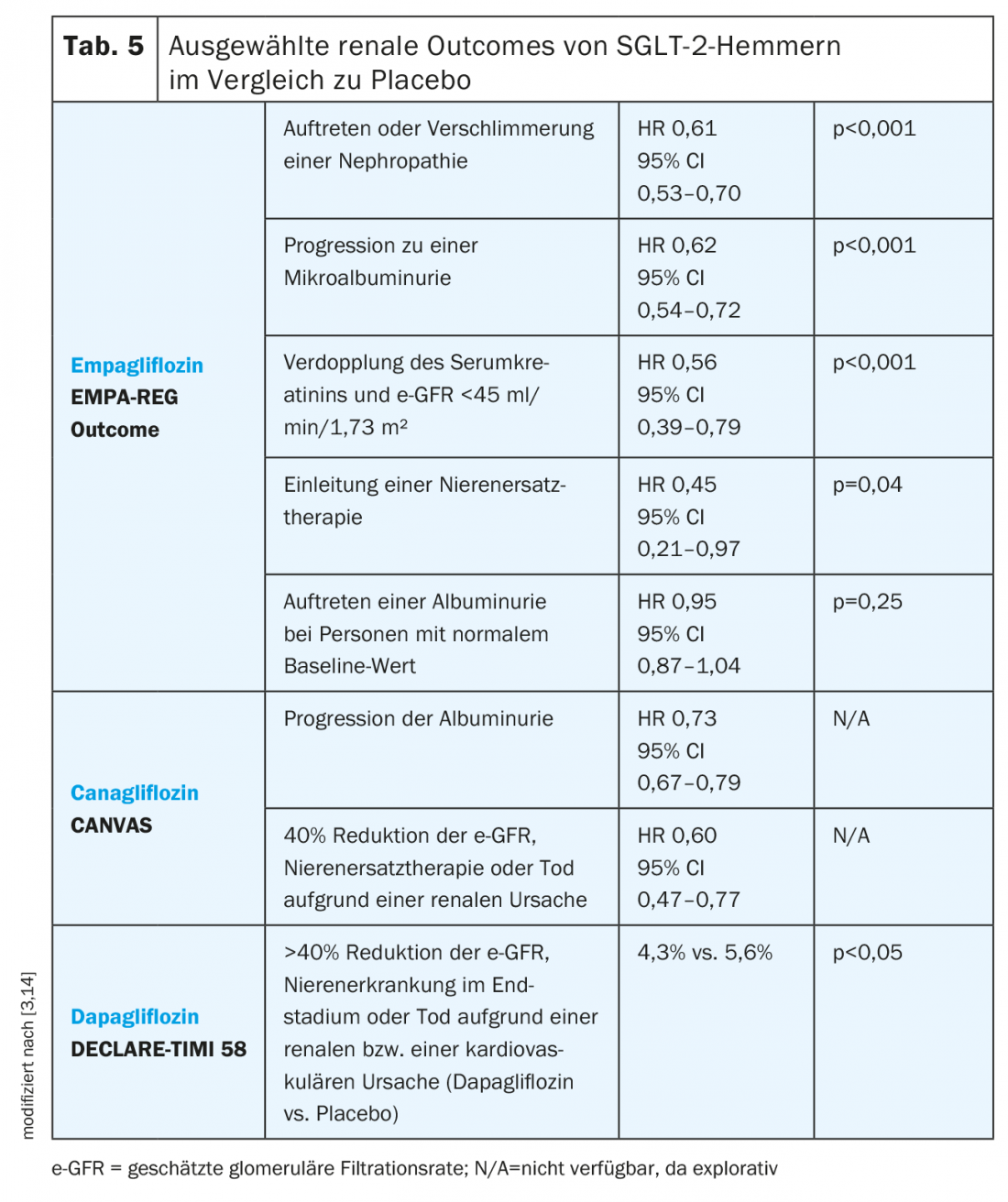
No EMPA-REG Outcome Study, a empagliflozina foi associada a uma menor incidência de nefropatia em agravamento, que foi definida como progressão para microalbuminúria, duplicação da creatinina sérica com um e-GFR <45 ml/min/1,73 m², início de terapia de substituição renal ou morte por doença renal. Todos os componentes individuais, excepto a morte por doença renal, atingiram significado estatístico. No grupo empagliflozina, o e-GFR diminuiu moderadamente nas primeiras quatro semanas, mas depois estabilizou e voltou à linha de base após o fim da terapia, enquanto que o e-GFR no grupo placebo diminuiu continuamente ao longo do estudo [3].
No estudo CANVAS, a progressão da albuminúria, definida como um aumento superior a 30% na albuminúria e uma mudança de normo para microalbuminúria ou micro para macroalbuminúria, foi menor no grupo canagliflozina do que com placebo. Além disso, a canagliflozina mostrou uma redução no ponto final composto de 40% de redução da e-GFR, terapia de substituição renal ou morte por uma causa renal em comparação com placebo [3]. Os resultados renais do canagliflozin também estão actualmente a ser investigados no estudo CREDENCE [27].
Como mostram os dados recentemente apresentados do ensaio DECLARE-TIMI 58, a dapagliflozina também tem um efeito positivo nos resultados renais e está associada a uma redução do parâmetro composto >. 40% de redução do e-GFR, doença renal em fase terminal ou morte devido a uma causa renal ou cardiovascular [14].
GLP-1 RA: No estudo ELIXA, não houve nenhum efeito significativo do lixisenatido de RA GLP-1 sobre a razão albumina/criadorina urinária depois de se ter em conta o HbA1c (Tabela 6) [3].
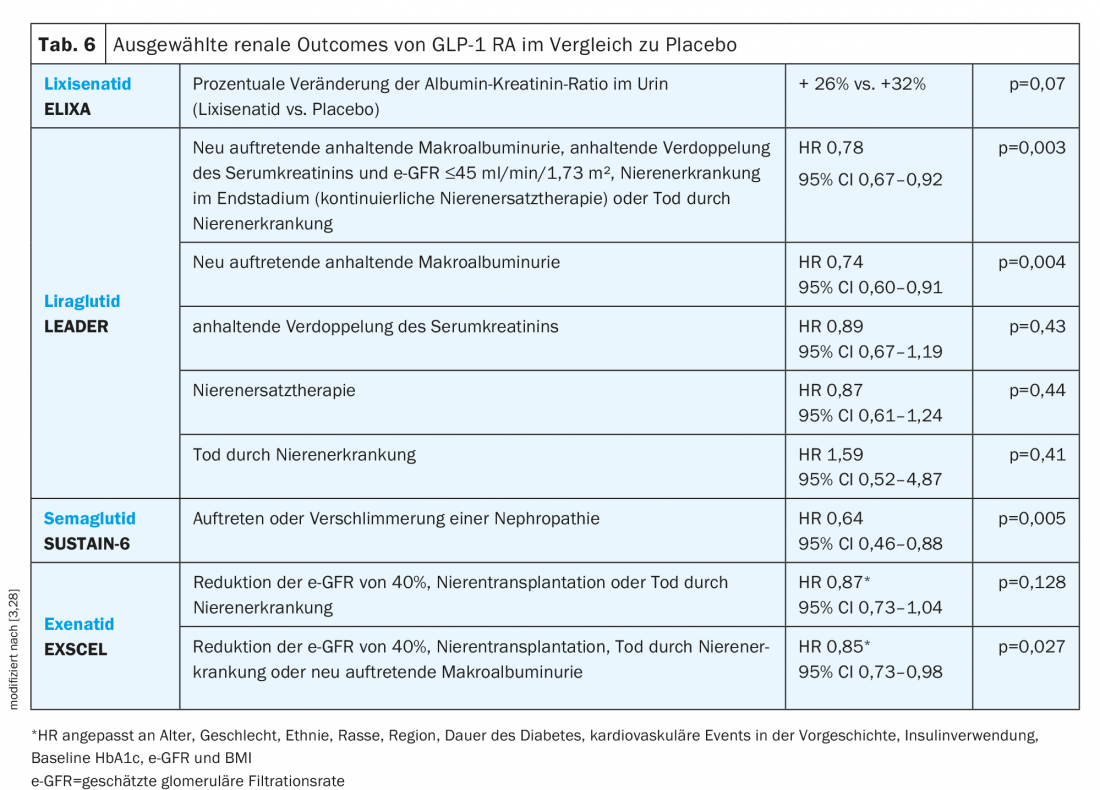
Em contraste, o tratamento com liraglútide no ensaio LEADER resultou num risco significativamente menor para o parâmetro renal composto. Além disso, apesar de uma redução global, o e-GFR foi moderadamente melhor no grupo liraglutido do que o placebo aos 36 meses (rácio e-GFR 1,02; 95% CI 1,00-1,03) [3].
No estudo SUSTAIN-6, foi demonstrado que os doentes que tomavam semaglutido tinham um risco mais baixo de nefropatia, que foi definida como macroalbuminúria, duplicação persistente da creatinina sérica e um e-GFR <45 ml/min/1,73 m² ou terapia de substituição renal contínua [3].
Dados recentemente apresentados do estudo EXSCEL mostram uma redução significativa do ponto final renal composto de 40% de redução da taxa de filtração glomerular total, transplante renal, morte por doença renal ou macroalbuminúria de novo início de vida com exenatide numa análise ajustada. A macroalbuminúria ocorreu em 2,2% dos pacientes do grupo exenatide e em 2,5% no grupo placebo. Não foi observada diferença no e-GFR (“least squares mean difference” +0,21; 95% CI -0,27 a 0,70 ml/min/1,73 m², p=0,39) [28].
Inibidores DPP-4: No estudo TECOS, o tratamento com o inibidor DPP-4 sitagliptin foi associado a uma ligeira mas sustentada diminuição da relação albumina-creatinina urinária durante o seguimento de 3 anos (tab. 7) [29]. A albumuminúria reduzida foi também observada com saxagliptin no estudo SAVOR-TIMI 53 [3]. Em relação ao e-GFR, foi observado um valor ligeiramente mas consistentemente mais baixo no estudo TECOS com sitagliptin do que com placebo. Este não foi o caso nos estudos SAVOR-TIMI 53 ou EXAMINE [24]. Esta redução sustentada difere da diminuição inicial e subsequente estabilização do e-GFR com empagliflozina observada no estudo dos resultados da EMPA-REG [3].
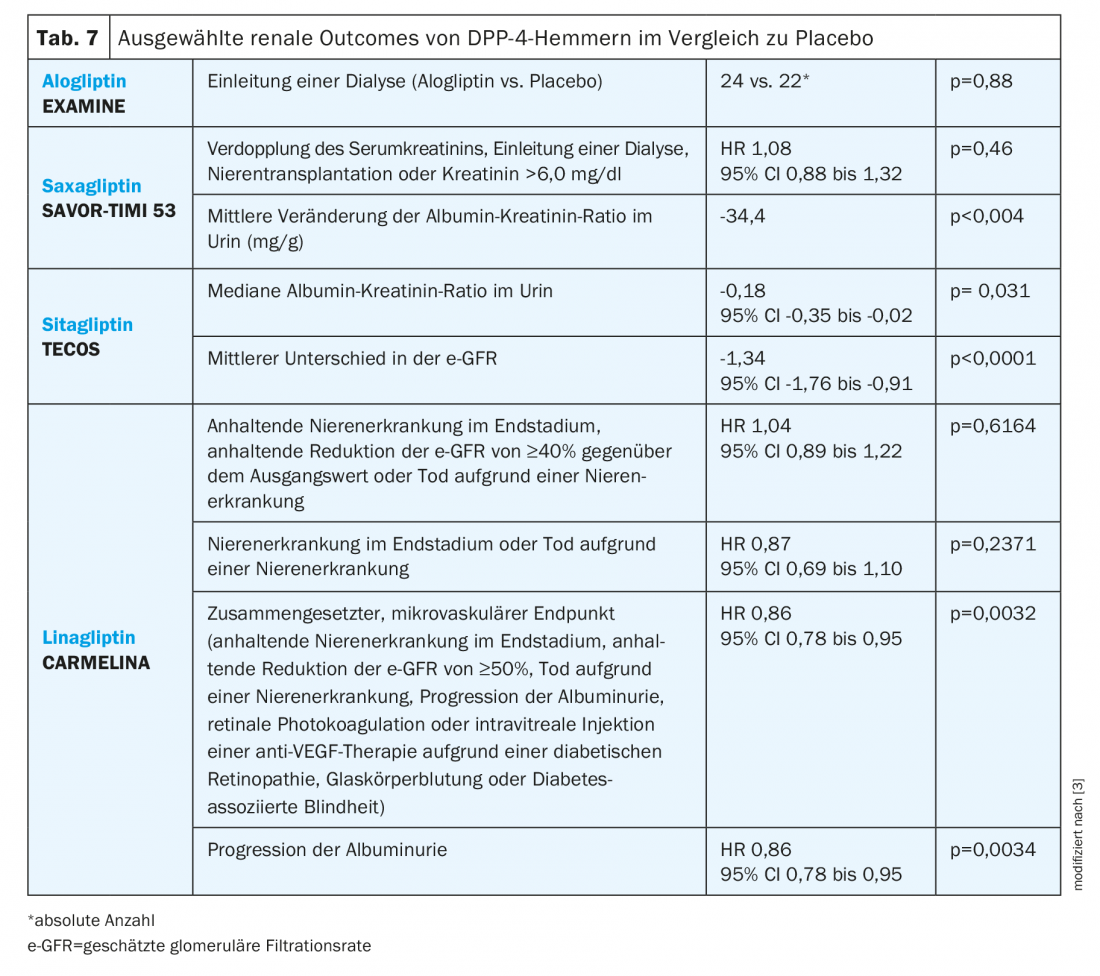
O estudo CARMELINA avaliou pacientes com doença cardiovascular e/ou doença renal crónica, confirmando a segurança tanto cardiovascular como renal. Além disso, houve diferenças significativas em relação ao placebo no ponto final composto, microvascular e em termos de progressão da albuminúria [21].
Selecção de terapia antidiabética
Com base em dados de segurança cardiovascular e potenciais propriedades protectoras, as recomendações SGED sugerem que os inibidores SGLT-2 ou o liraglutido, semaglutido ou dulaglutido de AR GLP-1 devem ser preferidos na presença de doença cardiovascular. As sulfonilureias não devem ser utilizadas em doentes com insuficiência renal moderada (e-GFR <45 ml/min/1,73 m2) [4]. Na insuficiência renal grave (e-GFR<30 ml/min/1,73 m2), a escolha dos agentes antidiabéticos é limitada aos inibidores de insulina, GLP-1 RA1 e DPP-4, embora a utilização de inibidores DPP-4 exija o ajuste da dose para quase todos os agentes deste grupo excepto linagliptin (Tabela 8) [4,7].

Os inibidores SGLT-2 não devem ser utilizados com um e-GFR <30 ml/min/1,73 m2 , uma vez que o efeito de diminuição do glucose-baixo do sangue também diminui com a diminuição da função renal. Contudo, os efeitos positivos na preservação da função renal e na redução dos eventos cardiovasculares e da mortalidade são mantidos até um e-GFR de 30 ml/min/1,73m2 [4].
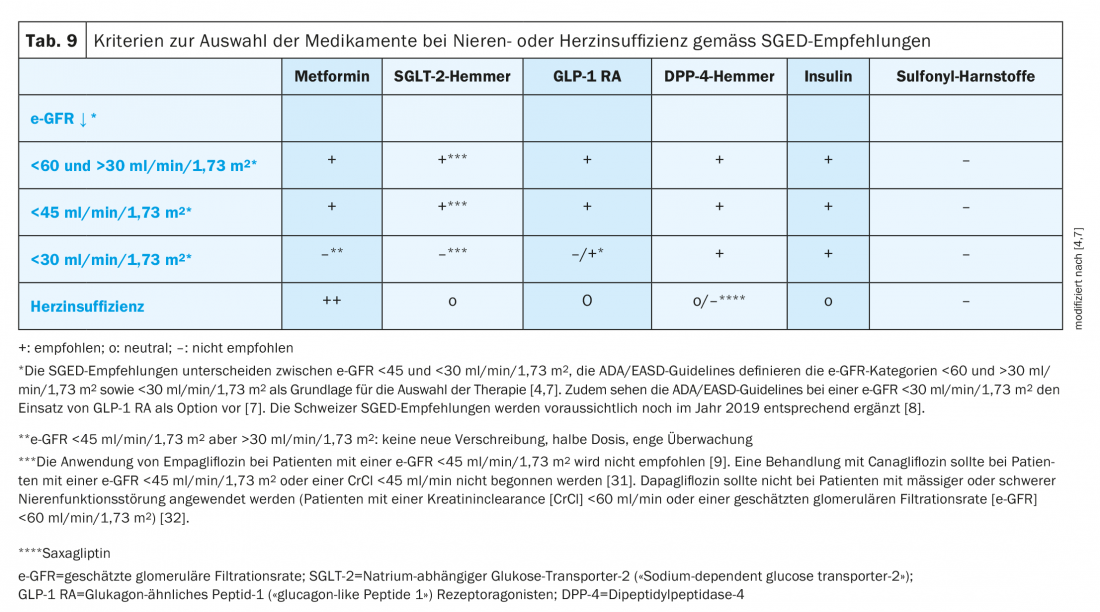
A Tabela 9 [4] apresenta uma visão geral dos critérios de selecção terapêutica em insuficiência renal ou cardíaca de acordo com as recomendações do SGED.
Pacientes com insuficiência cardíaca e renal
Muitas observações epidemiológicas mostraram uma associação entre morbidade e mortalidade cardiovascular e redução da função renal. Isto é independente de qual das duas doenças ocorre primeiro, em que se fala de uma síndrome cardio-renal ou reno-cardíaca, dependendo do gatilho inicial. Ambas as patologias mostram uma certa sobreposição e podem ser promovidas pela diabetes [33]. A classificação desta patologia distingue cinco tipos diferentes, com os primeiros quatro tipos a descreverem síndromes cardio-renais ou reno-cardíacas agudas ou crónicas. O tipo 5, por outro lado, refere-se a síndromes cardio-renais secundárias ou envolvimento cardio-renal em doenças sistémicas. Assim, pode-se falar de uma síndrome cardio-renal do tipo 5 no campo da diabetes [34].
Independentemente da classificação, a questão na prática clínica é que classe de fármacos deve ser usada em pacientes T2D com insuficiência cardíaca e renal concomitante. Se a gravidade da insuficiência renal o permitir, os inibidores SGLT-2 são inicialmente o tratamento de escolha. Se a função renal continuar a diminuir, a GLP1-RA pode então ser considerada. Na insuficiência renal grave, apenas os inibidores DDP-4, GLP1-RA1 e insulina são indicados. De um modo geral, é de notar que os diuréticos devem ser utilizados cuidadosamente nestes doentes para evitar a diurese excessiva [4,7].
Mensagens Take-Home
- Estão disponíveis classes de medicamentos com diferentes mecanismos de acção para o tratamento da diabetes tipo 2: Metformina, inibidores SGLT-2, GLP-1 RA, inibidores DPP-4, insulina e sulfonilureias.
- De acordo com as recomendações da SGED, a metformina é o medicamento de primeira linha de escolha, com o qual os outros medicamentos podem ser combinados desde cedo.
- A presença de insuficiência renal, doença cardiovascular, insuficiência cardíaca ou deficiência de insulina pode influenciar significativamente a escolha da terapia.
- Nos doentes com doenças cardiovasculares, as recomendações SGED declaram que deve ser preferido um inibidor SGLT-2 (empagliflozina, dapagliflozina, canagliflozina) ou uma AR GLP-1 (liragliflutido, semaglutido, dulaglutido).
- Na insuficiência renal grave (e-GFR<30 ml/min/1,73m2), a escolha de agentes antidiabéticos é limitada aos inibidores de insulina, GLP-1 RA1 e DPP-4, com todos os inibidores de DPP-4 excepto linagliptin a necessitarem de ajuste de dose.
Literatura:
- Instituto Estatístico Federal Suíço: Diabetes. www.bfs.admin.ch/bfs/de/home/statistiken/gesundheit/gesundheitszustand/krankheiten/diabetes.html, último acesso 29.10.2018.
- Diabetes Suíça: Diabetes mellitus. www.diabetesschweiz.ch/diabetes/, último acesso 29.10.2018.
- McHugh, KR, et al: The emerging role of novel antihyperglycemic agents in the treatment of heart failure and diabetes: A focus on cardiorenal outcomes. Clin Cardiol 2018; 41(9): 1259-1267.
- Lehmann, R, et al: Recommendations of the SGED/SSED: Measures for blood glucose control in patients with type 2 diabetes mellitus. Swiss Society of Endocrinology and Diabetology 2016.
- Chaudhury A, et al: Clinical review of antidiabetic drugs: Implications for type 2 diabetes mellitus management. Fronteiras em endocrinologia 2017; 8: 6. 10.3389/fendo.2017.00006
- Stein SA, Lamos EM, Davis, SN: Uma revisão da eficácia e segurança dos medicamentos antidiabéticos orais. Parecer de especialista sobre segurança dos medicamentos 2013; 12(2): 153-175.
- Davies MJ, et al: Management of hyperglycaemia in type 2 diabetes, 2018. Um relatório de consenso da Associação Americana de Diabetes (ADA) e da Associação Europeia para o Estudo da Diabetes (EASD). Diabetologia 2018; 61(12): 2461-2498.
- Lehmann R: Comunicação pessoal do Prof. R. Lehmann- Presidente do grupo de trabalho SGED/SSED.
- Swissmedic: Resumo actual das características do produto para Jardiance®. www.swissmedicinfo.ch. Estado da informação: Abril de 2018.
- Scheen AJ: Efeitos Cardiovasculares dos Novos Inibidores da Glucose-Lowering Oral: DPP-4 e SGLT-2. Circulation Research 2018; 122(10): 1439-1459.
- Zinman B, et al: Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. New England Journal of Medicine 2015; 373(22): 2117-2128.
- Fitchett D, et al: Resultados da insuficiência cardíaca com empagliflozina em doentes com diabetes tipo 2 com elevado risco cardiovascular: resultados do ensaio EMPA-REG OUTCOME®. European Heart Journal 2016; 37(19): 1526-1534.
- Neal B, et al: Canagliflozin e Eventos Cardiovasculares e Renais na Diabetes Tipo 2. New England Journal of Medicine 2017; 377(7): 644-657.
- Wiviott SD, et al: Dapagliflozin e Resultados Cardiovasculares na Diabetes Tipo 2. N. England J. Med 2019; 380: 347-357. doi: 10.1056/NEJMoa1812389. Epub 2018 Nov
- Cefalu WT, et al: Cardiovascular Outcomes Trials in Type 2 Diabetes: Where Do We Go From Here? Reflexões de um Fórum de Especialistas em Diabetes Care Editors’ Expert. Diabetes Care 2018; 41(1): 14-31.
- Swissmedic: Informação especializada actual sobre Victoza®. www.swissmedicinfo.ch, a partir de informação: Abril de 2018.
- Marso SP, et al: Semaglutide e resultados cardiovasculares em doentes com diabetes tipo 2. New England Journal of Medicine 2016; 375(19): 1834-1844.
- Holman RR, et al: Efeitos de exenatidez uma vez por semana nos resultados cardiovasculares na diabetes tipo 2. New England Journal of Medicine, 2017; 377(13): 1228-1239.
- Marso SP, et al: Liraglutide e resultados cardiovasculares na diabetes tipo 2. New England Journal of Medicine 2016; 375(4): 311-322.
- Pfeffer MA, et al: Lixisenatide em doentes com diabetes tipo 2 e síndrome coronária aguda. New England Journal of Medicine 2015; 373(23): 2247-2257.
- Rosenstock J, et al: Estudo de Resultados Cardiovascular e Microvascular Renal com Linagliptin em Pacientes com Diabetes Mellitus Tipo 2 (CARMELINA®). Apresentação oral na 54ª Reunião Anual da Associação Europeia para o Estudo da Diabetes (EASD), Berlim, quinta-feira, 4 de Outubro de 2018. https://www.easd.org/virtualmeeting/home.html#!contentsessions/2873.
- Scirica BM, et al: Saxagliptin e resultados cardiovasculares em doentes com diabetes mellitus tipo 2. New England Journal of Medicine 2013; 369(14): 1317-1326.
- White WB, et al: Alogliptin após síndrome coronária aguda em doentes com diabetes tipo 2. New England Journal of Medicine 2013; 369(14): 1327-1335.
- Zannad F, et al: Resultados de insuficiência cardíaca e mortalidade em doentes com diabetes tipo 2 que tomam alogliptin versus placebo em EXAMINE: um ensaio multicêntrico, aleatório e duplo-cego. The Lancet 2015; 385(9982): 2067-2076.
- Scirica BM, et al: Heart failure, saxagliptin and diabetes mellitus: observações do ensaio aleatório SAVOR-TIMI 53. Circulação 2014; 130(18): 1579-1588.
- Green JB, et al: Effect of sitagliptin on cardiovascular outcomes in type 2 diabetes. New England Journal of Medicine 2015; 373(3): 232-242.
- Jardine MJ, et al: A canagliflozina e os pontos terminais renais na diabetes com avaliação clínica da nefropatia estabelecida (CREDENCE) estudam a fundamentação, o desenho e as características de base. Revista americana de nefrologia 2017; 46(6): 462-472.
- Bethel MA, et al: Renal Outcomes in the EXenatide Study of Cardiovascular Event Lowering (EXSCEL). Diabetes, 2018. 67(Suplemento 1): https://doi.org/10.2337/db18-522-P
- Cornel JH, et al: Effect of Sitagliptin on Kidney Function and Respective Cardiovascular Outcomes in Type 2 Diabetes: Outcomes From TECOS. Diabetes Care 2016; 39(12): 2304-2310.
- Swissmedic: www.swissmedicinfo.ch.
- Swissmedic: Resumo actual do Invokana® das características do produto. www.swissmedicinfo.ch, a partir de informação: Abril de 2018.
- Swissmedic: Informação especializada actual Forxiga®. www.swissmedicinfo.ch, a partir de informação: Janeiro de 2018.
- Schrier RW: Síndrome cardiorrenal versus renocardia: há diferença? Nat Clin Pract Nephrol 2007; 3(12): 637.
- Di Lullo L, et al.: Síndrome Cardiorrenal Tipo 5 (CRS-5): uma actualização. Nephrology@ Point of Care 2017; 3(1): p. e23-e32, https://doi.org/10.5301/napoc.5000212
PRÁTICA DO GP 2019; 14(3): 18-27
CARDIOVASC 2019; 18(2): 16-23