A diabetes mellitus tipo 2 progressiva é caracterizada por uma diminuição contínua da secreção endógena de insulina. A insulina ainda é um medicamento antidiabético comprovado e muito eficaz. A escolha da insulinoterapia baseia-se em vários factores tais como a fase da diabetes, o controlo metabólico e os recursos dos pacientes. Inicialmente, a grande maioria dos diabéticos de tipo 2 pode ser tratada com insulinoterapia basal. Tem o menor risco de hipoglicemia e aumento de peso em comparação com outros regimes de insulina (insulinoterapia prandial, insulinoterapia mista). Na prática clínica, a combinação de insulina e análogos de GLP 1 está a tornar-se cada vez mais popular.
Patogenicamente, a diabetes mellitus tipo 2 caracteriza-se pela resistência à insulina e por uma restrição progressiva da secreção de insulina. Como resultado, são tipicamente encontrados níveis elevados de glicose no sangue em jejum e picos de glicose no sangue pós-prandial. A fim de manter um controlo metabólico adequado, a maioria dos doentes necessita, portanto, de terapia insulínica durante o curso da doença. A insulinoterapia ainda é frequentemente iniciada ou considerada demasiado tarde. As razões para tal são múltiplas e incluem o medo de efeitos secundários (aumento de peso, hipoglicemia), bem como numerosos outros factores (por exemplo, inibição da auto-injecção, medo de prejudicar a qualidade de vida, etc.) [1,2].
De um ponto de vista puramente terapêutico, a insulina oferece numerosas vantagens: A insulina é o medicamento antidiabético com maior eficácia terapêutica e é facilmente controlável, não tem potencial de interacção relevante com outros medicamentos, não está contra-indicada mesmo nas insuficiências cardíacas, renais ou hepáticas mais graves e tem ainda um efeito positivo nos lípidos plasmáticos [3]. Os efeitos secundários tais como hipoglicémia e aumento de peso podem muitas vezes ser bem controlados ou amplamente evitados com treino e ajuste adequados da dose ou escolha do regime terapêutico apropriado (por exemplo, combinação com agonistas receptores de GLP 1). A moderna terapia com insulina ainda representa, portanto, uma opção terapêutica muito eficiente e moderna no conceito de tratamento multimodal para diabéticos de tipo 2.
Este artigo visa fornecer uma visão geral actualizada e prática da insulinoterapia em pessoas com diabetes mellitus tipo 2.
Valores-alvo HbA1c e algoritmos de terapia
A gama de alvos do HbA1c é definida individualmente para cada paciente. Vários factores são tidos em conta, tais como idade ou esperança de vida, comorbilidades e risco de hipoglicemia [4]. A importância de um bom controlo metabólico no que diz respeito ao desenvolvimento e progressão de sequelas microvasculares como a retinopatia diabética ou nefropatia é indiscutível. Por outro lado, a influência de um bom controlo da glicemia nas complicações macrovasculares ainda não foi conclusivamente esclarecida. Embora o estudo UKPDS tenha mostrado alguns benefícios do controlo glicémico precoce e bom nos resultados cardiovasculares após anos [5], o estudo não mostrou qualquer benefício do controlo glicémico precoce e bom nos resultados cardiovasculares após anos. No entanto, em ensaios subsequentes (ADVANCE, ACCORD, VADT), que foram realizados principalmente em doentes com diabetes de longa data, o controlo glicémico intensivo com vista a níveis de HbA1c inferiores a 7% não reduziu a mortalidade cardiovascular [6–8]. Em geral, a maioria das sociedades profissionais especifica um HbA1c em torno ou abaixo de 7%, mas com a opção de valores alvo de HbA1c mais elevados (por exemplo, pacientes mais velhos com comorbilidade) ou mais baixos (por exemplo, pacientes mais jovens com curta duração de diabetes e baixo risco de hipoglicémia).
Nas actuais recomendações ADA/EASD para o tratamento da hiperglicemia em pacientes com diabetes tipo 2, o tratamento com insulina básica é considerado como uma opção terapêutica com a maior potência terapêutica a par dos medicamentos antidiabéticos orais. Uma vez que a insulinoterapia tem potenciais efeitos secundários, mas também envolve esforço em termos de treino e aplicação de medicamentos, faz sentido na prática ponderar a indicação para a insulinoterapia contra as outras opções de terapia antidiabética, tendo em conta a potência e os efeitos secundários.
Indicações para a insulinoterapia
Para além das indicações dependentes do metabolismo (deterioração do controlo metabólico sob dupla ou tripla combinação com antidiabéticos orais com aumento de HbA1cvalor), há várias situações independentes do metabolismo em que a insulinoterapia faz sentido (Tab. 1). Muitas vezes, na situação aguda com hiperglicemia pronunciada (“glucotoxicidade”), para além dos sintomas correspondentes com poliúria e polidipsia, existe uma espécie de “rigidez secretora” da secreção de insulina e uma diminuição da acção da insulina. Aqui, a insulinoterapia – que muitas vezes é apenas necessária temporariamente – ajuda a baixar o açúcar no sangue de forma rápida e eficiente, para que o funcionamento das células beta e a resistência à insulina voltem a melhorar. Além disso, foi demonstrado que em doentes com diabetes mellitus tipo 2 recentemente diagnosticada, a terapia com insulina precoce e intensificada (em comparação com os antidiabéticos orais) leva a uma recuperação significativamente melhor da função das células beta e a uma remissão glicémica mais longa [9]. Numa proporção considerável de doentes, a diabetes mellitus tipo 1 só se manifesta após os 35 anos de idade [10], e até 14% de todos os doentes que fenotípicamente se apresentam como do tipo 2 diabéticos têm autoanticorpos detectáveis de células de ilhotas como expressão de uma patogénese auto-imune da diabetes [11]. Se houver indicações de uma deficiência absoluta de insulina ou diabetes mellitus tipo 1, o início da insulinoterapia também é indicado nesta situação.

Os diferentes tipos de insulina
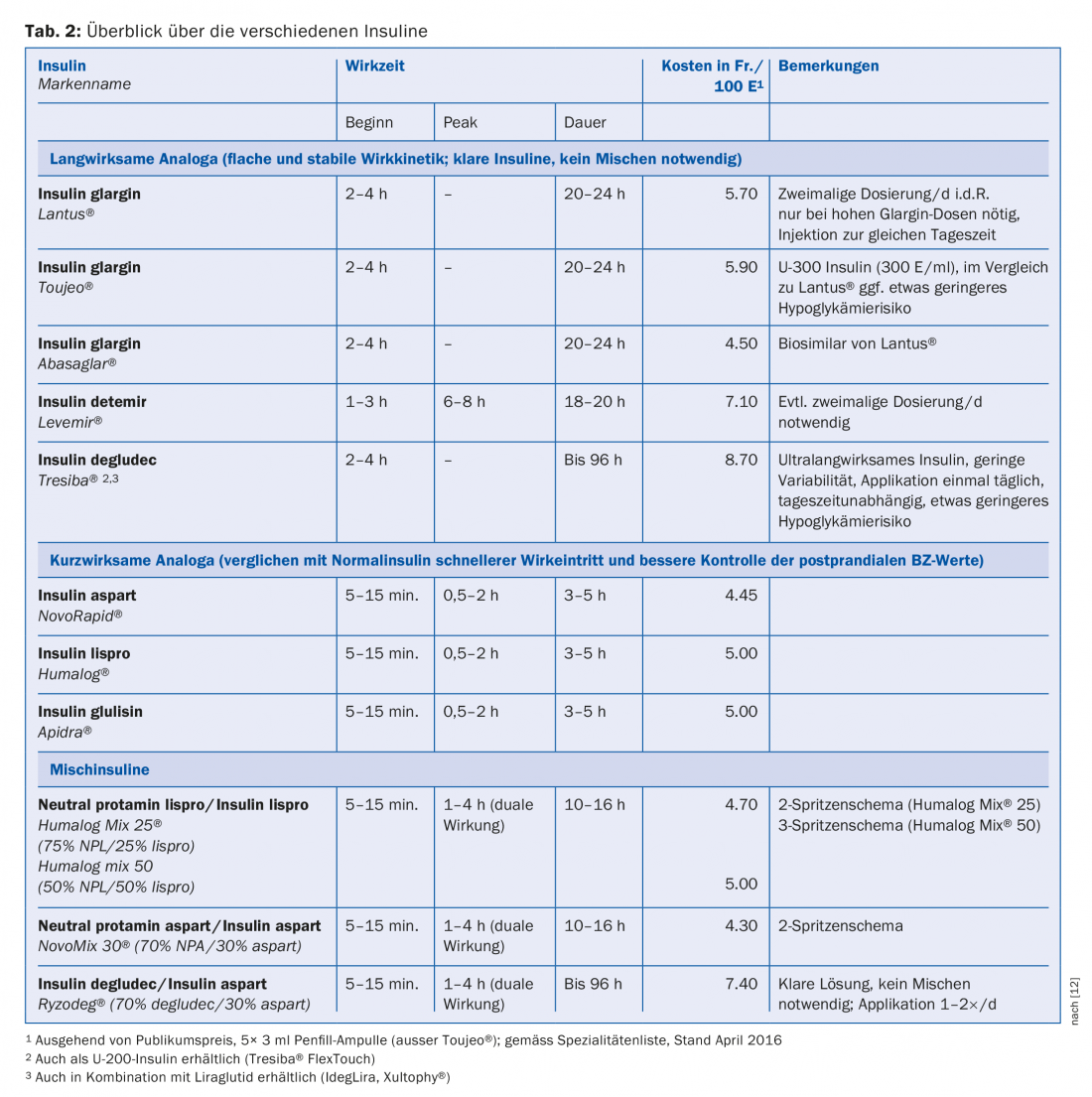
Com base na duração da acção, as insulinas dividem-se em insulinas de acção rápida (prandial), insulinas de acção longa (basal) e insulinas mistas [12]. Numa comparação directa, não há diferenças na redução de HbA1c entre análogos de insulina e insulinas regulares ou NPH. No entanto, na vida quotidiana e devido a aspectos práticos (aplicação, menor intervalo de injecção, melhor controlo dos valores de glicemia pós-prandial, menor risco de hipoglicemia), os análogos de insulina tornaram-se estabelecidos tanto para a terapia basal como para a terapia prandial. Os análogos diferem da insulina humana por uma estrutura molecular modificada. Ao substituir certos aminoácidos ou ao adicionar ácidos gordos, as propriedades farmacodinâmicas e farmacocinéticas, tais como duração da acção ou início da acção, são alteradas. Uma visão geral dos análogos de insulina (incluindo as insulinas mistas) frequentemente utilizados hoje em dia é apresentada no quadro 2.
Informações gerais sobre a aplicação prática da insulinoterapia
A terapia ideal com insulina normaliza os níveis de glicemia pré e pós-prandial sem provocar hipoglicémia ou aumento de peso. Os regimes de insulina conhecidos (tab. 3) diferem na sua complexidade e esforço para o doente.
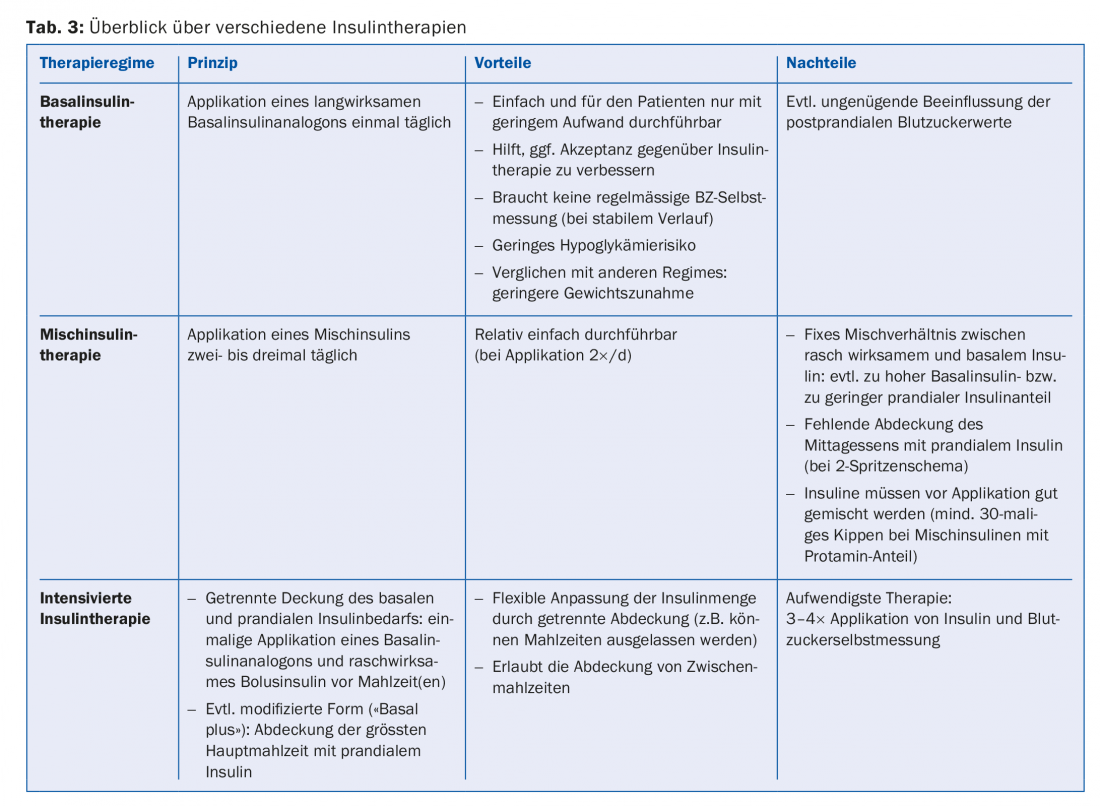
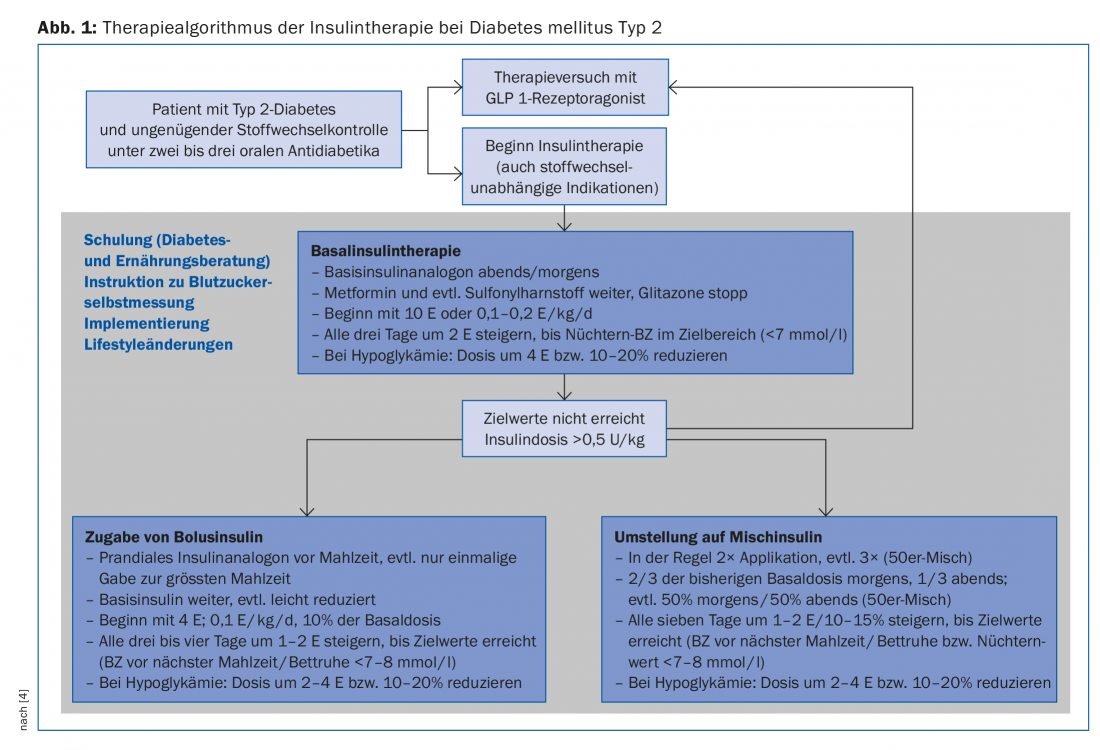
Numa primeira fase, portanto, a insulinoterapia basal é geralmente escolhida, e apenas intensificada se os valores alvo não forem alcançados ou se a insulinoterapia se deteriorar novamente (Fig. 1).
A motivação ou aderência a terapias injectáveis da diabetes é fundamental para o sucesso do tratamento. A insulinoterapia significa frequentemente uma mudança drástica no conceito de tratamento para o paciente; a terapia deve ser adaptada aos recursos específicos do paciente e requer uma quantidade considerável de formação por parte de uma equipa interdisciplinar.
Os efeitos secundários podem piorar significativamente a adesão e devem ser evitados tanto quanto possível desde o início e discutidos com o paciente mesmo antes de se iniciar a terapia. O risco de hipoglicémia pode ser reduzido de forma decisiva através de ajuste da dose e treino (por exemplo, prevenção de situações de risco, redução da dose de insulina após esforço físico, titulação lenta da dose). O aumento de peso é, por um lado, uma expressão de um melhor controlo metabólico (redução da glucosúria), mas também pode ter outras razões, por exemplo a ingestão de aperitivos para prevenir a hipoglicemia. Na prática clínica, este efeito secundário é provavelmente uma das razões mais frequentes para o fracasso da insulinoterapia ou um dos factores mais importantes para que a insulinoterapia seja recusada ou iniciada demasiado tarde. A combinação de terapias com terapias antidiabéticas mais recentes – além de enfatizar a importância das mudanças de estilo de vida nesta situação – pode ter aqui um efeito de apoio adicional.
Terapia de insulina basal
De longe a terapia mais fácil de executar é a insulinoterapia basal (Fig. 2), que é executada como uma terapia adicional à terapia existente com medicamentos antidiabéticos orais. Os medicamentos antidiabéticos orais – com excepção das glitazonas – são geralmente transmitidos; em particular, a combinação com metformina tem um efeito de poupança de insulina [13]. As sulfonilureias ajudam a controlar os níveis de glicemia pós-prandial, mas podem aumentar o risco de hipoglicemia em combinação com a insulina. Além disso, tornam-se cada vez mais ineficazes com o aumento da duração da diabetes e a diminuição da função das células beta.
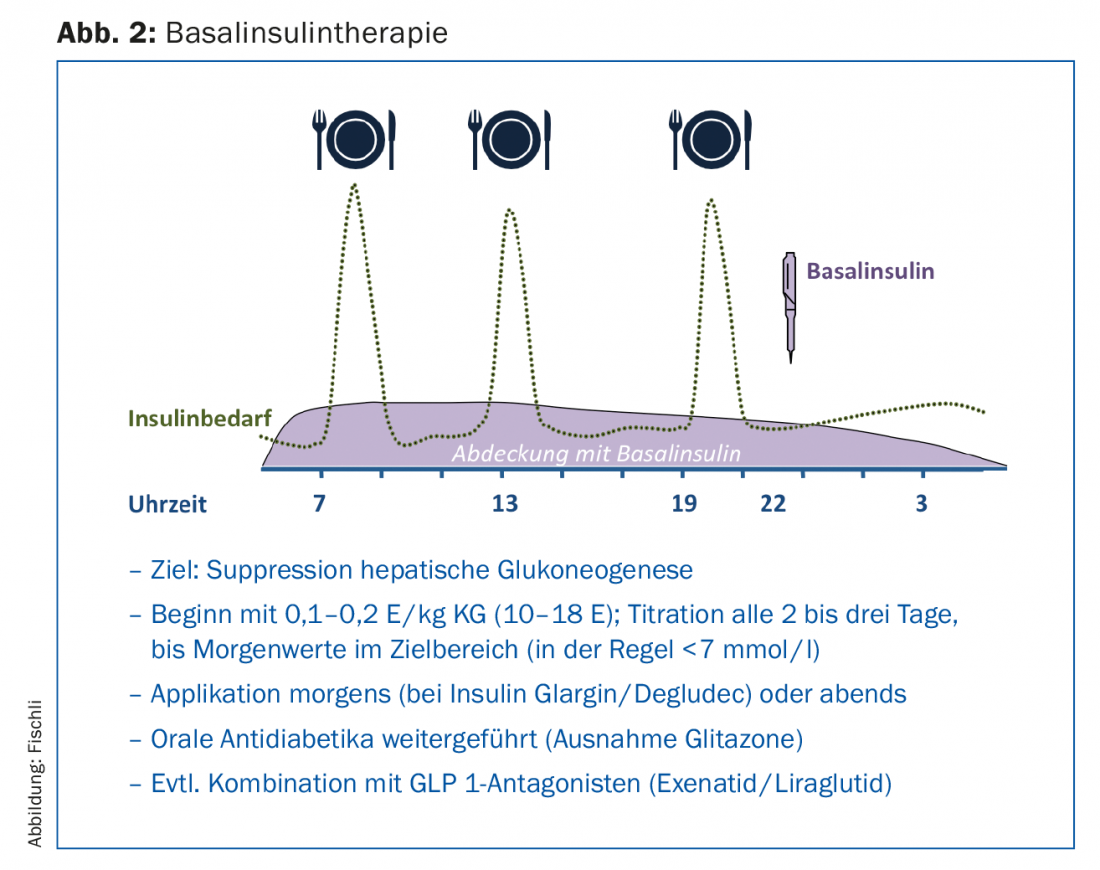
A aplicação de um análogo de insulina basal de acção prolongada inibe principalmente a gluconeogénese hepática e reduz assim os níveis elevados de glicemia em jejum, bem como os níveis na fase de pós-absorção. Com valores de HbA1c acima de 8,5%, valores elevados de glicemia em jejum influenciam em particular a situação metabólica [14], razão pela qual a insulinoterapia basal melhora decisivamente o controlo da glicemia também nestas situações. Em estudos, a glargina [15] ou insulina detemir [16] em combinação com metformina atingiu um valor de HbA1c inferior a 7% em cerca de dois terços dos pacientes. Ao dosear, deve notar-se que a insulina é gradualmente aumentada até que os valores-alvo sejam alcançados (estratégia “treat to target”). Este aumento pode ser feito pelo próprio paciente com formação adequada (Fig. 1).
Em comparação com a insulinoterapia prandial ou mista, a insulinoterapia básica oferece as vantagens de um menor ganho de peso e o menor risco de hipoglicémia [17]. Especialmente para os condutores de veículos motorizados, este último ponto é crucial. Em 2015, um grupo de trabalho interdisciplinar reviu as directrizes sobre aptidão para conduzir e capacidade de condução na diabetes mellitus [18]. As pessoas sem factores de risco (isto é, sem distúrbio de consciência da hipoglicémia e sem historial de hipoglicémia grave) que são tratadas exclusivamente com um análogo basal de insulina (por exemplo, glargina de insulina ou detemir) têm um risco global baixo de hipoglicémia, razão pela qual a medição de glicemia de rotina antes de cada viagem de automóvel já não é necessária.
Combinação com outros medicamentos antidiabéticos
A combinação da insulinoterapia com inibidores DPP IV ou agonistas receptores de GLP 1 é possível e oferece várias vantagens [19]. A combinação de insulina e GLP 1 analógica está a tornar-se cada vez mais popular. A sequência, ou seja, que classe de substância é dada em primeiro lugar, não importa realmente. A insulina basal pode ser iniciada primeiro, ou a insulina pode ser combinada com agonistas receptores de GLP 1 como terapia complementar.
Em termos farmacológicos, ambas as substâncias têm um efeito de redução de açúcar no sangue e sinérgico através de diferentes mecanismos [20]. No entanto, a influência do agonista receptor da GLP 1 na regulação do apetite central e da saciedade ajuda a prevenir o aumento de peso sob terapia insulínica. Cada vez mais dados apoiam agora também os benefícios desta terapia combinada em termos de progressão de peso, controlo metabólico e risco de hipoglicémia [21].
Na Suíça, o exenatide (Byetta®) e o liraglutido (Victoza®) são aprovados para combinação com insulina básica; o liraglutido também está disponível como combinação fixa com insulina degludec (Xultophy®). O mais recente dulaglutido uma vez por semana (Trulicity®) é aprovado em combinação com a insulina prandial. O mais recente grupo de medicamentos antidiabéticos, os inibidores SGLT 2, também têm um efeito de redução da insulina ou do peso em combinação com a insulina [22].
Intensificação da insulinoterapia
A intensificação ou alteração da insulinoterapia deve ser considerada se o controlo metabólico se deteriorar mais ou se os efeitos secundários (hipoglicemia, ganho de peso) complicarem a terapia (Fig. 1). Antes de adicionar uma insulina prandial ou mudar para uma mistura de insulina, vale a pena experimentar um agonista receptor de GLP 1 em combinação com a insulina básica.
A intensificação da insulinoterapia é feita ou adicionando um análogo de insulina de acção rápida antes das refeições como um regime básico clássico de bolo ou mudando para uma insulinoterapia mista. No entanto, esta última tem algumas desvantagens (tab. 3), e em comparação directa com a insulina bolus básica, as insulinas mistas têm pior desempenho em termos de controlo metabólico [23].
Literatura:
- Polonsky WH, et al: Psicological insulin resistance in patients with type 2 diabetes: the scope of the problem. Diabetes Care 2005; 28(10): 2543-2545.
- Nakar S, et al: Transição para a insulina na diabetes tipo 2: a concepção errada dos médicos de família sobre os receios dos pacientes contribui para as barreiras existentes. J Diabetes Complications 2007; 21(4): 220-226.
- Romano G, et al.: Terapia com insulina e sulfonilureia em doentes com NIDDM. Os efeitos no metabolismo das lipoproteínas são diferentes mesmo com um controlo semelhante da glucose no sangue? Diabetes 1997; 46(10): 1601-1606.
- Inzucchi SE, et al: Management of hyperglycemia in type 2 diabetes, 2015: a patient-centred approach: update to a position statement of the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care 2015; 38(1): 140-149.
- Holman RR, et al: 10 anos de acompanhamento do controlo intensivo da glicose na diabetes tipo 2. N Engl J Med 2008; 359(15): 1577-1589.
- Gerstein HC, et al: Efeitos da redução intensiva da glicose na diabetes tipo 2. N Engl J Med 2008; 358(24): 2545-2559.
- Patel A, et al: Controlo intensivo da glucose no sangue e resultados vasculares em doentes com diabetes tipo 2. N Engl J Med 2008; 358(24): 2560-2572.
- Duckworth W, et al: Controlo da glicose e complicações vasculares em veteranos com diabetes tipo 2. N Engl J Med 2009; 360(2): 129-139.
- Weng J, et al: Efeito da terapia intensiva com insulina na função das células beta e no controlo glicémico em doentes com diabetes tipo 2 recentemente diagnosticada: um ensaio multicêntrico randomizado de grupos paralelos. Lancet 2008; 371(9626): 1753-1760.
- Harris MI, Robbins DC: Prevalência de IDDM adulto na população dos EUA. Diabetes Care 1994; 17(11): 1337-1340.
- Laugesen E, et al: Latent autoimmune diabetes of the adult: current knowledge and uncertainty. Diabet Med J Br Diabet Assoc 2015; 32(7): 843-852.
- Wallia A, Molitch ME: Insulinoterapia para diabetes mellitus tipo 2. JAMA 2014; 311(22): 2315-2325.
- Hemmingsen B, et al: comparação de metformina e insulina contra insulina apenas para a diabetes tipo 2: revisão sistemática de ensaios clínicos aleatórios com meta-análises e análises sequenciais de ensaios. BMJ 2012; 344: e1771.
- Monnier L, et al.: Contribuições do jejum e do aumento da glicose plasmática pós-prandial para a hiperglicemia diurna global dos doentes diabéticos de tipo 2 Variações com níveis crescentes de HbA1c. Diabetes Care 2003; 26(3): 881-885.
- Riddle MC, et al: O ensaio treat-to-target: adição aleatória de glargina ou de insulina NPH humana à terapia oral de doentes diabéticos do tipo 2. Diabetes Care 2003; 26(11): 3080-3086.
- Hermansen K, et al: Um ensaio de 26 semanas, aleatório, paralelo, treat-to-target, comparando o detemir de insulina com a insulina NPH como terapia adicional aos medicamentos orais com baixo teor de glucose-baixo em pessoas ingénuas com diabetes tipo 2. Diabetes Care 2006; 29(6): 1269-1274.
- Holman RR, et al: Três anos de eficácia de regimes complexos de insulina na diabetes tipo 2. N Engl J Med 2009; 361(18): 1736-1747.
- http://sgedssed.ch/fileadmin/files/6_empfehlungen_fachpersonen/61_richtlinien_fachaerzte/Neue-Auto-Richtlinien_SGED_15-11-24_DE-DEFkorr.pdf
- Yki-Järvinen H, et al: Efeitos da adição de Linagliptin a regimes de insulina basal para a Diabetes tipo 2 inadequadamente controlada. Diabetes Care 2013; 36(12): 3875-3881.
- Del Prato S: combinação de relação fixa de insulina basal e agonista receptor GLP-1: dois é melhor do que um? Lancet Diabetes Endocrinol 2014; 2(11): 856-858.
- Eng C, et al: agonista do receptor do peptídeo 1 tipo Glucagon e tratamento de combinação de insulina basal para a gestão da diabetes tipo 2: uma revisão sistemática e meta-análise. Lancet 2014; 384(9961): 2228-2234.
- Nauck MA: Actualização sobre desenvolvimentos com inibidores SGLT2 na gestão da diabetes tipo 2. Drug Des Devel Ther 2014; 8: 1335-1380.
- Giugliano D, et al.: Eficácia dos análogos de insulina na consecução do objectivo de hemoglobinaA1c de <7% na diabetes tipo 2: meta-análise de ensaios controlados aleatórios. Diabetes Care 2011; 34(2): 510-517.
PRÁTICA DO GP 2016; 11(5): 8-14