Os tumores malignos do tracto gastrointestinal são frequentes, e a necessidade de mais opções terapêuticas é elevada. Na reunião anual da ASCO deste ano, foram apresentados novos resultados interessantes de estudos para carcinomas colorrectais, bem como para carcinomas do esófago, da junção gastro-esofágica e do estômago. Estes poderão em breve mudar a prática clínica diária.
Os tumores malignos do tracto gastrointestinal são comuns. Nos EUA, são esperados 338 090 novos casos (cerca de 20% de todos os casos malignos recentemente diagnosticados) e 169 280 mortes (cerca de 30% de todas as mortes causadas por casos malignos) este ano [1]. De acordo com o Registo Suíço do Cancro, 22.505 pessoas na Suíça foram diagnosticadas com cancro colorrectal (CRC) durante o período de observação 2013-2017, e 8939 mortes foram causadas pelo CRC. Durante o mesmo período, 5009 das 7727 pessoas que tinham carcinomas do esófago (O), da junção gastro-esofágica (GJ) e do estômago morreram [2]. Estes números sublinham a necessidade de mais opções terapêuticas para o tratamento de doenças tumorais destes sistemas de órgãos.
Na reunião anual da Sociedade Americana de Oncologia ( ASCO), em Junho de 2021, foram apresentados novos resultados de estudos para carcinomas colorrectais e para carcinomas do esófago, da junção gastro-esofágica e do estômago. A seguir, serão apresentados os actuais padrões de tratamento, bem como os avanços científicos de particular interesse recentemente apresentados.
Carcinomas do cólon
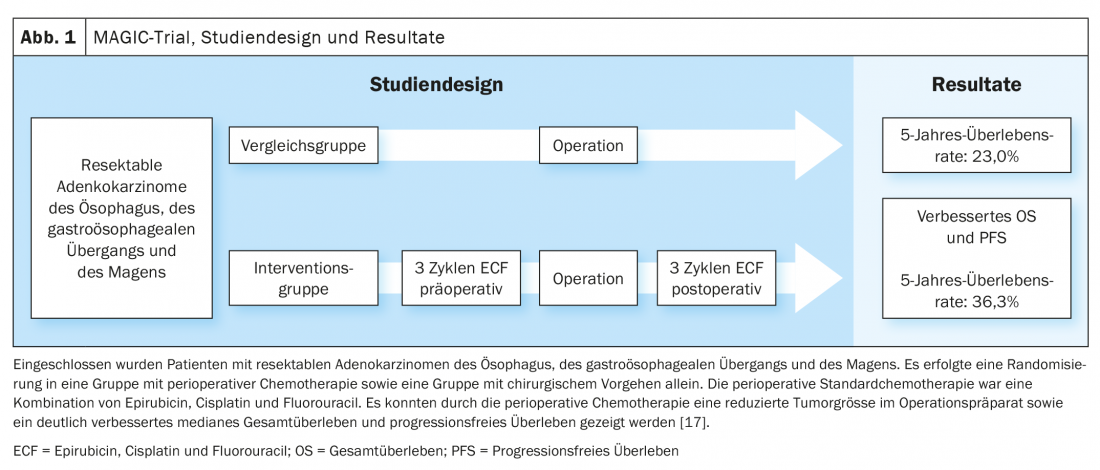
O tratamento padrão do cancro do cólon avançado na primeira linha de tratamento consiste actualmente numa combinação de dois a três agentes quimioterápicos com um anticorpo (Ab) contra o receptor do factor de crescimento epidérmico (EGFR) ou contra o factor de crescimento endotelial vascular (VEGF) (Tab. 1) .
Com o uso crescente da patologia molecular na prática clínica, a análise da instabilidade dos microssatélites (MSI) tornou-se também possível como uma aproximação de possíveis defeitos no sistema de reparação de incompatibilidades de ADN. Mesmo que a frequência da LME no CRC seja dependente de fases e se encontre mais frequentemente nas fases iniciais (I/II: cerca de 20%; III: cerca de 12%; IV: 4-5%) [3], a LME também tem interesse nas fases avançadas do tumor, especialmente em relação às opções de tratamento imunoterapêutico. Le et al. mostrou em 2015 que a presença de deficiência de reparação de desfasamentos (MMR-d) em carcinomas de diferentes origens tecidulares está associada a uma maior taxa de resposta (RR ), maior sobrevivência sem progressão (PFS) e maior sobrevivência global ( OS) quando tratados com pembrolizumab, um anticorpo anti-PD-1. O colectivo deste estudo consistiu numa grande proporção de doentes com CRC [4]. Com base nisto, a utilização do anti-PD-1 Ab pembrolizumab e nivolumab monoclonal – também em combinação com o anti-CTLA4 Ab ipilimumab – está actualmente a ser investigada em doentes com carcinomas avançados do cólon.
Nota-chave-177
O ensaio fase III KEYNOTE-177 comparou a utilização de pembrolizumab (nome comercial KEYTRUDA®; fabricante Merck/MSD) como tratamento de primeira linha para CRC avançado e metastático com um nível elevado de MSI-H (MSI-H) com quimioterapia padrão. 307 pacientes foram aleatorizados para um braço de intervenção com pembrolizumab 200 mg três vezes por semana e um braço comparador com quimioterapia padrão à base de fluorouracil +/- bevacizumab ou cetuximab. Os principais pontos finais foram OS e PFS. A segunda análise intercalar após um período de observação mediano de 32,4 meses já mostrou um mPFS claramente superior para a imunoterapia (16,5 vs. 8,2 meses). A taxa de resposta global (ORR) de acordo com os Critérios de Avaliação de Resposta em Tumores Sólidos (RECIST) foi também significativamente mais elevada no grupo pembrolizumab (43,8% vs. 33,1%). Além disso, houve significativamente menos eventos adversos graves relacionados com o tratamento ( TRAEs) no grupo de intervenção (22% TRAEs ≥grade3 vs. 66%) [5]. Na reunião anual da ASCO 2021, estes dados promissores puderam agora ser confirmados. Após 36 meses, a taxa PFS foi de 42% no braço de intervenção contra 11% no braço padrão. A vantagem ORR para o grupo pembrolizumab foi de 45,1% vs. 33,1%, o que foi ainda mais pronunciado do que na análise anterior. O tempo desde a aleatorização até à próxima linha de terapia ou até à morte do paciente (PFS 2) foi também significativamente mais longo no grupo pembrolizumab (54,0 vs. 24,9 meses). Além disso, o tratamento pembrolizumab mostrou uma taxa de OS significativamente mais elevada após 36 meses (61% vs. 50%). Está incluído no desenho do estudo um cruzamento, e o SO mediano do grupo pembrolizumab ainda não tinha sido alcançado na altura da apresentação na Reunião Anual da ASCO 2021 [6]. Pembrolizumab é aprovado para o tratamento de CRC metastásico com MSI-H como monoterapia na primeira linha de tratamento na Suíça [7].
CheckMate 142
No estudo CheckMate 142 fase II, o papel do nivolumab (nome comercial OPTIVO®; fabricante BMS) está a ser investigado em doentes com CRC MSI-H avançado ou metastático após a progressão sob/depois, ou em caso de intolerância ao fluorouracil em combinação com oxaliplatina e/ou irinotecano. 74 pacientes com ≥3linhas de tratamento prévio foram incluídos e receberam pelo menos uma dose de nivolumab 3 mg/kg de peso corporal de quinze em quinze dias. O ponto final primário foi ORR de acordo com RECIST. Após doze meses, o RR foi de 31% e 69% dos doentes tiveram um curso estável da doença durante pelo menos doze semanas. A duração mediana da resposta ao tratamento ainda não tinha sido alcançada na altura da inclusão dos dados [8]. O desenho do estudo foi alargado durante o curso e foi investigada uma combinação de imunoterapia com nivolumab e ipilimumab de baixa dose (nome comercial YERVOY®; fabricante BMS) como a primeira linha de tratamento para a população de doentes com CRC metastásico. Aqui, foi observado um RR de 64%, uma resposta completa (CR) em 9% e um controlo sustentado da doença após 24 meses em 79% dos casos [9]. Nivolumab é aprovado como monoterapia ou em combinação com ipilimumab para o tratamento de pacientes adultos com CRC metastásico com MMR-d/MSI-H após terapia prévia à base de fluoropyrimidina em combinação com irinotecano ou oxaliplatina na Suíça [7,10]. Está disponível uma recomendação sobre a cobertura de custos para o nivolumab do Gabinete Federal de Saúde Pública (FOPH) da Confederação Suíça, mas não para o ipilimumab [7].
Carcinomas do esófago, da junção gastro-esofágica e do estômago
CheckMate 648
Até agora, o prognóstico do carcinoma espinocelular avançado do esófago tem sido, infelizmente, significativamente limitado com um OS médio de cerca de dez meses – apesar do uso de agentes quimioterápicos. O ensaio CheckMate 648 está agora a comparar apenas a quimioterapia com a combinação de quimioterapia e nivolumab, e com a combinação da imunoterapêutica nivolumab e ipilimumab na primeira linha de tratamento. Cerca de 1000 doentes com carcinoma espinocelular avançado do esófago foram randomizados para três grupos de tratamento, independentemente do seu estatuto PD-L1: (1) nivolumab (240 mg quinzenalmente) e quimioterapia (fluorouracil e cisplatina quatro vezes por semana); (2) nivolumab (3 mg/kg de peso corporal quinzenalmente) e ipilimumab (1 mg/kg de peso corporal seis vezes por semana); (3) quimioterapia apenas. Os pontos finais primários foram OS e PFS no grupo de doentes com expressão PD-L1 ≥1%. Os pontos finais secundários foram definidos como OS, PFS e RR em todos os pacientes independentemente da expressão PD-L1.
Aos doze meses, a população com expressão PD-L1 ≥1%mostrou uma taxa de SO de 58% no grupo nivolumabe + quimioterapia contra 37% no grupo de quimioterapia e um benefício de sobrevivência mediano de 6,3 meses para a combinação nivolumabe + quimioterapia. Isto também foi confirmado nos pacientes que foram incluídos independentemente da expressão PD-L1, com uma taxa de SO de 54% vs. 44% e um benefício de sobrevivência de 2,5 meses. No entanto, uma análise mais atenta da análise do subgrupo com uma repartição do benefício de sobrevivência de acordo com o estatuto PD-L1 mostra que existe um efeito dominante da subpopulação PD-L1-positiva e que o benefício de sobrevivência detectável é impulsionado principalmente por este subgrupo. Se os doentes PD-L1-negativos beneficiam de PD-L1 continua a ser questionável. Houve também vantagens clinicamente significativas para o nivolumab + quimioterapia em termos de PFS e RR.
A comparação entre nivolumab + ipilimumab e a quimioterapia produziu resultados semelhantes com uma OS de 57% vs 37% aos 12 meses e um benefício de sobrevivência de 4,6 meses com imunoterapia na população de pacientes com expressão PD-L1 ≥1%. A análise dos subgrupos de acordo com o estatuto PD-L1 é muito semelhante à comparação de nivolumab + quimioterapia vs. quimioterapia. Com base nestes dados, o uso de nivolumab + quimioterapia e nivolumab + ipilimumab em doentes com carcinoma espinocelular PD-L1-positivo avançado do esófago deve ser considerado o novo padrão. Actualmente, o nivolumab e o ipilimumab ainda não estão aprovados para esta indicação na Suíça [7,10]. Para pacientes com cancro de esófago PD-L1-negativo, a quimioterapia por si só continua a ser uma opção.
Se o nivolumab fosse aprovado nesta indicação na primeira linha de terapia, isto alteraria a sequência de opções terapêuticas, pelo menos para os pacientes com tumores PD-L1-positivos. Até à data, o nivolumab foi indicado para o tratamento de adenocarcinoma avançado ou recorrente do estômago ou GEJ após duas ou mais terapias sistémicas prévias – actualmente é necessária uma aprovação de custos na Suíça [7,10]. Assim, se o uso for agora transferido para a primeira linha de tratamento, esta opção de medicamento deve ser reconsiderada em linhas de tratamento posteriores. A ponderação de factores específicos do doente – por exemplo a presença de doenças auto-imunes – poderia ser um princípio orientador aqui. Em princípio, a utilização das opções terapêuticas mais eficazes no início do tratamento é um princípio oncológico comum e sugere a utilização da imunoterapia na primeira linha de tratamento, desde que não haja contra-indicações.
CheckMate 649
Enzinger et al. estabeleceu o FOLFOX (fluorouracil, leucovorin, oxaliplatina) como regime de quimioterapia de primeira linha para o tratamento de doentes com carcinoma metastático da Ö/GEJ em 2016. O seu estudo mostrou OS e PFS comparáveis com a então terapia padrão ECF (epirubicina, cisplatina, fluorouracil) vs FOLFOX para esta população de doentes, predominantemente adenocarcinomas [11]. Tanto no braço de intervenção como no grupo de controlo, a quimioterapia foi combinada com o cetuximab. Contudo, isto não corresponde a um regime terapêutico padrão estabelecido para carcinomas da Ö/GEJ e do estômago e não permite tirar conclusões sobre o benefício específico do grupo ao utilizar o anti-EGFR-Ab em ambos os grupos de estudo.
CheckMate 649 compara agora apenas a quimioterapia padrão (CAPOX, capecitabina e oxalplatina três vezes por semana ou FOLFOX fluorouracil duas vezes por semana) com o tratamento combinado de quimioterapia e nivolumab (360 mg três vezes por semana ou 240 mg duas vezes por semana) e com a combinação de imunoterapia de nivolumab + ipilimumab na primeira linha de tratamento. Foram incluídos doentes com adenocarcinomas avançados da Ö/GEJ e estômago. Os pontos finais primários para o grupo nivolumab + quimioterapia e para o grupo de quimioterapia foram PFS e OS em pacientes com pontuação positiva combinada (ACP) ≥5%– onde a ACP descreve a proporção de células imunitárias e tumores PD-L1 positivos (linfócitos e macrófagos) em relação a todas as células tumorais. Após um período de observação de aproximadamente um ano, houve uma superioridade significativa de nivolumab + quimioterapia tanto em PFS como em OS. Este efeito também poderia ser verificado para os pacientes com uma SCP [12]%e todos os pacientes aleatorizados ≥1 . Dados adicionais de subgrupos foram agora apresentados na reunião anual da ASCO. Aqui, os benefícios de OS e PFS da nivolumab + quimioterapia foram mais pronunciados em doentes com carcinomas com limiares PD-L1 mais elevados. Na população em geral, foi observado um benefício para a imunoterapia independentemente do estatuto da PD-L1, embora, tal como no CheckMate 648, este tenha sido impulsionado pela subpopulação PD-L1-positiva. Para adenocarcinomas PD-L1 positivos da Ö/GEJ e estômago, FOLFOX combinado com nivolumab é assim um novo padrão. Nivolumab não está actualmente aprovado para esta indicação na Suíça [7]. Os dados sobre o braço de estudo com nivolumab + ipilimumab ainda estão pendentes [13].
KEYNOTE-811
O ensaio REAL-2, um estudo não-inferioritário, estabeleceu o CAPOX em 2008 como alternativa ao fluorouracil e ao cisplatina no tratamento do carcinoma avançado do oe/GEJ e do estômago, independentemente da histologia. Uma fluoropyrimidina e um composto de platina foram cada um combinado com a epirubicina anthracycline [14].
No ensaio ToGA, um estudo aleatório da fase III, a adição de trastuzumab, um anti-HER2-Ab, a esta quimioterapia padrão (capecitabina e cisplatina, ou fluorouracil e cisplatina) foi então investigada na terapia de primeira linha. Foram incluídos doentes com carcinomas HER-2 positivos avançados do estômago e GEJ. A combinação tripla existente de REAL-2 com uma antraciclina não foi integrada no desenho deste estudo devido à cardiotoxicidade deste grupo de fármacos e às propriedades cardiotóxicas do trastuzumabe. Devido a um aumento significativo do OS, a combinação de quimioterapia e trastuzumab tornou-se o novo padrão de cuidados nesta população de doentes [15].
No estudo KEYNOTE-811, a adição de pembrolizumab 200 mg de três em três semanas à norma acima referida no tratamento de primeira linha está agora a ser investigada para este mesmo grupo de pacientes. Os resultados iniciais foram apresentados na reunião anual da ASCO 2021: Houve uma RR significativamente melhorada de 74,4% vs. 51,9% e uma taxa de RC de 11,3% vs. 3,1% com pembrolizumab + quimioterapia. A taxa de remissão parcial foi de 63% contra 49%. Os pontos finais primários OS e PFS ainda estão pendentes [16].
CROSS Update/Neo-AEGIS Update
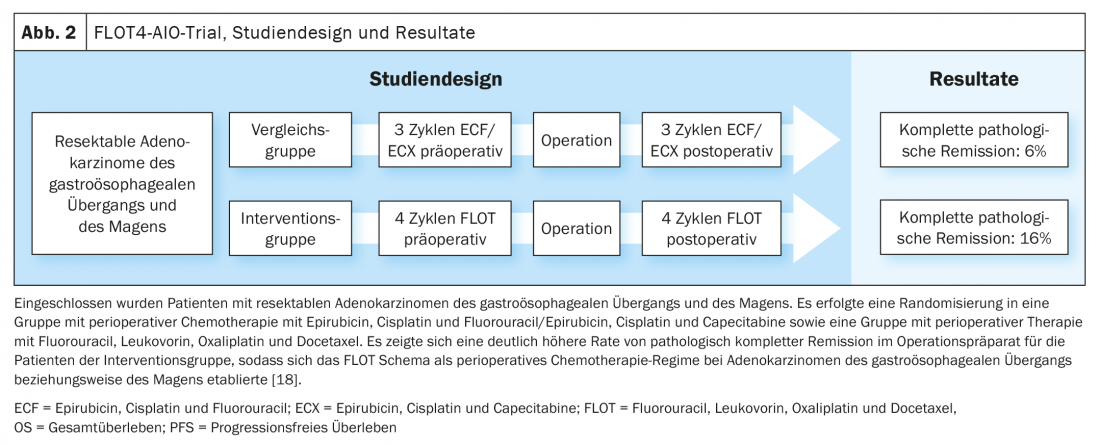
Com base nos dados do estudo MAGIC e no desenvolvimento do conceito de tratamento no estudo FLOT4-AIO, a quimioterapia perioperatória com FLOT (fluorouracil, leucovorina, oxaliplatina, docetaxel) tornou-se uma opção de tratamento curativa estabelecida para carcinomas gastroesofágicos (Fig. 1, Fig. 2) [17,18]. Isto contrasta com o conceito de terapia trimodal do estudo CROSS (Fig. 3) [19]. A questão de qual das duas abordagens – a quimioterapia perioperatória (protocolo MAGIC/FLOT) ou a radiochemoterapia neoadjuvante análoga à CROSS – oferece uma vantagem está actualmente a ser tratada pelo estudo Neo-AEGIS.
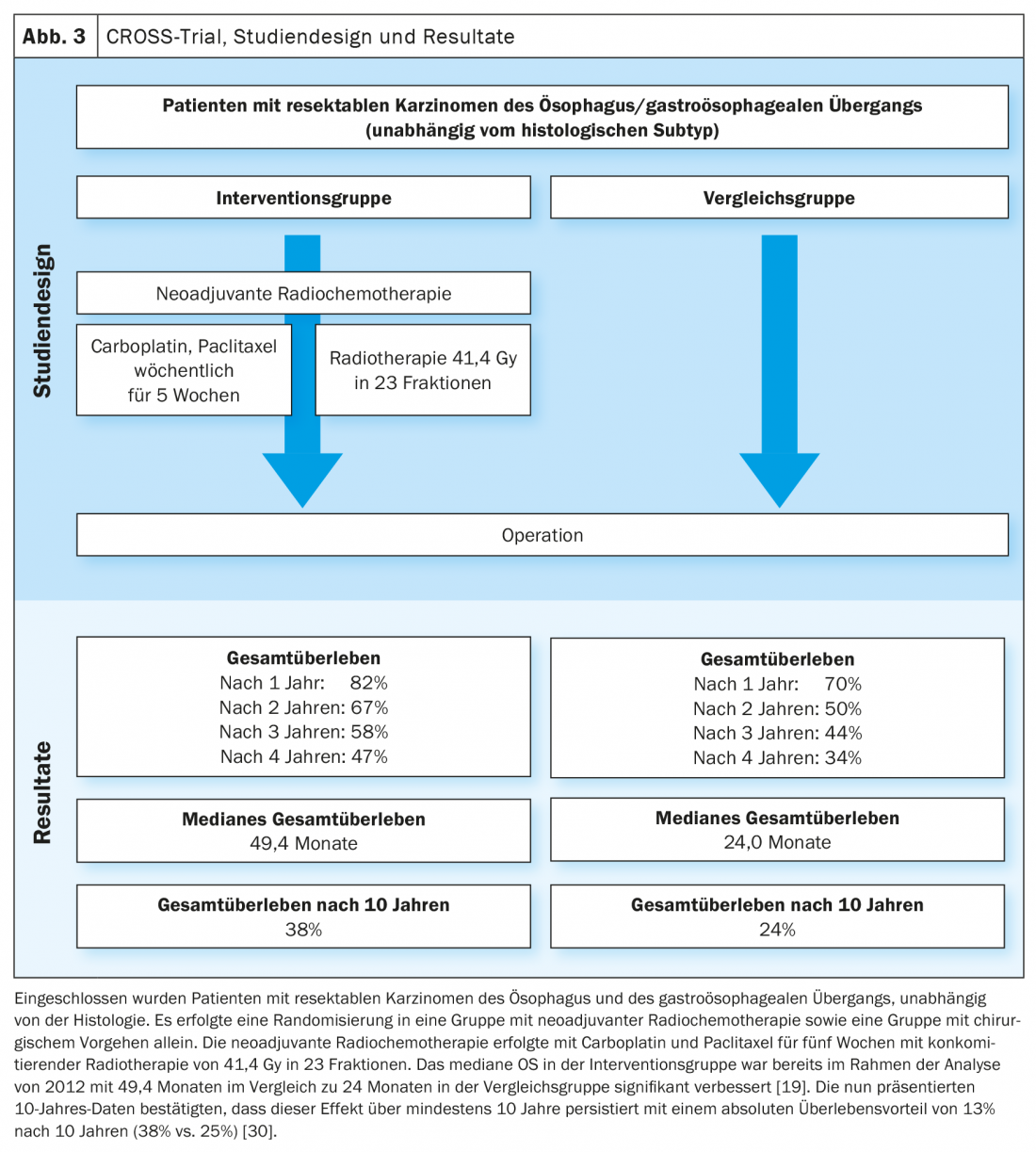
Para este efeito, os pacientes com adenocarcinomas ressecáveis da Ö/GEJ foram randomizados 1:1 para quimioterapia perioperatória (inicialmente análoga à MAGIC, no curso análogo à FLOT4-AIO) e a terapia trimodal análoga à CROSS [20]. Na análise actual (ASCO 2021), foi seguida uma abordagem de não-inferioridade. Não houve provas de clara inferioridade da quimioterapia perioperatória em comparação com a abordagem trimodal. No entanto, os pacientes tratados com CROSS mostraram uma taxa mais elevada de ressecção saudável (R0), mais gânglios linfáticos histologicamente negativos após terapia prévia (ypN0), um grau mais elevado de regressão tumoral e CR patológica. A taxa de neutropenia ≥Grade3 e o número de sepses neutropénicas foram mais elevados no grupo de quimioterapia perioperatória, enquanto as mortes pós-operatórias em pneumonia hospitalar/pós-operatória e SARA, bem como as insuficiências anastomóticas foram aproximadamente igualmente frequentes. O principal ponto final do estudo foi o OS, que mostrou um resultado comparável após um período de observação de três anos [21].
Assim, uma recomendação clara ainda não pode ser derivada dos dados actuais do estudo Neo-AEGIS. Os factores do paciente como as comorbilidades devem ser tidos em conta ao seleccionar o conceito terapêutico. Além disso, as opções terapêuticas subsequentes também devem ser incluídas na escolha da terapia. Assim, após o regime CROSS, a imunoterapia adjuvante com nivolumab é concebível, análoga ao estudo CheckMate 577. Para investigar isto, pacientes com evidência de células cancerígenas residuais na amostra cirúrgica após terapia trimodal foram randomizados para um grupo de intervenção com nivolumab e um grupo de controlo com placebo. No grupo nivolumab (22,4 meses vs. 11,0 meses), houve uma sobrevivência sem doenças significativamente mais longa [22]. Nivolumab é aprovado na Suíça para esta indicação, embora a FOPH não recomende actualmente que os custos sejam cobertos [7,10].
GO2
Muitos estudos que moldam a paisagem oncológica são baseados em populações com uma idade média de cerca de 60 anos. No entanto, isto reflecte apenas de forma limitada a realidade da vida quotidiana em oncologia, uma vez que a população de doentes oncológicos é cada vez mais composta por doentes mais velhos com comorbilidades ou limitações relacionadas com a idade no seu estado de saúde.
Esta questão foi abordada na Reunião Anual da ASCO de 2021 para pacientes com cancro gastroesofágico avançado. O ensaio GO2 fase III incluiu uma população de doentes com uma idade média de 76 anos. Quimioterapia paliativa trimestral com CAPOX foi administrada a três níveis de dose: dose completa (oxaliplatina 130 mg/m2 no dia 1 e capecitabina 625 mg/m2 duas vezes por dia nos dias 1-14) e 80% e 60% desta dose. Uma abordagem de não-inferioridademostrou PFS comparável, sem reduções significativas entre os três grupos de dosagem, com melhor tolerabilidade global do nível de dosagem mais baixo [23].
Mensagens Take-Home
- A imunoterapia com pembrolizumab leva a uma melhor sobrevivência sem progressão e sobrevivência global, bem como a uma maior taxa de resposta ao tratamento do que a quimioterapia padrão no tratamento de primeira linha do cancro do cólon avançado e metastásico com elevada instabilidade por microsatélite (MSI-H).
- A combinação de nivolumabe e quimioterapia, bem como a imunoterapia combinada com nivolumabe e ipilimumabe, resultam numa melhor sobrevivência global do que apenas a quimioterapia padrão no tratamento de primeira linha do carcinoma espinocelular avançado do esófago com expressão PD-L1 ≥1%.
- A combinação de nivolumab e quimioterapia resulta em melhor sobrevivência sem progressão e sobrevivência global do que apenas a quimioterapia padrão no tratamento de adenocarcinoma avançado do esófago, junção gastro-esofágica e estômago, particularmente na subpopulação PD-L1 positiva.
- A quimioterapia perioperatória não é inferior à abordagem do tratamento trimodal com radiochemoterapia neoadjuvante no tratamento curativo dos adenocarcinomas ressecáveis do esófago e da junção gastro-esofágica em termos de sobrevivência global, mas leva mais frequentemente à neutropenia e consegue menos ressecções R0 e
- Regressão tumoral em tumores primários e gânglios linfáticos.
Literatura:
- Siegel RL, et al: Cancer Statistics 2021. CA Cancer J Clin. 2021; 71: 7-33.
- Registo Nacional do Cancro, www.nkrs.ch/de/stat (acedido pela última vez em Setembro de 2021)
- Battaglin F, et al: Microsatellite instability in colorectal cancer: overview of its clinical significance and novel perspectives. Clin Adv Hematol Oncol. 2018; 16(11): 735-745.
- Le DT, et al: PD-1 Blockade in Tumors with Mismatch-Repair Deficiency. N Engl J Med. 2015; 372(26): 2509-2520.
- André T, et al: Pembrolizumab em Microsatellite-Instability-High Advanced Colorectal Cancer. N Engl J Med. 2020; 383(23): 2207-2218.
- André T, et al.: Sobrevivência global final para o estudo fase III KN177: pembrolizumab versus quimioterapia em microsatélite de instabilidade – deficiência de reparação de alta/melhança (MSI-H/dMMR) cancro colorrectal metastático (mCRC). Resumo 3500, Reunião Virtual ASCO 2021, 4-8 de Junho de 2021.
- Escritório Federal de Saúde Pública FOPH: Spezialitätenliste. www.spezialitätenliste.ch (acessado pela última vez em Setembro de 2021)
- Overman MJ, et al: Nivolumab em doentes com deficiência de reparação de incompatibilidade de ADN metastático ou de instabilidade por microsatélite – cancro colorrectal elevado (CheckMate 142): um estudo aberto, multicêntrico, fase 2. Lancet Oncol. 2017; 18(9): 1182-1191. erratum in: Lancet Oncol. 2017; 18(9).
- Helwick C: CheckMate 142 Análise Actualizada: Primeira Linha de Nivolumab Plus Ipilimumab em MSI-H/dMMR Metastatic Colorectal Cancer. Correio ASCO. 2020. https://ascopost.com/issues/april-25-2020/checkmate-142-updated-analysis/
- Compêndio OPTIVO. https://compendium.ch/product/1310903-opdivo-inf-konz-40-mg-4ml/mpro#MPro7100 (acedido pela última vez em Setembro de 2021)
- Enzinger PC, et al: CALGB 80403 (Alliance)/E1206: Um Estudo Aleatório de Fase II de Três Regimes de Quimioterapia Mais Cetuximab em Cancros de Junção Esofágica e Gastroesofágica Metástática. J Clin Oncol. 2016; 34(23): 2736-2742.
- Janjigian YY, et al: nivolumab de primeira linha mais quimioterapia versus quimioterapia apenas para junção gástrica avançada, gastro-esofágica, e adenocarcinoma esofágico (CheckMate 649): um ensaio aleatório, aberto, fase 3. Lanceta. 2021; 398(10294): 27-40.
- Moehler MH, et al: nivolumab de primeira linha (1L) mais quimioterapia (quimioterapia) versus quimioterapia no cancro gástrico avançado/ancerto gastroesofágico de junção cancro/adenocarcinoma do esófago (GC/GEJC/EAC): Dados de eficácia e segurança expandidos da Checkmate 649. Resumo 4002, Reunião Virtual ASCO 2021, 4-8 de Junho de 2021.
- Cunningham D, et al: Capecitabina e Oxaliplatina para Cancro Esofagogástrico Avançado. N Engl J Med. 2008; 358: 36-46.
- Bang YJ, et al: Trastuzumab em combinação com quimioterapia versus quimioterapia apenas para o tratamento do cancro de junção gástrico ou gastro-esofágico avançado HER2-positivo (ToGA): uma fase 3, rótulo aberto, ensaio controlado aleatório. Lanceta. 2010; 376: 687-697.
- Janjigian YY, et al: Pembrolizumab plus trastuzumab e quimioterapia para a junção gástrica ou gastroesofágica (G/GEJ) do HER2+ cancro: resultados iniciais do estudo global da fase 3 KEYNOTE-811. Resumo 4013, Reunião Virtual ASCO 2021, 4-8 de Junho de 2021.
- Cunningham D, et al: Quimioterapia Perioperatória versus Cirurgia Sozinha para Câncer Gastroesofágico Resectável. N Engl J Med. 2006; 355: 11-20.
- Al-Batran SE, et al: regressão histopatológica após docetaxel neoadjuvante, oxaliplatina, fluorouracil, e leucovorina versus epirubicina, cisplatina, e fluorouracil ou capecitabina em pacientes com adenocarcinoma de junção gástrico ou gastro-esofágico ressecável (FLOT4-AIO): resulta da parte da fase 2 de um ensaio multicêntrico, aberto, fase 2/3 aleatorizado. Lancet Oncol. 2016; 17: 1697-1708.
- Van Hagen P, et al: Quimioradioterapia peroperatória para o cancro esofágico ou juncional. N Engl J Med 2012; 366; 2074-2084.
- Reynolds JV, et al: ICORG 10-14: ensaio NEOadjuvant no Adenocarcinoma do esófago e da junção esofágica Estudo Internacional (Neo-AEGIS). BMC Cancro. 2017; 17: 401.
- Reynolds JV, et al: Neo-AEGIS (ensaio Neoadjuvant no Adenocarcinoma do Esophagus e Esophago-Gastric Junction International Study): Resultados preliminares da fase III RCT de CROSS versus quimioterapia perioperatória (Protocolo modificado MAGIC ou FLOT). Resumo 4004, Reunião Virtual ASCO 2021, 4-8 de Junho de 2021.
- Kelly RJ, et al: CheckMate 577 Investigadores. Nivolumab Adjuvante em Câncer de Junção Esofágica ou Gastroesofágica Ressecada. N Engl J Med. 2021; 384(13): 1191-1203.
- Hall PS, et al: Eficácia da quimioterapia de intensidade reduzida com Oxaliplatina e Capecitabina sobre Qualidade de Vida e Controlo do Cancro entre Pacientes Mais Velhos e Fracos com Cancro Gastroesofágico Avançado. O ensaio clínico aleatório da Fase 3 do GO2. JAMA Oncol. 2021; 7(6): 869-877.
- De Gramont A, et al: Leucovorin e fluorouracil com ou sem oxaliplatina como tratamento de primeira linha no cancro colorrectal avançado. J Clin Oncol. 2000; 18(16): 2938-2947.
- Douillard JY, et al: Irinotecan combinado com fluorouracil em comparação apenas com fluorouracil como tratamento de primeira linha para o cancro colorrectal metastático: um ensaio multicêntrico aleatório. Lanceta. 2000; 355(9209): 1041-1047. Erratum in: Lanceta. 2000; 355(9212): 1372.
- Saltz LB, et al: Bevacizumab em combinação com quimioterapia à base de oxaliplatina como terapia de primeira linha no cancro colorrectal metastático: um estudo aleatório de fase III. J Clin Oncol. 2008; 26(12): 2013-2019. erratum in: J Clin Oncol. 2008; 26(18): 3110. erratum in: J Clin Oncol. 2009; 27(4): 653.
- Douillard JY, et al: Tratamento Panitumumab-FOLFOX4 e mutações RAS no cancro colorrectal. N Engl J Med. 2013; 369(11): 1023-1034.
- Van Cutsem E, et al: Fluorouracil, leucovorin, e irinotecan mais tratamento com cetuximab e mutações RAS no cancro colorrectal. J Clin Oncol. 2015; 33(7): 692-700.
- Cremolini C, et al: FOLFOXIRI plus bevacizumab versus FOLFIRI plus bevacizumab como tratamento de primeira linha de pacientes com cancro colorrectal metastático: análises globais actualizadas de sobrevivência e subgrupos moleculares do rótulo aberto, estudo fase 3 TRIBE. Lancet Oncol. 2015; 16(13): 1306-1315.
- Eyck BM, et al: Dez anos de resultado da Quimioterapia Neoadjuvante Plus Cirurgia para o Cancro Esofágico: O Ensaio CROSS Controlado Aleatório. J Clin Oncol. 2021; 39(18): 1995-2004.
InFo ONCOLOGy & HaEMATOLOGy 2021; 9(5): 12-18