O prognóstico da amiloidose de cadeia leve (AL), uma discrasia de células plasmáticas, é largamente determinado pela presença de envolvimento cardíaco. O estadiamento convencional baseia-se em biomarcadores cardíacos e na diferença nas cadeias leves livres. Um novo estudo procurou agora avaliar o papel dos parâmetros ecocardiográficos como marcadores de prognóstico na amiloidose AL e investigar a sua utilidade em comparação com o estadiamento convencional.
A amiloidose cardíaca é o arquétipo da cardiomiopatia infiltrativa e apresenta-se frequentemente com o fenótipo clínico de insuficiência cardíaca com fração de ejeção preservada. A amiloidose sistémica de cadeias leves (amiloidose AL) é uma discrasia de células plasmáticas com envolvimento multissistémico; no entanto, o prognóstico da amiloidose AL está frequentemente relacionado com o envolvimento cardíaco. Isto reflecte-se na utilização da “pontuação de Mayo” no estadiamento da amiloidose AL. Este score inclui os biomarcadores cardíacos troponina de alta sensibilidade (hs-Trop) e o péptido natriurético N-terminal pró-cérebro (NT-proBNP), bem como a diferença de cadeias leves livres (dFLC) [2].
Embora as pontuações originais e revistas de Mayo para classificar a amiloidose AL tenham demonstrado a sua utilidade prognóstica, existem limitações à utilização destes biomarcadores. As diferenças entre os testes de troponina utilizados nos diferentes centros, por exemplo, hs-TropI e hs-TropT, cada um com os seus próprios intervalos definidos, dificultam as comparações ao longo do tempo. Os testes para NT-proBNP também mudaram ao longo do tempo, representando implicações semelhantes às da troponina. Além disso, tanto a troponina como o NT-proBNP são influenciados por factores como o índice de massa corporal e a insuficiência renal coexistente, sendo esta última relativamente comum na amiloidose AL sistémica.
Em contraste, os marcadores ecocardiográficos tradicionais da estrutura e função cardíacas são padronizados e têm intervalos normais universalmente definidos. Além disso, um ecocardiograma transtorácico (ETT) é realizado rotineiramente em pacientes com amiloidose AL para avaliar o envolvimento cardíaco, pois é barato e amplamente disponível. Novos índices ecocardiográficos, como o strain longitudinal global do ventrículo esquerdo (SLGVE), foram validados para uma vasta gama de processos patológicos e são cada vez mais utilizados na avaliação clínica da amiloidose AL [3]. Assim, um estudo recente investigou a utilidade prognóstica dos parâmetros ecocardiográficos em comparação com o estadiamento de Mayo em doentes com amiloidose AL [1].
Características dos doentes e parâmetros ecocardiográficos
Foram identificados retrospetivamente 75 doentes consecutivos com amiloidose AL que foram avaliados numa clínica de amiloidose de referência e submetidos a um exame ecocardiográfico completo. A idade média foi de 61,8 ± 10 anos e 51/75 doentes eram do sexo masculino. 71 dos 75 doentes receberam quimioterapia, a maioria com bortezomib (Velcade), ciclofosfamida e dexametasona (VCD; 30/75); 11 doentes foram submetidos a transplante alogénico de células estaminais. 25 doentes foram classificados como estádio I de Mayo, 22 como estádio II, enquanto os estádios III e IV incluíam 15 e 13 doentes, respetivamente.
Os parâmetros ecocardiográficos estudados incluíram a fração de ejeção do ventrículo esquerdo, a massa, os parâmetros da função diastólica, o strain longitudinal global (SLG) e o volume da aurícula esquerda (AE). A mortalidade foi determinada através de uma revisão dos registos clínicos. Durante um seguimento médio de 51 meses, 29/75 (39%) doentes morreram. Os pacientes foram divididos em dois subgrupos com base na mortalidade, que não diferiram em idade, sexo ou índice de massa corporal, embora a pressão arterial sistólica tenha alcançado significância estatística (p=0,051). 11 doentes tinham FA; a taxa de FA foi semelhante nos dois grupos: 6/46 (13%) nos sobreviventes versus 5/29 (17%) nos não sobreviventes (p=0,617). Os pacientes que morreram tinham um volume do AE significativamente maior (35 ± 10 vs. 47 ± 12 mL/m2, p<0,001) e maior E/e’ (14 ± 6 vs. 18 ± 10, p=0,026); tanto a massa do VE como o SLGVE aproximaram-se da significância estatística. Não se registaram diferenças entre os grupos na função sistólica do VE avaliada pela FEVE. Como esperado, a mortalidade aumentou com o aumento do estádio de Mayo e foi de 8, 45, 60 e 62%, respetivamente, para os doentes nos estádios I-IV de Mayo.
Estadio de Mayo e preditores ecocardiográficos univariados de sobrevivência
A análise univariada mostrou que os parâmetros ecocardiográficos que prediziam mortalidade com uma significância de p<0,1 incluíam o IAAV, velocidade e’, E/e’ e SLVE. O estádio de Mayo foi também um fator de previsão independente da sobrevivência. Os preditores ecocardiográficos univariados de mortalidade (significância de p<0,1) foram introduzidos num modelo multivariável de riscos proporcionais de Cox e incluíram E/e’ e volume do AE e SLVE (a velocidade e’ não foi incluída no modelo devido à colinearidade com E/e’). Neste modelo multivariável de parâmetros ecocardiográficos, o IAAV foi o único preditor ecocardiográfico independente de mortalidade. O volume indexado da aurícula esquerda correlacionou-se com o estadio de Mayo (coeficiente de correlação de Spearman 0,5, p<0,001), e todos os doentes nos estadios III e IV de Mayo tinham aurículas esquerdas dilatadas (LAVI ≥34 mL/m2).
Classificação dos doentes em três grupos de risco diferentes
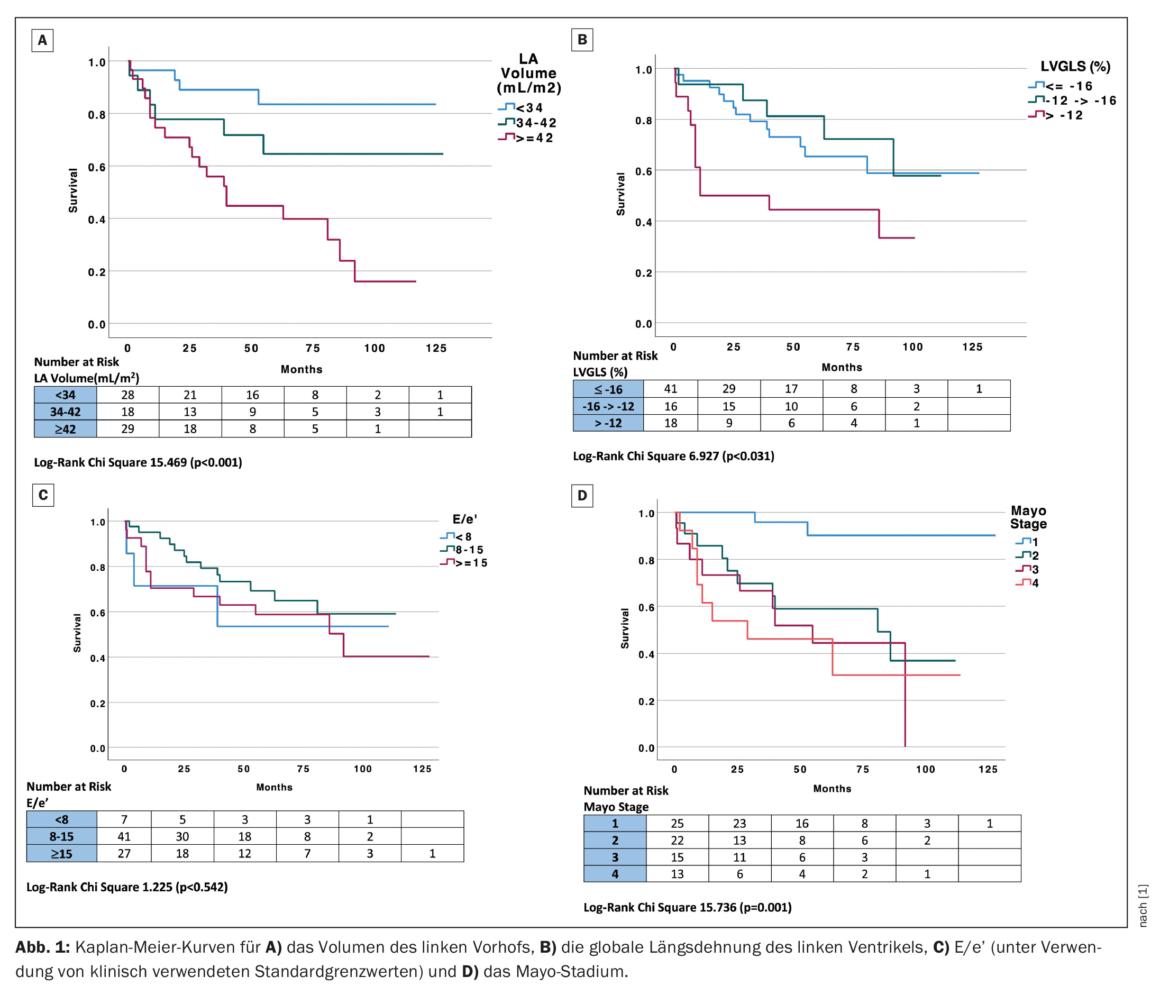
LVGLS (função sistólica do ventrículo esquerdo), LAVI e E/e’ (função diastólica) foram analisadas como variáveis categóricas utilizando valores de corte clinicamente aplicáveis para avaliar o seu impacto na mortalidade em comparação com o estádio de Mayo. A deformação longitudinal global do ventrículo esquerdo foi dividida em três grupos com base no ponto de corte clínico previamente relatado de melhor que -16, -12 a -16% e pior que -12% para SLG normal, reduzido e gravemente reduzido, respetivamente [4]. O volume indexado da aurícula esquerda foi dividido em três grupos utilizando um cut-off clínico de ≤34, 34-42 e ≥42 mL/m2, correspondendo a normal, dilatação ligeira a moderada da VAE ou dilatação superior a moderada da VAE [5]. A ‘E/e’ foi classificada em três grupos com base em valores clínicos de <8, 8-15 e ≥15, correspondendo a pressão de enchimento do VE normal, provavelmente anormal e elevada [6]. A estratificação por grupo clínico de LAVI (p<0,001), LVGLS (p=0,031) e estádio de Mayo (p=0,001) foram preditores significativos de mortalidade, enquanto que E/e’ não atingiu significância na análise de Kaplan-Meier (Fig. 1) [1]. De notar que os doentes com um LAVI normal <34 mL/m2 tiveram resultados particularmente bons a longo prazo (seguimento mediano de 60,5 ± 46 meses) e, inversamente, os doentes com um SLVE inferior a -12% tiveram um mau resultado.
Sistema de pontuação para dilatação da aurícula esquerda e redução da tensão longitudinal global do ventrículo esquerdo
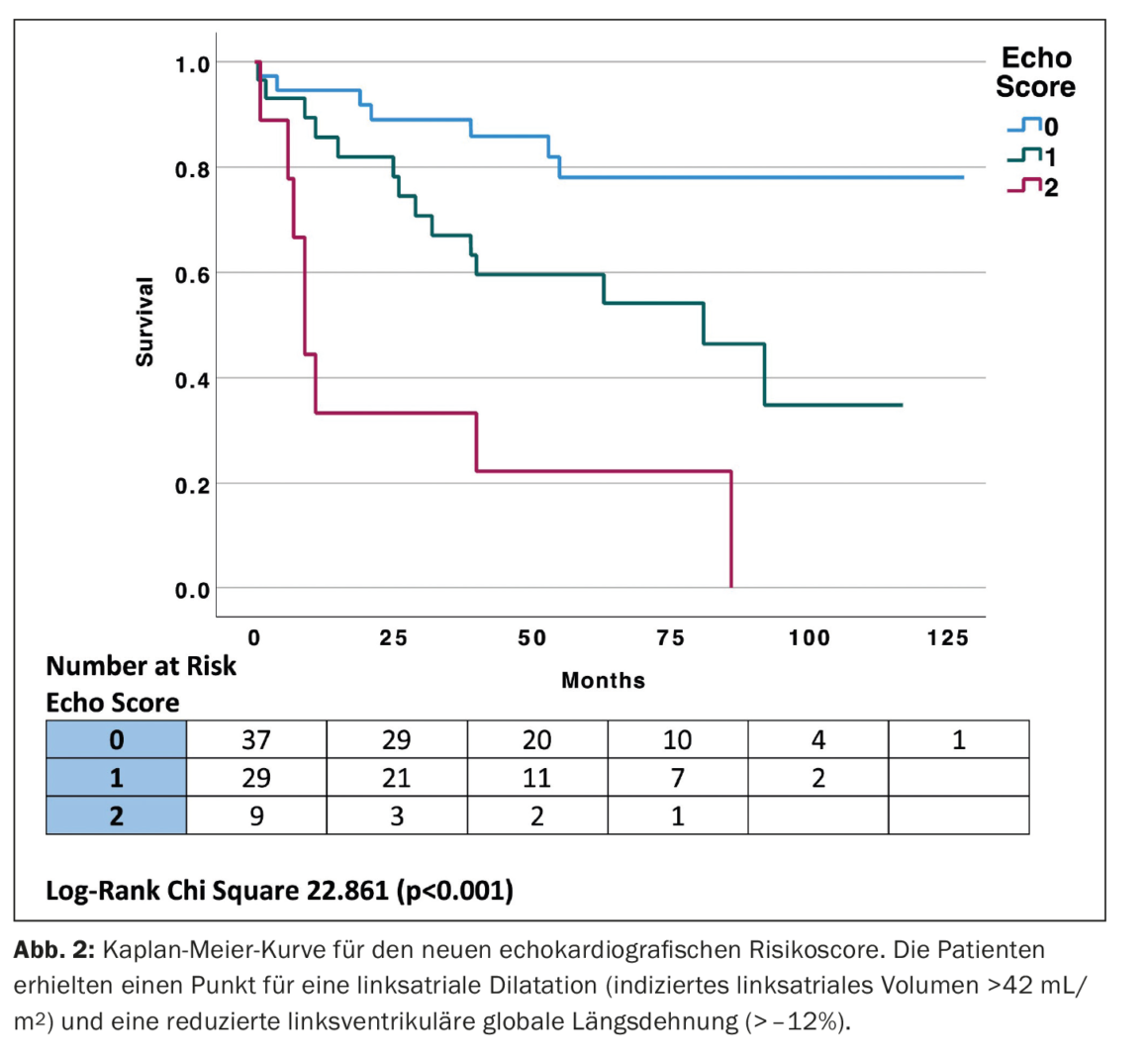
Utilizando os valores de corte clínicos para LVGLS e LAVI para gerar uma pontuação ecocardiográfica simples, o grupo de maior risco apresentou tanto LVGLS (pior que -12%) como LAVI (>42 mL/m2), o grupo de risco intermédio tinha um SLVE -12 a -16% e um IAF 34-42 mL/m2, e o grupo de risco mais baixo tinha um SLVE melhor que -16% e um IAF <34 mL/m2. Um escore de risco foi então gerado atribuindo um ponto para cada LVGLS pior que -12% e LAVI >34 mL/m2, colocando os pacientes em um dos três grupos. O grupo de risco mais elevado tinha tanto LVGLS (pior que -12%) como LAVI (>42 mL/m2), o grupo de risco intermédio tinha um SLVE pior do que -12% ou um IVLA >42 mL/m2 e o grupo de risco mais baixo tinha um SLVE melhor que -12% e um IVLA <42 mL/m2 com dois, um e zero pontos, respetivamente. Foram criadas curvas de Kaplan-Meier para o novo score de risco ecocardiográfico (Echo Score) (Fig. 2) [1]. A nova “pontuação eco” teve um desempenho prognóstico semelhante ao estádio de Mayo [AUC 0,745, intervalo de confiança (IC) de 95% 0,638-0,853 vs AUC 0,752, IC de 95% 0,645-0,858, p=0,911].
Previsão de mortalidade por todas as causas comparável com o atual sistema de estadiamento de Mayo
A variabilidade intra e interobservador da LAVI foi excelente, com um coeficiente de correlação intraclasse de 0,987 (IC 95% 0,946-0,997), enquanto o coeficiente de correlação interobservador foi de 0,935 (IC 95% 0,731-0,984). O SLVE também foi altamente reprodutível com um coeficiente de correlação intraclasse de 0,989 (IC 95% 0,864-0,998), enquanto o coeficiente de correlação interobservador foi de 0,980 (IC 95% 0,924-0,995). A fração de ejeção do ventrículo esquerdo mostrou uma boa variabilidade intra e interobservador, com um coeficiente de correlação intraclasse de 0,871 (IC 95% 0,517-0,967) e um coeficiente interobservador de 0,772 (IC 95% 0,115-0,943). Estes resultados mostram que a imagiologia cardíaca pode ser utilizada para identificar doentes com maior mortalidade, de modo a que essa estratificação de risco possa potencialmente levar à seleção de terapias óptimas.
Mensagens Take-Home
- Um parâmetro ecocardiográfico simples, o IVAS, foi um marcador de prognóstico independente em doentes com amiloidose AL.
- O volume indexado do átrio esquerdo e o SLVE estratificados por valores de corte clínicos mostraram piores resultados com um SLVE pior e um LAVI crescente.
- Um score ecocardiográfico composto derivado do LAVI e do LVGLS tem um valor preditivo semelhante ao estadiamento de Mayo.
Literatura:
- Genty P, et al.: A novel echocardiographic risk score for light-chain amyloidosis. Eur Heart J 2023; https://doi.org/10.1093/ehjopen/oead040.
- Kumar S, et al.: Revised prognostic staging system for light chain amyloidosis incorporating cardiac biomarkers and serum free light chain measurements. J Clin Oncol 2012; 30: 989–995.
- Cohen OC, Ismael A, Pawarova B, et al.: Longitudinal strain is an independent predictor of survival and response to therapy in patients with systemic AL amyloidosis. Eur Heart J 2021; 43: 333–341.
- Potter E, Marwick TH: Assessment of left ventricular function by echocardiography: the case for routinely adding global longitudinal strain to ejection fraction. JACC Cardiovasc Imaging 2018; 11: 260–274.
- Lang RM, et al.: Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J Am Soc Echocardiogr 2015; 28: 1–39.e14.
- Ommen SR, et al.: Clinical utility of Doppler echocardio-graphy and tissue Doppler imaging in the estimation of left ventricular filling pressures: a comparative simultaneous Doppler-catheterization study. Circulation 2000; 102: 1788–1794.
CARDIOVASC 2023; 22(2): 50–52
| Imagem da capa: Micrografia de grande ampliação de amiloidose cardíaca senil. Congo red stain. Amostra de autópsia. ©Wikimedia (Nephron) |