Os metabolitos presentes nas amostras de soro, urina e fezes podem identificar as pessoas com insuficiência hepática aguda e crónica entre os doentes com cirrose hepática aguda descompensada, servindo de base para medidas de diagnóstico e terapêuticas precoces. Esta é a conclusão de um projeto de estudo atual. Num projeto de outra equipa de investigação, o sistema repórter “EXSISERS” forneceu informações interessantes sobre a relevância do estado do p53 na peritonite bacteriana espontânea, uma complicação infecciosa associada à cirrose hepática.
A fibrose hepática avançada e a cirrose são resumidas como “doença hepática crónica avançada” (DHC). A doença hepática crónica avançada caracteriza-se por danos persistentes e cicatrizes crescentes no fígado. A fase final da fibrose hepática é a cirrose hepática. Os doentes com cirrose com descompensação aguda (DA) têm um risco acrescido de desenvolver insuficiência hepática aguda ou crónica (IAFC). A ACLF caracteriza-se pela falência de órgãos extra-hepáticos e pela inflamação sistémica. A FHCA está associada a um risco grave de complicações infecciosas e a uma elevada mortalidade a curto prazo. A fim de melhorar o prognóstico dos doentes afectados, são necessárias medidas de diagnóstico e terapêuticas precoces na FCA [1]. Dechaumet et al. apresentaram um projeto de investigação no congresso da EASL deste ano, no qual foram identificadas assinaturas metabolómicas para diferenciar entre doentes com DA com ou sem ACLF. [2,3]Segue-se um resumo deste e de outro projeto de investigação no domínio das doenças hepáticas avançadas.
Análise dos dados da coorte MUCOSA-PREDICT
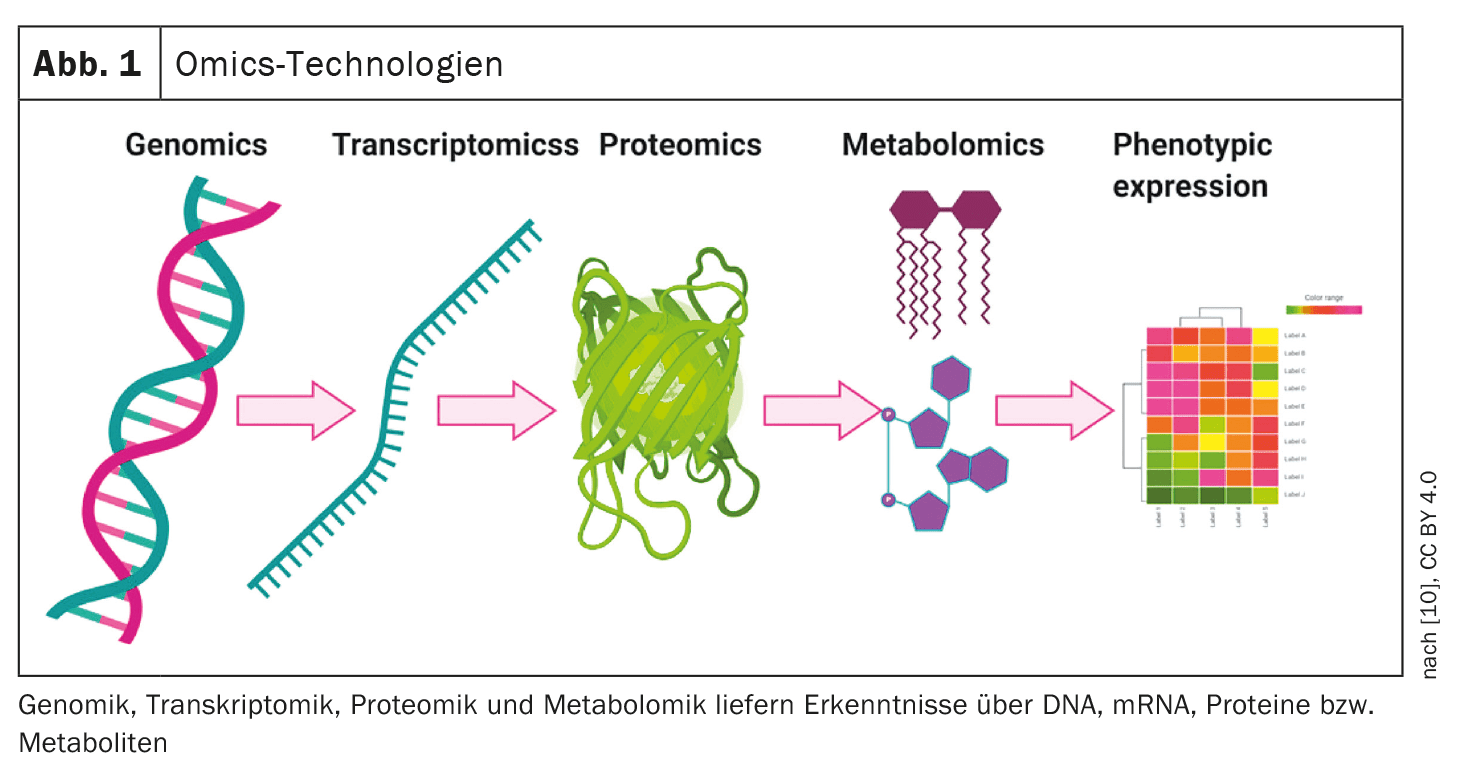
A totalidade das substâncias de baixo peso molecular (metabolitos) é designada por metaboloma. O metaboloma pode ser medido, por exemplo, por cromatografia, espetrometria de massa ou espetroscopia de ressonância magnética nuclear. [10]O fígado é um órgão metabolicamente muito ativo e as doenças hepáticas estão a ser cada vez mais investigadas através de métodos multiómicos (Fig. 1). Moreau et al. relataram em 2020 no Journal of Hepatology que foram capazes de identificar uma impressão digital específica da ACLF de 38 metabolitos no sangue utilizando uma abordagem multiómica em amostras de tecido, que se correlaciona com a inflamação sistémica e actua como um indicador de disfunção mitocondrial em órgãos periféricos [4].
Objectivos e metodologia do estudo: O projeto de Dechaumet et al. teve como objectivos, (i) investigar se a análise de metabolitos em amostras de urina e fezes tem valor acrescentado para a caraterização do metaboloma em doentes cirróticos descompensados e (ii) avaliar de que forma a metabolómica multi-matriz contribui para melhorar a estratificação dos doentes com cirrose descompensada [2]. Para tal, os investigadores analisaram amostras de soro, urina e fezes da coorte MUCOSA-PREDICT, na qual estão a ser acompanhados 93 doentes cirróticos com descompensação aguda, utilizando cromatografia líquida acoplada a espetrometria de massa de alta resolução. Foi detectado e identificado um total de 402 metabolitos nas três matrizes biológicas.
Resultados: O maior número de metabolitos cujas concentrações são influenciadas pela ACLF foi observado em amostras de soro [2]. Curiosamente, as concentrações de alguns metabolitos na urina e nas fezes que não foram detectadas no soro também foram influenciadas pelo ACLF. No entanto, as análises da curva ROC realizadas para as assinaturas metabolómicas em matrizes simples ou combinadas mostraram que a assinatura do soro teve o melhor desempenho na discriminação entre a DA e o ACLF. Trata-se de uma descoberta clinicamente relevante, uma vez que ambas as doenças se sobrepõem em casos individuais, mas são entidades diferentes em termos de fisiopatologia e terapia.
Aplicação do sistema de informação “EXSISERS
O eixo intestino-fígado descreve as diversas interações entre o intestino e o fígado, incluindo a troca de componentes celulares e moleculares, e é de importância central para a regulação de processos (pato)fisiológicos essenciais. Os doentes com cirrose hepática têm uma espessura reduzida da mucosa, o que facilita o contacto direto das bactérias com as células epiteliais e a degradação dos compostos celulares [5]. A translocação bacteriana é considerada um passo crucial na patogénese das infecções bacterianas [6]. Por exemplo, a translocação de bactérias intestinais para os gânglios linfáticos mesentéricos é um evento chave na peritonite bacteriana espontânea. A peritonite bacteriana espontânea** é uma inflamação do líquido ascítico que ocorre com particular frequência na cirrose hepática e pode ter consequências graves.
[11]** As bactérias mais comuns que causam peritonite bacteriana espontânea são a Escherichia coli Gram-negativa e a Klebsiella pneumoniae e o Streptococcus pneumoniae Gram-positivo.
Objectivos e metodologia do estudo: De acordo com Ernst et al. o stress celular desencadeado pelo contacto direto com as bactérias afecta a família p53 de factores de transcrição, que actuam como reguladores-chave do ciclo celular, dos mecanismos de reparação e da morte celular (apoptose) [3]. Na sua forma de tipo selvagem, o p53 (wtp53) actua como um supressor tumoral central [7]. As proteínas homólogas, estrutural e funcionalmente, p63 e p73 estão incluídas na família p53 de factores de transcrição. A função da p53 está alterada num grande número de tumores (mutações TP53). No seu estudo, Ernst et al. investigaram os efeitos da bactéria da ascite na expressão das isoformas$ do p53 em relação à indução da morte celular em células epiteliais. Aplicaram um novo sistema repórter biotecnológico [3]. O sistema repórter denominado EXSISERS pode monitorizar a expressão de isoformas ao longo do tempo em células vivas [8].
$ As isoformas são variantes de proteínas que surgem a partir de um único gene.
Foram integrados três sistemas repórteres de luciferase inteínos específicos do exão (EXSISERS) nos exões 2, 4 e 7 do gene TP53. As inteínas clivadas permitem a clivagem da enzima luciferase do polipeptídeo p53, mantendo a integridade estrutural das isoformas do p53 [9]. Este método pode ser utilizado para quantificar com precisão os rácios das isoformas da proteína p53 a nível celular. As células HCT116-EXISERS foram co-cultivadas com Escherichia coli derivada de doentes e foram medidos os três principais grupos de isoformas de p53 – p53 indutor de paragem do ciclo celular de comprimento total, Δ40p53 indutor de morte celular, Δ133p53/Δ160p53 pró-proliferativo. Ao mesmo tempo, a morte celular induzida por bactérias foi quantificada em células HCT116 p53 de tipo selvagem e p53 knockout. A microscopia eletrónica foi utilizada para determinar o tipo de morte celular.
Resultados: A co-cultura de bactérias derivadas de doentes com células HCT116-EXISERS levou inicialmente a um aumento da produção da isoforma p53 indutora de morte celular Δ40p53 em 15 minutos [3]. Seguiu-se uma diminuição das isoformas pró-proliferativas de p53 Δ133p53/Δ160p53. Ao mesmo tempo, foi observada apoptose em resposta ao contacto bacteriano, que mostrou caraterísticas morfológicas de paraptose, incluindo inchaço mitocondrial e vacuolização citoplasmática. Paralelamente às alterações morfológicas observadas, a citometria de fluxo confirmou danos nas mitocôndrias e na membrana plasmática. O conhecido inibidor da paraptose acinomicina D bloqueou eficazmente a morte celular induzida por bactérias. De acordo com a indução medida da isoforma Δ40p53, a indução da morte celular foi significativamente atrasada por um knockout p53 mediado por CRISPR/Cas9.
| Resumo |
| Na cirrose hepática com descompensação aguda (DA), o risco de desenvolver insuficiência hepática aguda ou crónica (IAFC) é maior. No estudo de Dechaumet et al. demonstrou que as assinaturas metabólicas do sangue, mas também da urina e das fezes, diferenciam os doentes com DA com e sem ACLF. Os dados obtidos a partir do compartimento sanguíneo parecem fornecer o melhor desempenho de estratificação. |
| Em doentes com cirrose hepática, a translocação bacteriana ocorre devido a uma integridade epitelial deficiente. As respostas celulares ao stress bacteriano são reguladas por isoformas específicas de p53. O estudo de Ernst et al. mostra que o estado da p53 exerce uma influência decisiva na suscetibilidade à paraptose. A indução ou estabilização de isoformas específicas de p53 poderia, por conseguinte, representar uma opção terapêutica para o tratamento da peritonite bacteriana espontânea. |
| para [2,3] |
Congresso: Congresso EASL 2024
Literatura:
- Hübener P, Braun G, Fuhrmann V: Med Klin Intensivmed Notfmed 2018; 113(8): 649-657.
- Dechaumet S, et al: Multi-compartment metabolomics for stratifying cirrhotic patients with acute decompensation, WED-083, Congresso EASL, Milão, 5-8 de junho de 2024.
- Ernst M, et al: Liver cirrhosis and epithelial damage – The gut-liver axis in spontaneous bacterial peritonitis and its modulation by p53, WED-106, EASL Congress, Milan, 5-8 June 2024.
- Moreau R, et al: J Hepatol 2020; 72: 688-701.
- Haderer, M. et al: Gut 2022; 71: 580-592.
- Rayes N: Experimental and clinical investigation of the influence of pre- and probiotics on bacterial translocation and postperative infections after abdominal surgery, tese de habilitação, 2004, https://core.ac.uk,(último acesso em 27/08/2024)
- Weilbacher A: The role of p53 status for the sensitivity of tumours to different p53 activators, Dissertação, 2017, https://elib.uni-stuttgart.de,(último acesso em 27.08.2024) .
- “Novas proteínas de design tornam as isoformas visíveis de forma não invasiva”, Helmholtz Munique, 04.06.2021.
- Truong, D-JJ, et al: Non-Invasive and High Throughput Interrogation of Exon-Specific Isoform Expression [Interrogação não invasiva e de elevado rendimento da expressão de isoformas específicas do exão]. Nature Cell Biology 2021, doi:10.1038/s41556-021-00678-x
- Raja G, et al.: Recent Advances of Microbiome-Associated Metabolomics Profiling in Liver Disease: Principles, Mechanisms, and Applications. International Journal of Molecular Sciences 2021; 22(3): 1160. www.mdpi.com/1422-0067/22/3/1160#, (letzter Abruf 27.08.2024)
- “Spontaneous bacterial peritonitis (SBP)”, Danielle Tholey, MD, www.msdmanuals.com/de,(último acesso em 27/08/2024).
HAUSARZT PRAXIS 2024; 19(9): 38-39 (publicado em 18.9.24, antes da impressão)