Existem agora quatro inibidores JAK aprovados na Europa: tofacitinibe, baricitinibe, upadacitinib e filgotinibe. Embora não houvesse muitas notícias a relatar sobre os dois primeiros nos últimos 12 meses, muita coisa aconteceu, especialmente no que diz respeito ao upadacitinib, como foi resumido no Rheumatism Update 2021.
Por exemplo, o primeiro estudo cabeça a cabeça (SELECT-CHOICE) em pacientes bDMARD-IR foi publicado: 612 pacientes com artrite reumatóide activa apesar da terapia csDMARD e da falha no tratamento de pelo menos uma biologia precoce foram aleatorizados de forma cega e controlada por placebo para abatacept i.v. (n=309) ou upadacitinib (n=303) [2]. O ponto final primário foi DAS28(CRP) desde a linha de base até à semana 12. Upadacitinib (UPA) teve um desempenho melhor que o abatacept (ABA) em todos os parâmetros estudados. A proporção de doentes com DAS28(CRP) foi de quase 30% com UPA vs. 13% com ABA. Dr. Andrea Rubbert-Roth do Departamento de Reumatologia do Hospital Cantonal St. Gallen, que é também o primeiro autor do estudo, concluiu que a terapia UPA é superior à abatacept em termos de eficácia em pacientes de AR com uma resposta inadequada aos bDMARD, com uma incidência ligeiramente superior de eventos adversos graves (3,3% vs. 1,6%, 2 VTE e 1 MACE* ocorreram com UPA, curiosamente, o herpes zoster ocorreu com igual frequência em ambos os grupos com 4 pacientes cada).
Num outro estudo (SELECT-COMPARE), os pacientes cuja AR estava activa apesar do metotrexato foram randomizados para UPA 15 mg/dia (n=651) vs adalimumab (ADA, n=327) vs placebo (n=651). Em caso de resposta insuficiente (definida como sem ACR20 após 14 semanas = não resposta ou CDAI >10 = resposta parcial), podem ser mudados para o outro regime de medicamentos activos sem interrupção a partir da semana 14 em diante.
* Grandes eventos cardiovasculares adversos (= morte cardiovascular, enfarte do miocárdio não fatal, CHD, eventos cerebrovasculares).
Filgotinib “altamente potente“ para a terapia RA
O resultado da troca: Os pacientes que foram trocados de ADA para UPA fizeram melhor do que aqueles que tinham trocado de UPA para ADA. Ao passar de adalimumab para upadacitinib, 47% dos não-respondedores e 58% dos respondedores incompletos alcançaram CDAI-LDA; inversamente, estes números foram de 36% e 45%, respectivamente. Estes são os primeiros dados a mostrar o que pode ser feito quando se verifica uma resposta inadequada a um inibidor JAK, diz o Prof.
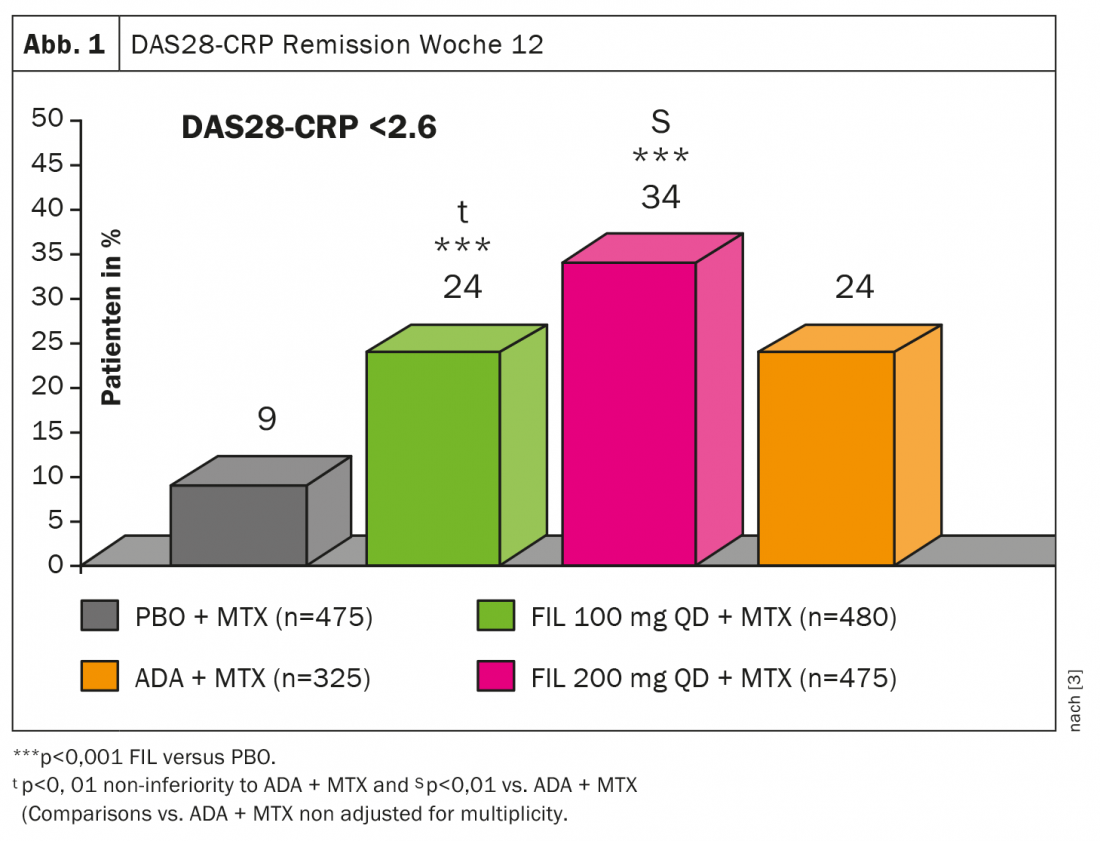
Em relação ao filgotinib (FIL), os dados do estudo FINCH1, um ensaio de fase 3 duplo-cego, controlado por placebo, envolvendo 1755 doentes com RA activa apesar do metotrexato (MTX), foram publicados recentemente [3]. Foi fixado em FIL 100 mg (n=480), FIL 200 mg (n=475), ADA (n=325) ou placebo (n=475), o ponto final primário era ACR20 na semana 12. a emissão de DAS28(CRP) na semana 12 estava sob a combinação FIL 200 mg mais MTX melhor do que ADA + MTX ou FIL 100 mg + MTX (Fig.1). Embora a superioridade só fosse visível na dose mais elevada: “O filgotinibe é também um inibidor altamente potente do JAK para o tratamento da AR”, concluiu o perito.
Resultados do estudo sobre biologia
Várias novas descobertas surgiram também na investigação em biologia. Um estudo analisou se existe um benefício em iniciar a biologia cedo. O estudo NORD-STAR, um ensaio randomizado e multicêntrico em 812 doentes com AR precoce, publicado no ano passado, comparou quatro braços de tratamento diferentes [4]:
- MTX + prednisona (cónico a 5 mg /d) ou MTX + SSA + HCQ + esteróides intra-articulares
- MTX + certolizumab pegol
- MTX + Abatacept
- MTX + tocilizumab
Como resultado, não houve nenhum benefício significativo. MTX + abatacept alcançou a taxa mais alta de remissão de CDAI, e a terapia convencional combinada foi não-inferior ao certolizumab + MTX ou ao tocilizumab + MTX. No entanto, o estudo não foi suficientemente potente para comparar os três braços bDMARD. Se o fizesse, sentiria, pelo menos numericamente, que a taxa de remissão CDAI sob MTX + Abatacept é afinal mais elevada, a 56,3%, do que a que vê sob certolizumab (52,6%) ou tocilizumab (48,7%), disse o Prof. No entanto, o estudo continuará, com a segunda parte a examinar e comparar 2 estratégias de desescalonamento.
O risco de linfoma não aumentou
Os linfomas foram um grande tópico relacionado com a terapia de bloqueio de TNF durante anos: Por um lado, foi demonstrado que ocorrem mais linfomas quando a actividade da doença é elevada. Por outro lado, foram também encontradas taxas aumentadas de linfomas em pacientes com AR inicialmente sob terapia com inibidores de TNF, “e admito que nunca compreendi isto, porque os pacientes experimentam uma redução na actividade da doença sob bloqueadores de TNF”, disse o Prof. Ela pensou que era provavelmente porque os pacientes tinham tido AR durante muito tempo. Um estudo de 2020 analisou novamente este fenómeno e analisou os dados do registo sueco da AR.
Para pacientes com bDMARD (n=16 392) e para aqueles sem biologia (n=55 253), foram registados todos os linfomas de início de vida de 2001-2016. A análise dos pacientes que foram tratados com uma biologia após 2006 mostrou que os primeiros tinham mesmo um risco reduzido de desenvolver linfoma (FC ajustado 0,69; IC 95% 0,28-0,73) em comparação com os pacientes com uma biologia ingénua. “Estes são dados muito positivos, o que certamente ajuda a apoiar os biólogos em benefício”, explicou o reumatologista.
Finalmente, o Prof. Rubbert-Roth também relatou resultados positivos sobre a utilização e segurança de biólogos em pacientes de AR com antecedentes de malignidade. Numa meta-análise baseada em 12 estudos com 13.598 doentes de AR, 10 estudos sobre bloqueadores de TNF e 3 estudos com rituximab, foi investigado o risco relativo de recorrência ou um segundo carcinoma [5]. Aqui, os resultados mostraram que o risco era comparável entre os bloqueadores de TNF, rituximab e csDMARD e era independente da duração e do intervalo da terapia inibidora de TNF.
Mensagens Take-Home
- Upadacitinib: dados interessantes do ensaio SELECT-COMPARE, primeiro estudo cabeça a cabeça em pacientes bDMARD-IR vs. abatacept
- Filgotinib: superioridade vs. ADA apenas na dose mais elevada
- Não houve superioridade nas terapias combinadas contendo bDMARD para o tratamento de AR precoce em comparação com a estratégia csDMARD.
- O risco de linfoma em doentes com AR permanece elevado em comparação com a população normal, mas nem os inibidores de TNF nem os biólogos não-TNF aumentam o risco. Há mesmo uma tendência para uma redução do risco de linfoma sob terapia biológica.
- No caso de uma história de malignidade, os bloqueadores de TNF, rituximab e csDMARD são comparáveis em termos de risco de recidiva ou segundo tumor.
Literatura:
- RA: Therapy, Rheumatism Update 2021 (online), 12.03.2021.
- Rubbert-Roth A, et al: Ensaio de Upadacitinib ou Abatacept em Artrite Reumatóide. N Engl J Med 2020; 383: 1511-1521; doi: 10.1056/NEJMoa2008250.
- Combe B et al. Filgotinibe versus placebo ou adalimumab em doentes com artrite reumatóide e resposta inadequada ao metotrexato: um ensaio clínico aleatório fase III. Ann Rheum Dis 2021; doi: 10.1136/annrheumdis-2020-219214.
- Hetland ML, et al: Tratamento activo convencional e três tratamentos biológicos diferentes na artrite reumatóide precoce: fase IV investigador iniciado, aleatorizado, ensaio clínico cego pelo observador. BMJ 2020; 371: m4328; doi: 10.1136/bmj.m4328.
- Xie W, et al: Uma meta-análise de terapias biológicas sobre o risco de cancro novo ou recorrente em pacientes com artrite reumatóide e uma malignidade anterior. Reumatologia 2020; 59: 930-939; doi: 10.1093/rheumatology/kez475.
InFo PAIN & GERIATURA 2021; 3(1): 34-36 (publicado 3.7.21, antes da impressão).