Os opiáceos formam um grupo farmacologicamente heterogéneo de substâncias activas sintéticas, semi-sintéticas e naturais cuja característica comum é a ligação aos receptores opiáceos. Em relação ao desenvolvimento dos efeitos analgésicos, os receptores opióides no sistema nervoso central são decisivos. A activação de receptores opióides pré-sinápticos no corno posterior da medula espinal inibe a transmissão de impulsos de dor.
O termo opióide é extraído do grego e significa “semelhante ao ópio”. Os opiáceos formam um grupo farmacologicamente heterogéneo de substâncias activas sintéticas, semi-sintéticas e naturais cuja característica comum é a ligação aos receptores opiáceos. Os receptores opióides encontram-se tanto no sistema nervoso periférico como no sistema nervoso central. Em relação ao desenvolvimento de efeitos analgésicos, os receptores opióides no sistema nervoso central são decisivos. Ao activar os receptores opióides pré-sinápticos no corno posterior da medula espinal, a transmissão de impulsos de dor é inibida. A activação de receptores opióides induzida por opiáceos em certas regiões do tronco cerebral causa estimulação adicional das vias neurais inibitórias descendentes. Isto inibe a transmissão dos sinais de dor que chegam na buzina posterior. Em regiões subcorticais do sistema límbico, a activação de receptores opióides leva a uma atenuação da componente emocional-afectiva da percepção de uma sensação de dor [1].
O próprio corpo humano produz opiáceos endógenos, que são libertados no contexto de reacções ao stress e levam à supressão da dor e dos sentimentos de fome. Na prática médica, os opiáceos sintéticos são geralmente utilizados. As diferenças farmacodinâmicas entre os vários opiáceos podem ser vistas nas diferentes afinidades com os receptores opióides ou com os subtipos de receptores individuais. O conhecimento preciso destas diferenças farmacodinâmicas ajuda na prática clínica diária a poder estimar o efeito esperado de um determinado opióide.
Epidemiologia
O Inquérito de Saúde Suíço de 2017 mostrou que cerca de 2,5 milhões de pessoas na Suíça sofrem de dor crónica. Aproximadamente 0,6 milhões de pessoas sofrem de condições de dor moderada a severa que têm um efeito limitador na actividade e qualidade de vida. As mulheres são mais propensas a relatar dores crónicas [2].
Embora existam várias abordagens terapêuticas para o tratamento da dor, os opiáceos também são cada vez mais prescritos na Suíça. O uso de opiáceos é bem reconhecido e geralmente muito útil para o tratamento de dores agudas graves, por exemplo, no ambiente perioperatório. Os opiáceos são também frequentemente uma opção terapêutica indispensável e mundialmente reconhecida para o tratamento da dor relacionada com o tumor [3]. A dor crónica não cancerígena, em contraste, é geralmente uma indicação menos boa para o tratamento a longo prazo com opiáceos. Não é claro se a utilização de opiáceos altamente potentes melhora o controlo da dor crónica não cancerígena a médio e longo prazo [4].
É precisamente por esta razão que é alarmante que 85% de todos os opiáceos prescritos actualmente sejam utilizados para tratar dores não cancerígenas [5]. Cerca de 25% dos doentes afectados recebem os opiáceos prescritos durante um período de >90 dias. A utilização a longo prazo ao longo dos anos é frequentemente o resultado.
Taxonomia dos mecanismos da dor
Uma terapia farmacológica da dor adequada e eficaz pode ser alcançada de forma mais fiável se os mecanismos da causa da dor forem reduzidos o mais possível. Uma história detalhada e um exame clínico focalizado são fundamentais para identificar um mecanismo de dor. Os exames radiológicos, laboratoriais e outros exames adicionais são úteis em situações específicas. Os seguintes mecanismos de dor devem ser identificados ou excluídos:
Dor nociceptiva: Este mecanismo é responsável pela manutenção da integridade corporal e é também entendido como a sensação “normal, habitual” de dor. Os sinais de dor nociceptiva ajudam a prevenir lesões. A dor é dependente do estímulo, geralmente de curta duração e o tecido estimulado permanece intacto. Os estímulos nociceptivos contínuos podem levar a alterações neuronais no corno posterior da medula espinal. Estas mudanças são geralmente de curta duração e recuam. Não são de esperar fenómenos persistentes de sensibilização à dor.
Dor nociceptiva-inflamatória: A dor aguda a subaguda ocorre quando já ocorreram danos nos tecidos. Os gatilhos são libertados mediadores inflamatórios (por exemplo, interleucinas). Por um lado, há activação directa das terminações periféricas das fibras da dor, por outro lado, são recrutadas e adicionalmente sensibilizadas no decurso deste processo fibras da dor novas, anteriormente inactivas. Globalmente, há uma diminuição do limiar de excitabilidade electrofisiológica. Isto torna possível a formação de fenómenos de sensibilização periférica.
Dor neuropática: A dor neuropática também ocorre de forma aguda ou subaguda. No entanto, a causa do sinal de dor aqui não é o tecido circundante, mas o próprio sistema somatossensorial [6]. Os danos nas próprias células nervosas formam a base da dor neuropática. Praticamente sempre, ocorrem fenómenos de sensibilização periférica e central. Como regra, podem ser documentados fenómenos de sensibilização “positivos” e/ou “negativos”. Existe frequentemente uma grande discrepância entre a intensidade da dor reclamada pelo paciente, a extensão da área afectada pela dor e os resultados objectivos que podem ser determinados pelo examinador.
Um importante fenómeno de sensibilização é a hiperalgesia. Ocorre tanto em condições de dor neuropática como inflamatória. A hiperalgesia pode ser definida como uma condição durante a qual um estímulo normalmente ligeiramente doloroso é experimentado como excessivamente doloroso (por exemplo, picada com um palito de dente). A alodinia é outro fenómeno de sensibilização “positivo” e é uma exacerbação da hiperalgesia. Numa área de pele afectada por alodinia, um estímulo que na realidade é indolor é visto como doloroso (por exemplo, tocar com um pincel).
Dor não disciplinar: Dor nociceptiva/inflamatória e dor neuropática são entidades definidas mecanicamente, em última análise. A diferença crucial é que no contexto de condições de dor nociceptiva, existe uma função normal do sistema somatosensorial, enquanto que é precisamente esta que é danificada em condições de dor neuropática. Muitos pacientes com dor crónica não podem ser atribuídos a nenhuma destas entidades sem dúvida [7]. Nestes pacientes, não se pode assumir nem uma activação de nociceptores nem uma lesão do sistema somatossensorial. Nesses casos, está presente um problema de dor não disciplinar. Um grande grupo de doentes é afectado: Dor não específica nas costas, dor não específica nas articulações periféricas, fibromialgia, Síndrome da Dor Regional Complexa (CRPS) tipo 1.
Sobreposição de mecanismos de dor/”Dor Mista”: Muito frequentemente, uma sobreposição dos mecanismos de dor acima mencionados pode ser detectada/assumida em pacientes com dor crónica. Em “dor mista”, todos os mecanismos descritos acima estão frequentemente envolvidos no desenvolvimento ou modulação do sinal de dor. Normalmente, um ou outro mecanismo de dor está em primeiro plano.
Os opiáceos desempenham um papel importante no tratamento da dor nociceptiva, mas também podem contribuir para um bom controlo da dor em dores neuropáticas. No caso de não existirem condições de dor disciplinares, o valor terapêutico dos opiáceos é geralmente inexistente.
Os 4 pilares da analgesia
A fim de conseguir o tratamento analgésico mais satisfatório possível, o reconhecimento da dor e dos mecanismos de sensibilização acima apresentados é central. Independentemente da modalidade terapêutica, uma terapia orientada para as condições de dor, ou a realização de “analgesia”, baseia-se portanto nos quatro pilares seguintes: “antinocicepção”, “anti-inflamação”, “anti-hiperalgesia” e “antineuropatia” [8].
No âmbito de uma terapia analgésica farmacológica, é portanto crucial utilizar medicamentos de uma ou mais classes de substâncias que possam cobrir todo o espectro dos mecanismos de dor diagnosticados, na medida do possível.
Medidas recomendadas antes de iniciar a terapia da dor com um opiáceo
Se uma tentativa de tratamento com um analgésico opióide é ou não útil requer uma cuidadosa consideração conjunta entre médico e paciente. A utilização de opiáceos de acção fraca ou forte desempenha um papel subordinado. Os seguintes pontos devem ser especificamente considerados [9]:
- Os mecanismos subjacentes ao problema da dor devem ser especificamente procurados e identificados.
- Recomenda-se que se faça um historial psicossocial mais detalhado e que se verifique a presença de influências psicológicas sobre o problema da dor.
- As dores crónicas não cancerosas nunca devem ser tratadas exclusivamente com opiáceos, se possível. Dados científicos indicam que os opiáceos não são mais eficazes que outros analgésicos para o tratamento da dor crónica não-cancerígena.
- Antes de considerar a terapia da dor com opiáceos, várias outras medidas terapêuticas já deveriam ter sido tomadas ou, pelo menos, tentadas (físicas, fisioterapêuticas, medicinais, intervencionais, psicológicas).
- Objectivos terapêuticos significativos e realizáveis devem ser trabalhados em conjunto com o paciente. O enfoque deve ser em objectivos como a redução da dor de pelo menos 30%, o regresso ao trabalho ou também a conclusão das tarefas quotidianas, por exemplo, no agregado familiar.
- Os doentes devem ser informados em pormenor sobre os possíveis perigos que podem ocorrer no decurso da terapia a longo prazo com opiáceos. Para além dos efeitos secundários conhecidos, tais como obstipação, boca seca, náuseas, mal-estar, estados de confusão, quedas, também se deve chamar a atenção para a depressão respiratória potencialmente ameaçadora de vida em resultado de incorrecções/sobredoses.
- Os pacientes devem ser informados de que a terapia com um opióide conduz normalmente à dependência física.
- Durante as primeiras 1-2 semanas de terapia, durante a fase de ajustamento, quando a dose é aumentada ou quando se muda para outro opiáceo, se deve evitar conduzir ou operar máquinas. Durante este tempo, os efeitos secundários que limitam a capacidade de resposta são comuns.
Quando pode ser considerada uma terapia de longo prazo >120 dias com opiáceos?
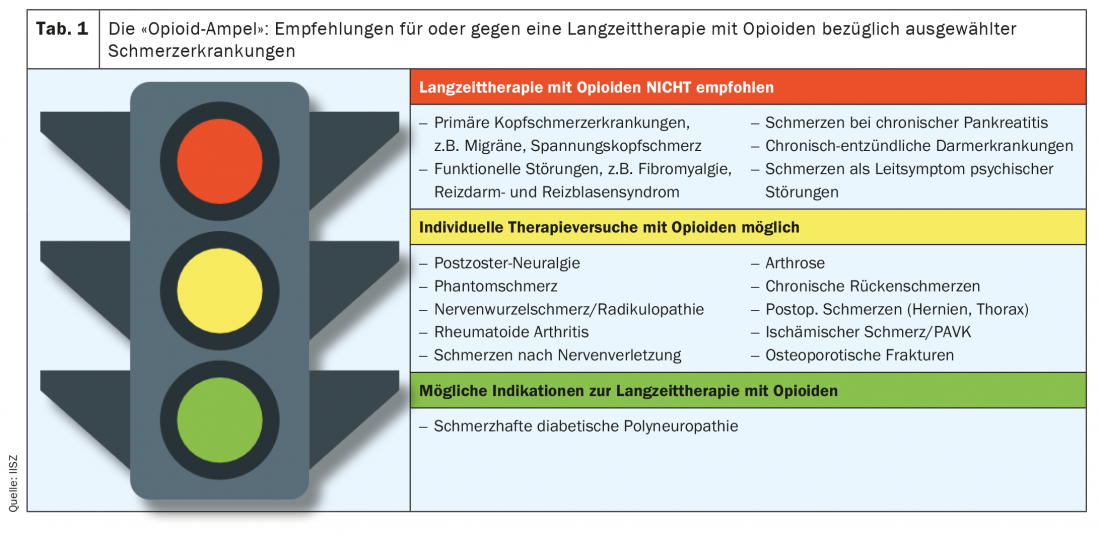
O princípio aplica-se que os opiáceos só devem ser utilizados para a terapia a longo prazo (>120 dias) de uma condição dolorosa crónica se o paciente em causa for capaz de registar uma redução significativa da dor e/ou melhoria da sua condição geral durante uma terapia de ensaio de 4 a 12 semanas. Além disso, as directrizes aplicáveis a nível nacional e internacional devem ser incluídas nas considerações em torno de uma indicação. Um recurso recomendável é, por exemplo, a orientação sobre “Utilização a longo prazo de opiáceos para dor crónica não relacionada com o tumor (LONTS)” [9] da Sociedade Alemã da Dor. Actualmente, a terapia com opióides a longo prazo só é recomendada na presença de polineuropatia diabética dolorosa. Em contraste, a terapia a longo prazo com opiáceos é mesmo especificamente desencorajada no caso de várias outras condições de dor crónica (ver também Quadro 1).
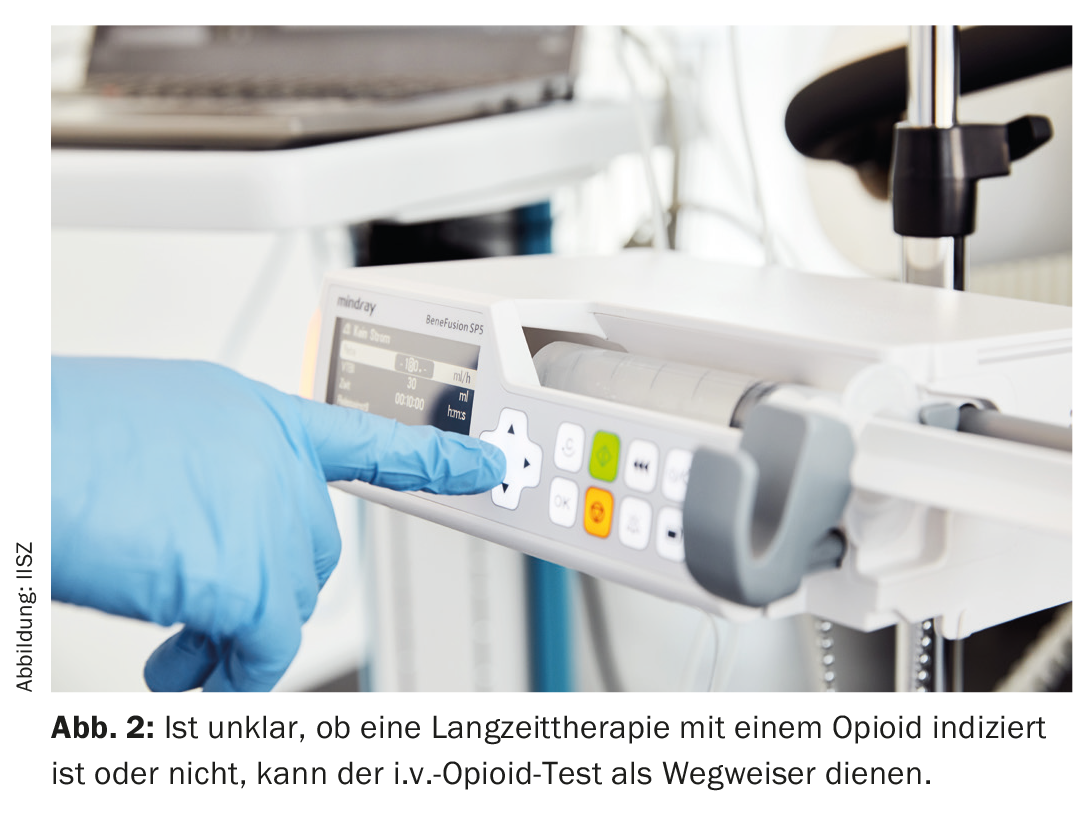
Em caso de dúvida: O teste i.v. opióide como sinal de aviso
Se houver incerteza sobre se a terapia da dor com opiáceos deve ser continuada por mais de 12 semanas, um teste intravenoso (i.v.) de opiáceos realizado em regime ambulatório pode ser útil [10] (Fig. 2). Tais testes são oferecidos por vários centros de medicina da dor na Suíça. Através da administração i.v. protocolizada de um opiáceo de acção ultra-curta, é geralmente possível descobrir se uma condição dolorosa pode ser tratada eficazmente por um opiáceo ou não.
Preparativos opióides de acção curta vs. acção longa
Para o tratamento da dor crónica, devem ser utilizadas preparações com galénicos de libertação lenta ou uma longa duração de acção, se possível. O consumo deve seguir um calendário fixo. A experiência mostra que um melhor controlo da dor e uma melhor aderência terapêutica podem ser conseguidos desta forma. Além disso, este procedimento pode reduzir o risco de complicações.
Os opiáceos de acção curta e ultra-intencional só devem ser utilizados em casos excepcionais no tratamento de dores crónicas não relacionadas com o tumor. Também não são recomendados como um medicamento a pedido. A experiência clínica mostra que os opiáceos de acção curta também podem conduzir rapidamente à dependência psicológica. Infelizmente, isto resulta muitas vezes numa utilização indevida.
Resultados da terapia de opiáceos a longo prazo
As provas científicas actualmente disponíveis para avaliar a eficácia da terapia opióide >120 dias para dores crónicas não relacionadas com o tumor são insuficientes. Isto implica automaticamente perspectivas incertas de sucesso [11].
No contexto da utilização crónica de opiáceos, não é raro que a medicação opiácea utilizada diminua em efeito. Há vários diagnósticos diferenciais que podem explicar este desenvolvimento. Mesmo no caso de dor crónica não relacionada com o tumor, a progressão da doença pode ocorrer, levando a uma intensificação do problema da dor. No entanto, o tratamento opióide crónico leva frequentemente ao desenvolvimento da tolerância com uma consequente redução do efeito analgésico do opióide utilizado. Pensa-se que a causa é uma migração de receptores opióides da superfície celular para o interior da célula, de modo a que já não estejam disponíveis para o efeito analgésico. Outro fenómeno que pode ocorrer em ligação com um aumento da dor durante a terapia em curso com opiáceos é a hiperalgesia induzida por opiáceos. Os mecanismos discutidos da hiperalgesia induzida por opiáceos são complexos e vão desde uma desregulação dos receptores de opiáceos até uma possível sensibilização central e uma potenciação sináptica a longo prazo.
Efeitos adversos com utilização a longo prazo
A longo prazo, a utilização de opiáceos pode resultar nos seguintes efeitos adversos:
- Perda do desejo sexual
- Impotência
- Perturbações menstruais nas mulheres
- Aumento da mortalidade por todas as causas
- Passividade / indiferença
- Memória deficiente
- Aumento do risco de queda
Quando deve ser interrompida a terapia de opiáceos a longo prazo?
A terapia a longo prazo com um opiáceo deve ser reavaliada periodicamente. Se não estiver claro se a terapia com um opióide proporciona alívio da dor, trabalhar no sentido de descontinuar esta terapia. Recomenda-se a interrupção gradual da terapia com um opióide se:
- Na fase de ajustamento (4 a 12 semanas), os objectivos terapêuticos individualmente definidos não puderam ser alcançados e/ou ocorreram efeitos secundários significativos.
- No decurso do tratamento, tem de ser determinada uma perda do efeito do opióide utilizado e isto não pode ser ainda mais evitado por um ajustamento moderado da dose ou uma mudança para outro opióide.
- Indicações de uso indevido ocorrem durante o tratamento (aumentos de dose independentes, prescrição por vários médicos).
Conclusão
Os opiáceos são uma das classes mais importantes de substâncias para o tratamento de dores fortes. Nunca são utilizados como opção de primeira linha e devem ser sempre acompanhados por medidas não relacionadas com a droga. A terapia a longo prazo só é realizada com os responsáveis terapêuticos, pelo que o efeito deve ser avaliado regularmente através da definição e monitorização dos objectivos da terapia. Uma terapia não funcional com opiáceos deve ser interrompida a tempo.
Take-Home-Messagess
- Antes de iniciar uma terapia farmacológica da dor em geral e um tratamento com opiáceos em particular, o mecanismo da dor subjacente deve ser estreitado.
- Os opiáceos são frequentemente o tratamento de escolha para dores agudas graves e relacionadas com tumores.
- A terapia a longo prazo da dor crónica não relacionada com o tumor, pelo contrário, só deve ser realizada em casos excepcionais e, sempre que possível, deve ser combinada com medidas não relacionadas com a droga.
- A terapia a longo prazo com opiáceos deve ser orientada para objectivos mensuráveis. Se estes objectivos não forem alcançados, o tratamento opiáceo deve ser suspenso.
- No contexto da terapia a longo prazo com opiáceos, desenvolve-se sempre uma dependência física, que por vezes é acompanhada por uma componente psicológica, no sentido de uma dependência.
Literatura:
- Ossipov MH, Dussor GO, Porreca F: modulação central da dor. J Clin Invest 2010; 120: 3779-3787.
- Swiss Health Interview Survey 2017, Health and Gender, Serviço Federal de Estatística, FSO número 213-1718. 2020.
- Wertli MM, Steurer J: Em Processo de Citação. Prática 2015; 104(11): 541-542.
- Breivik H, Stubhaug A: O fardo da doença é frequentemente agravado pelo tratamento opióide de pacientes com dor crónica: Etiologia e prevenção. DOR 2014; 155(12): 2441-2443.
- Wertli M, Held U, Signorell A, et al: Análise do desenvolvimento de práticas de prescrição de medicamentos para a dor e o sono entre 2013 e 2018 na Suíça. Hospital Universitário Berna 2020.
- Jensen T, Barão R, et al: Uma nova definição de dor neuropática. Dor 2011; 152: 2204-2205.
- Trouvin AP, Perrot S: Novos conceitos de dor. Melhores Práticas & Investigação Reumatologia Clínica 2019; 33(3).
- Maurer K: Terapia prática passo-a-passo para o clínico geral. O Médico Informado 2017.
- Utilização a longo prazo de opiáceos para dor crónica não relacionada com o tumor (LONTS), 2ª actualização 2020; AWMF guideline register no. 145/003.
- Gustorff B: Testes opióides intravenosos em doentes com dor crónica não cancerígena. Eur J Pain 2005; 9(2): 123-125.
- Chou R, Turner JA, et al: The Effectiveness and Risks of Long-Term Opioid Therapy for Chronic Pain: A Systematic Review for a National Institutes of Health Pathways to Prevention Workshop. Ann Int Med 2015; doi: 10.7326/M14-2559.
InFo DOR & GERIATURA 2021; 3(1): 10-14