A doença do refluxo gastro-esofágico (DRGE) é uma das doenças mais comuns nos países industrializados ocidentais. Novos métodos de diagnóstico e conhecimentos sobre a fisiopatologia (por exemplo, bolsa de ácido), tornam possíveis novas terapias. A formação concentra-se nos inibidores da bomba de protões (PPI) e nos antiácidos de alginato.
| Graças ao patrocínio da empresa Reckitt Benckiser, a participação nesta formação é gratuita para si. A formação foi preparada por peritos e com absoluto respeito pela nossa liberdade editorial. Em nenhum momento a empresa teve e tem qualquer influência sobre o conteúdo da formação. Todos os textos estão sujeitos apenas à soberania científica dos autores e do corpo editorial da PPM MEDIC. |
A doença do refluxo gastro-esofágico (DRGE) é uma condição definida pelo refluxo do conteúdo gástrico para o esófago e os sintomas e/ou complicações perturbadoras resultantes [1]. Com uma prevalência de 10% a 20% e uma incidência de cerca de 5 por 1000 pessoas por ano, é uma das doenças mais comuns nos países industrializados ocidentais [2]. De acordo com os inquéritos epidemiológicos, a prevalência até aumentou significativamente nas últimas duas décadas, o que consequentemente leva ao aumento dos custos no sistema de cuidados de saúde [3].
Novos métodos de diagnóstico e conhecimentos associados em fisiopatologia, tais como o desenvolvimento pós-prandial de uma bolsa de ácido, permitem novas terapias.
Patogénese e factores de risco
A DRGE tem uma patogénese multifactorial, com função prejudicada da barreira anti-refluxo, que consiste no esfíncter esofágico inferior e nos músculos diafragmáticos, desempenhando um papel crucial [4]. A doença de refluxo grave é mais comum em doentes com uma grande hérnia hiatal axial. A causa mais comum de refluxo ligeiro a moderado é a relaxão esofágica inferior transitória dos esfíncteres (TLESR). Além disso, factores como a redução do tom de repouso do esfíncter esofágico, motilidade ineficaz do esófago com consequente depuração inadequada, esvaziamento gástrico retardado, salivação reduzida ou resistência reduzida do tecido podem influenciar o desenvolvimento da doença [5].

Vários factores de risco podem também favorecer o desenvolvimento do GERD. Estes incluem a velhice, obesidade, consumo de álcool e tabagismo, mas também a gravidez [5,6]. Além disso, vários medicamentos podem levar à doença de refluxo. Estes incluem medicamentos que têm um efeito relaxante sobre o esfíncteresofágico inferior, tais como antagonistas do cálcio, anticolinérgicos, teofilina e nitratos. Os opiáceos e esteróides, que causam gastroparese, e os anti-inflamatórios não esteróides, que afectam a resistência dos tecidos, também podem aumentar o risco de GERD [7].
O espectro clínico
O quadro clínico cobre um amplo espectro clínico que pode ser dividido em diferentes categorias [8]:
- doença de refluxo nãoerosivo (NERD)
- esofagite de refluxo erosivo (ERD)
- O esófago de Barrett
- Complicações do DRGE (por exemplo, estenose péptica, adenocarcinoma de esófago)
- Manifestações extra-esofágicas (por exemplo, globus, tosse, rouquidão, erosões dentárias).
- esófago hipersensível
- Queixas de refluxo funcional (ou seja, sem provas objectivas de DRGE).
Até 70% dos pacientes com sintomas típicos de DRGE têm uma mucosa esofágica normal e podem, portanto, ser classificados no subgrupo DRGE [9]. Isto significa que o refluxo do ácido gástrico leva a sintomas mas não desencadeia alterações endoscopicamente visíveis da mucosa. Em contraste, as erosões endoscopicamente detectáveis da mucosa são referidas como ERD.
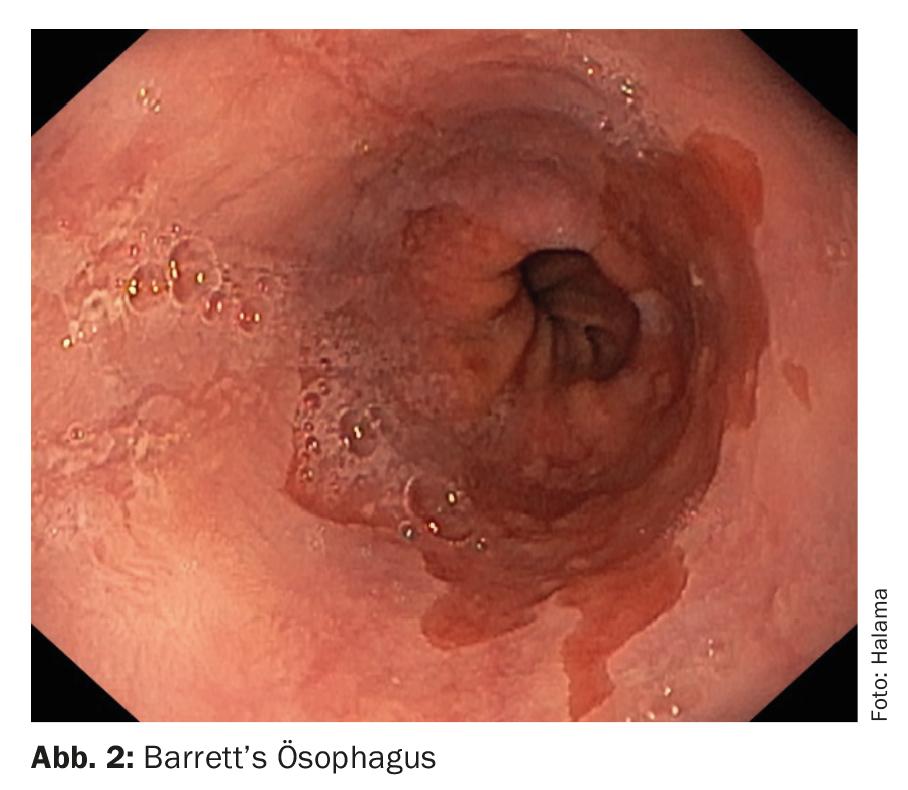
O esófago de Barrett encontra-se em 5-15% dos pacientes submetidos a endoscopia para sintomas de refluxo crónico. Isto é definido pelo epitélio escamoso multicamadas do esófago metaplasticamente transformando-se num epitélio cilíndrico altamente prismático, de camada única. O esófago de Barrett é uma condição pré-cancerígena com um risco de 0,5% por ano de desenvolvimento de adenocarcinoma por paciente. No entanto, uma proporção não insignificante de doentes com esófago de Barrett (Fig. 2) são assintomáticos e, portanto, difíceis de diagnosticar a tempo [10].
As complicações do GERD podem manifestar-se tanto dentro como fora do esófago. No esôfago, pode ocorrer esofagite, estenose ou esôfago de Barrett, já descrito. As complicações extra-esofágicas incluem laringite, tosse crónica, asma não atópica e erosões dentárias. Existe também uma possível associação entre GERD e faringite, sinusite, fibrose pulmonar idiopática e otite média recorrente.
O esófago hipersensível descreve pacientes que têm uma percepção aumentada dos sintomas devido ao aumento da sensibilidade, embora os eventos de refluxo estejam formalmente dentro da norma. A diminuição do limiar da dor esofágica pode ter causas tanto nervosas centrais como periféricas. As alterações erosivas endoscopicamente reconhecíveis não estão presentes num esófago hipersensível. Os sintomas podem ter várias causas, incluindo o estiramento do esófago devido ao refluxo ou estimulação química por ácido. A percepção dos sintomas pode ser exacerbada pelo stress físico (por exemplo, privação de sono nos trabalhadores por turnos) ou por distúrbios de ansiedade, podendo nesse caso ocorrer sintomas esofágicos mesmo na ausência de estimulação fisiológica ou patológica do esófago [11].
Diagnósticos
Uma anamnese diferenciada é crucial para o diagnóstico do GERD. O primeiro passo consiste em registar os sintomas (tab. 1) . Os sintomas típicos de refluxo são queimadura no estômago e regurgitação ácida. Mas outros sintomas tais como dor epigástrica, dor torácica, dificuldade de deglutição (disfagia), deglutição dolorosa (odynophagia), ardor na garganta ou aumento da limpeza da garganta também podem ser associados ao GERD. Para além do registo dos sintomas, deve também ser efectuado um esclarecimento de outras queixas no tracto gastrointestinal (por exemplo, sintomas de estômago ou intestino irritáveis) e deve ser tomado um historial detalhado de medicação [8].

Se os doentes experimentarem sintomas típicos de refluxo uma ou duas vezes por semana, o que por sua vez leva a uma deterioração da qualidade de vida, a DRGE é considerada provável. Se não houver sintomas de alarme tais como disfagia, odynophagia, perda de peso involuntária ou anemia, a terapia empírica com inibidores da bomba de prótons (PPI) pode ser inicialmente administrada sem mais diagnósticos.
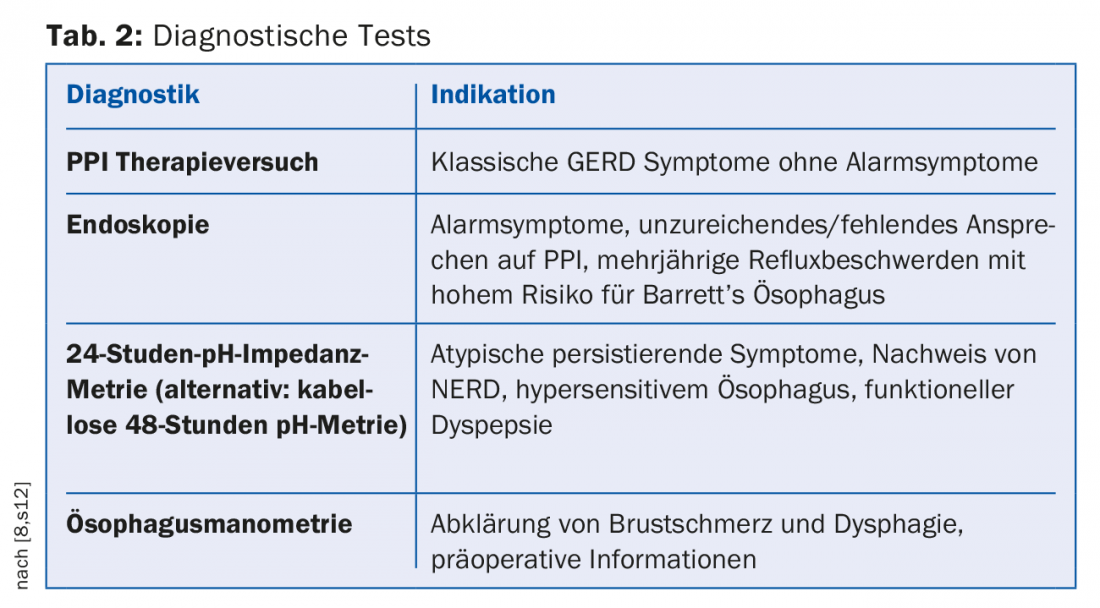
É necessário um diagnóstico adicional se os pacientes apresentarem sintomas de alarme, não responderem à terapia PPI ou se os sintomas estiverem presentes há muito tempo (separador 2) [12].
A esofagogastroduodenoscopia proporciona a oportunidade de avaliar as alterações na mucosa esofágica e fazer biopsias mucosas, se necessário. É especialmente necessário quando estão presentes sintomas de alarme. Contudo, o rastreio endoscópico geral de pacientes com sintomas de GERD não é recomendado [8].
Se forem detectados por endoscopia defeitos epiteliais (erosões) irregulares, estriados ou circularmente confluentes, a classificação da esofagite de refluxo deve ser baseada nos critérios de Los-Angeles. De notar que a esofagite de refluxo de grau A e B (Tab. 3) pode ser encontrada em pelo menos 15% da população em geral [13].

http://www.sciencedirect.com/science/article/pii/S2212097113700463#cesec50
Além disso, outras descobertas tais como estenose, úlcera, anel de Schatzki, metaplasia ou hérnias hiatais devem ser documentadas no relatório de descobertas. Outras anomalias tais como eritema, granulação, transição indistinta da área da mucosa de epitélio escamoso para cilíndrico, aumento das marcações vasculares no esófago distal, edema ou proeminência das pregas mucosas, não são, no entanto, diagnosticamente relevantes [8].
Se estiverem presentes erosões ou NERD, não é necessário fazer biopsias de mucosas. No entanto, se houver suspeita de esofagite eosinofílica, pelo menos quatro a seis biópsias devem ser tiradas de diferentes alturas do esófago.
Se os sintomas de refluxo estiverem presentes há vários anos, é necessária uma endoscopia para descartar o esófago de Barrett. O diagnóstico do esófago de Barrett é feito com base em provas histológicas de epitélio de cilindro metaplásico intestinal especializado. A descrição endoscópica deve ser baseada na classificação de Praga, que inclui uma indicação da extensão circunferencial (C) e máxima (M) da metaplasia epitelial do cilindro. Além disso, é necessária uma biopsia direccionada de áreas de mucosas suspeitas com biopsia subsequente de quatro quadrantes a cada 1-2 cm para permitir a localização da área neoplásica. Se estiverem presentes alterações inflamatórias, a biopsia de quatro quadrantes deve ser realizada novamente após quatro semanas de terapia com PPI. Se for detectada neoplasia intra-epitelial de baixo ou alto grau ou carcinoma da mucosa no esófago de Barrett, deve ser efectuada uma ressecção endoscópica [8].
A medição 24 horas de pH-metria ou medição combinada de pH-impedância é tipicamente utilizada em pacientes com sintomas de refluxo atípico, manifestações extra-esofágicas ou sintomas persistentes, especialmente na ausência de provas endoscópicas para GERD. Isto torna-o importante no diagnóstico do NERD. Através deste método, podem ser feitas afirmações sobre a presença de refluxo patológico, o tipo de refluxo e a duração dos episódios de refluxo. É a única forma de estabelecer uma ligação directa entre sintomas e episódios de refluxo ácido [12]. Isto significa que pode ser utilizado para diagnosticar esófago hipersensível ou dispepsia funcional. Especialmente no caso do esófago hipersensível, a correlação de sintomas e episódios de refluxo é crucial, uma vez que este diagnóstico sugere um número fisiológico de episódios de refluxo com percepção simultânea de um número aumentado.
A manometria esofágica não é adequada apenas para o diagnóstico da doença de refluxo. No entanto, pode ser utilizado para avaliar as dores no peito e a disfagia.
Além disso, deve ser utilizado pré-operatoriamente para obter informações sobre a localização do esfíncter esofágico inferior ou caracterização da motilidade tubular, bem como para excluir diagnósticos diferenciais relevantes, tais como acalasia ou hipomotilidade na esclerodermia [8].
A medição do refluxo duodenogastroesofágico, exames de raios X ou cintilografia não deve ser realizada devido à sua baixa sensibilidade [8].
Terapias
As mudanças de estilo de vida podem ajudar a melhorar os sintomas de refluxo. Isto inclui evitar refeições nocturnas e evitar alimentos e bebidas individualmente intoleráveis. A redução do peso é recomendada para pacientes com excesso de peso. Além disso, levantar a cabeceira da cama pode aliviar os sintomas.
O principal objectivo da terapia medicamentosa é o controlo satisfatório dos sintomas de GERD, independentemente da manifestação clínica. Além disso, se a esofagite de refluxo endoscopicamente comprovada, as lesões devem sarar e a ocorrência de complicações como hemorragia, estenose ou carcinoma deve ser evitada.
Inibidores da bomba de prótons
Os inibidores da bomba de prótons (PPIs) são medicamentos utilizados para suprimir a acidez. Bloqueiam a função do H+/K+-ATPase nas células vestibulares gástricas e impedem assim a secreção do ácido gástrico. Isto proporciona alívio dos sintomas.
Na síndrome típica de refluxo com resultados endoscópicos desconhecidos, recomenda-se o tratamento empírico com a dose padrão de PPI durante quatro semanas. O mesmo se aplica à esofagite de refluxo suave sintomática ou assintomática, que pode ser classificada de acordo com o grau A ou B de Los Angeles. Subsequentemente, se necessário, pode ser feita uma mudança para uma terapia “on-demand” com metade da dose padrão. Os doentes com NERD também devem receber meia dose padrão de PPI durante quatro semanas, embora a dose possa ser aumentada ou a duração da terapia prolongada se houver uma resposta inadequada a esta terapia [8]. Além disso, é possível a utilização de outro PPI. A terapia de PPI em dose completa durante quatro semanas pode geralmente conseguir um controlo adequado dos sintomas e a cura de quaisquer lesões em doentes com NERD ou esofagite erosiva.
Os PPIs também podem ser utilizados em terapia a longo prazo. Isto pode ser intermitente, contínuo ou a pedido. Contudo, a dose efectiva mais baixa deve ser determinada através de uma redução gradual da dose (degressiva). No caso de uma remissão estável a longo prazo no âmbito de uma terapia contínua, é também possível uma tentativa de descontinuação [8]. Se a esofagite de refluxo C ou D grave de Los Angeles for sintomática ou assintomática, aconselha-se uma terapia contínua com medicamentos de PPI em dose padrão (duas vezes por dia para inflamação e/ou sintomas persistentes) [8].
Alginato
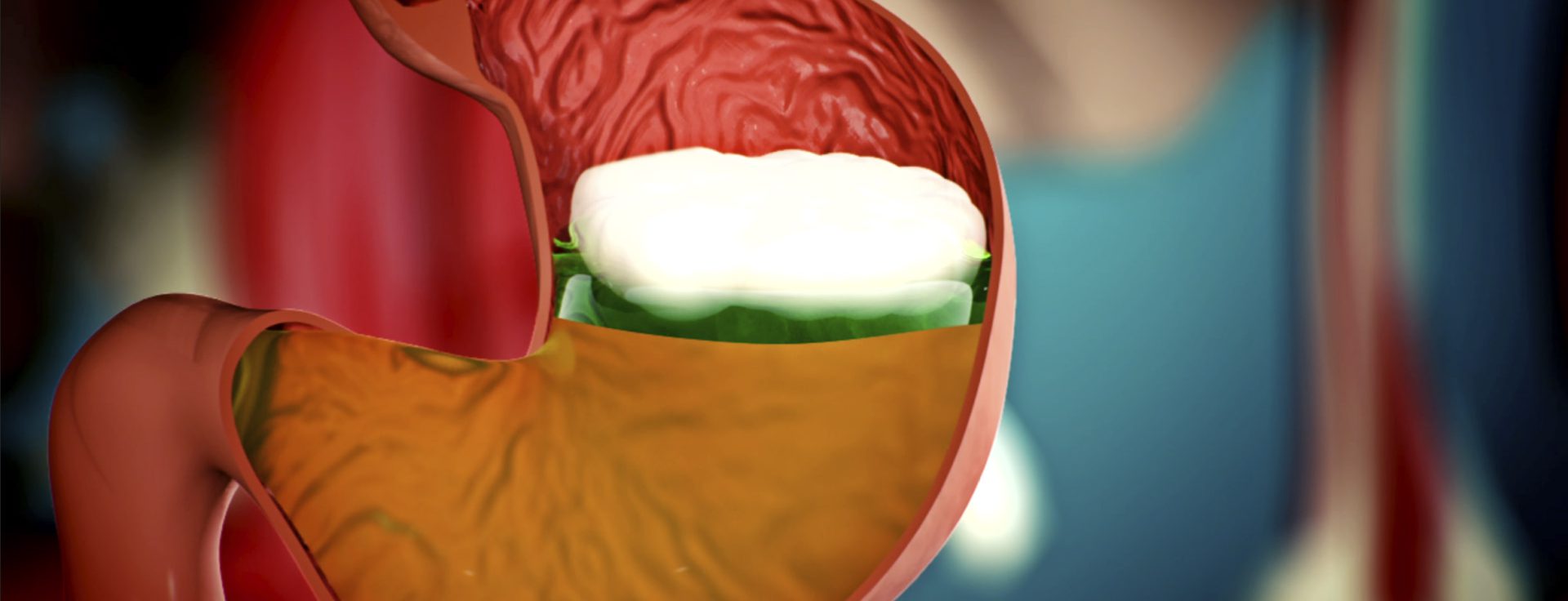
Os antiácidos de alginato permitem o controlo dos sintomas mesmo sem supressão de ácido. Apenas alguns minutos após a ingestão, os antiácidos de alginato, como o Gaviscon®, formam uma camada semelhante a um gel na superfície da acumulação de ácido no estômago através do contacto com o ácido estomacal, prevenindo assim mecanicamente episódios de refluxo [14,15]. Esta barreira de protecção física em frente da junção gastro-esofágica suprime episódios de refluxo ácido e não ácido durante o dia e também na posição supina [14,16]. Além disso, o alginato adere ao epitélio esofágico, onde forma uma camada protectora que pode aliviar os sintomas ao longo do tempo.
Assim, o alginato fornece um tratamento alternativo para os sintomas de refluxo persistente. O alginato também pode ser utilizado para o controlo dos sintomas no processo de redução gradual quando se afina o PPI. Além disso, a combinação com PPI é possível para proporcionar um alívio mais eficaz dos sintomas [17,18].
Outros medicamentos
Embora os antiácidos sejam inferiores aos PPIs e alginato no seu efeito, podem ser utilizados se necessário. Isto inclui casos individuais ou a terapia necessária em doentes com TERDN. Além disso, o tratamento de mulheres grávidas também é possível. Se os sintomas forem ligeiros durante a gravidez, a terapia inicial pode ser com um antiácido. Contudo, se este tratamento não funcionar ou se os sintomas forem graves, deve ser prescrito PPI [8]. Como os antiácidos servem apenas para neutralizar o ácido, não podem reduzir o número de episódios de refluxo e não têm qualquer efeito na bolsa de ácido. Os medicamentos procinéticos como a domperidona ou o baclofeno também podem prevenir o refluxo gastroesofágico aumentando o tom do esfíncter esofágico inferior e acelerando o esvaziamento gástrico [7].
Os antidepressivos tricíclicos (TADs) e os inibidores de recaptação de serotonina (SSRIs) servem para reduzir a sensibilidade da mucosa do esófago e podem por isso ser utilizados para tratar o esófago hipersensível e o desconforto gástrico funcional. Tanto uma única prescrição como uma terapia combinada com um PPI são possíveis [8].
Os antagonistas dos receptores de H2 desempenham um papel bastante menor na terapia de GERD na Suíça.
Terapia cirúrgica
A intervenção cirúrgica só deve ser feita se houver uma necessidade de terapia a longo prazo. Além disso, a cirurgia pode ser necessária se os critérios de indicação também forem cumpridos, se ocorrerem sintomas residuais intoleráveis induzidos por refluxo ou se existir intolerância a PPI. Antes de tal procedimento, o refluxo patológico deve ser detectado por medição de impedância de pH-metria 24 horas e a manometria esofágica deve ser realizada para excluir uma perturbação de motilidade. Se a cirurgia anti-refluxo for indicada, a fundoplicação laparoscópica é o procedimento preferido. O sucesso terapêutico é comparável ao da terapia PPI [8].
Terapia adicional com alginato
Os inibidores da bomba de prótons (PPIs) desempenham um papel crucial no tratamento da doença do refluxo gastroesofágico (DRGE). A sua eficácia sobre os tratamentos com placebo e superioridade sobre outros medicamentos tem sido demonstrada em numerosos estudos [19]. No entanto, há sempre doentes que não respondem à terapia PPI. Os ensaios aleatórios mostram que a proporção de doentes com sintomas persistentes de GERD apesar do tratamento com PPI é de cerca de 30% [20]. Números semelhantes são observados no tratamento a longo prazo das queixas de refluxo crónico. Num inquérito a 333 doentes que tinham recebido terapia de PPI há pelo menos um ano, 46% referiram sofrer de queimaduras e/ou regurgitação do estômago em pelo menos dois dias por semana [21].
Em caso de sintomas de refluxo, apesar da terapia PPI adequada, o procedimento posterior deve ser adaptado em conformidade. Por esta razão, foi publicado um algoritmo actual (Fig. 4), que apresenta o trabalho e tratamento dos sintomas de refluxo persistente sob PPI no GERD [22].
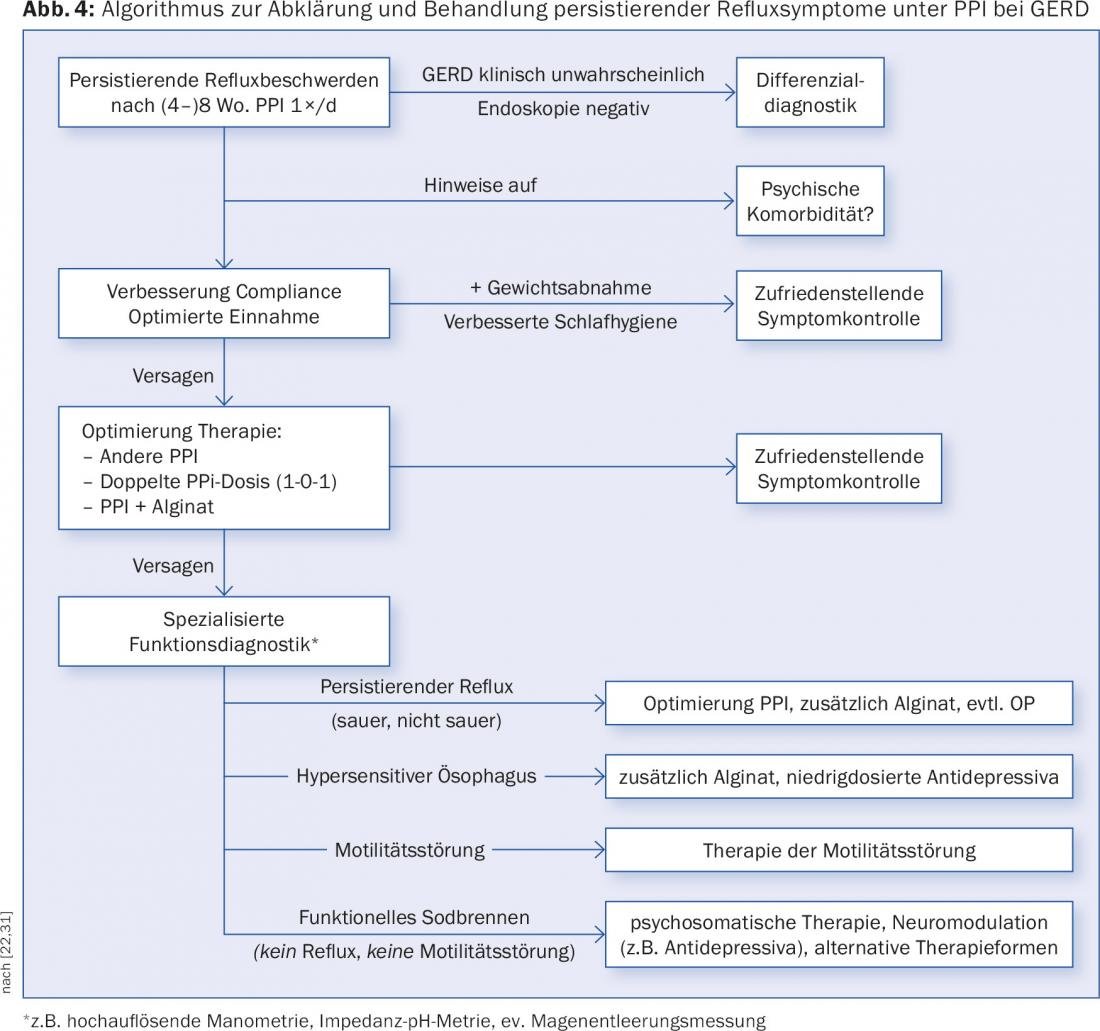
Um primeiro passo importante é confirmar o diagnóstico de GERD. Se os PPIs só fossem prescritos com base em sintomas clínicos, deveriam ser realizados diagnósticos diferenciais adicionais. Isto requer tanto um historial médico cuidadoso como uma endoscopia adicional, caso isto ainda não tenha sido feito. Se não houver explicação macroscópica para os sintomas, é também aconselhável fazer biópsias do duodeno, do estômago e do esófago. Em casos individuais, as comorbidades psicológicas podem também desempenhar um papel e devem ser tidas em conta [22].
Se o GERD tiver sido detectado, é possível trabalhar primeiro com o paciente para melhorar o cumprimento e/ou optimizar a ingestão. Alterações no estilo de vida, tais como dormir o suficiente ou reduzir o peso em pacientes com excesso de peso, também podem contribuir para um controlo satisfatório dos sintomas [22].
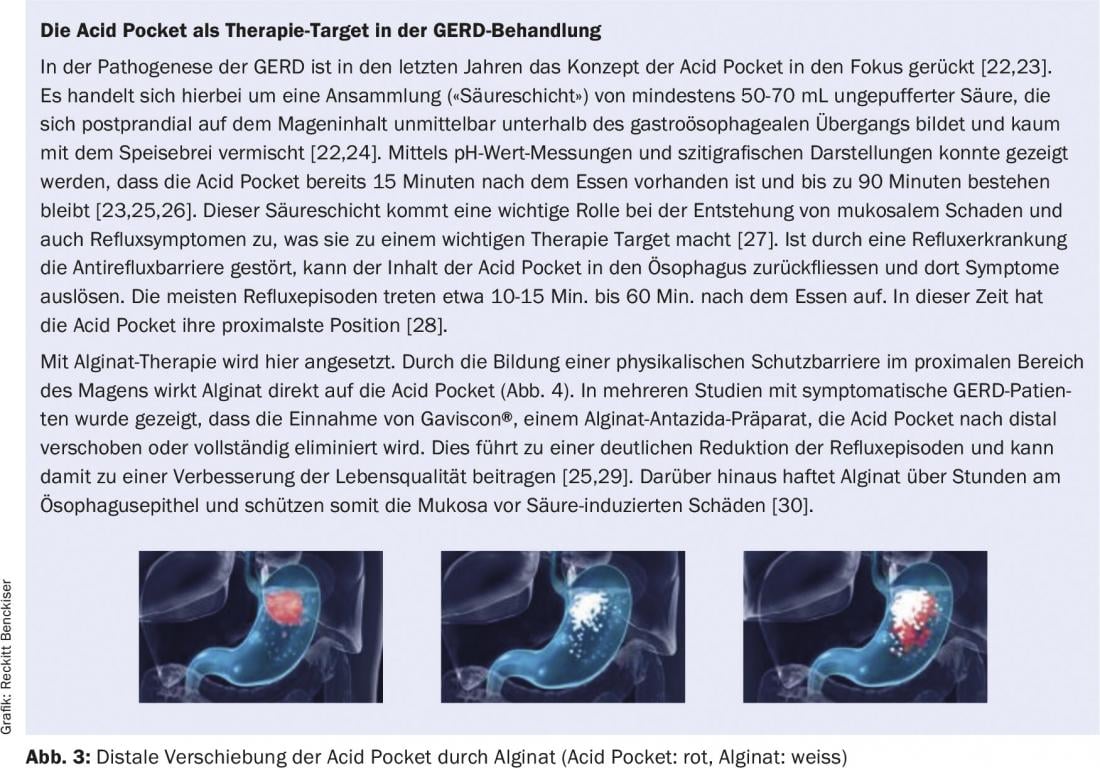
Se estas medidas não conduzirem ao sucesso desejado, uma alteração da preparação do PPI e/ou um aumento da dose são uma possibilidade de optimizar a terapia [22]. Contudo, devido ao facto de que em muitos pacientes a terapia com PPI por si só não é suficiente para aliviar eficazmente os sintomas, recomenda-se neste momento um tratamento adicional com alginato (ver caixa “O Bolso Ácido como alvo terapêutico no tratamento de GERD”). Em pacientes com doença de refluxo nãoerosivo (NERD), uma combinação com alginato leva a uma melhoria significativa dos sintomas em comparação com a monoterapia PPI (omeprazol) [32].
Se os sintomas persistirem, é aconselhável consultar um gastroenterologista para mais esclarecimentos, utilizando diagnósticos funcionais especializados [22]. Aqui são importantes diagnósticos diferenciais:
- um esófago hipersensível
- Perturbações de motilidade do esófago
- azia funcional
De acordo com o diagnóstico, podem então ser consideradas opções terapêuticas adaptadas ou adicionais.
Antiácidos e alginato no processo de redução gradual
Embora os PPIs sejam na sua maioria muito bem tolerados, podem ocorrer efeitos secundários (caixa “Efeitos secundários dos PPIs”). No entanto, os PPIs são normalmente utilizados para tratamento prolongado ou a longo prazo do GERD. Contudo, deve ser utilizada uma redução gradual da dose para determinar a dose eficaz mais baixa, a fim de minimizar o risco de efeitos adversos. No caso de uma remissão estável a longo prazo sob terapia PPI contínua, mesmo uma tentativa de descontinuação pode ser feita [8].
Tanto durante a redução gradual da dose, o chamado processo step-down, como ao descontinuar os PPIs no processo step-off, é útil um tratamento adicional orientado para os sintomas. Como demonstrado em estudos controlados por placebo em voluntários saudáveis, a interrupção abrupta dos PPI após quatro ou oito semanas de tratamento leva a uma recuperação ácida com um risco acrescido de sintomas dispépticos [34,35]. Embora o valor destes resultados em doentes com doença de refluxo seja controverso, o risco de ricochete de ácido sintomático deve ser minimizado. Por conseguinte, para além da redução gradual da dose, aconselha-se o uso de um antiácido ou alginato, conforme necessário [36].
Mensagens Take-Home
- No caso de sintomas típicos de refluxo sem sintomas de alarme, a terapia empírica com inibidores de bomba de protões (PPI) pode ser realizada sem mais diagnósticos.
- Em caso de sintomas de alarme, não resposta à terapia PPI ou queixas a longo prazo, são necessários mais diagnósticos. Se não for encontrado um diagnóstico definitivo na endoscopia, então deve ser considerada uma medição de impedância de pH combinada de 24 horas.
- Uma preparação antiácida de alginato pode ser usada em combinação com PPI, bem como monoterapia para a intolerância a PPI ou durante a afinação de PPI para o controlo dos sintomas no processo step-down e step-off.
- A terapia cirúrgica só é indicada em casos de necessidade de terapia a longo prazo, sintomas residuais intoleráveis ou intolerância à PPI.
Literatura:
- Vakil N, et al: A definição e classificação de Montreal da doença do refluxo gastroesofágico: um consenso global baseado em provas. Am J Gastroenterol, 2006. 101(8): 1900-1920.
- Dent J, et al: Epidemiologia da doença do refluxo gastro-esofágico: uma revisão sistemática. Gut, 2005. 54(5): 710-717.
- El-Serag HB: Tendências temporais da doença do refluxo gastroesofágico: uma revisão sistemática. Clin Gastroenterol Hepatol, 2007. 5(1): 17-26.
- Labenz J: Doença do refluxo gastroesfágico. DGIM Medicina Interna, 2015: 1-11.
- Bredenoord AJ, Pandolfino JE, Smout AJ: Doença do refluxo gastro-esofágico. The Lancet, 2013. 381(9881): 1933-1942.
- Fox M, Forgacs I: Doença do refluxo gastro-esofágico. BMJ: British Medical Journal, 2006. 332(7533): 88.
- Halama M, Frühauf H: Refluxo e doenças funcionais do esófago – uma doença generalizada? ARS MEDICI, 2010. 21: 852-857.
- Koop H, et al.: S2k-Leitlinie: Gastroösophageale Refluxkrankkheit unter Federführung der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS). Z Gastroenterol, 2014. 52: 1299-1346.
- Martinez SD, et al: doença de refluxo nãoerosivo (NERD) – refluxo ácido e padrões de sintomas. Aliment Pharmacol Ther, 2003. 17(4): 537-545.
- Shaheen NJ, Richter JE: esófago de Barrett. The Lancet, 2009. 373(9666): 850-861.
- Gyawali CP: Hipersensibilidade esofágica. Gastroenterologia & hepatologia, 2010. 6(8): 497.
- Badillo R, Francis D: Diagnóstico e tratamento da doença do refluxo gastroesofágico. World J Gastrointest Pharmacol Ther, 2014. 5(3): 105-112.
- Ronkainen J, et al: Prevalência do esófago de Barrett na população em geral: um estudo endoscópico. Gastroenterologia, 2005. 129(6): 1825-1831.
- Sweis R, et al.: Supressão do refluxo pós-prandial por um alginato formador de jangadas (Gaviscon Advance) em comparação com um simples antiácido documentado por ressonância magnética e monitorização de pH-impedância: avaliação mecanicista em voluntários saudáveis e estudo aleatório, controlado e duplo-cego em doentes com refluxo. Alimentary pharmacology & therapeutics, 2013. 37(11): 1093-1102.
- Rohof WO, et al: Uma formulação alginato-antacid localizada na bolsa de ácido para reduzir o refluxo ácido em doentes com doença de refluxo gastroesofágico. Gastroenterologia Clínica e Hepatologia, 2013. 11(12): 1585-1591.
- De Ruigh A, et al.: Gaviscon Double Action Liquid (antiácido e alginato) é mais eficaz que o antiácido no controlo da exposição pós-prandial ao ácido esofágico em doentes com DRGE: um estudo cruzado duplo-cego. Alimentary pharmacology & therapeutics, 2014. 40(5): 531-537.
- Reimer C, et al.: Ensaio clínico aleatório: alginato (Gaviscon Advance) versus placebo como terapia adicional em doentes com refluxo com resposta inadequada a um inibidor da bomba de protões, outrora diário. Aliment Pharmacol Ther, 2016.
- Labenz J, Koop H: Doença do refluxo gastroesofágico – o que fazer quando os PPIs não são suficientemente eficazes, tolerados ou desejados? DMW-Deutsche Medizinische Wochenschrift, 2017. 142(05): 356-366.
- Mössner J: As Indicações, Aplicações, e Riscos dos Inibidores da Bomba de Protões: Uma Revisão Após 25 Anos. Deutsches Ärzteblatt International, 2016. 113(27-28): 477.
- El-Serag H, Becher A, Jones R: Revisão sistemática: sintomas persistentes de refluxo na terapia com inibidores de bomba de protões nos cuidados primários e estudos comunitários. Farmacologia e terapêutica alimentar, 2010. 32(6): 720-737.
- Labenz J, et al: Controlo inadequado dos sintomas sob terapia de PPI a longo prazo para GERD – facto ou ficção? MMW Advances in Medicine, 2016. 158(4): 7-11.
- Labenz J, Koop H: Doença do refluxo gastroesofágico – o que fazer quando os PPIs não são suficientemente eficazes, tolerados ou desejados? DMW-Deutsche Medizinische Wochenschrift, 2017. 142(05): 356-366.
- Kahrilas PJ, et al: A bolsa de ácido: um alvo para tratamento na doença de refluxo? The American journal of gastroenterology, 2013. 108(7): 1058-1064.
- Steingoetter A., et al.: Volume, distribuição e acidez da secreção gástrica dentro e fora do tratamento inibidor da bomba de protões: um estudo randomizado duplo-cego controlado em doentes com doença de refluxo gastro-esofágico (DRGE) e sujeitos saudáveis. BMC gastroenterology, 2015. 15(1): 111.
- Rohof, W.O., et al.: Uma formulação alginato-antacídica localiza-se na bolsa de ácido para reduzir o refluxo ácido em doentes com doença de refluxo gastroesofágico. Gastroenterologia Clínica e Hepatologia, 2013. 11(12): 1585-1591.
- Fletcher J, et al: O sumo gástrico altamente ácido não tampão existe na junção gastroesofágica após uma refeição. Gastroenterologia, 2001. 121(4): 775-783.
- Boeckxstaens G, et al: Doença de refluxo sintomático: o presente, o passado e o futuro. Gutjnl, 2014: gutjnl-2013-306393.
- Rohof W, et al: Efeito da azitromicina no refluxo ácido, hérnia de hiato e bolsa de ácido proximal no período pós-prandial. Gutjnl, 2012: gutjnl-2011-300926.
- Kwiatek MA, et al.: Uma formulação alginato-antacídica (Gaviscon Líquido de Dupla Acção) pode eliminar ou deslocar a “bolsa de ácido” pós-prandial em doentes com DRGE sintomáticos. Alimentary pharmacology & therapeutics, 2011. 34(1): 59-66.
- Woodland, P., et al.: Protecção tópica da integridade da mucosa esofágica humana. American Journal of Physiology-Gastrointestinal and Liver Physiology, 2015. 308(12): G975-G980.
- Heinrich H, Fox M, Schwizer W: Diagnóstico e terapia no refluxo gastroesofágico: Refluxo – uma doença generalizada? Family Practice, 2014. 9(9): 26-30.
- Manabe N, et al.: Eficácia da adição de alginato de sódio ao omeprazol em doentes com doença de refluxo nãoerosivo: um ensaio clínico aleatório. Doenças do Esophagus, 2012. 25(5): 373-380.
- Halama M, Frühauf H: Refluxo e doenças funcionais do esófago – uma doença generalizada? ARS MEDICI, 2010. 21: 852-857.
- Niklasson A, et al.: Desenvolvimento de sintomas dispépticos após descontinuação de um inibidor de bomba de protões: um ensaio controlado por placebo duplo cego. The American journal of gastroenterology, 2010. 105(7): 1531-1537.
- Reimer C., et al.: A terapia com inibidores de bomba de prótons induz sintomas relacionados com ácido em voluntários saudáveis após a retirada da terapia. Gastroenterologia, 2009. 137(1): 80-87. e1.
- Cawston J, Evans N: Dyspepsia: considerações chave para uma gestão rentável. Prescriber, 2007. 18(5): 21-30.
PRÁTICA DO GP 2017; 12(6): 24-31